Содержание
Введение. 3
1. Антибиотики пенициллинового ряда, эритромицин,
левомицетин, тетрациклины.. 5
2. Характеристика физических, химических и
фармакологических свойств. 10
3. Методы идентификации и контроль качества. 18
Заключение. 25
Список литературы.. 26
Введение
Макролиды давно и
широко применяются в клинической практике. Эритромицин и спирамицин известны с
начала пятидесятых годов, а рокситромицин, кларитромицин и мидекамицин
появились относительно недавно. Спектр антимикробной активности всех этих
препаратов весьма сходен. Они обладают хорошей активностью против пневмококков
и внутриклеточных патогенов, и малоактивны в отношении гемофильной палочки.
Любопытно, что самый первый макролид эритромицин более активен против
Haemophilus, чем современные препараты.
Рокситромицин (Рулид)
кларитромицин (Клацид), и спирамицин (Ровамицин), в отличие от эритромицина и
мидекамицина (Макропена), принимают два раза в день.
Принципиальным же
отличием "новых макролидов" от традиционных является меньшее число
расстройств со стороны желудочно-кишечного тракта. Дело в том, что метаболиты
эритромицина стимулируют мотилиновые рецепторы кишечника, повышающие тонус и
моторику кишечника. Известны случаи настолько полной имитации "острого
живота", что больной поступал к хирургам. Для новых макролидов этот эффект
выражен существенно меньше[1].
С внедрением в
клиническую практику таких высокоэффективных лекарственных средств, как
антибиотики, гормоны, противовирусные препараты, в том числе активных
антиретровирусных средств, нейролептиков, иммуномодуляторов, цитокинов и многих
других существенно расширяются возможности лечения различных заболевании.
Однако с ростом эффективности лекарственных средств сужается спектр их
терапевтического действия и увеличивается риск осложнений лекарственной
терапии.
Внедрение новых
высокоэффективных лекарственных средств позволяет значительно улучшить
оказание лечебной помощи, но ведет к нарастанию побочных реакций организма на
лекарства, нежелательных эффектов на них вплоть до тяжелых осложнений медикаментозной
терапии.
Цель данной работы –
рассмотреть вопросы применения, стандартизации и контроля качества эритромицина
и других антибиотиков.
Задачи:
-
изучить характеристики и применение
антибиотиков;
-
выявить характеристики физических, химических и
фармакологических свойств;
-
рассмотреть методы идентификации и вопросы
контроля качества.
1. Антибиотики
пенициллинового ряда, эритромицин, левомицетин, тетрациклины
Пенициллин является антимикробным веществом, продуцируемым
различными видами плесневого гриба пенициллиума. В результате жизнедеятельности
этих грибов образуются различные виды пенициллина. Одним из наиболее активных
является бензилпенициллин.
По химическому
строению пенициллин является кислотой и из него гут быть получены различные
соли (натриевая, калиевая и др.). Препараты группы пенициллина эффективны при
инфекциях, вызванными грамположительными бактериями (стрептококки,
стафилококки, пневмококки и др.), спирохетами и другими патогенными
микроорганизмами. Они оказывают бактерицидное действие на микроорганизмы,
находящиеся в фазе роста.
Бензилпенициллин и другие
препараты группы пенициллина неэффективны
в отношении вирусов (возбудителей гриппа, полиомиелита, оспы и
др.), микобактерий туберкулеза, возбудителя амебиаза, а также большинства
патогенных грамотрицательных микроорганизмов.
Между отдельными
препаратами этой группы существуют различия в скорости наступления и
продолжительности антибактериального действия, эффективности при разных путях
введения, способности накапливаться разных органах и тканях, а также активности
в отношении различных микроорганизмов.
Характерной особенностью
некоторых полусинтетических пенициллинов (метициллина
и оксациллина) является их
эффективность в отношении штаммов микроорганизмов (стафилококков), резистентных
к пенициллину. Эта особенность связана с устойчивостью упомянутых
полусинтетических пенициллинов к ферменту пенициллиназе, разрушающему
биосинтетические пенициллины. Ампициллин
действует на ряд грамотрицательных микроорганизмов[2].
Эритромицин является антибактериальным веществом, продуцируемым
Streptomyces erythreus или другими родственными микроорганизмами. Относится к
группе макролидов - соединений, содержащих в молекуле макроциклическое
лактонное кольцо. По спектру антимикробного действия эритромицин близок к
пенициллинам. Он активен в отношении грамположительных и грамотрицательных микроорганизмов
(стафилококки, пневмококки, стрептококки, гонококки, менингококки). Действует
также на ряд грамположительных бактерий, бруцелл, риккетсий, возбудителей
трахомы и сифилиса. Слабо или совсем не действует на большинство
грамотрицательных бактерий, микобактерий, мелкие и средние вирусы, грибы.
Эритромицин переносится больными лучше, чем пенициллины, и может при- меняться
при аллергии к пенициллинам. В терапевтических дозах эритромицин действует
бактериостатически. Устойчивость к антибиотику развивается быстро, причем с
другими антибиотиками группы макролидов (олеандомицин) наблюдается перекрестная
устойчивость. При комбинированном применении со стрептомицином, тетрациклинами
и сульфаниламидами наблюдается усиление действия эритромицина. Применяют эритромицин
при пневмонии, пневмоплевритах, бронхоэктатической болезни и стадии обострения
и при других инфекционных заболеваниях легких, вызванных чувствительными к
антибиотику микроорганизмами; при септических состояниях, рожистом воспалении,
мастите, остеомиелите, перитоните, гнойном отите и других гнойно-воспалительных
процессах.
Побочные явления при
лечении эритрамицином наблюдаются относительно редко (тошнота, рвота, понос).
При длительном применении возможны нарушения функции печени (желтуха). В отдельных
случаях может наблюдаться повышенная чувствительность к препарату с появлением
аллергических реакций. При длительном применении эритромицина возможно развитие
устойчивости микроорганизмов. Препарат противопоказан при индивидуальной
повышенной чувствительности к нему и при тяжелых нарушениях функции печени.
Эритромицин повышает концентрацию в плазме крови карбамазепина, теофиллина и
усиливает их токсический эффект (тошноту, рвоту и др.)[3].
Левомицетин является антибиотиком широкого спектра действия; эффективен
в отношении многих грамположительных и грамотрицательных бактерий, риккетсий,
спирохет и некоторых крупных вирусов (возбудители трахомы, пситтакоза, пахового
лимфогранулематоза и др.); действует на штаммы бактерий, устойчивые к
пенициллину, стрептомицину, сульфаниламидам. В обычных дозах действует
бактериостатически. Слабоактивен в отношении кислотоустойчивых бактерий,
синегнойной палочки, клостридий и простейших. Механизм антимикробного действия
левомицетина связан с нарушением синтеза белков микроорганизмов. Лекарственная
устойчивость к препарату развивается относительно медленно, при этом, как
правило, перекрестной устойчивости к другим химиотерапевтическим средствам не
возникает. Левомицетин легко всасывается из желудочно-кишечного тракта. После приема
внутрь максимальная концентрация в крови создается через 2 - 3 ч; в течение 4 -
5 ч после однократного приема лечебной дозы в крови сохраняется терапевтически
активная концентрация, затем происходит значительное снижение концентрации.
Препарат хорошо проникает в органы и жидкости организма; проникает через
гематоэнцефалический барьер, через плаценту, обнаруживается в материнском
молоке. Терапевтические концентрации левомицетина при назначении его внутрь или
местно создаются в стекловидном теле, роговице, радужной оболочке, в водянистой
влаге глаза; в хрусталик препарат не проникает. Левомицетин хорошо всасывается
при ректальном введении. Выводится в основном с мочой, главным образом в виде
неактивных метаболитов; частично - с желчью и калом. В кишечнике под действием
кишечных бактерий происходит гидролиз левомицетина с образованием неактивных
метаболитов. Применяют левомицетин при брюшном тифе, паратифах,
генерализованных формах сальмонеллезов, бруцеллезе, туляремии, менингите,
риккетсиозах, хламидиазах. При инфекционных процессах иной этиологии, вызванных
возбудителями, чувствительными к действию левомицетина, препарат показан в
случае неэффективности других химиотерапевтических препаратов. Применяют также
левомицетин местно для профилактики и лечения глазных инфекционных заболеваний
(конъюнктивит, блефарит и др.)[4].
При лечении
левомицетином могут наблюдаться диспепсические явления (тошнота, рвота, жидкий
стул), раздражение слизистых оболочек рта, зева, кожная сыпь, дерматиты, сыпь и
раздражение вокруг заднего прохода и др. Следует учитывать, что левомицетин
может оказывать токсическое влияние на кроветворную систему (ретикулоцитопения,
гранулоцитопения, иногда уменьшение числа эритроцитов). В тяжелых случаях
возможна апластическая анемия. Тяжелые осложнения со стороны кроветворной
системы чаще связаны с применением больших доз левомицетина. Наиболее
чувствительны к препарату дети раннего возраста. Большие дозы левомицетина
могут вызвать психомоторные расстройства, спутанность сознания, зрительные и слуховые
галлюцинации, снижение остроты слуха и зрения. Применение левомицетина иногда
сопровождается подавлением микрофлоры кишечника, развитием дисбактериоза,
вторичной грибковой инфекцией. При применении левомицетина в виде глазных
капель и мазей возможны местные аллергические реакции. Лечение левомицетином
следует проводить под контролем картины крови и функционального состояния
печени и почек больного. Нельзя допускать бесконтрольного назначения
левомицетина и применения его при легких формах инфекционных процессов,
особенно в детской практике. Не следует назначать левомицетин при острых
респираторных заболеваниях, ангине и с профилактической целью. Левомицетин не
назначают вместе с препаратами, угнетающими кроветворение (сульфаниламиды,
производные пиразолона, цитостатики). Вследствие возможного изменения
метаболизма ряда лекарственных препаратов левомицетин не рекомендуется
применять совместно с дифенином, неодикумарином, бутамидом, барбитуратами[5].
Тетрациклин является антимикробным веществом, продуцируемым
Streptomyces аurefaciens или другими родственными организмами. Применяют
тетрациклин внутрь и наружно. Внутрь назначают больным пневмонией, бронхитом,
гнойным плевритом, подострым септическим эндокардитом, бактериальной и амебной
дизентерией, коклюшем, ангиной, скарлатиной, гонореей, бруцеллезом, туляремией,
сыпным и возвратным тифами, пситтакозом, при инфекционных заболеваниях мочевых
путей, хронических холециститах, гнойном менингите и при других инфекционных
заболеваниях, вызванных микроорганизмами, чувствительными к этому антибиотику.
Тетрациклин можно также применять для предупреждения инфекционных осложнений у
хирургических больных. Местно назначают тетрациклин при инфекционных
заболеваниях глаз, ожогах, флегмонах, маститах и т. п. При тяжелых септических
заболеваниях тетрациклин можно применять вместе с другими антибиотиками.
Тетрациклин обычно
хорошо переносится, однако, как и другие антибиотики, обладающие широким
спектром антибактериального действия, может вызывать побочные явления:
понижение аппетита, тошноту, рвоту, расстройство функции кишечника (легкий или
сильный понос), изменения слизистых оболочек рта и желудочно-кишечного тракта
(глоссит, стоматит, гастрит, проктит); могут возникать аллергические кожные
реакции, отек Квинке и др. Тетрациклин и другие препараты этого ряда могут
повысить чувствительность кожи к действию солнечных лучей (фотосенсибилизация).
Отмечено, что длительное применение тетрациклина и других препаратов этой группы
в период образования зубов (назначение детям в первые месяцы жизни) может
вызвать у детей темно-желтую окраску зубов (отложение препарата в зубной эмали
и дентине). При длительном применении препаратов группы тетрациклинов могут
возникнуть осложнения, обусловленные развитием кандидоза (поражения кожи и слизистых
оболочек, а также септицемии, вызываемые дрожжевидным грибом Сandida аlbicans)[6].
2.
Характеристика физических, химических и фармакологических свойств
1. Группа пенициллина
Продуцируется
различными видами плесневого гриба пенициллиума. В результате жизнедеятельности
этих грибов образуются различные виды пенициллина.
Один из наиболее
активных представителей этой группы – бензилпенициллин – имеет следующее
строение:
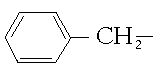
Другие виды пенициллина
отличаются от бензилпенициллина тем, что вместо бензильной группы содержат
другие радикалы.
По химическому
строению пенициллин представляет собой кислоту, из него могут быть получены
различные соли. Основой молекулы всех пенициллинов является
6-аминопенициллановая кислота – сложное гетероциклическое соединение, состоящее
из двух колец: тиазолидинового и бета-лактамного.
Характерной
особенностью некоторых полусинтетических пенициллинов является их эффективность
в отношении штаммов микроорганизмов, резистентных к бензилпенициллину.
Резистентность
устойчивых штаммов микроорганизмов к группе пенициллинов обусловлена их
способностью продуцировать специфические ферменты – бета-лактамазы
(пенициллиназы), гидролизующие бета-лактамное кольцо пенициллинов, что лишает
их антибактериальной активности.
В последнее время
получены не только антибиотики, устойчивые к действию бета-лактамаз, но также
соединения, разрушающие эти ферменты.
Препараты этой группы
оказывают бактерицидное действие на микроорганизмы, находящиеся в фазе роста.
Антибактериальный эффект связан со специфической способностью пенициллинов
ингибировать биосинтез клеточной стенки микроорганизмов. Мишенями для них
являются транспептидазы, которые завершают синтез пептидогликана клеточной
стенки. Транспептидазы представляют собой набор белков-ферментов,
локализованных в цитоплазматической мембране бактериальной клетки. Отдельные бета-лактамы различаются по
степени сродства к тому или иному ферменту, которые получили название
пенициллинсвязывающих белков[7].
Побочные действия:
головная боль, повышение температуры тела, крапивница, сыпь на коже и слизистых
оболочках, боли в суставах, эозинофилия.
2. Группа цефалоспорина
Это группа природных антибиотиков,
продуцируемых грибами рода Cephalosporium, и их синтетических производных.
Эта группа антибиотиков имеет в своей
основе 7-аминоцефалоспорановую кислоту (7-АЦК):
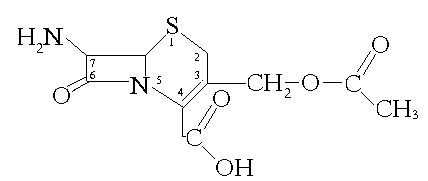
Цефалоспорины первого поколения
обладают высокой антистафилококковой активностью, включая
пенициллиназообразующие штаммы. Цефалоспорины второго поколения также обладают
высокой антистафилококковой активностью, в том числе в отношении
пенициллиназообразующих штаммов. Они активны в отношении эшерихий, клебсиелл,
протеев.
Цефалоспорины третьего поколения
обладают более широким спектром действия, чем цефалоспорины первого и
второго поколений, и большей активностью в отношении грамотрицательных бактерий.
По химическому строению основа этих
антибиотиков (7-АЦК) имеет элементы сходства с основой структуры антибиотиков
группы пенициллина - 6-аминопенициллановой кислотой, однако различия в
структуре цефалоспоринов и пенициллинов в целом создают условия для
устойчивости цефалоспоринов к стафилококковой пенициллиназе и их высокой
эффективности в отношении устойчивых к бензилпенициллину
пенициллиназообразующих бактерий.
Механизм бактерицидного действия
цефалоспоринов связан с повреждением клеточной мембраны бактерий, находящихся в
стадии размножения, что обусловлено специфическим ингибированием ферментов
клеточных мембран.
Побочные явления: аллергические
реакции, нарушение функции почек. Рекомендуется соблюдать осторожность при
назначении цефалоспоринов больным, имеющим гиперчувствительность к
пенициллинам.
3. Тетрациклины
Это группа природных антибиотиков,
продуцируемых Streptomyces aurefaciens, Str. rimosus и другими родственными
микроорганизмами, и их полусинтетических производных.
В основе их химического строения лежит
конденсированная четырехциклическая система:
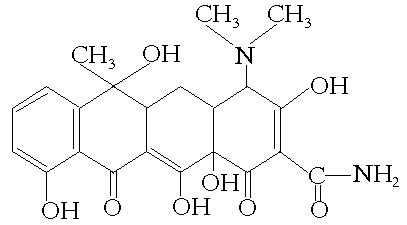
В основе механизма антибактериального
действия тетрациклинов лежит подавление ими биосинтеза белка микробной клетки
на уровне рибосом; они блокируют связывание аа-тРНК на А участке рибосомы 70S.
Тетрациклины легко проникают через
плацентарный барьер, поэтому препараты этой группы не назначают беременным
женщинам. Вследствие возможного образования нерастворимых комплексов
тетрациклинов с кальцием и отложения их в костном скелете, эмали и дентине
зубов препараты этой группы нельзя, как правило, назначать детям до 8 лет[8].
4.
Аминогликозиды
Часть антибиотиков этой группы
образуется в природе лучистыми грибами Actinomyces (неомицин, канамицин,
тобрамицин), продуцентом другой части антибиотиков является Micromonospora
(гентамицин), в последнее время получены полусинтетические производные этой
группы (амикацин, являющийся производным канамицина А).
Механизм действия основан на
блокировании биосинтеза белка на уровне рибосом бактериальной клетки.
Побочное действие: нефротоксичность и
ототоксичность (кохлеарная и вестибулярная).
5.
Макролиды
Это группа природных антибиотиков,
продуцируемых лучистыми грибами Streptomyces erythreus, Str. Antibioticus и др.
родственными микроорганизмами, и их полусинтетических производных.
Макролиды содержат в своем составе
макроциклическое лактонное кольцо, связанное с углеводородными остатками:
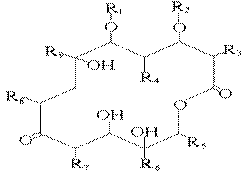 где R - углеводородный радикал.
где R - углеводородный радикал.
Действие этих антибиотиков основано на
подавлении биосинтеза белка микроорганизмов на уровне рибосом (блокирование
реакции транслокации).
Побочные явления:
тошнота, рвота, понос, при длительном применении возможны нарушения функции печени (желтуха). В
отдельных случаях возможно появление аллергических реакций[9].
6.
Группа левомицетина
Это природные антибиотики,
продуцируемые Streptomyces venezuelae, и их синтетические аналоги.
В их основе лежит следующая структура:
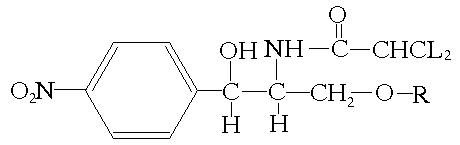
Большинство штаммов бактерий,
устойчивых к пенициллинам, стрептомицинам сохраняет свою чувствительность к
этой группе антибиотиков.
Механизм
действия антибиотиков основан на подавлении биосинтеза белка микроорганизмов на
уровне рибосом (подавление пептидилтрансферазной реакции).
Побочные явления: диспепсические
явления (тошнота, рвота, жидкий стул), раздражение слизистых оболочек рта,
зева, кожная сыпь, дерматиты, иногда развивается дисбактериоз в кишечнике,
вторичная грибковая инфекция. Токсическое действие на кроветворную систему
(ретикулоцитопения, иногда уменьшение числа эритроцитов). Большие дозы
левомицетина могут вызвать психомоторные расстройства, спутанность сознания,
зрительные и слуховые галлюцинации, снижение остроты слуха и зрения[10].
7. Синтетические антибиотики
Одним из самых активных производных
нафтиридина являются соединения, содержащие в положении 7 хинолонового ядра
незамещенный или замещенный пиперазиновый цикл, а в положении 6 атом фтора. Эти
соединения названы фторхинолонами:
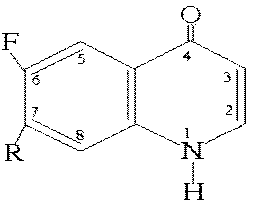
В механизме действия фторхинолонов
особое значение имеет их влияние на метаболизм ДНК бактерий; эти препараты
ингибируют фермент ДНК-гиразу, содержащуюся в бактериальных клетках и
относящуюся к топоизомеразам, контролирующим структуру и функции ДНК.
Антибактериальная активность хинолонов
обусловлена влиянием на РНК бактерий и синтез бактериальных белков, а также на
стабильность мембран.
Обычно фторхинолоны хорошо переносятся,
однако могут возникать побочные явления в виде тошноты, рвоты, диареи.
Хинолоны могут вызывать головную боль,
бессонницу или сонливость, беспокойство, тремор и др. Возможно, что эти явления
связаны со способностью хинолонов накапливаться в ЦНС и угнетать рецепторное
связывание ГАМК или вытеснять этот тормозной нейромедиатор из мест связывания.
При больших дозах хинолонов возможно развитие судорожных припадков.
Хинолоны противопоказаны детям и
подросткам (в период формирования скелета), а также беременным и кормящим
матерям. Следует учитывать, что хинолоны ингибируют окислительные ферменты
печени и могут усиливать действие лекарств метаболизируемых системой цитохрома
P-450 (таблица 1).
Таблица 1
Характеристика групп
антибиотиков[11]
|
Группа
|
Продуцент
|
Основа молекулы
|
Эффективность
|
Не эффективны
|
|
1
|
2
|
3
|
4
|
5
|
|
пенициллина
|
Penicillium
chrysogenum, Penicillium notatum и
др.
|
6-аминопенициллановая кислота
|
при инфекциях, вызванных грамположительными бактериями
(стрептококками, стафилококками, пневмококками), спирохетами и другими
патогенными микроорганизмами
|
в отношении вирусов (возбудители гриппа, полиомиелита,
оспы и др.), микобактерий туберкулеза, возбудителя амебиаза, риккетсий,
грибов, а также большинства патогенных грамотрицатель-ных микроорганизмов.
|
|
цефалоспорина
|
Cephalospori-um
|
7-аминоцефало-спорановую
кислоту
(7-АЦК)
|
в отношении всех видов стрептококков (за исключением
энтерококков), гонококков.
|
не действует на микобактерии туберкулеза, риккетсии,
вирусы, простейшие
|
|
левомицети-на
|
Streptomyces venezuelae, и их синтетические аналоги.
|
|
в отношении многих видов грамотрицательных, включая,
риккетсии и спирохеты, и грамположительных бактерий.
|
слабо активен в отношении кислотоустойчивых бактерий,
синегнойной палочки, клостридий, простейших
|
Окончание таблицы 1
|
1
|
2
|
3
|
4
|
5
|
|
Тетрацикли-ны
|
Streptomyces
aurefaciens, Str. rimosus и другими родственными микроорганизмами
|
|
в отношении грамположительных грамотрицательных бактерий,
спирохет, лептоспир, риккетсий, крупных вирусов (возбудители трахомы,
орнитоза).
|
в отношении
протея, синегнойной палочки, большинства грибов и мелких вирусов (гриппа,
полиомиелита, кори и др.), недостаточно активны в отношении
кислотоустойчи-вых бактерий
|
|
Аминоглико-зиды
|
Actinomyces,
Micromonospora и
полусинтети-ческие производные этой группы
|
олигосахаридная и
псевдоолигосахаридная
|
широкого спектра действия, оказывающими бактерицидное
влияние на грамположительные и особенно грамотрицательные бактерии.
|
не действует на анаэробные бактерии, грибы, вирусы и
большинство простейших
|
|
Макролиды
|
Streptomyces
erythreus, Str. Antibioticus и др. родственны-ми микроорганизмами, и их
полусинтети-ческих производных
|
макроциклическое
лактонное кольцо, связанное с углеводород-ными остатками
|
в отношении грамположительных бактерий (стафилококки,
стрептококки и др.), а также в отношении некоторых грамотрицательных бактерий
(бруцеллы, холерный вибрион, риккетсии и др.)
|
слабо или совсем не действует на большинство
грамотрицательных бактерий, микобактерий, мелкие и средние вирусы, грибы
|
|
Производные нафтидина.
Хинолоны. Фторхиноло-ны.
|
|
7 хинолонового
ядра незамещенный или замещенный пиперазино-вый цикл, а в положении 6 атом
фтора
|
на аэробные грамотрицательные бактерии, большинство
штаммов стафилококков чувствительны к хинолонам, стрептококки более
устойчивы.
|
в отношении грамположительных кокков (стафилококки,
стрептококки, пневмококки) и патогенных анаэробов
|
3. Методы
идентификации и контроль качества
По направленности
своего действия все антибиотики можно разделить на следующие основные группы:
1. противобактериальные
антибиотики;
2. противогрибковые
антибиотики;
3. противовирусные
антибиотики;
4. противоопухолевые
антибиотики[12].
Некоторые авторы
относят к антибиотикам не только те химические вещества, которые синтезируются
микроорганизмами, но и неприродные соединения, синтезируемые химическими
способами, полагая, что дело не столько в происхождении препарата, сколько в
его антимикробной активности и полезности для человека.
Они включают в себя
природные пенициллины, несколько поколений полусинтетических пенициллинов,
несколько поколений цефалоспоринов, нетрадиционные бета-лактамы.
Бета-лактамные антибиотики включают в себя природные
пенициллины, несколько поколений полусинтетических пенициллинов, несколько
поколений цефалоспоринов, нетрадиционные бета-лактамы. Группа бета-лактамных
антибиотиков активна против многих грамположительных и грамотрицательных,
аэробных и анаэробных бактерий[13].
Качество лекарственных средств можно с уверенностью гарантировать,
если на всех этапах жизненного цикла лекарственных препаратов строго
соблюдаются все правила обращения, в частности проведения доклинических и
клинических исследований, производства, оптовой и розничной реализации
фармацевтической продукции. Немаловажную роль при этом играют наиболее
оптимальные своды международных требований - GLP, GCP, GMP, GDP, GPP. Особое
значение в деятельности работников фармацевтической отрасли имеют требования
GSP - надлежащей практики хранения лекарственных средств.
В настоящее время
изучение и соблюдение этого стандарта качества является весьма актуальной
задачей для фармбизнеса. Хранение и транспортировка фармацевтических материалов
и продукции имеет место на всех этапах их обращения, и в этих операциях
задействованы практически все участники фармрынка. Поэтому нельзя с
уверенностью говорить о качестве, безопасности и эффективности лекарственных
средств, не разработав национального или хотя бы внутрифирменного стандарта
хранения лекарственных средств, соответствующего нормам GSP, и не соблюдая его
на практике.
По мнению
специалистов, в улучшении качества функционирования оптового звена позитивную
роль также может сыграть разработка и принятие участниками фармрынка
отечественного стандарта GDP.
Основными принципами
стандарта GDP - Good Distribution Practice (правила надлежащей оптовой торговли
фармпродукцией) являются следующие положения. В индустриально развитых странах
фармацевтическая промышленность гарантирует высокий уровень качества
лекарственных средств, достигая его посредством следования требованиям GMP. В
странах ЕС, США, Канаде, Японии и ряде других фармпродукция может быть допущена
к реализации только в случае, если ее производство было осуществлено в
соответствии с указанными требованиями. Эта политика гарантирует, что продукты,
выпущенные для реализации, имеют соответствующее качество.
Высокий (надлежащий)
уровень качества должен поддерживаться в сфере обращения фармпродукции таким
образом, чтобы допущенные к продаже лекарственные средства реализовывались
оптовой и розничной торговлей без изменения их свойств. Концепция управления
качеством в фармацевтической промышленности описана в руководствах по GMP и
должна по возможности использоваться при реализации лекарственных средств.
Кроме того, чтобы
поддержать качество фармпродукции и уровень обслуживания, предлагаемого
оптовиками, они должны применять принципы и правила GDP.
Система качества,
используемая дистрибьюторами (оптовиками) лекарственных средств, должна
гарантировать, что лекарственные средства, которые они реализуют, разрешены к
использованию в соответствии с законодательством, все условия хранения всегда
соблюдаются, в том числе во время транспортирования, принимаются меры по
предотвращению загрязнения и перекрестного загрязнения, имеет место адекватная
ротация запаса фармпродукции и продукты хранятся в безопасных и надежных зонах
хранения. Должна быть в наличии система возврата недоброкачественной продукции
и эффективная схема отзыва лекарственных средств.
Правила GDP устанавливают требования по отношению к персоналу, документальному
оформлению (заказов, операций, отчетов), помещениям и оборудованию, поставкам
клиентам, возврату продукции (доброкачественной и бракованной), самоинспекциям
и т.д.
Еще более подробно
условия хранения и транспортировки изложены в стандарте GSP, содержащем
специфические требования, обеспечивающие сохранение исходного высокого качества
фармпродукта на промежуточном этапе от производства до потребителя[14].
В аптечной организации
должна быть сформирована система управления качеством аптечной организации.
Каждая аптечная
организация должна иметь правила
внутреннего трудового распорядка, утвержденные руководителем организации, с
отметкой об ознакомлении сотрудников. Пересмотр правил и повторное ознакомление
с ними сотрудников аптечной организации
производится ежегодно.
Аптечной
организацией должны регулярно
проводиться внутренние проверки на соответствие требованиям ГОСТа.
При проведении
проверок следует обращать внимание на наличие в аптечной организации соответствующих документов на занимаемые
помещения, должностных инструкций сотрудников, стандартов, иных необходимых
документов.
Проверки могут
проводиться как сотрудниками аптечной организации независимыми от лиц,
непосредственно осуществляющих проверяемую деятельность, так и независимыми
экспертами.
Частота проверок
определяется самой аптечной организацией.
Результаты проверок
протоколируются и доводятся до сведения персонала, ответственного за
проверяемый участок работы, и руководства аптечной организации.
При последующих
проверках контролируется выполнение рекомендаций и их эффективность.
Каждый сотрудник
аптечной организации должен быть
ознакомлен с ГОСТом, порядком выполнения закрепленных за ним обязанностей,
нормативными правовыми актами и стандартами, относящимися к деятельности
организации. В аптечных организациях на каждого сотрудника должны быть
должностные инструкции, утвержденные в соответствующем порядке.
В аптечных
организациях должна быть предусмотрена система постоянного повышения
профессионального образования сотрудников по вопросам действующего законодательства,
применения лекарственных средств и др. План и темы занятий утверждаются
руководителем аптечной организации.
Руководитель аптечной
организации назначает из
руководящего персонала
уполномоченного по качеству.
Аптечная
организация обеспечивает ведение
документации в соответствии с законодательными и нормативными правовыми актами
Российской Федерации[15].
Выборочному контролю
качества лекарственных средств подлежат лекарственные средства отечественного и
зарубежного производства, находящиеся в сфере обращения лекарственных средств в
Российской Федерации.
Номенклатура и
периодичность отбора образцов лекарственных средств на выборочный контроль
качества лекарственных средств регламентируется планом выборочного контроля,
который утверждается в установленном порядке и доводится до сведения
предприятий-производителей лекарственных средств в виде планов-заданий.
В течение календарного
года план-задание может корректироваться с учетом изменения номенклатуры
лекарственных средств, находящихся в сфере обращения в Российской Федерации,
или выявленного несоответствия их качества требованиям государственных
стандартов качества лекарственных средств.
Процедура выборочного
контроля качества лекарственных средств включает следующие этапы:
-
принятие Минздравом России решения о проведении
выборочного контроля качества лекарственных средств в соответствии с
утвержденным планом выборочного контроля качества лекарственных средств;
-
отбор образцов лекарственных средств для целей
выборочного контроля качества лекарственных средств;
-
направление на экспертизу качества лекарственных
средств образцов лекарственных средств;
-
проведение экспертизы качества представленных
образцов лекарственных средств;
-
принятие Минздравом России решения по
результатам проведенной экспертизы качества лекарственного средства[16].
Экспертиза качества
лекарственного средства проводится в срок, не превышающий 40 рабочих дней со
дня получения образцов лекарственного средства и комплекта документов, если в
государственном стандарте качества лекарственного средства не предусмотрены
методы контроля качества, требующие более длительных сроков их выполнения.
Территориальные органы
контроля качества, на территории которых находятся в обращении другие партии
некачественной серии лекарственного средства, обязаны принять меры для
проведения проверки качества данного лекарственного средства. Информация о
результатах такой проверки направляется в Минздрав России.
Выборочный контроль
качества сертифицированных лекарственных средств, находящихся в сфере обращения
лекарственных средств на территории Российской Федерации, при поступлении их по
месту назначения осуществляется территориальными органами контроля качества в
рамках инспекционного контроля качества лекарственных средств.
При возникновении
сомнений в достоверности данных, полученных в результате проверки
сопроводительной документации и контроля качества лекарственного средства по
показателям «описание», «упаковка», «маркировка» могут проводиться
дополнительные испытания. Выбор объема проводимых испытаний для выборочной
проверки показателей качества лекарственных средств, позволяющих полно и
достоверно подтвердить соответствие лекарственных средств требованиям,
установленным государственными стандартами качества, в каждом конкретном случае
определяется территориальным органом контроля качества лекарственных средств[17].
Согласно официальной
статистике Минздрава России, после введения обязательной сертификации ЛС
количество контрафактной продукции в розничной аптечной сети значительно
снизилось. Правда, сколько фальсификата находилось там на самом деле, не знал
никто, - в каждую таблетку, как говорится, не заглянешь, - но то, что немалое
количество некачественных лекарств выявлялось, - несомненно. Чрезвычайно важно
и то, что окружные центры сертификации собирали и доводили до аптек ценнейшую
информацию о выявленной контрафактной и некачественной продукции.
Безусловно, введение обязательной сертификации потребовало от
фармпроизводителей определенных материальных затрат - за проведение анализа
продукции и хранение партий препаратов на таможне, пока идет процесс
сертификации[18].
В последние годы объем
государственного контроля лекарственных средств значительно сократился. Попытка
заменить его сертификацией, как выясняется, тоже не самый удачный вариант.
Гарантии в полном объеме по обеспечению качества лекарств могут быть даны
только через выстраивание адекватной сегодняшней ситуации системы
государственного контроля ЛС, как и предписывает Федеральный закон «О
лекарственных средствах».
Заключение
Каждый антибиотик
обладает специфическим избирательным действием на определенные виды микробов.
Благодаря такому избирательному действию многие антибиотики способны подавлять
жизнедеятельность патогенных микроорганизмов в безвредных для организма
концентрациях. Такие антибиотики широко используют для лечения различных
инфекционных болезней. Основное требование, которое предъявляется к
антибиотикам, как и к другим лекарственным средствам – правильное назначение и
применение. Только в этом случае антибиотики будут приносить пользу, а не вред.
За годы, прошедшие
после открытия фармацевтического рынка, в стране зарегистрированы несколько
десятков оригинальных антибиотиков, не считая сотен различных наименований. За
рубежом этот процесс был растянут на десятилетия, поэтому клиницисты имели
возможность разобраться в сильных и слабых сторонах препаратов и найти
оптимальное место для каждого из них в лечебном процессе. Для российских же
врачей все произошло лавинообразно, в слишком короткий промежуток времени.
Естественно, что практическим докторам, которые занимаются своим
непосредственным делом - лечением - разобраться в этом многообразии за
имеющееся время оказалось практически невозможно.
Чтобы оценить
эффективность антибиотика, далеко не обязательно иметь мощную
микробиологическую поддержку. Любой врач знает, что в подавляющем большинстве
случаев при удачном назначении препарата выраженная положительная динамика
наблюдается на 2 - 3 сутки после его назначения. Но из этого вытекает, что если
на третьи сутки положительной динамики нет, то антибиотик необходимо менять.
Потому что он оказался неэффективен[19].
Список
литературы
1. Приказ
Министерства здравоохранения РФ «Об утверждении порядка осуществления
государственного контроля качества лекарственных средств на территории РФ» от 4
апреля 2003 г.
№ 137
2. Отраслевой
стандарт «Правила отпуска (реализации) лекарственных средств в аптечных
организациях. Основные положения» ОСТ 91500.05.0007-2003
3. Балкайс
Я.Я., Фатеев В.А. Взаимодействие лекарственных веществ. – М.: Медицина. – 1991.
– 301с.
4. Белозеров
Е.С. Лекарство-друг, лекарство-враг. – Алма-Ата: Наука, 1996. – 180с.
5. Белозеров
Е.С. Медикаментозные осложнения. – Алма-Ата: Наука, 1989. – 191с.
6. Довжанский
С.И. Клиническая фармакология. – М.: Медицина, 1987. – 286с.
7. Змушко
Е.И., Белозеров Е.С. Лекарственные препараты.- СПб.: Питер, 2000. - 318с.
8. Колипова
Ю. Введение в правила
организации хранения лекарственных средств. // Российские аптеки. – 2004. - №6.
9. Косарев
В.В. Фармакотерапия. – Самара: Медицина.
– 1994. – 180с.
10.
Косарев В.В. Фармацевтическая продукция. – М.:
Медицина. – 1999. – 242с.
11.
Кречикова О.И. Клиническая микробиология и
антимикробная химиотерапия. – 2000. - №1
12.
Крылов Ю.Ф., Смирнов П.А. Мир фармакологии. – М.:
Знание, 1998. – 176с.
13.
Машковский М.Д. Лекарственные средства: В 2 тт. – Т.1. –
М.: Новая волна, 2002. – 430с.
14.
Нифантьев О.Е. Основные принципы инспектирования систем
качества на фармацевтических предприятиях. // Фарматека. – 2004. - №1 (37)
15.
Пухлик Б.М. Антибиотики. – Киев: Здоровье, 1999.- 94с.
16.
Синев Д.Н., Гуревич И.Я. Пособие для фармацевтов аптек.
– М.: Медицина, 1982. – 252с.
17.
Ушкалова Е.А. Современные аспекты антибиотикотерапии.
// Фарматека. – 2004. - №3.
18.
Фармакологический словарь. / Сост. Фадеева П.М. – М.:
Медицина, 2003. – 680с.
19.
Федотова О. Кто поставит заслон фальсификатам. //
Российские аптеки. – 2004. - №9.
[1] Довжанский С.И.
Клиническая фармакология. – М.: Медицина, 1987. – 286с.
[2] Фармакологический словарь.
/ Сост. Фадеева П.М. – М.: Медицина, 2003. – 680с.
[3] Крылов Ю.Ф., Смирнов П.А.
Мир фармакологии. – М.: Знание, 1998. – 176с.
[4] Машковский М.Д.
Лекарственные средства: В 2 тт. – Т.1. – М.: Новая волна, 2002. – 430с.
[5] Белозеров Е.С.
Лекарство-друг, лекарство-враг. – Алма-Ата: Наука, 1996. – 180с.
[6] Косарев В.В. Фармацевтическая
продукция. – М.: Медицина. – 1999. – 242с.
[7] Косарев В.В.
Фармакотерапия. – Самара: Медицина. –
1994. – 180с.
[8] Балкайс Я.Я., Фатеев В.А.
Взаимодействие лекарственных веществ. – М.: Медицина. – 1991. – 301с.
[9] Белозеров Е.С.
Медикаментозные осложнения. – Алма-Ата: Наука, 1989. – 191с.
[10] Синев Д.Н., Гуревич И.Я.
Пособие для фармацевтов аптек. – М.: Медицина, 1982. – 252с.
[11] Пухлик Б.М. Антибиотики.
– Киев: Здоровье, 1999.- 94с.
[12] Кречикова О.И. Клиническая микробиология и
антимикробная химиотерапия. – 2000. - №1
[13] Змушко Е.И., Белозеров Е.С. Лекарственные препараты.-
СПб.: Питер, 2000. - 318с.
[14] Колипова Ю. Введение в правила организации хранения
лекарственных средств. // Российские аптеки. – 2004. - №6.
[15] Отраслевой стандарт «Правила отпуска (реализации)
лекарственных средств в аптечных организациях. Основные положения» ОСТ
91500.05.0007-2003
[16] Нифантьев О.Е. Основные
принципы инспектирования систем качества на фармацевтических предприятиях. //
Фарматека. – 2004. - №1 (37)
[17] Приказ Министерства здравоохранения РФ «Об
утверждении порядка осуществления государственного контроля качества
лекарственных средств на территории РФ» от 4 апреля 2003 г. № 137
[18] Федотова О. Кто поставит
заслон фальсификатам. // Российские аптеки. – 2004. - №9.
[19] Ушкалова Е.А. Современные
аспекты антибиотикотерапии. // Фарматека. – 2004. - №3.