СОДЕРЖАНИЕ
ЗАДАЧА № 704 (вариант 3)............................................................................... 3
Условие............................................................................................................ 3
Решение............................................................................................................ 4
ЗАДАЧА № 733 (вариант 2)............................................................................... 6
Условие............................................................................................................ 6
Решение............................................................................................................ 6
ЗАДАЧА № 753 (вариант 3)............................................................................... 7
Условие............................................................................................................ 7
Решение............................................................................................................ 7
ЗАДАЧА № 757 (вариант 4)............................................................................... 8
Условие............................................................................................................ 8
Решение............................................................................................................ 8
ЗАДАЧА 3 773 (вариант 4)................................................................................ 9
Условие............................................................................................................ 9
Решение............................................................................................................ 9
ЗАДАЧА № 783................................................................................................ 11
Условие.......................................................................................................... 11
Решение.......................................................................................................... 11
ЗАДАЧА № 704 (вариант 3)
Условие
При
нефеломитрическом определении хлорид-иона для построения калибровочного графика
20,0 мл раствора КСl, содержащего 0,5 мг/мл Cl, поместили в мерную колбу
емкостью 100 мл. Затем в мерных колбах на 50 мл, содержащих 8,0; 6,0; 4,0 и 2,0
мл этого раствора, приготовили суспензии AgCl и измерили их кажущиеся
оптические плотности:
VКСl, мл 8,0 6,0
4,0 2,0
Dкаж 0,12
0,22 0,39 0,66
По этим
данным построили калибровочный график.
Анализируемый
раствор 25,0 мл разбавили в мерной колбе емкостью 100 мл. Затем 5,00 мл
раствора поместили в мерную колбу емкостью 50 мл, приготовили в ней суспензию
AgCl и довели водой до метки. Кажущаяся оптическая плотность этого раствора
оказалась 0,15.
Определить
содержание хлорид-иона в анализируемом растворе (мг/л).
Решение
Определяем массу хлорид-иона в растворах, используемых для построения
калибровочного графика. Для этого используемый объем стандартного раствора
умножаем на его плотность – 0,5 мг/л. Полученные данные заносим в таблицу 1.
Таблица 1
|
VКСl, мл
|
8,0
|
6,0
|
4,0
|
2,0
|
|
масса Сl, мг
|
4,0
|
3,0
|
2,0
|
1,0
|
|
Dкаж
|
0,12
|
0,22
|
0,39
|
0,66
|
На основании
полученных данных строим калибровочный график (рис. 1). Который должен иметь
вид прямой, при этом расстояние до точек, находящихся над линией, должно
соответствовать расстоянию до точек, находящихся ниже линии.
По калибровочному графику
определяем, что кажущейся оптической плотности анализируемого раствора (0,15),
взятого для измерения, соответствует масса хлора 3,58 мг.
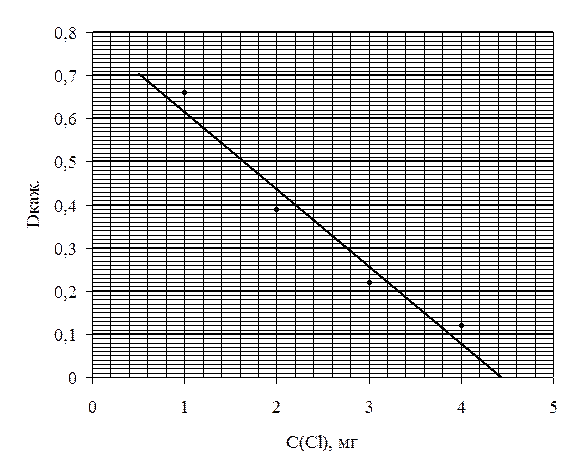 Рис. 1.
Рис. 1.
Для измерения
кажущейся оптической плотности было взято 5 мл исследуемого раствора,
разбавленного в 4 раза по сравнению с исходным 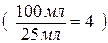 , поэтому и масса хлорид-ионов в нем выше в 4 раза: 3,58 мг×4
= =14,32 мг.
, поэтому и масса хлорид-ионов в нем выше в 4 раза: 3,58 мг×4
= =14,32 мг.
В 25 мл
анализируемого раствора содержится 14,32 мг хлора, а
в 1 мл - х мг.
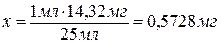
Масса хлора в
1 л анализируемого раствора равна: 1000 мл×0,5728 мг = 572,8
мг.
Ответ:
содержание Сl в
анализируемом растворе равно 572,8мг/л.
ЗАДАЧА № 733 (вариант 2)
Условие
Для
определения концентрации HF используют зависимость удельной электропроводности c от
содержания кислоты в растворе:
СHF, моль/л
0,004 0,007
0,015 0,030 0,060
0,121 0,243
c×104,
Ом-1×см-1 2,5
3,8 5,0 8,0
12,3 21,0 36,3
Построить по
этим данным калибровочный график в координатах lgc-lg СHF и с его
помощью определить концентрацию фтористоводородной кислоты, если ее удельная
электропроводность равна 9,2×104, Ом-1×см-1.
Решение
Рассчитываем
десятичный логарифм исходных данных (табл. 2).
Таблица
2
|
СHF,
моль/л
|
0,004
|
0,007
|
0,015
|
0,030
|
0,060
|
0,121
|
0,243
|
|
lg СHF
|
-2,4
|
-2,16
|
-1,82
|
-1,52
|
-1,22
|
-0,92
|
-0,61
|
|
c×104,
Ом-1×см-1
|
2,5
|
3,8
|
5,0
|
8,0
|
12,3
|
21,0
|
36,3
|
|
lgc
|
0,40
|
0,58
|
0,70
|
0,90
|
1,09
|
1,32
|
1,56
|
Строим градуировочный график
(рис. 2).
Рис. 2.
Удельная
электропроводность исследуемой HF равна 9,2×104, Ом-1×см-1,
логарифм данного значения равен 4,96. По калибровочному графику определяем, что
этому показателю соответствует lg СHF =-1,5. Антилогарифм этого
числа – 0,5.
Ответ:
концентрация фтористоводородной кислоты равна 0,5 моль/л.
ЗАДАЧА № 753 (вариант 3)
Условие
После
соотвествующей обработки соответствующих образцов стали, содержащих хром, сняли
их полярограммы и получили следующие результаты:
Образцы 1 2
3 4
СCr,
% 0,30
0,42 0,96 1,40
h, мм 8,0
10,0 20,0 28,0
Построить
калибровочный график и определить процентное содержание хрома в анализируемом
образце, если при его полярографировании высота волны оказалась 18,0 мм.
Решение
Строим
калибровочный график (рис. 3).
Рис. 3.
Полярограмме,
высотой 18,0 мм, соответствует концентрация Cr 0,85 %.
Ответ:
содержание хрома в исследуемом образце составляет 0,85 %.
ЗАДАЧА № 757 (вариант 4)
Условие
Для
определения содержания кадмия в сплаве методом добавок навеску сплава а 2,5080 г растворили и после
соответствующей обработки объем раствора довели до 250,0 мл. Для снятия
полярограммы взяли 18,0 мл этого раствора. Высота волны оказалась 19,5 мм.
После добавки 4,0 мл 0,043 н. CdSO4 (Vст) высота волны
увеличилась до h¢
26,0 мм. Определить процентное содержание кадмия в сплаве.
Решение
0,043 н. CdSO4
означает, что
в 1 л раствора содержится 0,043 эквивалента CdSO4,
тогда
в 0,004 л раствора
- х.
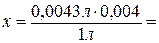 1,72×10-5
1,72×10-5
Рассчитываем массу 1 эквивалента
CdSO4:
Мэкв.(CdSO4)
= Mr(CdSO4)×2
= (Ar(Cd) + Ar(S) + Ar(О)×4)×2 = (112 + 32 + 16×4)×2 = =416 г.
Если масса 1 эквивалента CdSO4 равна 416 г,
то масса 1,72×10-5 эквивалента - х г.
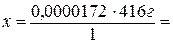 71,552×10-4 г = 7,155 мг.
71,552×10-4 г = 7,155 мг.
Mr(CdSO4)×= Ar(Cd) + Ar(S) + Ar(О)×4 = 112 + 32 + 16×4= =208
Если в 208 мг CdSO4 содержится 112 мг Cd, то
в 7,155
мг - х.
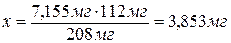
Рассчитываем
высоту волны, приходящуюся на 3,853 мг Cd:
26 мм – 19,5 мм = 6,5 мм.
Волна, высотой 6,5 мм соответствует 3,853 мг Cd, тогда
волна, высотой 19,5 мм - х.
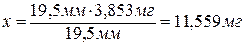
Следовательно,
в 18 мл раствора содержится 11,559 мг Cd, тогда
в 250 мл - х.
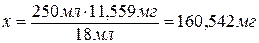
Масса 2508 мг
составляет 100 %, а
масса
160,542 мг - х.
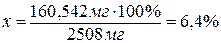
Ответ:
содержание кадмия в сплаве составляет 6,4 %.
ЗАДАЧА 3 773 (вариант 4)
Условие
Для
хроматографического определения никеля на бумаге, пропитанной раствором
диметилглиоксима, приготовили три стандартных раствора. Для этого навеску NiCl2×6Н2О, массой
0,2946 г, растворили в мерной колбе на 50 мл. Затем из этой колбы взяли 5,0;
10,0 и 20,0 мл и разбавили в колбах на 50 мл. Исследуемый раствор также
разбавили в мерной колбе на 50 мл.
Построить
калибровочный график в координатах h-CNi и определить содержание
никеля (мг) в исследуемом растворе, если высота пиков стандартных растворов
равна 30,0; 45,0 и 78,0 мм, а высота исследуемого раствора равна 54,0 мм.
Решение
Определяем
молекулярную массу NiCl2×6Н2О:
М(NiCl2×6Н2О)
= Ar(Ni) + Ar(Cl)×2
+ ((Ar(Н)×2
+ Ar(О))×6) = 59 + 35,5×2 + ((1×2
+ 16)×6) = 238
В 238 мг NiCl2×6Н2О
содержится 59 мг Ni, а
в 294,6 мг
- х.
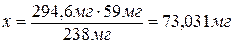
Определяем
содержание Ni в 1 мл
стандартных растворах. Если 73,031 мг Ni содержится в 50 мл раствора, то в 1 мл данного раствора
содержится 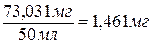 .
.
На
основе этих данных определяем массу никеля в каждом из стандартных растворов
(табл. 3).
Таблица 3
|
Высота
пиков, мм
|
30,0
|
45,0
|
78,0
|
|
Объем
раствора, мл
|
5,0
|
10,0
|
20,0
|
|
Масса
никеля, мг
|
7,305
|
29,22
|
52,596
|
Строим
калибровочный график (рис. 4).
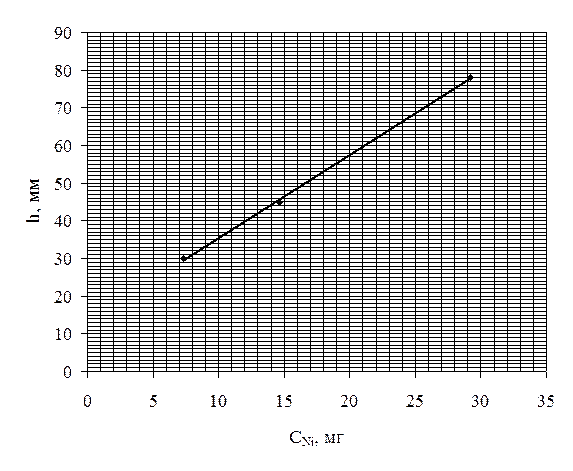 Рис. 4.
Рис. 4.
По
калибровочному графику определяем, что концентрация никеля в исследуемом
растворе равна 18,3 мг.
Ответ:
содержание никеля в исследуемом растворе равно 18,3 мг.
ЗАДАЧА № 783
Условие
При
определении сурьмы в сплаве объемным методом получили следующие данные, %:
11,95; 12,03; 11,98; 12,04. Вычислить стандартное отклонение единичного
определения и доверительный интервал среднего значения (для a =
0,95).
Решение
Рассчитываем
среднее для данного массива значений:
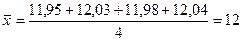 .
.
Стандартное
отклонение – это мера того, насколько широко разбросаны точки данных
относительно их среднего. Оно определяется по формуле:
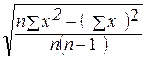
å(х) = 48
åх2 = 11,952+12,032+11,982+12,042
= 576,0054
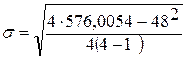 = 0,042
= 0,042
Доверительный
интервал – это интервал с обеих сторон от среднего выборки.
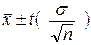 .
.
t – та часть
стандартной нормальной кривой, которая равняется (1 – альфа). Это значение
равно ± 0,063.
Доверительный
интервал равен:
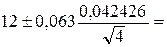 12 ± 0,001317.
12 ± 0,001317.
Ответ:
стандартное отклонение единичного определения равно 0,042; доверительный
интервал среднего значения равен 12 ± 0,001317.