Содержание
2.1.В
чем состоит явление радиоактивности? Каков основной закон радиоактивного
распада? Как был измерен возраст археологических находок, Земли, метеоритов? В
какой элемент превратится 92U238
после трех α-распадов и двух β-распадов?. 4
3.1. Как
соединяются атомы в молекулы? Поясните понятие «валентность» и «химическая
связь». Какова роль энергии и энтропии в образовании молекул? Как связаны
энергетическая прочность химической связи со структурой молекулы? Приведите
примеры изомеров. 5
4.1. Дайте
характеристику жидкого состояния. Определите картину процессов при явлениях
вязкости, капиллярности, смачивании, поверхностном натяжении. Что такое
«тройная точка» воды? Как объясняют ее большую теплоемкость, поверхностное
натяжение и свойство капиллярности? Какое значение имеют эти особенности в
живой природе? Почему морская вода замерзает при более низкой температуре, чем
речная? 9
5.1.
Охарактеризуйте реакции деления ядер. Приведите примеры таких реакций и укажите
их роль в изучении вещества. Что такое «дефект массы»? как удалось сделать
управляемой цепную реакцию деления тяжелых ядер? Укажите проблемы энергетики,
связанные с такими реакциями. 12
6.1.
Назовите современные космологические модели Вселенной. Почему в результате
первичного нуклеосинтеза не могли образоваться химические элементы,
существующие сейчас во Вселенной?. 17
7.1.
Клетка как элементарная единица жизни. Опишите строение, состав, типы живых
клеток. Что такое «межклеточные структуры»? Является ли одноклеточность
признаком прокариот? Каково значение неорганических компонентов клетки в
обеспечении процессов ее жизнедеятельности?. 20
9.1.
Прокомментируйте высказывание Гельмгольца: «Электрон – есть нечто, обозначаемое
буквой е». Какими свойствами обладает электрон в разных экспериментах?
Определите длину волны электромагнитного излучения, энергия кванта которого
равна энергии покоя электрона. Масса покоя электрона равна 9,1*10-31 кг. 25
10.1.
Охарактеризуйте распространенность химических элементов на Земле и ее биосфере.
В чем принципиальное единство химического состава живых организмов и неживой
природы?. 26
Список
литературы.. 28
2.1.В чем состоит явление радиоактивности? Каков
основной закон радиоактивного распада? Как был измерен возраст археологических
находок, Земли, метеоритов? В какой элемент превратится 92U238 после трех
α-распадов и двух β-распадов?
Явление радиоактивности было открыто в 1896 году французским
ученым Анри Беккерелем. В настоящее время оно широко используется в науке,
технике, медицине, промышленности. Радиоактивные элементы естественного
происхождения присутствуют повсюду в окружающей человека среде. В больших
объемах образуются искусственные радионуклиды, главным образом в качестве
побочного продукта на предприятиях оборонной промышленности и атомной
энергетики. Попадая в окружающую среду, они оказывают воздействия на живые
организмы, в чем и заключается их опасность. Для правильной оценки этой
опасности необходимо четкое представление о масштабах загрязнения окружающей
среды, о выгодах, которые приносят производства, основным или побочным
продуктом которых являются радионуклиды, и потерях, связанных с отказом от этих
производств, о реальных механизмах действия радиации, последствиях и существующих
мерах защиты. Радиоактивность - неустойчивость ядер некоторых атомов,
проявляющаяся в их способности к самопроизвольным превращениям (распаду),
сопровождающимся испусканием ионизирующего излучения или радиацией.
Радиация, или ионизирующее излучение - это частицы и
гамма-кванты, энергия которых достаточно велика, чтобы при воздействии на
вещество создавать ионы разных знаков. Радиацию нельзя вызвать с помощью
химических реакций
Возраст археологических находок, Земли, метеоритов был
определен с помощью радиоактивного облучения.
Он превратиться в радон-222
3.1. Как соединяются атомы в молекулы? Поясните понятие «валентность» и
«химическая связь». Какова роль энергии и энтропии в образовании молекул? Как
связаны энергетическая прочность химической связи со структурой молекулы?
Приведите примеры изомеров.
В середине XIX века атомно-молекулярное учение завоевало
полное признание. На международном съезде химиков в г. Карлсруэ в 1860 г. были
приняты чёткие определения понятий атома и молекулы.
Молекула — наименьшая частица вещества, способная к
самостоятельному существованию и обладающая химическими свойствами данного
вещества.
Такие физические свойства, как температура плавления и
кипения, механическая прочность и твёрдость, зависит от прочности связи между
молекулами в данном веществе, поэтому для отдельной молекулы они не имеют
смысла. Такие величины, как плотность существуют как для молекулы в целом, так
и для вещества. Плотность молекулы всегда значительно больше, чем для твёрдого
вещества, так как в каждом веществе при любом агрегатном состоянии между
молекулами всегда есть свободное пространство.. Электропроводность,
теплоёмкость определяются структурой вещества в целом, а не свойствами
отдельных молекул. Это подтверждается резким изменением электропроводности при
переходе от одного агрегатного состояния вещества в другое. Изменение этих
свойств не являются изменением состава молекул, которые при плавлении или
кипении вещества, как правило, не претерпевают существенных превращений.
Атом — наименьшая частица химического элемента, входящая в
состав молекул и сохраняющая химические свойства данного элемента.
Молекулы могут содержать различное число атомов. Так,
молекулы благородных газов одноатомны, простых газов — двухатомны. воды —
трёхатомны и т. д., а молекулы белков построены из сотен тысяч атомов.
В атоме водорода на электрон действует только сила
притяжения положительно заряженного ядра. В многоэлектронном атоме к этому
взаимодействию прибавляется взаимное отталкивание электронов. Электроны
внутренних слоёв атома ослабляют притяжение внешнего электрона ядром, как бы
экранируют внешний электрон от ядра.
При этом экранирование оказывается различным для электронов
с неодинаковой формой электронного облака. Поэтому в многоэлектронных атомах
энергия электрона зависит не только от главного квантового числа n, но и от
орбитального квантового числа l, определяющего форму электронного облака.
Самой низкой энергией обладают электроны s-орбитали,
составляющие первый электронный слой. Энергия электронов второго слоя намного
больше энергии электронов первого; между энергиями 2s- и 2p-электронов,
составляющих второй электронный слой, есть небольшое различие. Энергетические
уровни всех орбиталей третьего электронного уровня ещё выше. Однако при
переходе к четвёртому электронному слою и далее это правило нарушается:
отдельные орбитали следующего слоя обладают меньшей энергией, чем наиболее
высокие орбитали предыдущего слоя. Например, 4s-орбиталь имеет меньшую энергию,
чем 3d-орбиталь предыдущего слоя. В общем случае энергия электронов
(n–1)d-орбитали всегда больше энергии электронов ns-орбитали и меньше энергии
электронов np-орбитали. Энергия 4f-электронов оказывается выше энергии 5s-, 5p-
и 6s-электронов.
При заполнении электронных слоёв атома в стационарном
(невозбуждённом) состоянии выдерживается принцип наименьшей энергии электрона,
в соответствии с которым
наиболее устойчивому состоянию электрона в атоме отвечает
минимальная из возможных энергия этого электрона.
Поэтому заполнение электронных слоёв начинается с уровней,
характеризующихся самой низкой энергией.
Русский учёный В. М. Клечковский установил, что энергия
электрона возрастает по мере увеличения суммы главного и орбитального квантовых
чисел (n + l). В соответствии с правилом Клечковского
заполнение электронных слоёв происходит в порядке увеличения
сумм главного и орбитального квантовых чисел (n + l).
Так, сумма (n + l) для электронов 3d-орбитали равна 5 (3 +
2), для электронов 4s-орбитали — 4 (4 + 0). Поэтому вначале электронами
заполняется 4s-орбиталь, а затем 3d-орбиталь. Сумма (n + l) для электронов
4f-орбитали равна 7 (4 + 3), что также больше суммы (n + l) для электронов 5s-,
5p- и 6s-орбиталей. Если для двух орбиталей суммы (n + l) имеют одинаковые
значения, то вначале электронами заполняется орбиталь с меньшим значением
главного квантового числа. Например, для электронов 3d- и 4p-орбиталей сумма n
+ l = 5 (соответственно 3 + 2 и 4 + 1). Но так как для электронов 3d-орбитали
главное квантовое число n = 3, а для электронов 4p-орбитали n = 4, в первую
очередь заполняются 3d-орбитали. Лишь после того как заполнены орбитали меньших
энергий, начинается заполнение орбиталей бóльших энергий.[1]
При заполнении электронных слоёв кроме принципа наименьшей
энергии выполняется принцип (запрет) Паули, согласно которому
в атоме не может быть двух электронов с одинаковым значением
всех квантовых чисел.
Из этого следует, что на каждой орбитали, характеризующейся
определёнными значениями главного n, орбитального l и магнитного ms квантовых
чисел, может находиться не более двух электронов, спины которых имеют
противоположные знаки. Два электрона, находящиеся на одной орбитали (и
характеризующиеся противоположно направленными спинами), называются спаренными.
Спины одного направления называют параллельными, а противоположно направленные
— антипараллельными.
Принцип Паули позволяет рассчитать максимальное число
электронов на каждом энергетическом уровне и подуровне в атоме. Максимальное
число электронов на подуровне с орбитальным квантовым числом l равно 2(2l + 1).
При l = 0 (s-подуровень) магнитное квантовое число тоже равно нулю.
Следовательно, на s-подуровне имеется всего одна орбиталь, и максимальное число
электронов на s-подуровне каждого электронного слоя равно двум. При l = 1
(p-подуровень) магнитное квантовое число ms может принимать три значения. На
трёх p-орбиталях может находиться не более шести электронов. При l = 2
(d-подуровень) магнитное квантовое число может принимать пять значений и,
следовательно, на пяти d-орбиталях может находиться до 10 электронов. Итак, на
одной s-орбитали может находиться не более 2, на трёх p-орбиталях — не более 6,
на пяти d-орбиталях — не более 10, на семи f-орбиталях — не более 14
электронов.
Строение каждого электронного слоя зависит от значения
главного квантового числа. Так, K-слой (n = 1) состоит лишь из одной
s-орбитали; L-слой (n = 2) содержит одну 2s-орбиталь и три 2p-орбитали; M-слой
(n = 3) состоит из одной 3s-орбитали, трёх 3p-орбиталей и пяти 3d-орбиталей и
т. д. Электронная ёмкость слоя, определяемая максимальным количеством
электронов N в данном электронном слое, описывается формулой:
N = 2n2,
где n — главное квантовое число. Рассчитанное по этой
формуле максимальное количество электронов в каждом слое оказывается равным:
для K-слоя — 2, для L-слоя — 8, для M-слоя — 18, для N-слоя — 32 электронам.
 СН3 – СН – СН2 –
СН2 – СН3 СН3
– СН – СН2 – СН3
СН3 – СН – СН2 –
СН2 – СН3 СН3
– СН – СН2 – СН3
 СН3 СН2
СН3 СН2
Диметилпентан СН3
Триметилпентан
4.1. Дайте характеристику жидкого состояния. Определите картину
процессов при явлениях вязкости, капиллярности, смачивании, поверхностном
натяжении. Что такое «тройная точка» воды? Как объясняют ее большую
теплоемкость, поверхностное натяжение и свойство капиллярности? Какое значение
имеют эти особенности в живой природе? Почему морская вода замерзает при более
низкой температуре, чем речная?
Жидкости по своим свойствам занимают промежуточное положение
между газами и твердыми веществами. Чем выше температура, тем больше свойства
жидкостей приближаются к свойствам газов, и, наоборот, чем ниже температура,
тем больше проявляются те свойства жидкостей, которые приближают их к твердым
веществам. Жидкости обычно не имеют собственной формы, а приобретают форму
сосуда, в котором находятся; только в очень небольших количествах они способны
сохранять форму капли. В отличие от газов жидкости при данной температуре
занимают совершенно определенный объем. Это объясняется наличием заметных сил
взаимного притяжения отдельных молекул жидкости. Молекулы в жидкостях
размещаются значительно плотнее, чем в газах; этим и объясняется очень малая
сжимаемость всех жидкостей. Рентгенографическое исследование жидкостей
показало, что они имеют зачатки кристаллического строения.[2]
Чистая вода
представляет собой бесцветную прозрачную жидкость. Плотность воды при переходе
ее из твердого состояния в жидкое не уменьшается, как почти у всех других
веществ, а возрастает. При нагревании воды от 0 до 4°С плотность ее также
увеличивается. При 4°С вода имеет максимальную плотность, и лишь при дальнейшем
нагревании ее плотность уменьшается. Если бы при понижении температуры и при
переходе из жидкого состояния в твердое плотность воды изменялась так же, как
это происходит у подавляющего большинства веществ, то при приближении зимы
поверхностные слои природных вод охлаждались. бы до 0°С и опускались на дно,
освобождая место более теплым слоям, и так продолжалось бы до тех пор, пока вся
масса водоема не приобрела бы температуру 0°С. Далее вода начинала бы
замерзать, образующиеся льдины погружались бы на дно и водоем промерзал бы на
всю его глубину. При этом многие формы жизни в воде были бы невозможны. Но так
как наибольшей плотность вода достигает при 4 °С, то перемещение ее слоев,
вызываемое охлаждением, заканчивается при достижении этой температуры. При
дальнейшем понижении температуры охлажденный слой, обладающий меньшей
плотностью, остается на поверхности, замерзает и тем самым защищает лежащие
ниже слои от дальнейшего охлаждения и замерзания. Большое значение в жизни
природы имеет и тот факт, что вода. обладает аномально высокой теплоемкостью
[4,18 Дж/(г К) ], Поэтому. в ночное
время, а также при переходе от лета к зиме вода остывает медленно, а днем или
при переходе от зимы к лету так же медленно нагревается, являясь, таким
образом, регулятором температуры на земном шаре. В связи с тем, что при
плавлении льда объем, занимаемый водой, уменьшается, давление понижает
температуру плавления льда. Эта вытекает из принципа Ле Шателье. Действительно,
пусть. лед и жидкая вода находятся в равновесии при О°С. При увеличении
давления равновесие, согласно принципу Ле Шателье, сместится в сторону
образования той фазы, которая при той же температуре занимает меньший объем.
Этой фазой является в данном случае жидкость. Таким образом, возрастание
давления при О°С вызывает превращение льда в жидкость, а это и означает, что
температура плавления льда снижается. Молекула воды имеет угловое строение;
входящие в ее состав ядра образуют равнобедренный треугольник, в основании
которого находятся два протона, а в вершине — ядро атома кислорода, Межъядерные
расстояния О—Н близки к 0,1 нм, расстояние между ядрами атомов водорода равно
примерно 0,15 нм. Из восьми электронов, составляющих внешний электронный слой
атома кислорода в молекуле воды 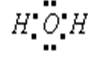 две электронные пары образуют ковалентные связи
О—Н, а остальные четыре электрона представляют собой две неподеленных
электронных пары. Атом кислорода в молекуле воды находится в состоянии sp3-гибридизации. Поэтому валентный угол НОН (104,3°)
близок к тетраэдрическому (109,5°).
две электронные пары образуют ковалентные связи
О—Н, а остальные четыре электрона представляют собой две неподеленных
электронных пары. Атом кислорода в молекуле воды находится в состоянии sp3-гибридизации. Поэтому валентный угол НОН (104,3°)
близок к тетраэдрическому (109,5°).
Морская вода замерзает при более низких температурах из-за
того, что в ее состав входят соли. На рисунке 1 приведена в схематической форме
(без строгого соблюдения масштаба) диаграмма состояния воды. Любой точке на
диаграмме отвечают определенные значения температуры и давления.
Диаграмма показывает те состояния воды, которые
термодинамически устойчивы при определенных значениях температуры и давления.
Она состоит из трех кривых, разграничивающих все возможные температуры и
давления на три области, отвечающие льду, жидкости и пару.
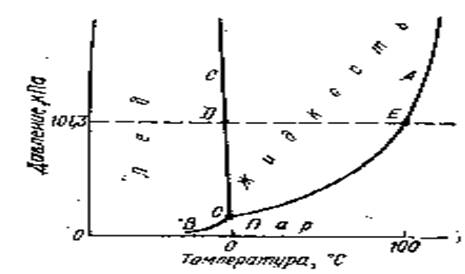
Рис.1
Все три кривые пересекаются в точке О. Координаты этой точки
— это единственная пара значений температуры и давления, при которых в
равновесии могут находиться все три фазы: лед, жидкая вода и пар. Она носит
название тройной точки.
5.1. Охарактеризуйте реакции деления ядер. Приведите примеры таких
реакций и укажите их роль в изучении вещества. Что такое «дефект массы»? как
удалось сделать управляемой цепную реакцию деления тяжелых ядер? Укажите
проблемы энергетики, связанные с такими реакциями.
Ядерные реакции подчиняются законам квантовой механики,
поэтому можно говорить лишь о вероятности протекания той или иной из них. Мерой
вероятности данного типа реакции является эффективное (микроскопическое)
сечение. Рассмотрим коротко два важных типа ядерных реакций - захвата
(поглощения) и рассеяния, а затем перейдем к подробному описанию третьего -
реакции деления ядер, которая необходима для поддержания цепной реакции.
Существует два типа реакций рассеяния: упругое
взаимодействие, при котором суммарная кинетическая энергия взаимодействующих
нейтрона и ядра не меняется после реакции и неупругое взаимодействие, при
котором часть кинетической энергии идет на возбуждение конечного ядра и затем
испускается в виде g -кванта. Нужно отметить, что реакция неупругого рассеяния
происходит лишь при определенных значениях энергии нейтрона (E пор » 0,1 МэВ),
в то время как энергия упругого рассеяния возможна всегда.
Значение реакции рассеяния в ядерной энергетике трудно
переоценить, поскольку именно на ней основаны системы замедления нейтронов в
реакторе. В качестве веществ-замедлителей обычно используют тяжелую и легкую
воду, графит.
Реакция поглощения
(захвата)
Данная реакция играет важную роль в физике реактора,
поскольку она является конкурирующей по отношению к реакции деления. В
результате нейтрон выбывает из цепной реакции. s c зависит от энергии нейтрона
и от массового числа A. В области тепловых нейтронов сечение подчиняется закону
s c (E) обратно пропорционально скорости нейтрона v (или квадратному корню из
E). При увеличении энергии нейтрона начинается резонансная область, в которой s
c имеет множество максимумов и минимумов.
Явление деления тяжелых атомных ядер на два осколка было
открыто Ганом и Штрассманом в 1939 г. При изучении взаимодействия нейтронов
различных энергий и ядер урана. Несколько позже, в 1940 г. Советские физики
К.А.Петржак и Г.И. Флеров обнаружили самопроизвольное (спонтанное) деление ядер
урана. При спонтанном деление и делении, вызванном нейронами, как правило,
образуется асимметричные осколки, отношение масс которых примерно равно 3:2.
При реакции деления выделяется очень большая энергия.
Энергия деления высвобождается в виде кинетической энергии ядер-осколков,
кинетической энергии испускаемых ядрами-осколками электронов, гамма-квантов,
нейтрино, нейтронов.
Основная часть энергии деления приходится на энергию
ядер-осколков, поскольку под действием кулоновских сил отталкивания они
приобретают большую кинетическую энергию. Основная часть энергии деления
выделяется в виде кинетической энергии ядер-осколков.[3]
Замечательным и чрезвычайно важным свойством реакции деления
является то, что в результате деления образуется несколько нейтронов. Это
обстоятельство позволяет создать условия для поддержания стационарной или
развивающейся во времени цепной реакции деления ядер. Действительно, если в
среде, содержащей делящиеся ядра, один нейтрон вызывают реакцию деления, то
образующиеся в результате реакции нейтроны могут с определенной вероятностью
вызвать деление ядер, что может привести при соответствующих условиях к
развитию неконтролируемого процесса деления. Число вторичных нейтронов не
постоянно для всех тяжелых ядер и зависит как от энергии вызвавшего деление
нейтрона, так и от свойств ядра-мишени. Среди нейтронов деления кроме так
называемых мгновенных нейтронов, испускаемых за 10 -15 с после процесса
деления, есть также и запаздывающие нейтроны. Они испускаются в течении
нескольких минут с постепенно убывающей интенсивность. Мгновенные нейтроны
составляют более 99% полного числа нейтронов деления, а их энергия заключена в
широком диапазоне: от тепловой энергии и до энергии приблизительно равной 10
МэВ.
Запаздывающие нейтроны испускаются возбужденными ядрами
образующихся после бета-распада продуктов деления - ядер-предшественников.
Поскольку испускание нуклонов возбужденным ядром происходит мгновенно, то во
время испускания запаздывающего нейтрона после акта деления будет определяться
постоянной распада ядра-предшественника.
В результате деления тяжелых ядер образуются, как правило,
два ядра-осколка с различной массой. В среднем отношение масс легких и тяжелых
осколков равно 2:3. Как правило, ядра-осколки имеют большой избыток нейтронов и
поэтому неустойчивы относительно бета-распада. Массовые числа А продуктов
деления меняются от 72 до 161, а атомные номера от 30 до 65. Вероятность
симметричного деления на два осколка с приблизительно равными массами
составляет всего 0,04%. Доля симметричного деления возрастает по мере
увеличения энергии первичного нейтрона, вызывающего деление атомного ядра.
При делении тяжелых ядер образуется несколько свободных
нейтронов. Это позволяет организовать так называемую цепную реакцию деления,
когда нейтроны, распространяясь в среде, содержащей тяжелые элементы, могут
вызвать их деление с испусканием новых свободных нейтронов. Если среда такова,
что число вновь рождающихся нейтронов увеличивается, то процесс деления
лавинообразно нарастает. В случае, когда число нейтронов при последующих
делениях уменьшается, цепная ядерная реакция затухает.
Для получения стационарной цепной ядерной реакции, очевидно,
необходимо создать такие условия, чтобы каждое ядро, поглотившее нейтрон, при
делении выделяло в среднем один нейтрон, идущий на деление второго тяжелого
ядра. Ядерным реактором называется устройство, в котором осуществляется и
поддерживается управляемая цепная реакция деления некоторых тяжелых ядер.[4]
Цепная ядерная реакция в реакторе может осуществляться
только при определенном количестве делящихся ядер, которые могут делиться при
любой энергии нейтронов. Из делящихся материалов важнейшим является изотоп 235
U , доля которого в естественном уране составляет всего 0,714 %.
Хотя U 238и
делится нейтронами, энергия которых превышает 1,2 МэВ, однако
самоподдерживающаяся цепная реакция на быстрых нейтронах в естественном уране
не возможна из-за высокой вероятности неупругого взаимодействия ядер U 238с быстрыми нейтронами. При
этом энергия нейтронов становится ниже пороговой энергии деления ядер 238 U.
Использование замедлителя приводит к уменьшению резонансного
поглощения в U 238, так как
нейтрон может пройти область резонансных энергий в результате столкновения с
ядрами замедлителя и поглотиться ядрами
U235, Pu239, U233, сечение деления
которых существенно увеличивается с уменьшением энергии нейтронов. В качестве
замедлителей используют материалы с малым массовым числом и небольшим сечением
поглощения ( вода, графит, бериллий и др.).
Для характеристики цепной реакции деления используется
величина, называемая коэффициентом размножения К . Это отношение числа
нейтронов определенного поколения к числу нейтронов предыдущего поколения. Для
стационарной цепной реакции деления К =1. Размножающаяся система (реактор), в
которой К =1, называется критической. Если К >1, число нейтронов в системе
увеличивается и она в этом случае называется надкритической. При К < 1
происходит уменьшение числа нейтронов и система называется подкритической. В
стационарном состоянии реактора число вновь образующихся нейтронов равно числу
нейтронов, покидающих реактор (нейтроны утечки) и поглощающихся в его пределах.
В критическом реакторе присутствуют нейтроны всех энергий. Они образуют так
называемый энергетический спектр нейтронов, который характеризует число
нейтронов различных энергий в единице объема в любой точке реактора. Средняя
энергия спектра нейтронов определяется долей замедлителя, делящихся ядер и
других материалов, которые входят в состав активной зоны реактора. Если большая
часть делений происходит при поглощении тепловых нейтронов, то такой реактор
называется реактором на тепловых нейтронах. Энергия нейтронов в такой системе
не превышает 0.2 эВ. Если большая часть делений в реакторе происходит при
поглощении быстрых нейтронов, такой реактор называется реактором на быстрых
нейтронах.
В активной зоне реактора на тепловых нейтронах наряду с
ядерным топливом находится значительная масса замедлителя-вещества,
отличающегося большим сечением рассеяния и малым сечением поглощения. Активная
зона реактора практически всегда, за исключением специальных реакторов,
окружена отражателем, возвращающим часть нейронов в активную зону за счет
многократного рассеяния. В реакторах на быстрых нейронах активная зона окружена
зонами воспроизводства. В них происходит накопление делящихся изотопов. Кроме
того, зоны воспроизводства выполняют и функции отражателя. В ядерном реакторе
происходит накопления продуктов деления, которые называются шлаками. Наличие
шлаков приводит к дополнительным потерям свободных нейтронов. Ядерные реакторы
в зависимости от взаимного размещения горючего и замедлителя подразделяются на
гомогенные и гетерогенные. В гомогенном реакторе активная зона представляет
собой однородную массу топлива, замедлителя и теплоносителя в виде раствора,
смеси или расплава. Гетерогенным называется реактор, в котором топливо в виде
блоков или тепловыделяющих сборок размещено в замедлителе, образуя в нем
правильную геометрическую решетку.[5]
6.1. Назовите современные космологические модели Вселенной. Почему в
результате первичного нуклеосинтеза не могли образоваться химические элементы,
существующие сейчас во Вселенной?
Древнегреческим философам принадлежит ряд гениальных догадок
об устройстве Вселенной. Анаксимандр высказал идею изолированности Земли, в
пространстве. Эйлалай первым описал пифагорейскую систему мира, где Земля как и
Солнце обращались вокруг некоего “гигантского огня” . Шарообразность Земли
утверждал другой пифагореец Парменид (VI-V в. в. до н.э.) Гераклит Понтийский
(V-IV в до н.э.) утверждал так же ее вращение вокруг своей оси и донес до
греков еще более древнюю идею египтян о том, что само солнце может служить
центром вращение некоторых планет (Венера, Меркурий) .
Французский философ и ученый, физик, математик, физиолог
Рене Декарт (1596-1650) создал теорию о эволюционной вихревой модели Вселенной
на основе гелиоцентрализма. В своей модели он рассматривал небесные тела и их
системы в их развитии. Для XVII в. в. его идея была необыкновенно смелой. По
Декарту, все небесные тела образовывались в результате вихревых движений,
происходивших в однородной в начале, мировой материи. Совершенно одинаковые
материальные частицы, находясь в непрерывном движении и взаимодействии, меняли
свою форму и размеры, что привело к наблюдаемому нами богатому разнообразию природы.
Солнечная система согласно Декарту, представляет собой один
из таких вихрей мировой материи. Планеты не имеют собственного движения – они
движутся, увлекаемые мировым вихрем. Декарт внес и новую идею для объяснения
тяжести: он считал, что в вихрях, возникающих вокруг планет частицы давят друг
на друга и тем вызывают явление тяжести (например на Земле). Таким образом
Декарт, первым стал рассматривать тяжесть не как врожденное, а как производное
качество тел.
Великий немецкий ученый, философ Иммануил Кант (1724-1804)
создал первую универсальную концепцию эволюционирующей Вселенной, обогатив
картину ее ровной структуры и представлял Вселенную бесконечной в особом
смысле. Он обосновал возможности и значительную вероятность возникновение такой
Вселенной исключительно под действием механических сил притяжения и
отталкивания и попытался выяснить дальнейшую судьбу этой Вселенной на всех ее
масштабных уровнях – начиная с планетной системных и кончая миром туманности.
Эйнштейн совершил радикальную научную революцию, введя свою
теорию относительности. Это было сравнительно просто, как и всё гениальное. Ему
не пришлось предварительно открыть новые явления, установить количественные
закономерности. Он лишь дал принципиально новое объяснение. Эйнштейн раскрыл
более глубокий смысл установленных зависимостей, эффектов уже связанных в некую
физико-математическую систему (в виде постулатов Пуанкаре). Заменив в данном
случае теорию абсолютности пространства и времени идей их относительности
“Пуанкаре” , которую теперь уже не связывали с идеей абсолютного в
пространстве, абсолютной системы отсчета. Такой переворот снимал основное
противоречие, создававшее кризисную ситуацию, в теоретическом осмыслении
действия. Более того, открылся путь для дальнейшего проникновения в свойства и
законы окружающего мира, настолько глубоко, что сам Эйнштейн не сразу осознал
степень революционности своей идеи. В статье от 30.06.1905 г., заложившей
основы специальной теории относительности Эйнштейн, обобщая принципы
относительности Галилея, провозгласил равноправие всех инерциальных систем
отсчета не только в механических, но также электромагнитных явлений.
Специальная или частная теория относительности Эйнштейна
явилась результатом обобщения механики Галилея и электродинамики Максвелла
Лоренца. Она описывает законы всех физических процессов при скоростях движения
близких к скорости света. Впервые принципиально новые космогологические
следствия общей теории относительности раскрыл выдающийся советский математик и
физик – теоретик Александр Фридман (1888-1925 гг.). Выступив в 1922-24 гг. он
раскритиковал выводы Эйнштейна о том, что Вселенная конечна и имеет форму
четырехмерного цилиндра. Эйнштейн сделал свой вывод исходя из предположения о
стационарности Вселенной, но Фридман показал необоснованность его исходного
постулата.
Фридман привел две модели Вселенной. Вскоре эти модели нашли
удивительно точное подтверждение в непосредственных наблюдениях движений
далёких галактик в эффекте “красного смещения” в их спектрах.
Этим Фридман доказал, что вещество во Вселенной не может
находится в покое. Своими выводами Фридман теоретически способствовал открытию
необходимости глобальной эволюции Вселенной. Существует несколько теории
эволюции: Теория пульсирующей Вселенной утверждает, что наш мир произошел в
результате гигантского взрыва. Но расширение вселенной не будет продолжаться
вечно, т.к. его остановит гравитация. По этой теории наша Вселенная расширяется
в течении 18 млрд. лет со времени взрыва. В будущем расширение полностью
замедлится и произойдет остановка, а затем она начнёт сжиматься до тех пор,
пока вещество опять не сожмется и произойдет новый взрыв. Теория стационарного
взрыва: согласно ей Вселенная не имеет ни начала, ни конца. Она все время
прибывает в одном и том же состоянии. Постоянно идет образование нового
водоворота, чтобы возместить вещество удаляющимися галактиками. Вот по этой
причине Вселенная всегда одинакова, но если Вселенная, начало которой положил
взрыв будет расширяться до бесконечности, то она постепенно охладится и совсем
угаснет.
Но пока ни одна из этих теорий не доказана, т.к. на данный
момент не существует ни каких точных доказательств хотя бы одной из них.
Открытие многообразных процессов эволюции в различных
системах и телах, составляющих Вселенную, позволило изучить закономерности
космической эволюции на основе наблюдательных данных и теоретических расчетов.
7.1. Клетка как элементарная единица жизни. Опишите строение, состав,
типы живых клеток. Что такое «межклеточные структуры»? Является ли
одноклеточность признаком прокариот? Каково значение неорганических компонентов
клетки в обеспечении процессов ее жизнедеятельности?
Все живые организмы состоят из клеток. Клетка - элементарная
единица строения, функционирования и развития живых организмов. Существуют
неклеточные формы жизни - вирусы, однако они проявляют свои свойства только в
клетках живых организмов. Клеточные формы делятся на прокариот и эукариот.
Открытие клетки принадлежит английскому ученому Р. Гуку,
который, просматривая под микроскопом тонкий срез пробки, увидел структуры,
похожие на пчелиные соты, и назвал их клетками. Позже одноклеточные организмы
исследовал голландский ученый Антони ван Левенгук. Клеточную теорию
сформулировали немецкие ученые М. Шлейден и Т. Шванн в 1839 г. Современная
клеточная теория существенно дополнена Р. Биржевым и др.
Типичная растительная клетка содержит хлоропласты и вакуоли
и окружена целлюлозной клеточной стенкой.
Плазматическая мембрана (плазмалемма), окружающая
растительную клетку, состоит из двух слоев липидов и встроенных в них молекул
белков. Молекулы липидов имеют полярные гидрофильные «головки» и неполярные
гидрофобные «хвосты». Такое строение обеспечивает избирательное проникновение
веществ в клетку и из нее.
Клеточная стенка состоит Из целлюлозы, ее молекулы собраны в
пучки микрофибрилл, которые скручены в макро-фибриллы. Прочная клеточная стенка
позволяет поддерживать внутреннее давление - тургор.
Цитоплазма состоит из воды с растворенными в ней веществами
и органоидов. Хлоропласты - это органеллы, в которых происходит фотосинтез;
различают зеленые хлоропласты, содержащие хлорофилл, хромопласты, содержащие
желтые и оранжевые пигменты, а также лейкопласты - бесцветные пластиды.
Для растительных клеток характерно наличие вакуоли с
клеточным соком, в котором растворены соли, сахара, органические кислоты.
Вакуоль регулирует тургор клетки. Аппарат Гольджи - это комплекс плоских полых
цистерн и пузырьков, где синтезируются полисахариды, входящие в состав
клеточной стенки. Митохондрии - двухмембранные тельца, на складках их
внутренней мембраны - кристах - происходит окисление органических веществ, а
освободившаяся энергия используется для синтеза АТФ. Гладкий эндоплазматический
ретикулум - место синтеза липидов. Шероховатый эндоплазматический ретикулум
связан с рибосомами, осуществляет синтез белков. Лизосомы- мембранные тельца,
содержащие ферменты внутриклеточного пищеварения. Переваривают вещества,
избыточные органеллы (аутофагия) или целые клетки (аутолиз). Ядро - окружено
ядерной оболочкой и содержит наследственный материал - ДНК со связанными с ней
белками - гистонами (хроматин). Ядро контролирует жизнедеятельность клетки.
Ядрышко - место синтеза молекул т-РНК, р-РНК и рибосомных субъединиц. Хроматин
содержит кодированную информацию для синтеза белка в клетке. Во время деления
наследственный материал представлен хромосомами. Плазмодесмы (поры) -
мельчайшие цитоплазматические каналы, пронизывающие клеточные стенки и
объединяющие соседние клетки.
Микротрубочки состоят из белка тубулина и расположены около
плазматической мембраны. Они участвуют в перемещении органелл в цитоплазме, во
время деления клетки формируют веретено деления. Клетка - самая мелкая единица
организма, граница его делимости, наделенная жизнью и всеми основными
признаками организма. Как элементарная живая система, она лежит в основе
строения и развития всех живых организмов. На уровне клетки проявляются такие
свойства жизни, как способность к обмену веществ и энергии, авторегуляция,
размножение, рост и развитие, раздражимость. Клетка состоит из тех же
химических элементов, что и неживая природа: в ней присутствует большинство
элементов периодической системы Менделеева. В клетках живых организмов особенно
велико содержание четырех элементов - кислорода (О), углерода (С), водорода
(Н), азота (N), называемых макроэлементами. В сумме они составляют около 98%
всего содержимого клетки. Вместе с серой и фосфором эти элементы входят в
состав биополимеров -белков, жиров, углеводов и нуклеиновых кислот.
Микроэлементы: сера (S), фосфор (Р), калий (К), натрий (Ма),
кальций (Са), магний (Мд), железо (Fe), хлор (CI), в сумме составляют около
1,9% содержимого клетки. Ультрамикроэлементы: цинк (Zn), медь (Си), иод (J),
фтор (F) и др., составляют менее 0,1% содержимого клетки. Все элементы играют в
клетке важную роль и необходимы в строго определенном количестве, их недостаток
или избыток приводит к различным нарушениям обмена в организме.
Белки - это макромолекулы, или биополимеры. Мономерами
белков живых клеток являются 20 разных аминокислот. Между карбоксильной группой
СООН (кислая) и аминной группой Н - N - Н (основная) двух соседних аминокислот
формируется пептидная (ковалентная) связь. Различные комбинации аминокислот в
белковых молекулах придают белкам специфичность. Последовательное соединение
аминокислот в белке образует его первичную структуру - полипептид. В
большинстве случаев полипептид закручивается в спираль - вторичную структуру
белка. Функции белков:
Строительная: белки входят в состав клеточных структур.
Транспортная: способность белков связывать и переносить с
током крови многие химические соединения (например, транспорт гемоглобином
кислорода).
Рецепторная функция: обеспечивает взаимодействие клеток
между собой, а также различными макромолекулами белков к обратимому изменению
структуры в ответ на действие физических и химических факторов лежит в основе
раздражимости.
Сократительная функция обеспечивается особыми
сократительными белками, благодаря которым происходит движение жгутиков,
ресничек, сокращение мышц и т.п.
Энергетическая функция: белки - это запасной источник
энергии.
Каталитическая функция: белки-ферменты ускоряют химические
реакции.
Защитная функция: белки-антитела (иммуноглобулины)
обезвреживают антигены (инородные вещества), вызывающие заболевания организма.
Регуляторная функция обеспечивается белками-гормонами, которые
регулируют обмен веществ.
Углеводы делятся на простые - моносахариды (рибоза,
дезоксирибоза, глюкоза, фруктоза и др.) и сложные - дисахариды (сахароза,
лактоза, мальтоза) и полисахариды. Функции углеводов: входят в состав
нуклеиновых кислот и АТФ, являются универсальным источником энергии в
организме, участвуют в обезвреживании и выведении из организма ядовитых
веществ, полисахариды играют роль запасных продуктов.
Липиды - это нейтральные жиры, воска, фосфолипиды и
стероидные гормоны. Они нерастворимы в воде, но хорошо растворимы в
органических растворителях (бензине, эфире, бензоле и др.). В их состав, как
правило, входят глицерин и жирные кислоты. Функции липидов: используются как
запасной источник энергии; входят в состав клеточных мембран; выполняют
защитные функции (теплоизоляция).
Нуклвоновые кислоты - это молекулы ДНК
(дезоксирибонуклеиновой кислоты) и РНК (рибонуклеиновой кислоты). ДНК -
биополимер, ее мономеры - нуклео-тиды состоят из азотистого основания (аденин,
гуанин, цитозин, тимин), моносахарида (дезоксирибоза) и остатка фосфорной
кислоты. Сама молекула ДНК - это 2 закрученные в спираль полинуклеотидные цепи,
объединенные между собой водородными связями. Функция ДНК: запись, хранение и
воспроизведение наследственной информации.
Рибонуклеиновая кислота (РНК) одно-цепочечный биополимер,
состоящий из нуклеотидов, в которых азотистое основание тимин заменено
урацилом, а углевод дезоксирибоза — рибозой. Различают 3 вида РНК:
информационную (и-РНК), транспортную (т-РНК) и рибосомальную (р-РНК). Функции
РНК: участие в воспроизведении наследственной информации (в синтезе белка).
Аденозинтрифосфорная кислота (АТФ)- мононуклеотид, состоящий
из ри-бозы, аденина и трех остатков фосфорной кислоты. Функция: АТФ -
универсальный источник энергии в клетке.
Обмен веществ и энергии (метаболизм) осуществляется на всех
уровнях организма: клеточном, тканевом и организменном. Он обеспечивает
постоянство внутренней среды организма - гомеостаз - в непрерывно меняющихся
условиях существования. В клетке протекают одновременно два процесса - это
пластический обмен и энергетический обмен.[6]
Пластический обмен - это совокупность реакций биосинтеза,
или создание сложных молекул из простых. В клетке постоянно синтезируются белки
из аминокислот, жиры из глицерина и жирных кислот, углеводы из моносахаридов,
нуклеотиды из азотистых оснований и сахаров. Эти реакции идут с затратами
энергии. Используемая энергия освобождается в ходе энергитического обмена.
Энергетический обмен - это совокупность реакций расщепления сложных органических
соединений до более простых молекул. Часть энергии, высвобождаемой при этом,
идет на синтез богатых энергетическими связями молекул АТФ. Расщепление
органических веществ осуществляется в цитоплазме и митохондриях с участием
кислорода. Реакции ассимиляции и диссимиляции тесно связаны между собой и
внешней средой. Из внешней среды организм получает питательные вещества. Во
внешнюю среду выделяются отработанные вещества.
9.1. Прокомментируйте высказывание Гельмгольца: «Электрон – есть нечто,
обозначаемое буквой е». Какими свойствами обладает электрон в разных
экспериментах? Определите длину волны электромагнитного излучения, энергия
кванта которого равна энергии покоя электрона. Масса покоя электрона равна
9,1*10-31 кг.
Скорее всего, под «нечто» в своем высказывании Гельмгольц
имел в виду корпускулярно-волновую природу электрона, из-за которой всегда
существует неопределенность в установлении его места пребывания в атоме.
Электрон имеет двойственную природу. В разных экспериментах
он может проявлять свойства, как частицы, так и волны. Движение электрона
подчиняется законам квантовой механики.
Связь между волновыми и корпускулярными свойствами электрона
отражает соотношение де Бройля:
l =h/mv ,
где l - длина волны электрона; m - его масса; v - скорость;
h = 6.62*10-34 Дж*с - постоянная Планка.
Энергию и координаты электрона, как и других элементарных
частиц, невозможно одновременно измерить с одинаковой точностью (принцип
неопределенности Гейзенберга). Поэтому движение электрона в атоме или в
молекуле нельзя описать с помощью траектории. Электрон может находиться в любой
точке пространства, но с разной вероятностью. Часть пространства, в котором
велика вероятность нахождения электрона, называют орбиталью или электронным
облаком.
Энергия покоя электрона равна:
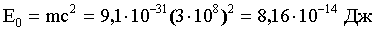
Энергия кванта электромагнитного излучения равна: 8,16*10-14
Дж
λ = E / hc
= 8,16*10-14 Дж /6.62*10-34 Дж*с * (3*108) с =
0,41*1012 с-2
10.1. Охарактеризуйте распространенность химических элементов на Земле
и ее биосфере. В чем принципиальное единство химического состава живых
организмов и неживой природы?
Сообщество живых организмов и абиотическая среда влияют друг
на друга, обе части биогеоценоза необхо димы для поддержания жизни.
Абиотические факторы регулируют существование и жизнедеятельность популяций. В
то же самое время эти факторы находятся под постоянным влиянием сам и х живых
организмов. Важные для жизни химические элементы (С, Н, О, N , Р) и
органические соединения образуют непрерывный поток между живым и неживым:
потребление и выделение углекислого газа, кислорода, воды, образование и
разложение растительного и животного опада, образование почвенных органических
соединений. Живые организмы черпают из среды жизненные ресурсы. Они поставляют
в среду продукты жизнедеятельности. Солнечная энергия аккумулируется зелеными
растениями и передается организмам всех популяций, населяющих биогеоценоз.
На суше Земли от полюсов к экватору биомасса постепенно
увеличивается. Наибольшее сгущение и многообразие растений имеет место во
влажных тропических лесах. Число и разнообразие видов животных зависит от
растительной массы и тоже увеличивается к экватору. Цепи питания, переплетаясь,
образуют сложную сеть передачи химических элементов и энергии. Между
организмами идет жесточайшая борьба за обладание пространством, пищей, светом,
кислородом. Живое вещество выполняет в биосфере следующие биогеохимические
функции: газовую — поглощает и выделяет газы; окислительно-восстановительную —
окисляет, например, углеводы до углекислого газа и восстанавливает его до
углеводов; концентрационную — организмы-концентраторы накапливают в своих телах
и скелетах азот , фосфор, кремний, кальций, магний. В результате выполнения
этих функций живое вещество биосферы из минеральной основы создает природные
воды и почвы, оно создало в прошлом и поддерживает в равновесном состоянии
атмосферу. При участии живого вещества идет процесс выветривания, и горные
породы включаются в геохимические процессы.
Газовая и окислительно-восстановительная функции живого
вещества тесно связаны с процессами фотосинтеза и дыхания. В результате
биосинтеза органических веществ автотрофными организмами было извлечено из
древней атмосферы огромное количество углекислого газа. По мере увеличения
биомассы зеленых растений изменялся газовый состав атмосферы — уменьшалось
содержание углекислого газа и увеличивалась концентрация кислорода. Весь
кислород атмосферы образован в результате процессов жизнедеятельности
автотрофных организмов. Живое вещество качественно изменило газовый состав
атмосферы — геологической оболочки Земли. В свою очередь, кислород используется
организмами для процесса дыхания, в результате чего в атмосферу вновь поступает
углекислый газ. Таким образом, живые организмы создали в прошлом и поддерживают
миллионы лет атмосферу нашей планеты. Увеличение концентрации кислорода в
атмосфере планеты повлияло на скорость и интенсивность
окислительно-восстановительных реакций в литосфере.
Многие микроорганизмы непосредственно участвуют в окислении
железа, что приводит к образованию осадочных железных руд, или восстанавливают
сульфаты, образуя биогенные месторождения серы.
Несмотря на то, что в состав живых организмов входят те же
химические элементы, соединения которых образуют атмосферу, гидросферу и
литосферу, организмы не повторяют полностью химический состав среды. Живое
вещество, активно выполняя концентрационную функцию, выбирает из среды обитания
те химические элементы и в том количестве, которые ему необходимы. Благодаря
осуществлению концентрационной функции живые организмы создали многие осадочные
породы, например залежи мела и известняка. Таким образом, живое вещество
биосферы, выполняя геохимические функции, создает и поддерживает компоненты
биосферы.
Список литературы
1. Кащеев
В.П. Ядерные энергетические установки. Минск: Высшая школа, 2000.-548с.
2. Найдыш В.М. Концепции современного естествознания.
Учебное пособие. М.: Высшая школа,1999. – 350 с.
3. Карпенков С. Х. Концепции современного
естествознания: Учебник для вузов. – М.: Академический проект, 2001. – 639 с.
4. Сидоренко А. В. Социально-философские проблемы
биосферы и рационального природопользования. – В кн.: Диалектика в науках о
природе и человеке. Т. 4. Человек, общество и природа в век НТР. – М.: Наука,
1983.– 45-51 с.
5. Торосян В. Г.
Концепции современного естествознания: Учеб. пособие. – М.: Высш. шк.,
2002. – 208 с.
[1] Шульпин
Г.Б. Химия для всех. М.:ИНФРА,2000.-193с.
[2] Овчинников
Ю.А. Химия жизни (Избранные труды). М.:Наука,2000.-95с.
[3]
Маргулова Т.Х. Атомная энергетика сегодня и завтра. Москва: Высшая школа,
2001.-331с.
[4]
Коллиер Дж., Дж.Хьюитт. Введение в ядерную энергетику. Москва: Энергоатомиздат,
2000.-138с.
[5]
Кесслер Г. Ядерная энергетика. Москва: Энергоиздат, 2000.-277с.
[6]
Кащеев В.П. Ядерные энергетические установки. Минск: Высшая школа, 2000.-142с.