Задача № 5
Получите углеводород 2-метил-1-бутен. Напишите уравнения
реакций взаимодействия этого углеводорода с: а) хлороводородом;
б) водой; в) бромом; г) водородом. Назовите продукты реакций.
Решение:
 СH2=C―CH2―CH3 2-метил-1-бутен
СH2=C―CH2―CH3 2-метил-1-бутен
CH3
Данное соединение можно получить отщеплением галогеноводорода от соответствующего алкилгалогенида
(1-хлор-2-метилбутан) под действием спиртового раствора щелочи:
 Cl H
Cl H
СH2―C―CH2―CH3
+ KOH СH2=C―CH2―CH3
CH3 CH3
 Cl
Cl
а) СH2=C―CH2―CH3
+ HCl → СH3―C―CH2―CH3
CH3 CH3
2-хлор-2-метилбутан
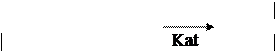 OH
OH
б) СH2=C―CH2―CH3
+ H2O СH3―C―CH2―CH3
CH3 CH3
2-метил-2-бутанол
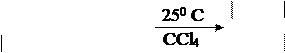 Br Br
Br Br
в) СH2=C―CH2―CH3
+ Br2 СH2―C―CH2―CH3
CH3 CH3
1,2-дибром-2метилбутан
 г) СH2=C―CH2―CH3
+ H2 СH3―CH―CH2―CH3
г) СH2=C―CH2―CH3
+ H2 СH3―CH―CH2―CH3
CH3 CH3
2-метил-бутан
Задача № 12
Как можно получить: а) 2-хлорбутан, б) 2-бром-2-метилпропан;
в) 2,2-дихлорпропан? Напишите соответствующие уравнения реакций. Как осуществить
следующие превращения: 2-хлорбутан → 2-бутанол → бутанон? Назовите все промежуточные соединения.
Решение:
 а) CH3CH2CHCH3
+ SOCl2 → CH3CH2CHCH3 + SO2
+ HCl
а) CH3CH2CHCH3
+ SOCl2 → CH3CH2CHCH3 + SO2
+ HCl
OH Cl
бутанол-2
тионил-
хлорид
 Br
Br
б) СH2=C―CH3 + HBr → СH3―C―CH3
CH3 CH3
2-метилпропен
 Cl
Cl
в) СH≡C―CH3 + 2HCl → СH3―C―CH3
Cl
пропин
 Цепочка
превращений:
Цепочка
превращений:
CH3CH2CHCH3 + H2O
CH3CH2CHCH3
Сl
OH
2-хлорбутан 2-бутанол
 CH3CH2CHCH3
+ [O] → CH3CH2C=O + H2O
CH3CH2CHCH3
+ [O] → CH3CH2C=O + H2O
OH CH3
2-бутанол
бутанон
Задача № 28
Как можно осуществить указанные превращения:
С6Н6 → С6Н5Cl → С6Н5OH → С6Н5―O―CH3?
Напишите соответствующие уравнения реакций. Назовите
полученные соединения. Как можно химическим путем доказать, что одно из этих
веществ является фенолом?
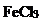 Решение:
Решение:
 С6Н6
+ Cl2 С6Н5Cl + HCl
С6Н6
+ Cl2 С6Н5Cl + HCl
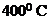 хлорбензол
хлорбензол
 С6Н5Cl + H2O С6Н5OH + HCl
С6Н5Cl + H2O С6Н5OH + HCl
фенол
С6Н5OH + CH2N2 → С6Н5―O―CH3
диазо- метиловый эфир бензола
метан
(анизол)
Чтобы доказать, что одно из этих веществ является фенолом
необходимо добавить в раствор FeCl3, при этом если в
растворе имеется фенольный гидроксил, то образуется окрашенное соединение –
качественная реакция на фенольный гидроксил.
Задача № 36
Где в природе встречается молочная кислота? Приведите один
из способов получения молочной кислоты. Какими реакциями можно подтвердить: а)
ее кислотные свойства; б) свойства спиртов.
Решение:
Природные источники молочной кислоты: кислое молоко, сыр,
квашеная капуста, силос.
Для производственного получения молочной кислоты,
кисломолочных продуктов и кислого теста, квашения овощей, силосования кормов
применяется молочнокислое брожение. При развитии молочнокислых бактерий в
молоке происходит сбраживание лактозы с образованием молочной кислоты;
последняя отнимает кальций от казеината, а образующийся нерастворимый казеин,
выпадает в виде хлопьев, т.е. происходит свертывание молока. Молочная кислота,
образуемая молочнокислыми бактериями, действует угнетающим образом на
большинство других видов бактерий (поэтому молочнокислое брожение наряду с
энергетическим имеет приспособительное значение).
Молочнокислые бактерии подразделяют на 2 группы —
гомоферментативные и гетероферментативные. Гомоферментативные бактерии
расщепляют моносахариды с образованием двух молекул молочной кислоты в
соответствии с суммарным уравнением:
C6H12O6
= 2CH3CHOH·COOH.
Гетероферментативные бактерии ведут сбраживание с
образованием молочной кислоты, уксусной кислоты, этилового спирта и CO2,
а также образуют небольшое количество ароматических веществ — диацетила, эфиров
и т.д.
Гомоферментативное молочнокислое брожение используется для
получения молочной кислоты, при изготовлении различных кислых молочных
продуктов, хлеба и в силосовании кормов в сельском хозяйстве.
Гетероферментативное молочнокислое брожение происходит при консервировании
различных плодов и овощей путем квашения.
В химических реакциях оксикислоты (к которым относится
молочная кислота) ведут себя как кислоты, либо как спирты:
а) взаимодействуют со щелочами с образованием солей:
 CH3―CH―COOH +
NaOH → CH3―CH―COONa + H2O
CH3―CH―COOH +
NaOH → CH3―CH―COONa + H2O
ОН ОН
б) взаимодействуют с кислотами с образованием эфиров:
 CH3―CH―COOH +
OH―C―CH3 → CH3―C―O―CH―COOH
+ H2O
CH3―CH―COOH +
OH―C―CH3 → CH3―C―O―CH―COOH
+ H2O
ОН O О CH3
Задача № 43
Напишите структурные формулы глицеридов: а) триолеина, б) тристеарина. Чем отличаются эти глицериды по
физическим и химическим свойствам? Напишите соответствующие уравнения реакций.
|
 O O
а) H2C―O―C―C17H33
O
HC―O―C― C17H33
O
H2C―O―C―C17H33
|
O
б) H2C―O―C―C17H35
O
HC―O―C― C17H35
O
H2C―O―C―C17H35
|
Триолеин – жидкий жир, так как в состав его входит
ненасыщенная кислота (олеиновая); тристеарин – твердый жир, так как в состав
его входит насыщенная кислота (стеариновая).
Триолеин, в отличие от тристеарина, вступает в реакции
присоединения по двойной связи – гидрогенизация, галогенирование и др.:
|
 O O
а) H2C―O―C―C17H33
O
HC―O―C― C17H33
+ 3Н2
O
H2C―O―C―C17H33
|
O
H2C―O―C―C17H35
O
HC―O―C― C17H35
O
H2C―O―C―C17H35
|
|
 O O
б) H2C―O―C―C17H33
O
HC―O―C― C17H33
+ 3Cl2
O
H2C―O―C―C17H33
|
O
H2C―O―C―(CH2)7
―CHCl―CHCl―(CH2)7―CH3
O
HC―O―C―(CH2)7
―CHCl―CHCl―(CH2)7―CH3
O
H2C―O―C―(CH2)7
―CHCl―CHCl―(CH2)7―CH3
|
Задача № 60
Что собой представляют редуцирующие сахара? Охарактеризуйте
существенное различие в строении и химических свойствах редуцирующих
(восстанавливающих) и не редуцирующих сахаров. Напишите схемы соответствующих
реакций.
Различают дисахариды двух типов: восстанавливающие
(редуцирующие) и не восстанавливающие (не редуцирующие).
Восстанавливающие (редуцирующие) дисахариды:
мальтоза, лактоза, целлобиоза.
Молекулы этих дисахаридов построены таким образом, что одна
молекула моносахарида участвует в образовании связи своим полуацетальным
гидроксилом, вторая - спиртовым. В молекуле такого дисахарида один полуацетальный (гликозидный) гидроксил
остается свободным. Дисахариды такого типа могут переходить в альдегидную
форму, следовательно, могут проявлять восстанавливающие свойства (дают реакцию
серебряного зеркала, восстанавливают раствор Фелинга).
Восстанавливающие дисахариды проявляют свойства альдегидов, многоатомных
спиртов, образуют гликозиды.
Не восстанавливающие дисахариды:
сахароза, трегалоза и др.
Молекулы этих дисахаридов построены таким образом, что оба
моносахарида участвуют в построении молекулы дисахарида полуацетальными
гидроксилами. Дисахариды такого типа не могут переходить в альдегидную форму,
следовательно, не обладают восстанавливающими свойствами (не дают реакцию
серебряного зеркала, не восстанавливают раствор Фелинга).
а) Реакция серебряного зеркала:
 С12Н22О11
+ Ag2O C12H22O12 + Ag
С12Н22О11
+ Ag2O C12H22O12 + Ag
мальтоза
 С12Н22О11
+ Ag2O реакция не идет
С12Н22О11
+ Ag2O реакция не идет
сахароза
 б)
Реакция с раствором Фелинга:
б)
Реакция с раствором Фелинга:
 С12Н22О11
+ Cu(OH)2 C12H22O12 + Cu2O
С12Н22О11
+ Cu(OH)2 C12H22O12 + Cu2O
мальтоза
 С12Н22О11
+ Cu(OH)2 реакция не идет
С12Н22О11
+ Cu(OH)2 реакция не идет
сахароза
Задача № 67
Расскажите о протеинах: классификация, свойства. В каких
пищевых продуктах они встречаются?
Протеины – это простые белки, состоящие только из
α-аминокислот. В основу классификации простых белков положены некоторые
физико-химические, а также химические их особенности. К простым белкам относятся:
альбумины, глобулины, гистоны, протамины, протеиноиды, проламины, глютелины и др.
Альбумины — группа весьма распространенных белков,
встречающихся в тканях животных и растений, а также в жидкостях организмов (в
сыворотке крови, спинномозговой жидкости и др.). К альбуминам относятся белки,
растворимые в воде и нерастворимые в насыщенных растворах сернокислого аммония.
Альбумины содержатся в яичном белке (овальбумины), в сыворотке крови
(сывороточные альбумины), в сыворотке молока (лактальбумины),
в зеленых частях растений, в зернах злаков (в зародышах), в семенах бобовых
растений и т. д. Различные альбумины могут отличаться друг от друга по
способности высаливаться при различных концентрациях нейтральной соли
(сернокислого аммония).
Глобулины, подобно альбуминам, широко представлены в
организмах. Отличаются они от альбуминов тем, что нерастворимы в воде, но
растворимы в водных растворах различных солей. Эти признаки используются для
разделения альбуминов и глобулинов. Глобулины отличаются от альбуминов и тем,
что в отличие от альбуминов, или вовсе не содержат глицина, или же содержат эту
аминокислоту в незначительных количествах.
Гистоны — группа белков, в состав молекул которых
входит от 20 до 30% диаминомонокарбоновых кислот
(лизина, аргинина) и циклической основной аминокислоты — гистидина. Эти белки
обладают щелочными свойствами, так как из двух аминогрупп диаминомонокарбоновых
кислот при построении белковой молекулы только одна (α-аминогруппа) используется
для образования пептидной связи. Вторая же аминогруппа (в гистидине иминогруппа) остается в белковой молекуле свободной, и это
обусловливает щелочное свойство гистонов. Гистоны встречаются в значительных
количествах в белках эритроцитов и
зобной железы.
Протамины — группа белков, отличающихся особенно
высоким содержанием диаминомонокарбоновых кислот —
до 80%. Отсюда понятно, почему протамины обладают еще более ярко выраженной
щелочностью, чем гистоны. В большом количестве протамины содержатся в сперме и
икре рыб, а также в тканях, богатых клетками с ядрами. Протамины, а также и
гистоны, составляют белковую часть сложных белков нуклеопротеидов и с этой точки зрения представляют
значительный биологический интерес.
Протамины построены из очень ограниченного числа
аминокислот. В составе их отсутствуют серосодержащие аминокислоты. Молекулярный
вес протаминов не превышает 10 000. Все это позволяет считать протамины
наиболее просто построенными белками.
Протеиноиды — группа белков, содержащихся в опорных
тканях организма животных,— в костной ткани, хрящах, сухожилиях, волосах и шерсти.
Протеиноиды нерастворимы ни в воде, ни в солевых растворах, ни в разведенных
кислотах и щелочах, т.е. они находятся в денатурированном состоянии. Они не гидролизируются пищеварительными ферментами (не
перевариваются) и поэтому не могут быть использованы как продукты питания.
Протеиноиды по своей структуре являются волокнистыми (фибриллярными) белками.
К протеиноидам относится белок соединительной ткани коллаген, оссеин — белок
костной ткани, кератины — белки волос, шерсти, эпидермиса, рогов. Эти белки богаты
цистином. Протеиноидом является также фиброин,
образующийся в так называемых прядильных железах насекомых (гусениц
бабочек-шелкопрядов пауков). Из фиброина шелкопрядов изготавливаются шелковые
нити.
Проламины — группа
белков растительного происхождения — встречаются в семенах
злаков. Отличительную черту проламинов составляет хорошая растворимость в 60—80-процентном
этиловом спирте (другие белки под влиянием спирта денатурируются и выпадают в
осадок). Проламины слабо растворяются в воде. При гидролизе они образуют
большое количество пролина (отсюда название «проламины») и глютаминовой кислоты.
Проламины почти не содержат лизина. К проламинам относятся глиадин из семян
пшеницы и ржи, гордеин из семян ячменя, авенин из семян овса и др.
Глютелины — группа белков растительного происхождения
— обнаруживаются в семенах злаков и в зеленых частях растений. Отличительной
их чертой является растворимость только в растворах щелочей.
Задача № 74
Охарактеризуйте строение и свойства: а) пиррола, б) индола.
В состав каких органических веществ они входят?
а) Пиррол – пятичленное гетероциклическое соединение.
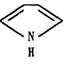
В пирроле все атомы цикла находятся в sр2-гибридизированном
состоянии, поэтому цикл имеет плоское строение; каждый атом углерода и азот
предоставляют по три электрона на связывание с тремя соседними атомами. После
этого у каждого атома углерода остается по одному электрону (всего четыре), а у
атома азота — свободная электронная пара. В результате кольцевого перекрывания орбиталей этих шести электронов образуются электронные
облака над и под плоскостью пиррольного кольца.
Следовательно, образуется устойчивый ароматический секстет (шесть) электронов
(4n + 2) при n = 1.
Свободная электронная пара азота в пирроле, остающаяся после
образования связей азота с атомами углерода и водорода, участвует в образовании
ароматического секстета, поэтому взаимодействие этой электронной пары атома с
протонами выражено слабо, и пиррол является чрезвычайно слабым основанием.
Пиррол, с другой стороны, проявляет свойства слабой кислоты: при взаимодействии
с сильными основаниями образует соответствующие производные.
Пиррол и ряд его производных являются неустойчивыми в кислых
средах (являются ацидофобными) — образуют смолообразные продукты.
Наиболее характерные для пиррола реакции электрофильного
замещения (нитрование, сульфирование, йодирование, азосочетание),
которые для этого соединений протекают даже легче, чем для бензола. Реакции электрофильного замещения для пиррола идет преимущественно
в положения 2. Если положение 2 занято, то реакции электрофильного
замещения могут идти в положение 3.
Производными пиррола являются такие важные природные соединения,
как гемоглобин и хлорофилл. Гемоглобин содержится в эритроцитах (красные
кровяные тельца крови) и выполняет функцию переноса кислорода от легких к
тканям тела. Хлорофилл — красящий пигмент листьев, осуществляющий усвоение
диоксида углерода растениями в процессе фотосинтеза.
б) Индол или бензо-[b]-пиррол является
ароматическим соединением [плоская структура, 10 делокализованных
электронов (4n + 2,
где n = 2) в сопряженной бициклической
системе]:
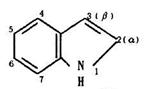
Индол ведет себя в химических реакциях подобно пирролу:
проявляется амфотерность (т.е. обладает как слабокислыми, так и слабоосновными
свойствами), вступает в реакции электрофильного
замещения. Однако атака электрофильных реагентов идет
преимущественно в положение 3 (β). Это объясняется тем, что в β-положении имеется максимальная электронная плотность.
Производными индола являются индоксил и индиго. Индоксил содержится
в виде производных в животных или растительных организмах. Индиго – широко используемый
ярко-синий краситель (порошок), который относится к кубовым красителям,
нерастворим в воде.
Задача № 81
Охарактеризуйте строение фенолфталеина (приведите
структурную формулу), свойства (отношение к кислотам и щелочам), практическое
использование.
Фенолфталеин
– бесцветное кристаллическое органическое вещество сложного строения, молекулы
которого включают три бензольных цикла, связанных через атом углерода, и две
гидроксильные группы.
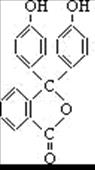
Фенолфталеин малорастворим в воде и хорошо растворяется в
этиловом спирте.
Бесцветный фенолфталеин, имеющий строение лактона, при
действии щелочей образует (с разрывом лактонного кольца) соль, причем одно из
бензольных ядер принимает хиноидное строение и становится, таким образом,
хромофором:
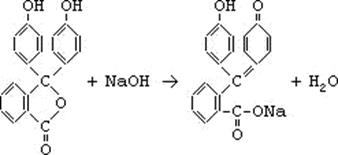
Вследствие чего его применяют в аналитической химии как
индикатор при титровании кислот и щелочей (в нейтральных и кислых растворах фенолфталеин
бесцветен, в слабощелочных – малиново-красного цвета; область перехода при pH 8,2=10). Его также используют в медицине – как
слабительное средство, лечебных эффект которого обусловлен усилением
перистальтики толстого кишечника.
Задача № 99
Охарактеризуйте строение витамина К (филлохинона) (приведите
структурную формулу), свойства. Какие факторы действуют на него разрушающе? Где
встречается в природе? Как влияет на организм человека?
В 1929 г. в опытах с кормлением цыплят искусственно составленной
пищей было открыто вещество, отсутствие которого в пище замедляет процесс
свертывания крови. В 1934 г. Дам назвал это вещество витамином К. При
отсутствии витамина К в пище, а также при нарушении его всасывания в кишечнике,
например, при недостаточном поступлении желчи в кишечник, наступает
К-авитаминоз, характеризующийся понижением содержания в крови протромбина —
одного из важных компонентов ферментной системы свертывания крови, прекращением
синтеза ряда иных белков, необходимых для свертывания крови, замедлением
образования кровяного сгустка (замедление свертывания крови) и подкожными и
внутримышечными кровоизлияниями (геморрагии).
Введение в организм авитаминозных животных витамина К
повышает у них содержание протромбина в крови до нормального уровня и устраняет
явления авитаминоза.
Витамин К выделен в 1939 г. из люцерны, и в том же году была
установлена его химическая структура. Молекула витамина К построена из
циклического компонента — 2-метил-1,4-нафтохинона и из фитола
Из гниющей рыбной муки было выделено вещество, аналогичное по действию витамину
К и несколько отличающееся от него по своим химическим и физическим свойствам.
Витамин, выделенный из люцерны, получил название витамина К1;
витамин же, изолированный из рыбной муки — витамина К2.
Витамин К2 отличается от витамина К1
структурой своей боковой цепи, которая содержит шесть двойных связей и 30
атомов углерода
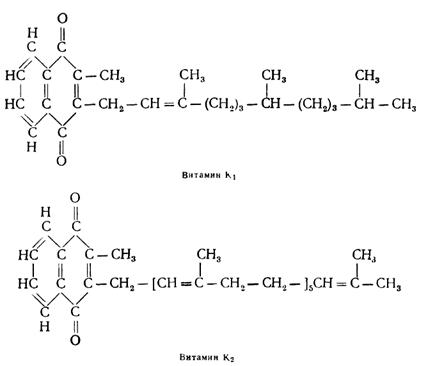
Активность витаминов К1
и К2 определяется наличием в их составе молекул
циклического компонента — 2-метил-1,4-нафтохинона. Сам 2-метил-1,4-нафтохинон
обладает при расчете на грамм-молекулу такой же активностью, как и витамин К1.
Витамин К1 доставляется в организм человека и
животных с пищей. Некоторое количество витамина К2 синтезируется
кишечной флорой и всасывается из кишечника. Наличие кишечной флоры,
синтезирующей витамин К2, уменьшает потребность в доставке витамина
К в организм с пищевыми продуктами. Применение
сульфамидных препаратов, ограничивающее развитие микрофлоры, уменьшает объем
синтеза витамина К2 в кишечнике.
Витамин К1 встречается, главным образом, в
продуктах питания растительного происхождения, особенно в зеленых частях
растений. Шпинат, крапива, капуста богаты витамином К1.
Витамин К разрушается на свету, в щелочных (содовых)
растворах. Избыточный приём кальция снижает синтез витамина К, а большой прием витамина Е снижает его усвоение.
Список литературы
1.
Ким А.М. Органическая химия. – Новосибирск: НГПУ, 1999.
2.
Петров А.А. и др. Органическая химия. – М.: Высшая школа,
1973.
3.
Фердман Д.Л. Основы биохимии. – М.: Высшая школа, 1972.
4.
Филлипович Ю.Б. Основы биохимии: Учебник. – М.: Высшая школа,
1985.
5.
Швехгеймер М.-Г.А., Кобраков К.И. Органическая химия. – М.: Высшая школа, 1994.