ШОК
Шок - это
чрезмерная неадекватная защитная реакция организма в ответ на действие
экстремального повреждающего фактора, попытка симпато-адреналовой системы
поддержать кровоток в жизненно важных органах в ущерб перфузии и метаболизму
остальных.
Патогенез шока
Общим звеном патогенеза любого вида шока является
синдром гиповолемии. Под этим термином следует понимать несоответствие объема циркулирующей крови емкости сосудистого русла, что ведет к снижению
гидростатического давления в капиллярах. Гиповолемия может быть истинной,
например, при шоке от кровопотери и относительной, связанной с увеличением
объема сосудистого русла, как это бывает при анафилактическом шоке и др.
Следствия
Рефлекторная компенсация
В ответ на
гиповолемию в организме происходят закономерные реакции направленные на
компенсацию этого состояния. Возникает импульсация с волюмо- и барорецепторов
сосудов, которая ведет к повышению тонуса симпатической нервной системы:
увеличивается выброс катехоламинов. Под действием катехоламинов (адреналина и
норадреналина) повышается тонус артериол (из-за действия на a рецепторы, расположенные в артериолах), что
ведет к уменьшению емкости сосудистого русла, возрастает сократимость миокарда,
увеличивается число сердечных сокращений (влияние на b1-рецепторы сердца),
повышается минутный объем сердца. В результате синдром гиповолемии может быть
компенсирован и тогда шок не развивается.
Если же,
несмотря на выброс колоссальных количеств катехоламинов в кровь (при шоке
содержание катехоламинов повышается в крови в 70 - 100 раз), этот
компенсаторный механизм оказался недостаточным, то, практически одновременно,
включается второй уровень компенсации.
Гемодинамическая компенсация
Поскольку
снижается гидростатическое давление в капиллярах, то суммарный вектор проницаемости
через сосудистую стенку оказывается направленным в сторону сосудистого русла из
тканей (механизм Старлинга), что вызывает значительный приток жидкости из
межтканевого пространства в сосуды. Это мощный механизм компенсации. За 15
минут шока из тканей в сосуды может быть мобилизовано до 3-х литров жидкости. И
шок развивается, если только сохраняется гиповолемия.
Централизация кровотока
Если
причина гиповолемии не связана с прямым сосудорасширяющим действием
повреждающего агента на микрососуды (анафилаксия, некоторые виды инфекционно
токсического шока), то под влиянием огромных количеств катехоламинов происходит
значительное повышение тонуса артериол, что вызывает выраженное повышение
периферического сопротивления, увеличение постнагрузки на сердце. Существенно
затрудняется вхождение крови в капиллярную сеть и поэтому большая часть
кровотока по шунтам сбрасывается, минуя капилляры, непосредственно в венулы. В
связи с тем, что сосуды сердца практически не содержат a-рецепторов, под влиянием катехоламинов происходит
расширение коронарных сосудов. Меньше, чем в других сосудистых областях,
подвержены спазму сосуды мозга. Таким образом, развивается так называемая
централизация кровотока, направленная на то, чтобы поддержать
кровообращение в жизненно важных органах.
Изменения микроциркуляции
В
остальных сосудистых областях происходят закономерные изменения:
¨
в связи с затруднением входа в систему капилляров, скорость движения
крови в них существенно снижается;
¨
Так как кровь является, так называемой, неньютоновской жидкостью,
вязкость которой тем меньше, чем больше скорость ее течения и, наоборот, тем
выше, чем медленнее кровоток, то вязкость крови, протекающей по капиллярам, то
есть внутреннее трение, возрастает.
¨
Это обстоятельство способствует склеиванию между собой форменных
элементов - агрегации форменных элементов.
Для
обозначения внутрисосудистой агрегации форменных элементов используется термин сладж-синдром от английского слова
sludge, которое переводится как тина или ил.[1]. Развитие сладжа, в свою
очередь повышает вязкость крови.
Следствия
микроциркуляторных нарушений:
¨
увеличиваются энергозатраты сердца, из-за повышенного периферического сопротивления;
¨
снижается венозный возврат к сердцу той части крови, которая находится
в капиллярах, что ведет к снижению сердечного выброса, нарастанию гиповолемии.
То есть,
развивается порочный круг.
|
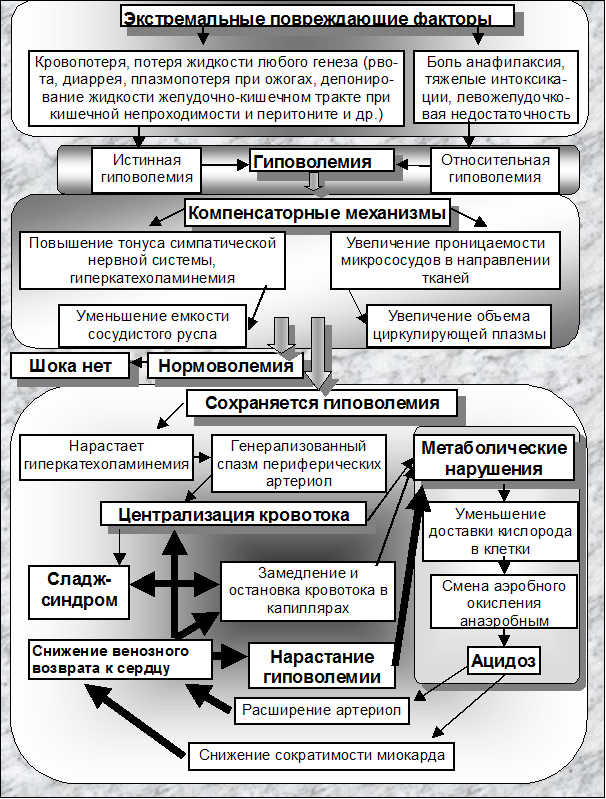
Рисунок 1 Принципиальная схема патогенеза шока[2]
Рисунок 2. Патогегез шока
|
Метаболические расстройства
Сладж
препятствует поступлению эритроцитов в капилляры, снижается доставка кислорода
в ткани. Аэробное окисление сменяется анаэробным. Из каждой молекулы глюкозы
вместо 6 молекул воды и 6 молекул углекислого газа с выделением энергии,
запасаемой в 38 молекулах АТФ, образуются только 2 молекулы пировиноградной
кислоты, которые превращаются в молочную кислоту, то есть в тканях
накапливаются недоокисленные продукты. Развивается ацидоз.
Следствия ацидоза
Выраженный
ацидоз обладает кардиодепрессивным действием, за счет снижения чувствительности
b1-рецепторов сердца к
действию катехоламинов ведет к дальнейшему снижению сердечного выброса,
нарастанию гиповолемии.
Ацидоз
уменьшает дзета-потенциал
эритроцитов (потенциал взаимного отталкивания). Нарастает сладж. Снижается
венозный возврат крови к сердцу. Нарастает гиповолемия.
Под
влиянием выраженного ацидоза снижается чувствительность a-рецепторов артериол к катехоламинам. Спазм
артериол сменяется их полным расслаблением. Вход в капиллярную сеть
открывается. Но это не приводит к активизации кровотока в капиллярах, так как
протеканию крови в капиллярах мешает сладж. Поэтому поступление дополнительных
порций крови в капилляры ведет к дальнейшему снижению венозного возврата крови
к сердцу и уменьшению сердечного выброса, то есть нарастанию гиповолемии.
Таким
образом, при шоке все попытки организма уменьшить гиповолемию, наоборот,
приводят к дальнейшему снижению венозного возврата крови к сердцу, к снижению
сердечного выброса и, в конечном итоге, к полной остановке кровообращения, т.е.
к смерти.
|
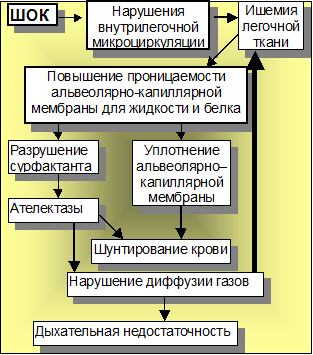
Рисунок 3. Схема патогенеза шокового легкого
|
Е. Поражения внутренних органов
1 Шоковое легкое
Феномен
шокового легкого или, как его называют в англоязычной литературе
"респираторный дистресс-синдром у взрослых", или "синдром острой
дыхательной недостаточности у взрослых" проявляется обычно через 1-2 дня
после шока. На фоне кажущегося хорошего состояния появляется тяжелая,
устойчивая к терапии дыхательная недостаточность: парциальное давление
кислорода в артериальной крови ниже должного уровня (снижается до 60 мм рт.ст.
и ниже), а парциальное давление углекислоты выше 50 мм рт.ст.
Симптомы
при шоковом легком связаны с шунтированием крови. Это значит, что большая часть
крови, минуя альвеолы, сбрасывается сразу из легочных артериол в легочные вены.
В патогенезе шокового легкого играют
роль и иммунные нарушения, в частности, придают значение фракции комплемента
C5a, которая вызывает агрегацию и стаз лейкоцитов в легких. Стаз крови в легких
может вызвать явления отека легких даже на фоне гиповолемии. При этом
локальное, пусть даже незначительное, повышение гидростатического давления в
легочных капиллярах может оказаться выше сопротивления, которое оказывает
пораженная альвеолярно-капиллярная мембрана давлению жидкости. Т.е. основное
звено патогенеза отека легких на фоне шока - это повышение проницаемости.
2 Шоковая почка
Следует
различать функциональную почечную недостаточность, т.н. "почка при
шоке" и шоковую почку. При падении АД ниже 80 мм рт.ст. нарушается ауторегуляция
фильтрации. При давлении ниже 60-70 мм рт.ст. уже может наступать олигурия,
однако еще возможна обратная реабсорбция. При АД ниже 40 мм рт.ст. клубочковая
фильтрация полностью прекращается.
При
функциональной почечной недостаточности происходит резкое снижение или полное
прекращение диуреза, но сама почка при этом функционально способна.
При
шоковой почке почечная недостаточность сохраняется даже после устранения
функциональных нарушений. Основной причиной развития шоковой почки является
ишемия, которая, развившись во время шока (спазм почечных артерий), в свою
очередь, активизирует вазоконстрикторный механизм (ренин-ангиотензиновый),
который поддерживает ишемию почек (порочный круг). Сладж в сосудах почек также
препятствует восстановлению почечного кровотока и удлиняет феномены ишемии.
Меньшее значение в развитии синдрома шоковой почки играет закупорка канальцев
цилиндрами и обратная диффузия при поражении канальцев. Существенное значение в
развитии острой почечной недостаточности при шоке придается неоправданному
лечению шока агонистами a-рецепторов (мезатон, норадреналин)
Особенности патогенеза различных видов шока
Говоря об
особенностях различных видов шока, в первую очередь, необходимо выяснить, какие
факторы ведут к развитию гиповолемии,
Кардиогенный шок
Причины
кардиогенного шока: острый инфаркт миокарда и реже острый миокардит.
По
классификации Е.И.Чазова выделяют 4 вида кардиогенного шока:
¨
рефлекторный,
¨
истинный кардиогенный,
¨
ареактивный и
¨
аритмический.
В
зависимости от выраженности коллаптоидной реакции и от реакции на прессорные
амины А.С.Сметнев выделяет 4 степени тяжести кардиогенного шока:
¨
1 степень соответствует рефлекторному шоку,
¨
2-я и 3-я истинному кардиогенному шоку и
¨
4-я ареактивному шоку.
Рефлекторный кардиогенный шок. (1 ст. по
А.С.Сметневу)
Запускающим
фактором рефлекторного кардиогенного шока является боль в связи с развитием
некроза в сердечной мышце. Сильная боль вызывает рефлекторное повышение тонуса
симпатической нервной системы, выброс больших количеств катехоламинов. Под
влиянием катехоламинов развивается генерализованный спазм прекапиллярных
артерий. Это ведет к кратковременному повышению артериального давления
(эректильная фаза). Но затем из-за того, что вход в капиллярное русло
значительно затрудняется, та часть крови, которая находилась в капиллярах и
венулах в момент развития шока, не покидает систему микроциркуляции, а
задерживается в ней и перестает возвращаться к сердцу. Этот механизм носит
название секвестрации крови. Из-за секвестрации крови венозный возврат к сердцу
резко снижается и сердечный выброс падает. Развивается гиповолемия.
Истинный кардиогенный шок (2-я и 3-я степень
по А.С.Сметневу)
В связи с
развитием некроза в сердечной мышце появляется зона акинезии, т.е. участок
миокарда, который не участвует в сокращении, или зона дискинезии - часть
миокарда, которая в момент систолы выпячивается наружу и, тем самым,
поглощающая значительную часть энергии сокращения сердца. Появление участков
акинезии и (или) дискинезии приводит к снижению сердечного выброса. Снижается
давление крови на стенки сосудов, т.е. развивается синдром гиповолемии.
Ареактивный кардиогенный шок (4-я степень по
А.С.Сметневу)
Ареактивный
шок является той фазой истинного кардиогенного шока, когда из-за выраженного
ацидоза тканей снижается чувствительность a-рецепторов сосудов к
действию катехоламинов, что проявляется отсутствием прессорной реакции на
вводимые для лечения шока катехоламины.
Аритмический шок
Из-за
укорочения фазы диастолы при таких нарушениях ритма, как пароксизмальная тахикардия
и мерцательная тахиаритмия, уменьшается время наполнения сердца кровью, это
ведет к снижению сердечного выброса и развитию синдрома гиповолемии.
Анафилактический шок
При
повторном поступлении в сенсибилизированный организм разрешающей дозы аллергена
происходит массивный выброс биологически активных веществ, таких как гистамин,
серотонин, кинины. Эти биологически активные вещества, действуя на стенку
прекапиллярных артериол, вызывают их активное расширение, что приводит к
резкому увеличению емкости сосудистого русла, т.к. открываются все резервные
микроциркуляторные модули. Емкость сосудистого русла увеличивается в 2-3 раза,
развивается выраженная гиповолемия. Но, в отличие от других видов шока, несмотря
на то, что количество катехоламинов повышается в крови в десятки раз, в борьбе
за рецепторы побеждают биологически активные вещества и поэтому не развивается
централизация кровообращения, т.е. не проявляется рефлекторный механизм
компенсации шока. Именно поэтому анафилактический шок является таким опасным и
требующим самых неотложных врачебных мероприятий.
Инфекционно-токсический шок (септический
шоковый синдром)
Септический
шоковый синдром (СШС) - внезапная бурная
реакция организма на микробы. СШС является анафилактическим по физиологическим
механизмам. Возможно, эндотоксиновый шок с массивным лизисом безвредных до
этого момента микробов является результатом цитолитической реакции
сенсибилизирующих антител. Помимо аллергической природы перечисленных реакций,
мало зависящих от дозы токсина, на органы и ткани, несомненно, воздействуют
экзо - и эндотоксины, как простые токсические вещества, действие которых
пропорционально их количеству.
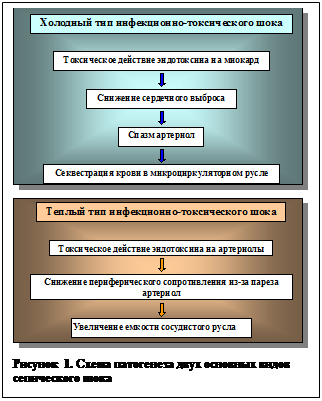
Поражения
гемодинамики может быть связано с двумя возможными механизмами (Рисунок 4)
Оба эти
механизма, особенно на фоне других проявлений интоксикации, ведущих к потере
жидкости (рвота, диарея) приводят к снижению венозного возврата крови к сердцу,
снижению сердечного выброса, к развитию синдрома гиповолемии.
Кроме того, при СШС часто наблюдается
диссеминированное внутрисосудистое свертывание (ДВС) из-за следующих механизмов:
¨
гемолитические и другие цитолитические реакции, в том числе лизис самих
микроорганизмов, поставляют в организм активный тромбопластин, запускающий
коагуляцию крови с образованием сгустков фибрина;
¨
биологически активные вещества, вышедшие из клеток, вызывают агрегацию
тромбоцитов, а эти агрегаты являются фокусами, обрастающими фибрином;
¨
 генерализованное повреждение эндотелия сосудов вызывает агрегацию тромбоцитов;
генерализованное повреждение эндотелия сосудов вызывает агрегацию тромбоцитов;
¨
на клеточных агрегатах из-за сладж-синдрома осаждается фибрин.
Если
фибринолитическая система не справляется с возникшими трудностями, то
развиваются некрозы из-за тромбоза, а если справляется, то тратится слишком
много факторов свертывания - тромбоцитов, фибрина, антитромбина III[3]и развивается геморрагический
синдром.
Ишемия
тканей, сопутствующая шоку, а также действие микробных токсинов вызывают
разрушение лизосом и повышение в крови уровня протеолитических ферментов,
которые взывают дополнительное повреждение органов и тканей.
Патогенез истинного гиповолемического шока
Причины:
¨
массивная кровопотеря,
¨
потеря жидкости при неукротимой рвоте и диарее, например, при холере
или при крайне тяжелой лучевой болезни.
Потеря
жидкости вызывает истинную гиповолемию.
Клинические проявления шока
Клиника
шока является проявлением его патогенетических механизмов.
Гиповолемия
проявляется низким систолическим давлением (менее 80 мм рт.ст.) и снижением
пульсового давления (менее 25 мм рт.ст.), малым, "нитевидным"
пульсом. Снижение перфузии почек проявляется олигурией (менее 50 мл мочи в час)
или анурией.
Гиперкатехоламинемия
проявляется тахикардией, возбуждением, относительным
повышением диастолического давления.
Микроциркуляторные
расстройства вызывают бледность кожных покровов (спазм артериол),
"мраморность" кожи из-за сочетания участков спазма (бледность) и
локального стаза крови (цианоз). Холодная кожа из-за замедления кровотока. В
терминальной стадии при развитии пареза артериол появляется диффузный цианоз.
Учащенное
дыхание из-за возбуждения дыхательного центра в связи с ацидозом.
В своем
развитии инфекционно-токсический шок проходит фазовые состояния, крайне
несхожие между собой и даже противоположные во внешних проявлениях.
Различают
"горячий" период, который начинается бурной гипертермической реакцией
с ознобом, гиперемией кожи, мышечными болями. Почти всегда наблюдаются
возбуждение, бред, судороги, нередко рвота и диарея. Этот период бывает
довольно кратковременным (иногда менее получаса).
"Холодный"
период характеризуется классическими проявлениями шока: бледно-цианотичная,
холодная кожа, коллапс, олигурия. Нередко возникают кровотечения, желтушная
окраска кожи, кожные кровоизлияния. Смерть может наступить в течение нескольких
часов от начала "холодного" периода.
Лечение шока
При любом
виде шока из-за расстройств микроциркуляции все медикаменты должны вводится
непосредственно в кровеносное русло, т.е. подкожные и внутримышечные инъекции
не только бесполезны, т.к. препараты не покидают капилляры, но и вредны:
тратится драгоценное время, когда могла быть оказана действительно эффективная
помощь.
Рефлекторный (болевой) шок
Главное -
быстрое купирование болевого синдрома, т.к. при промедлении (более получаса)
развиваются выраженные микроциркуляторные расстройства. Лечение рефлекторного
кардиогенного шока следует начинать с внутривенного введения наркотических
анальгетиков. Методом выбора является нейролептаналгезия. Наиболее удачными
являются аналгетик фентанил в сочетании с нейролептиком дроперидолом. Обычно
терапию начинают с введения 2.0 р-ра фентанила и 2.0 дроперидола. При
отсутствии достаточного эффекта введение можно через 3-5 минут повторить в той
же дозе. В большинстве случаев эти препараты за 1-2 минуты купируют боль, что
обрывает основное звено патогенеза рефлекторного шока: снижается гиперкатехоламинемия,
прекращается спазм артериол, прекращается секвестрация крови, исчезает синдром
гиповолемии. Именно поэтому рефлекторный шок, когда лечение проводится на
ранних этапах, является самым благодарным видом шока. Продолжительность
действия фентанила 30 минут, дроперидола до 90 минут, поэтому, при
необходимости, введение этих медикаментов можно повторять в указанных дозах с
учетом прошедшего времени. Кроме того, что дроперидол потенцирует
аналгетический эффект фентанила, он сам по себе является довольно эффективным
блокатором a-рецепторов, поэтому его применение
является патогенетически обоснованным еще потому, что он сам прекращает эффект
секвестрации крови. Поэтому не следует опасаться возможного кратковременного
снижения АД после введения дроперидола, поскольку это снижение АД
сопровождается явным улучшением микроциркуляции, потеплением кожных покровов,
увеличением пульсового давления, и, в конечном итоге, увеличением венозного
возврата крови к сердцу.
При
отсутствии фентанила его можно заменить морфином, но следует иметь в виду, что
действие морфина продолжается до 3-4 часов и поэтому больше опасность
передозировки. Все наркотические анальгетики вызывают при передозировке
однотипные осложнения: угнетение дыхательного центра, рвоту, резкое урежение
ритма сердца, повышение тонуса гладкой мускулатуры внутренних органов, запоры
на следующие сутки. Достоинством фентанила в случае передозировки является
кратковременность его действия. А также, если произошла остановка дыхания,
возможно "речевое управление дыханием", поскольку с пациентом
сохраняется речевой контакт и можно, подавая команды голосом: "Дышите!
Вдох! Выдох!", поддерживать адекватную вентиляцию.
Вместо
дроперидола (при отсутствии последнего) возможно применение 0.5 мл 1% р-ра аминазина.
Не потерял
значения метод аналгезии с использованием 70 -80% закиси азота с кислородом.
После
купирования интенсивных, т.н. "морфинных" болей для борьбы с
"остаточными" тупыми болями возможно применение клофелина. Клофелин
снижает уровень катехоламинов в крови, уменьшает потребность сердца в
кислороде, потенцирует действие аналгетиков, обладает самостоятельным
противошоковым действием. Рекомендуется применять клофелин по 1-2 таблетки под
язык или по 1.0 п/к (Шок уже был купирован!). Противопоказанием (относительным)
к клофелину является стойкая гипотония, когда систолическое АД ниже 100 мм
рт.ст.
Истинный кардиогенный шок (ИКШ)
Этиопатогенетическая терапия.
Идеальная
терапия должна увеличивать коронарный кровоток и одновременно снижать
потребность сердца в кислороде. Для этого проводится внутрикоронарный или
системный лизис тромбов. Раннее введение стрептокиназы или других
фибринолитических препаратов внутривенно или даже внутрикоронарно позволяет
добиться растворения тромба у 2/3 и даже у 3/4 больных. Это может привести к
восстановлению коронарного кровотока и предотвращает развитие кардиогенного
шока или облегчает выведение из шока.
Но эти
препараты эффективны, если тромболизис проводится в первые 3, максимум, 6 часов
с момента развития тромбоза. Позднее проведение тромболизиса может вызвать
активизацию перекисного окисления, развитие так называемого синдрома no-reflow,
который заключается в том, что, несмотря на восстановление проходимости крупных
сосудов, микроциркуляторный кровоток в миокарде не восстанавливается и явления
острой сердечной недостаточности (шок) не проходят и даже могут усилиться.
В больших
центрах, располагающих соответствующими техническими возможностями показано
хирургическое лечение.
Есть
литературные данные об эффективности
хирургического лечения у 60% больных острым инфарктом миокарда, который
осложнился шоком.
Патогенетическая и симптоматическая терапия.
При
истинном кардиогенном шоке в распоряжении медиков нет средств, которые бы,
воздействуя на основное звено патогенеза - снижение сердечного выброса, не
вызывали бы при этом повышения потребности сердца в кислороде. Катехоламины,
повышающие сократимость, воздействуя на b1-рецепторы, вызывают
одновременно увеличение потребности сердца в кислороде (очень опасно при остром
инфаркте!), кроме того, при шоке и так имеет место выраженная
гиперкатехоламинемия. Сердечные гликозиды, основным механизмом действия которых
является повышение входа кальция в клетку, не имеют точки приложения, поскольку
доказано, что в ишемизированной зоне в миокардиоцитах и так имеется избыток
ионов кальция, а избыточные ионы кальция, накапливаясь не в тех локусах
митохондрий, ведут не к повышению, а, наоборот, к снижению сократимости сердца,
способствуют развитию электрической нестабильности миокарда.
Нет
возможности при истинном кардиогенном шоке бороться с гиповолемией, вливая в
больших количествах жидкость в кровеносное русло, поскольку существует
серьезная опасность спровоцировать развитие отека легких. Поэтому обычная
рекомендация при лечении истинного кардиогенного шока ограничиваться суточным
количеством вводимой жидкости от 1.5 до 3.0 л.
Именно в
связи с этим лечение истинного кардиогенного шока до настоящего времени
является не только наукой, но и одним из высших проявлений врачебного
искусства.
При
лечении истинного кардиогенного шока рекомендуется следующая стратегия:
А. Введение b-1-адреномиметиков
Введение
этих препаратов, несмотря на очевидные противопоказания (гиперкатехоламинемия,
повышение потребности сердца в кислороде), основывается на следующих обстоятельствах:
1. Временное повышение
диастолического давления увеличит перфузионное давление в коронарных сосудах,
которые, как известно, снабжаются кровью в фазу диастолы, а временное повышение
давления в полости желудочков приведет к улучшению кровоснабжения сердца по
системе Тебезиевых сосудов, что может привести к уменьшению зоны периинфарктной
ишемии и к увеличению сократимости миокарда;
2. Временное повышение
сердечного выброса за счет положительного инотропного эффекта будет
способствовать увеличению скорости кровотока, может вызвать уменьшение
сладж-синдрома в капиллярном русле, уменьшить секвестрацию крови и увеличить
венозный возврат крови к сердцу, что, свою очередь, увеличит сократимость
миокарда по механизму Франка-Старлинга;
3. Вызванное временным
увеличением сократимости улучшение микроциркуляции будет способствовать
коррекции метаболических расстройств, в частности, ацидоза и его
неблагоприятных воздействий.
Препаратом
выбора из этой группы средств является раствор допамина, который обладает
следующими особенностями:
¨
в дозах до 5 мкг/кг/мин он действует на дельта-рецепторы, вызывая
улучшение микроциркуляции в почках, стимулируя диурез, даже при низком
фильтрационном давлении;
¨
в дозах 5-10 мкг /кг/мин проявляется их действие на b1-рецепторы, что приводит к
усилению насосной функции сердца, учащению сердечного ритма, увеличению
минутного объема кровообращения;
¨
в дозах от 10-15 мкг/кг/мин - наряду с действием на b1-рецепторы, начинает
выявляться и действие на a1 рецепторы, то есть, увеличивается
тоническое сокращение периферических артериол, повышается периферическое
сопротивление, растет нагрузка на миокард;
¨
в больших дозировках
превалирует только действие на a1 рецепторы, неблагоприятное
при большинстве видов шока.
Передозировка
допамина проявляется усилением бледности и цианоза, уменьшением пульсового
давления, сохранением всех периферических признаков шока, несмотря на возможное
повышение АД.
Недостаточная
доза будет проявляться отсутствием учащения ритма сердца, сохранением признаков
шока, дальнейшим снижением систолического давления.
Оптимальная
доза - потепление кожных покровов, увеличение пульсового давления, уменьшение
или исчезновение холодного пота и других вегетативных проявлений и т.д.
Сложность
и неоднозначность действия допамина требуют применения метода биологического
титрования при использовании этого препарата. Обычно, капельное вливание
допамина в дозе 5.0 мл 4% р-ра в 400 мл реополиглюкина начинают со скоростью
4-5 капель в минуту и, постепенно повышая скорость введения, оценивают
клинический эффект, который проявляется или в улучшении или в ухудшении
состояния. Скорость капельного вливания сохраняют на том уровне, когда был
получен наилучший клинический эффект. Не следует ориентироваться на уровень
артериального давления! Повышение
систолического давления одновременно с уменьшением пульсового давления -
показание к уменьшению скорости вливания
препарата.
Менее
эффективным препаратом из этой группы является норадреналин, который почти
лишен действия на b1-рецепторы, поэтому введение
его необходимо проводить с еще большей осторожностью и уменьшать скорость
введения при снижении пульсового давления.
Не
правильно назначать адреналин, который перераспределяет кровоток в сторону
скелетной мускулатуры и, тем более, мезатон, действующий только на a-рецепторы, еще больше угнетающий
микроциркуляцию и, как следствие, в конечном итоге, ведущий к снижению
венозного возврата к сердцу.
Б. Назначение больших доз глюкокортикостероидов.
В больших
дозах (от 5 до 30 мг/кг) глюкокортикоиды повышают тонус венул, уменьшая емкость
сосудистого русла, но, действуя на уровне венул, в отличие от катехоламинов, не
ухудшают микроциркуляцию, а даже улучшают ее.
Это
объясняется тем, что приток жидкости в капилляры не затруднен, а отток
несколько замедляется. Происходит разведение крови в капиллярах, агрегаты
форменных элементов начинают распадаться, снижается внутреннее трение,
увеличивается текучесть крови, увеличивается возврат крови к сердцу и, как
следствие, растет сердечный выброс.
Преднизолон
вводится внутривенно струйно в дозе 90-150 мг и затем внутривенно капельно в
дозе 300-600 мг, причем, эту дозу необходимо ввести в течение 4-6 часов. Более
эффективен в качестве противошокового препарата метипред, который обладает
менее выраженным минералокортикоидным эффектом. Он назначается в той же дозе,
что и преднизолон.
В. Введение противошоковых растворов.
При шоке
обязательно вводятся гипертонические растворы: 10% раствор глюкозы,
реополиглюкин. Назначение гипертонических растворов связано с двумя основными
факторами:
1. Повышение осмотического давления
в капиллярах ведет по механизму Старлинга к дополнительной мобилизации жидкости
из межтканевого пространства в сосудистое русло, что дополнительно уменьшает
гиповолемию, вызывает гемодилюцию, ведущую к уменьшению внутрисосудистой агрегации.
2. Гипертонические растворы
активизируют лимфообращение, что ведет к уменьшению отечности в периинфарктной
зоне, увеличению за счет этого сердечного выброса.
Препаратом
выбора при кардиогенном шоке является реополиглюкин. Эффект реополиглюкина
многообразен.
¨
Во-первых, 1 г реополиглюкина связывает 30-40 г воды, чем усиливает
гемодилюцию (разведение крови) и снижает вязкость крови.
¨
Во-вторых, вызывает дезагрегацию эритроцитов, увеличивая их
электрический отрицательный потенциал взаимного отталкивания.
¨
В-третьих, образует комплексное соединение с фибриногеном, связывает протромбин
и фактор YIII.
¨
В-четвертых, снижает липиды плазмы, что также противодействует
агрегации клеток.
¨
Кроме того, реополиглюкин является плазмозаменителем, улучшающим
кровообращение в системе микроциркуляции.
70%
препарата выделяется за сутки и 50% в первые 3 часа.
При
истинном кардиогенном шоке, к сожалению, приходится ограничивать количество
вводимой жидкости из-за опасности развития отека легких. Допустимое суточное
количество жидкости ~1.5 - 2.0 л + потери (рвота, потоотделение, диурез и т.п.)
Г. Введение вазодилататоров.
Введение
вазодилататоров при шоке является патогенетически обоснованным, ведь одним из
основных звеньев патогенеза является спазм периферических артериол. При
использовании вазодилататоров появляется возможность увеличить количество
вводимых противошоковых жидкостей. Наиболее показаны вазодилататоры при
сочетании шока с явлениями застоя в легких или отеком легких.
Лучше
использовать a-блокаторы, например,
дроперидол в дозе до 10-20 мл/сут (по 1.0 мл каждые 1.5 - 2 часа). Возможно
применение малых доз аминазина (по 0.5 мл каждые 3-4 часа). Можно использовать
празозин. Допустимо в качестве вазодилататора использовать малые дозы нифедипина
(5-15 мг/сут.)[4].
При
использовании вазодилататоров необходимо
ориентироваться не на уровень артериального давления, а только на клинический
эффект. Если появятся признаки улучшения микроциркуляции: повысится
температура и уменьшится мраморность кожи и цианоз, возрастет пульсовое
давление и т.д., введение вазодилататоров следует продолжить. Если же клинический
эффект будет неудовлетворительным, то не следует упорствовать. Значит, в этом
конкретном случае, снижение системного давления привело к снижению перфузии
коронарных сосудов.
Д. Коррекция кислотно-щелочных нарушений.
Показанием
для введения бикарбоната натрия (соды) в количестве 100-200 мл 8.4% раствора
является снижение pH крови ниже 7.0. При отсутствии возможности определения pH
допустимо ориентироваться на клинические показатели.
Если шок
продолжается более 2-х - 3-х часов, при этом отмечается толерантность к
проводимой терапии b-симпатомиметиками, то
вполне обосновано введения 100 мл 8.4% р-ра соды или трисамина.
Нередко
своевременная коррекция избыточного ацидоза приводит к восстановлению нормальной
реакции на вводимые симпатомиметики и купированию шока.
Е. Вспомогательное кровообращение.
При
отсутствии эффекта от медикаментозной терапии можно прибегнуть к методике
внутриаортальной контрпульсации. Принцип метода заключается в том, что через
бедренную артерию в нисходящий отдел аорты вводится зонд-баллон объемом 30-50
мл, который раздувается в фазу диастолы. Тем самым повышается давление выше
баллона, т.е. повышается перфузионное давление в коронарных сосудах, за счет
чего может быть уменьшена зона инфаркта. Спадение баллона в фазу систолы
снижает постнагрузку на миокард.
Своевременное
(в первые 12 часов шока) применение этого метода позволяет наполовину снизить
летальность при шоке. Но если в течение 3-х суток у больного не
восстанавливается гемодинамике при пробном отключении аппарата, дальнейшее
лечение признается бесперспективным.
Лечение ареактивного шока
Ареактивность
можно объяснить двумя основными причинами:
¨
выраженный некоррегированный ацидоз,
¨
большой размер некроза и периинфарктной ишемии.
Лечение
ареактивного кардиогенного шока не отличается от истинного кардиогенного шока,
но повышается значимость своевременной коррекции ацидоза и хирургического
лечения.
Лечение аритмического шока
|
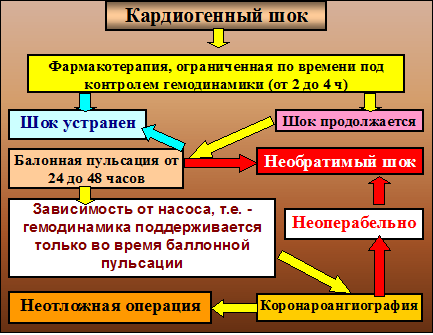
Рисунок 5 Схема лечения кардиогенного шока (по M.McEnany и E.Austin)
|
При
тахисистолических формах нарушения ритма патогенетически наиболее обосновано
раннее применение электрической кардиоверсии. И только, если нет возможности
провести электроимпульсную терапию, наиболее безопасную с точки зрения отрицательного
влияния на сократительную функцию сердца, проводят медикаментозную терапию (лидокаин,
новокаинамид, блокаторы кальциевых каналов, кордарон и т.д.)
При шоке,
который развился на фоне нарушений проводимости, показана электростимуляция.
При
аритмическом варианте кардиогенного шока восстановление сердечного ритма ведет
к восстановлению гемодинамики.
При
необходимом техническом оснащении может применяться следующая схема лечения
кардиогенного шока (по M.McEnany и E.Austin) (Рисунок 5)
Лечение анафилактического шока
Основным
лекарственным препаратом, применяемым при лечении анафилактического шока,
является адреналин, (Таблица 1)который восполняет относительный
дефицит катехоламинов в конкуренции за рецепторы с гистамином и другими
биологически активными веществами.
Таблица 1 План мероприятий в зависимости от пути поступления антигена
|
Подкожная инъекция
|
Внутримышечная инъекция
|
Внутривенное вливание
|
Капельное вливание
|
|
1. Жгут выше места инъекции
2. Обколоть место инъекции адреналином (4-6 инъекций по
0.3 мл)
|
1. Обколоть место инъекции
адреналином (4-6- инъекций по 0.3 мл)
|
1. Прекратить вливание
2. Отсоединить шприц. (Игла
остается в вене!)
|
1. Прекратить вливание
2. Отсоединить капельницу.
(Игла остается в вене!)
|
Следующие
мероприятия проводятся независимо от пути поступления антигена.
1. Внутривенно струйно 0.3 -
0.5 мл адреналина.
2. Наладить капельное вливание.
Лучше использовать коллоидные растворы: реополиглюкин (самое лучшее),
полиглюкин, желатиноль. Но при отсутствии этих препаратов, возможно
использование любого раствора для внутривенных вливаний (физиологический
раствор, глюкоза 5, 10 или 20% и др.). Объем первоначально вводимой жидкости 400.0.
3. В эту капельницу добавить
8.0 мл 0.1% раствора адреналина. Капельное вливание проводить со скоростью 100
капель в 1 минуту (0.1 мл адреналина /мин) до стабилизации гемодинамики:
отчетливый пульс, исчезновение цианоза, систолическое АД выше 90-100 мм рт.ст[5]. После этого переходят на
капельное вливание со скоростью 20-30 капель в 1 минуту, но при необходимости
опять увеличивают скорость введения.
4. Внутривенно струйно вводят
180-300 мг преднизолона (6-10 ампул).
Капельное вливание
прекращают, если АД остается стойко нормальным или при капельном вливании АД
повышается выше нормы (из-за адреналина). В течение суток больному вводят при
необходимости глюкокортикоиды внутривенно до 1000 - 1500 мг в сутки или per os
до 300-600 мг/сут.
5. Если имеется нейтрализатор
антигена, то применяют его. Например, при шоке, вызванном пенициллином, вводят
пенициллиназу.
Анафилактический
шок из-за особенностей патогенеза является самым тяжелым, т.к. при нем
невозможно развитие централизации кровотока, быстро падает венозный возврат
крови к сердцу и наступает смерть (молниеносная форма шока). В этом случае
проводятся реанимационные мероприятия в полном объеме, но на фоне проводимой
терапии адреналином.
Необходимо,
чтобы в каждом отделении больницы имелись наборы для проведения неотложных
противошоковых мероприятий. Этот набор содержит
¨
разовую капельницу,
¨
10 ампул адреналина,
¨
флакон реополиглюкина,
¨
10 ампул преднизолона и
¨
флакон пенициллиназы.
Ни в коем
случае не следует проводить лечение анафилактического шока в иной
последовательности. Только наладив капельное вливание адреналина, можно
переходить к использованию других препаратов, поскольку промедление в этом
случае с восстановлением гемодинамики, действительно, смерти подобно!
Персонал
больницы должен четко знать свои функциональные обязанности по выведению из
анафилактического шока:
¨
медсестра должна самостоятельно диагностировать шок, прекратить
внутривенное или капельное вливание, отсоединив шприц или систему, но, оставив
иглу в вене, и вызвать реаниматолога;
¨
врачу необходимо твердо помнить, что основной метод лечения анафилаксии
- это введение адреналина и только потом иных медикаментов;
¨
реаниматолог, несмотря на предшествующий шок, должен проводить
реанимационные мероприятия, т.к. это единственный вид шока, при котором
реанимация показана и может быть эффективной.
¨
Весь персонал должен знать, где хранятся противошоковые наборы.
Несоблюдение
любого из этих правил приводит к смерти больного, причем, по вине медицинского
персонала.
Лечение инфекционно-токсического шока
Основной
метод лечения ИТШ - это инфузионная терапия: реополиглюкин, в меньшей степени
полиглюкин, возможно применение плазмы, альбумина и др. Суточное количество
вводимой жидкости может быть довольно большим (до 6 и более литров), поскольку,
проводя такую терапию, мы осуществляем и дезинтоксикацию и борьбу с
гиповолемией.
При
"теплой" форме шока внутривенно капельно вливается допмин в дозе до
10 мкг на кг/мин, а при "холодной" форме в сочетании с вазодилататорами:
малыми дозами ганглиоблокаторов, празозина или дроперидола и др.
Патогенетически
обоснованным для борьбы с анафилаксией (основное звено патогенеза), а также для
профилактики развития и лечения шокового легкого является использование больших
доз глюкокортикоидов (600-1500 мг преднизолона в сутки).
Учитывая,
что одной из причин развития ИТШ является массивная гибель микроорганизмов,
прекращают на время введение бактерицидных препаратов и переходят на
бактериостатические средства.
Одним из
тяжелых и, к сожалению, нередких осложнений ИТШ является синдром дессиминированного
внутрисосудистого свертывания, поэтому для профилактики этого в комплексе с
другими лечебными мероприятиями обязательно используется гепарин в суточной
дозе 20-25 тыс. ед.
Для борьбы
с действием протеолитических ферментов рекомендуется использовать ингибиторы
протеаз: контрикал (трасилол, гордокс) внутривенно капельно в максимальных
дозах.
Лечение гиповолемического шока
Главное -
это введение жидкости для восполнения потерянного объема. Основное правило при
этом шоке: вводить жидкости столько, сколько необходимо.
Препаратом
выбора является полиглюкин, который долго удерживается в сосудистом русле и
прекрасно выполняет свою основную задачу восполнения потерь. Правда,
рекомендуется начинать инфузионную терапию все равно с реополиглюкина (400-800
мл) для того, чтобы улучшить микроциркуляцию и вовлечь в кровоток
секвестрированную кровь. Скорость введения жидкости должна быть большой.
Желательно вводить ее в две, а иногда и в четыре центральных вены до тех пор,
пока не исчезнут признаки гиповолемии. Единственным ориентиром для регуляции
скорости введения жидкости является динамика изменения центрального венозного
давления. Скорость введения жидкости максимальна при отрицательном ЦВД и когда
оно ниже 60 см водного столба (возможно даже струйное вливание). Скорость
вливания уменьшают при ЦВД 60-120 см вод.ст. и при дальнейшем увеличении ЦВД,
особенно при быстром росте ЦВД вливание прекращают или существенно замедляют.
Клинические признаки повышения ЦВД:
¨
набухание шейных вен,
¨
появление или усиление одышки,
¨
появление влажных хрипов в легких.
Высокое
ЦВД - показание к применению вазодилататоров (нитропруссид натрия, празозин,
дроперидол).
При
выраженных расстройствах гемодинамики и для профилактики развития шоковой почки
на начальном этапе возможно кратковременное применение допмина, который вливают
со скоростью 5-10 мкг/кг/мин.
Если шок
развился от кровопотери, нет необходимости спешить с переливаниями эритромассы [6]. Дело в том, что в
организме в депо содержится столько же эритроцитов, сколько и в циркулирующей крови.
Эти эритроциты находятся в обезвоженном состоянии и не участвуют в кровотоке.
Но как только развивается гемодилюция (разведение крови), эти эритроциты возвращаются
в кровеносное русло. Поэтому абсолютным показанием к переливанию эритромассы
является острое снижение уровня гемоглобина ниже 60 г/л. Относительным
показанием к переливанию эритромассы является снижение гемоглобина ниже 80 г/л.
Но переливание эритромассы (особенно при относительных показаниях) проводится
уже после стабилизации гемодинамики.
Вопросы
Пояснение: За каждым из пронумерованных вопросов или
незаконченных утверждений следуют обозначенные буквами ответы или
пронумерованные утверждения. Выберите обозначенный буквой ответ или завершенное
утверждение, которые лучше всего подходят для каждого случая. ПРАВИЛЬНЫХ
ВАРИАНТОВ МОЖЕТ БЫТЬ БОЛЬШЕ ОДНОГО.
1.
При любом шоке ВСЕГДА развивается
A.
Спазм артериол
B.
Расширение артериол
C.
Гиповолемия
D.
Повышение проницаемости микрососудов в направлении тканей
E.
Централизация кровотока
2.
Поставьте в соответствие основное звено патогенеза и вид шока
A.
Кардиогенный
B.
Анафилактический
C.
Инфекционно токсический (теплый)
D.
Инфекционно токсический (холодный)
E.
Гиповолемический
F.
Рефлекторный (болевой)
i)
Секвестрация крови в микроциркуляторном русле в связи с
генерализованным спазмом периферических сосудов
ii)
Генерализованное расширение артериол
iii)
Значительная потеря жидкости
iv)
Снижения сердечного выброса
3.
Выберите лечебные мероприятия, с которых надо начинать лечение шока
A.
Кардиогенный
B.
Анафилактический
C.
Инфекционно токсический (теплый)
D.
Инфекционно токсический (холодный)
E.
Гиповолемический
F.
Рефлекторный (болевой)
i)
Вливание допмина со скоростью 5-10 мкг./кг в мин
ii)
Вливание адреналина внутривенно
iii)
Вливание 400 мл реополиглюкина и 800 мл полиглюкина
iv)
Вливание больших количеств реополиглюкина
v)
Вливание преднизолона в дозе 5-30 мг/кг
vi)
Проведение нейролептаналгезии
vii)
Интенсивная антибиотикотерапия с учетом чувствительности микроорганизмов
viii)
Проведение внутриаортальной контрпульсации
4.
Рекомендуемое суточное количество введенной жидкости при шоке
A.
Кардиогенный
B.
Анафилактический
C.
Инфекционно токсический (теплый)
D.
Инфекционно токсический (холодный)
E.
Гиповолемический
F.
Рефлекторный (болевой)
i)
Противошоковые растворы можно не использовать
ii)
Скорость введения жидкости и ее количество регулируются в зависимости
от уровня центрального венозного давления.
iii)
Количество введенной жидкости не имеет решающего значения и вливание
можно прекратить после стабилизации гемодинамики
iv)
Вводится не более 1,5-3,0 л жидкости
v)
Количество жидкости ограничивается количеством потерь (литр на литр)
[1]
Автор термина Knisely (1936), наблюдая микроциркуляцию в брыжейке
лягушки при шоке, отметил выпадение в осадок агрегатов форменных элементов,
подобно тому, как оседает ил на дно пруда
[2] Толстыми стрелками на
рисунке обозначены звенья патогенеза, которые приводят к нарастанию гиповолемии
и формированию порочного круга патогенеза шока.
[3] Это, так
называемая, коагулопатия потребления
[4]
Не следует использовать венозные дилататоры, типа нитроглицерина,
которые действуют прямо противоположным образом, в сравнении с глюкокортикоидами.
С этой же точки зрения, видимо, не совсем удачным является нитропруссид натрия,
рекомендуемый многими авторами, который также снижает тонус венул.
[5] В случае отсутствия
растворов для вливаний нужно вводить адреналин внутривенно струйно по 0.1 мл
каждую минуту.
[6]
Показаний к переливанию цельной крови не существует!