Экспериментальная часть
2.1 Введение в эксперимент
Рассматривая возможность
применения диатомита для мелиорации и реанимации антропогенно нарушенных почв,
необходимо принимать во внимание, что глинистые минералы являются постоянным
компонентом породы. По данным многочисленных исследований алюмосиликатная
составляющая почвенного поглотительного комплекса (ППК) и минералы гидроокислов
железа при кислой реакции среды становятся источником подвижных форм алюминия и
железа, которые оказывают прямое токсичное воздействие на растения и
способствуют дальнейшему снижению
pH почвенного раствора.
Высокая пористость диатомита и
хорошие адсорбционные характеристики предполагают его участие в процессах
поглощения катионов из раствора, а значит и создания кислотно-основной
буферности почв. Именно поэтому мы поставили перед собой задачи:
·
экспериментально определить возможный выход
алюминия и железа из диатомита при различных значениях pH раствора извлечения,
·
исследовать способность к адсорбции катионов из
раствора и связанное с ней буферное
действие породы.
Для расчёта относительного выхода
исследуемых элементов в раствор необходимы данные об их валовом содержании в
породе, и в начале был определён химический состав исследуемых образцов
диатомита.
В ходе экспериментов были
получены данные, отражающие взаимодействие различных компонентов диатомита
(твёрдой фазы) с катионами раствора извлечения. Отслеживались следующие
параметры: pH раствора
извлечения, pH соляной
вытяжки (фильтрата), концентрации ионов Al3+и Fe3+. На основе полученных
экспериментальных данных рассчитывались показатели относительного выхода
алюминия и железа в раствор.
2.2. Материал и методы исследования
Материалом для
исследования послужил диатомит, добываемый на первом участке Инзенского
месторождения Ульяновской области (его светлая разность).
Химический состав исследуемого
диатомита был определён методом
рентгеноспектрального анализа, используемый для определения
макрокомпонентов. Он основан на измерении флуоресцентного излучения
определяемых элементов в пробе, приготовленной сплавлением с тетраборатом лития
при t=1150°.
В ходе экспериментов проводилось фотоколориметрическое определение ионов
Al3+и Fe3+ в исследуемых растворах. В основе метода лежит
образование окрашенных комплексных соединений солями алюминия и трёхвалентного
железа с веществами-красителями. Интенсивность окрашивания измеряется
оптической плотностью D,
которая в свою очередь определяется содержанием исследуемых веществ в
растворах. Для измерения оптической плотности был задействован фотоэлектроколориметр
КФК-2. Определение концентраций алюминия и железа осуществлялось методом построения градуировочных графиков.
Он предполагает приготовление шкалы растворов сравнения с известными
концентрациями этих элементов, определение их оптической плотности и построение
на основе полученных данных калибровочных кривых. Они дают возможность, зная
величину D, установить
значение CAl3+
или CFe3+.
Фотоколориметрия является одним
из наиболее чувствительных и широко используемых методов определения металлов в
природных водах и почвенных растворах. Содержание Al3+определялось по
стандартной методике с ксиленоловым оранжевым [32, 231], Fe3+ – сульфосалициловым
методом.[34, 96].
Измерение рН исследуемых растворов проводилось
потенциометрическим методом. Для этого использовали лабораторный рН-метр
ЛПУ-01 с хлорсеребряным и стеклянным электродами соответственно в качестве
электрода сравнения и измерительного электрода.
Оборудование
и реактивы
Эксперименты проводились с
использованием следующего лабораторного оборудования:
·
Аквадистиллятор ДЭ-4-2;
·
Аппарат для встряхивавния АВУ-6с;
·
Весы аналитические;
·
Весы лабораторные равноплечие 2 класса ВЛР-200;
·
Весы торсионные ВТ-500;
·
Колориметр фотоэлектрический концентрированный
КФК-2;
·
Кюветы с толщиной просвечивающего слоя 1 см;
·
Лабораторный рН-метр ЛПУ-01;
·
Шкаф вытяжной;
·
Шкаф сушильно-стерилизационнный ШСС-80п;
·
Штатив лабораторный ШЛ-02;
·
Электропечь сопротивления, камерная лабораторная
СНОЛ-1,6.2,5 111ИЗ;
и реактивов:
·
Алюминий металлический х.ч. (по ГОСТ 13736-68)
·
Аммиак водный ч.д.а.
·
Железоаммонийные квасцы ч.
·
Калий фосфорнокислый однозамещённый ч.
·
Калий хлористый х.ч.
·
Калий щавелекислый ч.
·
Кислота аскорбиновая х.ч.
·
Кислота серная ч.д.а. (ρ=1,83)
·
Кислота соляная ч.д.а. (ρ=1,19)
·
Кислота сульфосалициловая х.ч.
·
Кислота уксусная, ледяная х.ч.
·
Ксиленоловый оранжевый ч.д.а.
·
Натрий фосфорнокислый двузамещённый ч.
·
Натрий тетраборнокислый ч.
2.3 Методики проведения экспериментов
1. Нами была разработана методика
определения выхода алюминия и железа из диатомита в зависимости от рН раствора
извлечения.
Д. С. Орловым было показано, что
при трансформации поверхностных слоёв кристаллической решётки алюмосиликатов и
растворении минералов гидроксида железа в растворе появляются вместе с простыми
ионами Al3+и Fe3+ гидроксокомплексы переменной
основности [36, 28]. Концентрация и формы
соединений алюминия и железа регулируются главным образом степенью кислотности
или щёлочности раствора [28,
126]. Их состав и роль в почвенно-химических процессах ещё недостаточно
изучены, поэтому мы сочли нужным определять выход алюминия и железа из
диатомита по концентрации простых ионов, для которых разработан ряд стандартных
методик.
Чтобы подавить реакции гидролиза
этих элементов в качестве раствора извлечения был взят 1 М раствор KCl – нейтральной соли, полностью
диссоциирующей на ионы в растворе и не оказывающей влияние на его реакцию.
Нужные значения рН раствора устанавливались с помощью сильноразбавленных
растворов соляной кислоты и аммиака.
Для проведения опытов брались
навески порошка нативного диатомита и диатомита, прокалённого в муфельной печи
при 850°С в течение 4 часов, массой 10 г. Взвешивание производилось на
лабораторных весах ВЛР-200. Навески помещали в 50 мл раствора с измеренным рН.
Опытным путём было установлено, что рН суспензии устанавливается приблизительно
в течение получаса, эта цифра и была выбрана в качестве времени экспозиции tэкс. Через 0,5
часа постоянного перемешивания с использованием аппарата для встряхивания
исследуемую суспензию пропускали через бумажный фильтр, затем определяли рН
фильтрата и концентрации ионов Al3+и Fe3+
(С Al3+ и С Fe3+ ).
По данным валового химического
состава рассчитывались показатели относительного выхода алюминия и железа из
диатомита (в пересчёте
на 100 г породы и в массовых процентах).
2. Кроме того, в серии опытов
исследовалось поглощение нативным диатомитом алюминия из раствора AlCl3 и влияние
порошка на значение рН раствора. Раствор соли готовился как один из рабочих
растворов сравнения по методике определения алюминия с ксиленоловым оранжевым [32, 231]
(с 1 М раствором KCl в
качестве растворителя для предотвращения гидролиза). Концентрация Al3+ в нём составила
0,0086 мг/см3. Подкисляя и подщелачивая исходный раствор с
помощью сильноразбавленных растворов соляной кислоты и аммиака, мы получили
серию растворов извлечения с известными значениями рН и концентрации алюминия.
Соотношение масса порошка/объём раствора и время
экспозиции – те же, что при определении выхода алюминия в зависимости от рН
раствора извлечения. Пропустив исследуемую суспензию через бумажный фильтр,
проводили определение рН фильтрата и концентрации в нём ионов Al3+
(С Al3+).
Определение
содержания алюминия в исследуемых растворах
Алюминий в растворе образует комплекс с ксиленоловым
оранжевым алого цвета., поэтому CAl3+ определяется
по интенсивности окрашивания, возникающего при прибавлении к анализируемой
пробе раствора этого красителя. Чтобы устранить мешающее влияние ионов Fe3+, которые
также способны реагировать с ксиленоловым оранжевым, перед окрашиванием
раствора к нему приливают раствор аскорбиновой кислоты, восстанавливающей
железо до трёхвалентного состояния. Интенсивность окрашивания измеряется
оптической плотностью D,
которая в свою очередь определяется концентрацией Al3+ в растворах. Для
измерения оптической плотности используют фотоэлектроколориметр КФК-2.
Предварительно готовят и
окрашивают рабочую шкалу растворов сравнения для построения калибровочной
кривой, отражающей зависимость оптической плотности раствора от содержания в
нём алюминия.
Исходный образцовый раствор
алюминия с СAl3+ 0,1 мэкв/см3
(0,9 мг/см3),
необходимый для приготовления образцовых растворов, запасной окрашивающий
раствор и раствор аскорбиновой кислоты готовят по методике определения алюминия
с ксиленоловым оранжевым [32,
231].
Приготовление образцовых
растворов алюминия:
а) исходного: 0,450 г металлического алюминия, взвешенного с точностью
0,001 г, помещают в мерную колбу вместимостью 500 см3. Туда же
приливают 10 см3 разбавленной соляной кислоты. Колбу закрывают
клапаном Бунзена и после прекращения бурного выделения водорода ставят на
кипящую водяную баню до полного растворения алюминия. Затем колбу с раствором
охлаждают и добавляют 37,5 г хлористого калия. Объём раствора доводят до метки
дистиллированной водой и перемешивают. Полученный раствор содержит 0,1 мэкв/см3 (0,9 мг/см3) алюминия в виде иона Al3+ и может
храниться в склянке с притёртой крышкой в течение одного месяца.
б) рабочего: берут 25 см3 исходного образцового раствора,
приливают в мерную колбу на 250 см3, доводят объём до метки 1 М раствором
KCl. Концентрация Al3+ в полученном
растворе 0,09 мг/см3.
Приготовление шкалы
образцовых растворов алюминия.
Рабочую шкалу растворов сравнения
готовят в мерных колбах вместимостью 100 см3, отбирая мерной
пипеткой следующие объёмы рабочего образцового раствора, указанные в таблице
2.1.
Таблица
2.1
Приготовление шкалы образцовых
растворов алюминия
|
№ раствора
|
1
|
2
|
3
|
4
|
|
Объём рабочего р-ра, мл
|
0
|
4
|
12
|
24
|
|
С Al3+, мг/см3
|
0
|
0,0036
|
0,0108
|
0,0216
|
Содержимое колб доводят 1 М
раствором KCl до метки
и тщательно перемешивают.
Приготовление
окрашивающих растворов:
а) запасного: в небольшом
количестве дистиллированной воды растворяется 10.9 г уксуснокислого натрия,
взвешенного с погрешностью не более 0.1 г. Полученный раствор заливают в колбу
на 1000 мл, добавляют 500 мл дистиллированной воды и 58 мл концентрированной
уксусной кислоты и перемешивают. Затем добавляют растворенные в воде 0.4 г
ксиленолового оранжевого, взвешенного с погрешностью не более 0.01 г и доводят
дистиллированной водой до метки.
б) рабочего:
он готовится посредством разведения запасного окрашивающего раствора в 5 раз
дистиллированной водой.
Рабочий окрашивающий раствор и
0,02% раствор аскорбиновой кислоты готовят непосредственно в день проведения
опытов.
Реактивы:
1. алюминий металлический;
2. калий хлористый, 1М раствор;
3. кислота аскорбиновая, 0,02% – ный
раствор;
4. кислота соляная, разбавленный (3:2)
раствор;
5. рабочий образцовый раствор алюминия с CAl3+ 0,01 мэкв/см3;
6. рабочий окрашивающий раствор с
ксиленоловым оранжевым;
Ход определения
К 2 см3 фильтрата
прибавляют 15 см3 раствора аскорбиновой кислоты (реактива 3) и
содержимое перемешивают. Затем добавляют 15 см3 окрашивающего
раствора (реактива 6) и снова перемешивают. Устойчивое окрашивание наступает
не ранее чем через 2 часа после его прибавления.
По прошествии этого времени
проводят фотометрирование исследуемого раствора в кювете с толщиной
просвечивающего слоя 1 см относительно шкалы раствора сравнения №1 при
λ=540 нм.
Приготовление
и окрашивание, а затем и фотометрирование рабочей
шкалы растворов сравнения производится по аналогичной схеме: 2см3
раствора из шкалы образцовых растворов+15 см3 реактива 3+15см3
реактива 6. Полученные значения D наносят на график против соответствующих
концентраций алюминия в мг/см3, и на основе этих данных строится калибровочная кривая, по которой и определяется CAl3+ в
фильтратах.
Погрешность измерения оптической
плотности на КФК-2 составляет 0,5% (±0,005).
Таблица 2.2.
Зависимость оптической
плотности растворов сравнения от концентрации ионов Al3+
|
№ раствора
|
1
|
2
|
3
|
4
|
|
С Al3+, мг/см3
|
0
|
0,0036
|
0,0108
|
0,0216
|
|
D
|
0
|
0,045
|
0,125
|
0,182
|
Определение
содержания железа и в исследуемых растворах
Сульфосалициловая кислота
образует с солями железа окрашенные комплексные соединения, причём в
слабокислой среде она реагирует только с ионами Fe3+ (красное окрашивание). Концентрация железа (III)
в фильтратах определяется по интенсивности окрашивания, возникающего при
прибавлении к анализируемой пробе раствора этого красителя. Интенсивность
окрашивания измеряется оптической плотностью D, которая в свою очередь определяется концентрацией Fe3+ в растворах.
Для измерения оптической плотности используют фотоэлектроколориметр КФК-2.
Слабокислая реакция в исследуемой
пробе создаётся с помощью разбавленных растворов соляной кислоты и аммиака.
Предварительно готовят и
окрашивают рабочую шкалу растворов сравнения для построения калибровочной
кривой, отражающей зависимость оптической плотности раствора от содержания в
нём железа.
Стандартный раствор железа с
СFe3+ 0,1 мг/см3, необходимый для
приготовления образцовых растворов,
готовят согласно методике определения содержания трёхвалентного железа
сульфосалициловым методом [34,
96].
Приготовление стандартных растворов железа:
а) запасного: растворяют 0.8634 г
железо-аммонийных квасцов
Fe(NH4)
(SO4)2·12 H2O в мерной колбе вместимостью 1 л в небольшом
количестве дистиллированной воды, добавляют 10 мл крепкой серной кислоты и
доводят объём раствора до метки; 1 мл раствора содержит
0.1 мг Fe.
б) рабочего: 50 мл запасного стандартного раствора
разбавляют до 1 л дистиллированной водой, каждый раз приготовляют свежий
раствор; 1 мл раствора содержит 0.005 мг железа.
Приготовление шкалы
стандартных растворов железа.
В мерные колбы емкостью 50 мл отмеривают от 0 до 20
мл рабочего стандартного раствора железа и доводят объемы дистиллированной
водой до метки.
Таблица
2.3
Приготовление шкалы стандартных
растворов железа
|
№ раствора
|
1
|
2
|
3
|
4
|
5
|
|
Объём рабочего р-ра, мл
|
0
|
5
|
10
|
15
|
20
|
|
С Fe3+, мг/л
|
0
|
0,5
|
1,0
|
1,5
|
2,0
|
Реактивы:
1. аммиак, разбавленный (2:3) раствор;
2. кислота соляная, разбавленный (3:2)
раствор;
3. рабочий стандартный раствор железа с CFe3+ 0,005
мг/см3;
4. сульфосалициловая
кислота, 10 %-ный раствор;
Ход
определения
В колбу емкостью 50 мл наливают 20 мл
анализируемого раствора, затем прибавляют пипеткой 2 мл раствора
сульфосалициловой кислоты и, в зависимости от рН фильтрата, раствор соляной
кислоты или аммиака; затем содержимое колбы тщательно перемешивают. Спустя 10
мин оптическую плотность окрашенного раствора измеряют с помощью КФК-2 на длине
волны l=536—540 нм.
Приготовление
и окрашивание, а затем и фотометрирование
рабочей шкалы растворов сравнения производится
по аналогичной схеме: 20см3 стандартного раствора +
раствор сульфосалициловой кислоты и другие реактивы. Полученные значения D наносят на график против соответствующих
концентраций железа в мг/л, и на основе этих данных строится калибровочная кривая, по которой
определяют содержание трёхвалентного железа в фильтратах. Если значение
оптической плотности исследуемого раствора выходит за пределы, обозначенные на
графике, пробу следует разбавить и провести повторное фотометрирование.
Погрешность измерения оптической плотности на КФК-2
составляет 0,5% (±0,005).
Таблица 2.4
Зависимость оптической
плотности растворов сравнения от концентрации ионов Fe3+
|
№ раствора
|
1
|
2
|
3
|
4
|
5
|
|
С Fe3+, мг/л
|
0
|
0,5
|
1,0
|
1,5
|
2,0
|
|
D
|
0
|
0,014
|
0,030
|
0,035
|
0,050
|
Определение значения рН исследуемых
растворов
Во всех вышеперечисленных опытах
вместе с определением концентраций ионов Al3+ и Fe3+
в исследуемых растворах изучалось влияние порошка диатомита на реакцию
раствора. Проводилось измерение значений рН растворов извлечения и фильтратов
потенциометрическим методом, и затем вычислялось ΔрН по формуле:
ΔрН=рНисх-рНф, где рНисх
– значение рН раствора извлечения,
рНф –
значение рН фильтрата.
Замеры рН проводились с
использованием лабораторного рН-метра ЛПУ-01 с хлорсеребряным и стеклянным
электродами соответственно в качестве электрода сравнения и измерительного
электрода.
Нужное значение рН раствора
извлечения в диапазоне от 1 до 13 устанавливалось путём прибавления к 1 М
раствору хлористого калия разбавленных растворов соляной кислоты или аммиака.
Настройка рН-метра проводилась по буферным
растворам с рН 1.68 (0,05 М раствор тетраоксалата калия), 6,86 (0,025 М раствор
калия фосфорнокислого однозамещённого и 0,025 М раствор натрия фосфорнокислого
двузамещённого) и 9,18 (0,01 М раствор натрия тетраборнокислого).
|
Погрешность измерения рН:
|
в диапазоне рН 2-14 – ±0,04
в диапазоне рН -2-14 – ±0,40
|
2.4 Результаты исследований и обсуждение
Валовый химический состав
исследуемого диатомита
По данным рентгеноспектрального анализа диатомит
Инзенского месторождения, послуживший материалом для наших исследований, имеет
химический состав, приведённый в таблице 2.5.
Таблица 2.5
Химический состав диатомита Инзенского месторождения Ульяновской
области
|
Содержание,
в % на сухую породу.
|
|
Na2O
|
MgO
|
Al2O3
|
SiO2
|
P2O5
|
SO2
|
K2O
|
CaO
|
TiO2
|
Fe2O3
|
|
0,01
|
0,07
|
5,35
|
90,20
|
0,09
|
0,03
|
0,12
|
0,70
|
0,12
|
3,22
|
По сравнению с цифрами,
приведёнными в литературе, эта партия характеризуется повышенным содержанием
кремнезёма (90,2% против 88,15% по данным У. Г. Дистанова; см. таблицу 1.1).
Содержание полуторных окислов – в пределах среднего.
Опираясь на данные о содержании глинистого материала в
породе, приводимые У. Г. Дистановым и другими авторами [25, 27], можно считать эти цифры
косвенным подтверждением высокого содержания опалового кремнезёма в породе.
На основе полученных данных было
рассчитано, что в 100 г диатомита в среднем содержится 2,83 г Al и 1,127 г Fe.
Выход алюминия из диатомита в
зависимости от значения рН раствора извлечения
А) В ходе серии экспериментов
было установлено, что нативный диатомит становится источником алюминия только
при рН раствора извлечения менее 5,72 (±0,04) (интервал значений рНисх 1 – 10), а с уменьшением значения рН выход алюминия в раствор
возрастает.
В) Для диатомита, прокалённого
при 850°С, появление Al3+
в растворе отмечалось при рН<4,8.
Данные, отражающие зависимость CAl3+ в
фильтрате от рН раствора извлечения, приведены в таблицах 2.6 и 2.7 и отражены
на графиках, представленных на рисунках 2.1 и 2.2.
Таблица
2.6
Зависимость выхода алюминия от значения рН раствора извлечения для
нативного диатомита
|
рН исх
|
1,02
|
1,94
|
2,70
|
4,01
|
5,72
|
6,07
|
8,30
|
9,60
|
|
CAl3+,
мг/см3
|
0,0175
|
0,0129
|
0,0033
|
0,0011
|
0,0000
|
0,0000
|
0,0000
|
0,0000
|
Таблица 2.7
Зависимость выхода алюминия от рН раствора
извлечения для диатомита, прокалённого при 850°С
|
рН исх
|
1,08
|
2,15
|
3,12
|
4,80
|
5,72
|
6,48
|
8,30
|
9,60
|
|
CAl3+, мг/см3
|
0,0186
|
0,0109
|
0,0038
|
0,0000
|
0,0000
|
0,0000
|
0,0000
|
0,0000
|
В породе Al2O3 находится в
связанном состоянии в составе кристаллической решётки глинистых минералов –
гидрослюды и монтмориллонита.
Многочисленные исследования
механизма взаимодействия слоистых алюмосиликатов с протонами показывают, что
многие из них практически невозможно получить в моноионной Н+-форме,
так как они самопроизвольно и немедленно становятся насыщенными Al [36, 98], то есть в них он
занимает обменные позиции и способен переходить в раствор.
Д. С. Орлов, Т. А. Соколова и др.
объясняют этот факт разрушением кристаллической решётки минералов в ходе
реакций протонирования (см. рис. 1.8.). При действии на кристаллиты кислых
водных растворов (в природе или лаборатории) катионы оснований Mex+ вытесняются и замещаются на
ионы H+. В
первую очередь протоны реагируют с гидроксильными группами октаэдрического
слоя, находящимися на её боковых сколах. Но, имея достаточно малый радиус, они
сравнительно легко мигрируют внутрь кристаллической решётки, а также могут
взаимодействовать с ОН-группами, расположенными «на дне» гексагональных пустот
тетраэдрической сетки, если глинистый минерал характеризуется подвижной
решёткой. В гидрослюде калий с трудом вытесняется из своих обменных позиций,
связь между пакетами достаточно прочная, поэтому при слабо- и среднекислом рН
раствора взаимодействие с протонами ограничено поверхностными слоями
кристаллической решётки.
В результате таких реакций ион Al3+, занимавший центральную позицию в
алюмогидроксильном октаэдре, превращается в ион Al(OH)2+ или Al(OH)2+.
Структура октаэдра нарушается, и ионы алюминия приобретают способность к
обмену. Благодаря избытку ионов H+
и Cl‾ в
растворах извлечения весь алюминий переходит в форму простого иона Al3+, и катионы K+ вытесняют его в раствор.
Лабораторные эксперименты и
полевые исследования показали, что насыщение почвенного поглотительного
комплекса обменным алюминием и развитие процесса подзолообразования связаны с
разрушением алюмосиликатов даже при слабокислой реакции почвенного раствора [28, 140]. В результате
истощения буферной ёмкости почв и снижения рН до величины менее 4,2 количество
подвижного алюминия резко возрастает [4, 23], в том числе и за счёт вышеописанных процессов. Поскольку наши
исследования показали значительный рост CAl3+ в
фильтратах при 1<рНисх<4,01
(cм. Таблицу 2.6), то эти данные подтверждают предположение о том, что в
сильнокислой почве алюмосиликатная составляющая диатомита может стать
дополнительным источником обменного алюминия в почвенном растворе. При рН>5,72 не отмечалось его
выщелачивания из породы, что также согласуется с литературными данными о
поведении алюминия в почве.
При прокаливании диатомита
происходит частичное разрушение алюмосиликатов и переход Al2O3 в
неактивное состояние: он включается в состав силикатной плёнки на поверхности
частиц, устойчивой к воздействию протонов [20, 45]. Поэтому выход алюминия из термоактивированного
диатомита отмечался при меньшем, чем для нативного диатомита рН.
Выход железа из диатомита в зависимости от значения рН раствора извлечения
А) Выход железа из нативного
диатомита также отмечался только при кислой реакции раствора извлечения (1<рНисх<5,72):
·
рНисх 3,32 – 5,72 – было зафиксировано появление
ионов Fe3+ в фильтрате (при рН 4,50 их концентрация
максимальна на данном интервале
рН);
·
рНисх 3,32 – выхода железа из
диатомита не отмечалось (CFe3+в
фильтрате равна 0);
·
при рНисх <3,32 вновь начался выход железа из
диатомита, с уменьшением значения рН он постоянно возрастал.
В) Порошок диатомита,
прокалённого при 850°C,
становится источником железа при меньших значениях рН раствора извлечения (<3,12). В более щелочной среде
присутствие в фильтратах ионов Fe3+ не отмечалось.
Данные, отражающие зависимость CFe3+ в
фильтрате от рН раствора извлечения, приведены в таблицах 2. 8 и 2.9 и отражены
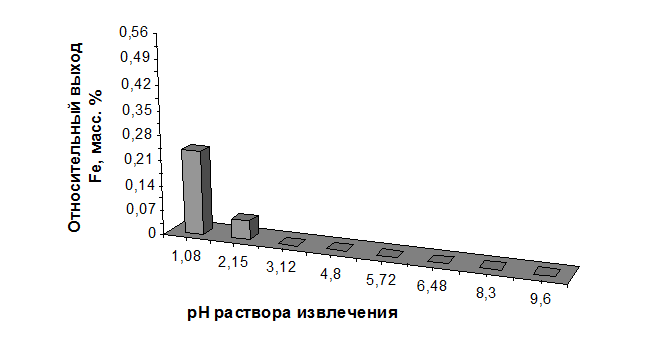
на графиках, представленных на рисунках 2.3 и 2.4.
Таблица
2.8
Зависимость выхода железа от значения рН раствора извлечения для
нативного диатомита
|
рН исх
|
1,02
|
1,37
|
1,94
|
2,70
|
3,32
|
4,01
|
4,50
|
6,07
|
8,30
|
9,60
|
|
CFel3+,
мг/л
|
11,07
|
3,56
|
0,79
|
0,40
|
0,00
|
0,59
|
0,79
|
0,00
|
0,00
|
0,00
|
Таблица 2.9
Зависимость выхода железа от значения рН
раствора извлечения для диатомита, прокалённого при 850°С
|
рН исх
|
1,08
|
2,15
|
3,12
|
4,80
|
5,72
|
6,48
|
8,30
|
9,60
|
|
CFel3+, мг/л
|
4,74
|
1,18
|
0,00
|
0,00
|
0,00
|
0,00
|
0,00
|
0,00
|
В диатомите железо заключено в
кристаллической решётке алюмосиликатов и частично присутствует в виде свободных
окислов. Силикатное железо появляется в кислом растворе вследствие разрушения
глинистых минералов по вышеописанному механизму. При замещении водородом
обменных катионов протоны взаимодействуют с дефектными тетраэдрами, в которых Si4+ замещён на Fe3+, или
октаэдрами c Fe3+ вместо
Al3+. Связи Fe—O или Fe—OH протонируются, железо занимает
обменные позиции и приобретает способность переходить в раствор. Но свободные
окислы железа начинают растворяться при более высоком значении рНисх,
так как разрушение ионных и ионно-ковалентных связей кристаллической решётки
требует большего количества энергии.
Способность ионов Fe3+ гидролизоваться
выше, чем у ионов Al3+, поэтому можно предположить, что при
3,32 <рН<5,72 на процесс выхода железа из нативного диатомита
накладывался процесс образования Fe3+ гидроксокомплексов Fe(OH)2+, Fe(OH)2+,
Fe(OH)°, который не полностью подавлялся присутствием ионов Сl‾ и
Н+ в растворе извлечения. В таком виде железо не определяется сульфосалициловым методом.
Этим можно объяснить «горб» на графике, представленном на рисунке 2.3.
Ульрихом [48, 709] было показано, что при рН<3,2 в почве начинается
растворение минералов гидроокисей и окисей железа, сопровождающееся появлением
ионов Fe3+ в
почвенном растворе. По данным наших исследований, резкое повышение
выщелачивания железа из диатомита отмечалось при рН<3,32 (от нулевого выхода при рН 3,32
до концентрации Fe3+
в фильтрате 11,07 мг/л
при рН 1,02), что в общем соответствуют закономерностям перехода железа в
подвижное состояние с понижением рН среды, подробно описанными Л. А. Воробьёвой
[28, 315].
Оранжевый цвет
термоактивированного диатомита объясняется переходом всего содержащегося в нём
железа в форму оксида железа (III).
Он отчасти включается в состав силикатной плёнки на поверхности частиц, поэтому
в фильтратах при рНисх>3.12 не отмечается присутствие ионов Fe3+. Но в
сильнокислой среде (рН<3)
Fe2O3 хорошо
растворим, и на концентрацию Fe3+
в растворе извлечения не влияют сопутствующие реакции образования
гидроксокомплексов. Поэтому в данных условиях из диатомита, прокалённого
при 850°С, также интенсивно выщелачивается железо.
Относительный выход алюминия и железа из диатомита.
На основе данных о валовом химическом составе и
выходе алюминия и железа из диатомита в зависимости от рН раствора извлечения,
были рассчитаны показатели относительного выхода этих элементов (в пересчёте на
100 г породы и в массовых процентах) для нативного диатомита и диатомита,
прокалённого при 850°С. Результаты приведены в таблицах 2.10, 2.11, 2.12 и 2.13
и на графиках, представленных на рисунках 2.5, 2.6, 2.7 и 2.8.
Таблица 2.10
Относительный выход алюминия из нативного
диатомита в зависимости от значения рН раствора извлечения
|
рН исх
|
1,02
|
1,94
|
2,70
|
4,01
|
5,72
|
6,07
|
8,30
|
9,60
|
|
CAl3+, мг/см3
|
0,0175
|
0,0129
|
0,0033
|
0,0011
|
0,0000
|
0,0000
|
0,0000
|
0,0000
|
|
Относительный
выход Al,
|
мг/100 г породы
|
9,397
|
6,708
|
1,650
|
0,591
|
0,000
|
0,000
|
0,000
|
0,000
|
|
масс. %
|
0,332
|
0,237
|
0,058
|
0,021
|
0,000
|
0,000
|
0,000
|
0,000
|
Таблица 2.11
Относительный выход алюминия из диатомита,
прокалённого при 850°С, в зависимости от
значения рН раствора извлечения
|
рН исх
|
1,08
|
2,15
|
3,12
|
4,80
|
5,72
|
6,48
|
8,30
|
9,60
|
|
CAl3+, мг/см3
|
0,0186
|
0,0109
|
0,0038
|
0,0000
|
0,0000
|
0,0000
|
0,0000
|
0,0000
|
|
Относительный выход Al,
|
мг/100 г породы
|
10,416
|
5,504
|
1,930
|
0,000
|
0,000
|
0,000
|
0,000
|
0,000
|
|
масс. %
|
0,368
|
0,194
|
0,068
|
0,000
|
0,000
|
0,000
|
0,000
|
0,000
|
Таблица 2. 12
Относительный выход железа из нативного
диатомита в зависимости от значения рН раствора извлечения
|
рН исх
|
1,02
|
1,37
|
1,94
|
2,70
|
3,32
|
4,01
|
4,50
|
6,07
|
8,30
|
9,60
|
|
CFe3+, мг/см3
|
11,07
|
3,56
|
0,79
|
0,40
|
0,00
|
0,59
|
0,79
|
0,00
|
0,00
|
0,00
|
|
Относительный выход Fe,
|
мг/100 г породы
|
5,944
|
1,957
|
0,004
|
0,002
|
0,000
|
0,003
|
0,004
|
0,000
|
0,000
|
0,000
|
|
масс. %
|
0,527
|
0,174
|
0,036
|
0,018
|
0,000
|
0,028
|
0,036
|
0,000
|
0,000
|
0,000
|
Таблица 2.13
Относительный выход железа из диатомита,
прокалённого при 850°С, в зависимости от значения рН раствора извлечения
|
рН исх
|
1,08
|
2,15
|
3,12
|
4,80
|
5,72
|
6,48
|
8,30
|
9,60
|
|
CFe3+, мг/см3
|
4,74
|
1,18
|
0,00
|
0,00
|
0,00
|
0,00
|
0,00
|
0,00
|
|
Относительный
выход Fe,
|
мг/100 г породы
|
2,650
|
0,006
|
0,000
|
0,000
|
0,000
|
0,000
|
0,000
|
0,000
|
|
масс. %
|
0,235
|
0,053
|
0,000
|
0,000
|
0,000
|
0,000
|
0,000
|
0,000
|
Буферное действие диатомита в системе твёрдая фаза – раствор
Проведённые эксперименты
показали, что порошок диатомита влияет на реакцию раствора извлечения: он
повышает значения рН кислых растворов, щелочных же, напротив, понижает.
Буферное действие породы гораздо сильнее проявляется в кислой среде, причём
нативный диатомит воздействует на величину рН раствора гораздо эффективнее
диатомита, прокалённого при 850°С: для него максимальное значение
│ΔрН│составило 4,34 при рНисх =2,7. Подвергнутый
термообработке диатомит способен изменять рН раствора извлечения максимум на
1,95 единицы рН при рНисх=3,12.
При исследовании влияния порошка
нативного диатомита на концентрацию Al3+ в растворах AlCl3
(исходное значение СAl3+ 0,0086 мг/см3) с
различными значениями рН были получены данные, особенно ярко демонстрирующие
его буферное действие в интервале значений рН 1,4-12,38, особенно в щелочной
среде.
Результаты исследований приведены в таблицах 2.14,
2.15 и 2.16 и отражены на графиках, приведённых на рисунках 2.9, 2.10 и 2.11.
Таблица 2.14
Влияние порошка нативного диатомита на
величину рН раствора извлечения (1 М раствора KCl c установленным
значением рН)
|
рН исх
|
1,02
|
1,94
|
2,70
|
4,01
|
6,07
|
8,30
|
9,60
|
|
ΔрН
|
-0,45
|
-1,48
|
-4,34
|
-1,66
|
-1,19
|
0,82
|
1,12
|
Таблица 2.15
Влияние порошка нативного диатомита на величину
рН раствора извлечения (раствора AlCl3 c установленным
значением рН)
|
рН исх
|
1,40
|
2,15
|
2,65
|
4,90
|
8,29
|
9,65
|
12,38
|
|
ΔрН
|
-0,23
|
-1,52
|
-3,03
|
-1,63
|
1,48
|
2,58
|
2,10
|
Таблица 2.16
Влияние порошка диатомита, прокалённого при
850°С,
на величину рН раствора извлечения (1 М
раствора KCl
c установленным значением рН)
|
рН исх
|
1,08
|
2,15
|
3,12
|
4,80
|
6,48
|
8,30
|
9,60
|
|
ΔрН
|
-1,71
|
-0,98
|
-1,95
|
-1,07
|
0,30
|
0,57
|
0,85
|
Буферное действие диатомита в кислой среде связано:
·
с адсорбцией протонов на сколах частиц
алюмосиликатов и последующим разрушением их кристаллической решётки;
·
с адсорбцией ионов H+ на гидроксилированной
поверхности опалового кремнезёма за счёт сил ионного притяжения вплоть до рН~2,
при котором число заряженных центров на поверхности кремнезёма равно нулю (точка
нулевого заряда).
Кроме того, Кольтгофом и
Стенжером было показано, что сильнокислой среде гидроксилированная поверхность
кремнезёма активно адсорбирует ионы Fe3+ и
Al3+ с образованием кислотных групп на его поверхности [2, 237].
Реакция сопровождается вытеснением протонов и снижением концентраций
исследуемых ионов в растворах. Можно предположить, что именно этим объясняется
уменьшение величины ΔрН при рНисх<2,7.
Гидроксилированная поверхность
кремнезёма имеет точку нулевого заряда при рН~2 [3, 913]. При более высоких значениях рН
она проявляет слабые кислотные свойства, а при рН >~6 степень ионизации возрастает, и водород Si―OH группы легче диссоциирует.
Переходя в раствор, протоны уменьшают степень его кислотности. Кроме того, при
рН>7 – 8 растворимость
кремнезёма начинает заметно расти [3, 66]. Как показано Р. Айлером, реакции гидратации и
деполимеризации происходят с участием гидроксил-ионов (см. рис. 1.3), но при рН<8 образовавшийся
силикат-ион гидролизуется с образованием молекул растворимого кремнезёма Si(OH)4 и ионов
ОН‾ [2, 91],
поэтому при рН<9,6
буферное действие породы, проявлялось слабее, чем в кислой среде. При рН>10,7 кремнезём весь
растворяется с образованием силикат-ионов, что приводит к понижению
концентрации гидроксил-ионов в растворе извлечения.
При термической активации
происходит частичная дегидратация силанольной поверхности аморфного кремнезёма
и для её регидратации требуется многодневное выдерживание образцов в
нейтральном водном растворе [3,
915]. Это значительно ослабляет буферное действие опаловой составляющей
диатомита, прокалённого при 850°С. Частичное разрушение алюмосиликатов снижает
адсорбцию протонов с их участием и изменяет значение показателей выхода железа
и алюминия. В целом диатомит, прокалённый при 850°С, обладает менее выраженным
буферным действием по сравнению с нативным.
Влияние порошка нативного
диатомита на концентрацию Al3+ в растворе AlCl3 в зависимости от
значения рН раствора извлечения
В присутствии порошка нативного
диатомита происходило заметное снижение концентрации алюминия в растворе AlCl3 c исходной CAl3+ 0,0086 мг/см3 и
установленными значениями рН:
·
рНисх
1,4-4,9 – отмечалось значительное уменьшение содержания алюминия в фильтрате по
сравнению с раствором извлечения вплоть до CAl3+ =0 при рН
4,9;
·
рНисх 4,9-12,4 – было зафиксировано
присутствие ионов Al3+
в исследуемых растворах, с максимальной концентрацией 0,0038 мг/см3
при рН 8,29;
·
рНисх 12,38 – CAl3+ в фильтрате равна
нулю.
Повышение концентрации исследуемого иона в фильтрате по
срав-
нению с раствором извлечения отмечалось только при рН<~2-2,5.
Данные, отражающие влияние нативного диатомита на
значение CAl3+ в фильтрате в зависимости от рН
раствора извлечения, приведены в таблице 2.17 и отражены на графике,
приведённом на рисунке 2.12.
Таблица
2.17
Влияние нативного
диатомита на значение CAl3+ в фильтрате в
зависимости от значения рН раствора извлечения:
|
рН исх
|
1,40
|
2,15
|
2,65
|
4,90
|
8,29
|
9,65
|
12,38
|
|
CAl3+,
мг/см3
|
0,0164
|
0,0062
|
0,0010
|
0,0000
|
0,0038
|
0,0017
|
0,0000
|
Резкое уменьшение концентрации исследуемого
иона в фильтратах при рНисх<4,9 связано с тем, что его адсорбция на обменных позициях
глинистых минералов и поверхности аморфного кремнезёма происходит быстрее, чем
трансформация поверхностных слоёв кристаллической решётки алюмосиликатов, так как
требует меньших затрат энергии. Адсорбировавшись на поверхности кристаллитов,
ионы Al3+
затрудняют проникновение протонов внутрь, защищая решётку от разрушения.
В кислой среде происходит наложение процессов поглощения Al3+ диатомитом и выщелачивания алюминия
из его глинистой составляющей.
Ульрихом [48, 708] было показано, что при рН
4,2-5,0 вытеснение Al
из кристаллических решёток минералов сопровождается образованием полимерных
аквагидроксокомплексов алюминия, занимающих их обменные позиции. Можно предположить,
что этим объясняется снижение поглощения диатомитом ионов Al3+ из раствора при рНисх
4,90-8,29. К тому же подщелачивание раствора извлечения способствует
активизации гидролиза, а образующиеся в растворе катионы Al(OH)x3-x нельзя определить по выбранной нами методике. При
более щелочной реакции среды весь алюминий раствора переходит в форму
комплексных ионов переменной основности и активно поглощается порошком
диатомита.