| Физико-химия конкретных промышленных каталитческих процессов.
Окислительный аммонолиз пропилена. Окислительное хлорирование этилена. Основные особенности процессов окисления в псевдоожиженном слое катализатора. «Воздушный» и «кислородный» процессы. Рециркуляционные технологии. Кинетика и механизм реакций.
Окислительный аммонолиз пропилена.
C3
H6
+ NH3
+ 1,5O2
= C3
H3
N + 3H2
O
C3
H6
+ NH3
+ nO2
Þ CH3
CN, HCN, CO, CO2
,H2
O
C3
H3
N + m O2
Þ CH3
CN, HCN, CO, CO2
,H2
O
  1 C3
H3
N 1 C3
H3
N
 C3
H6
3 C3
H6
3
2 CH3
CN, HCN, CO, CO2
,H2
O
Температура – 4300
С, давление – близкое к атмосферному.
Состав смеси на входе в реактор
C3
H6
– 10%
O2
- 16,8%
NH3
- 10%
N2
- 63,2%
Возможность подавать в реактор смесь, состав которой лежит внутри пределов взрываемости – следствие пламягасящих свойств псевдоожиженного слоя.
Сохранение постоянной активности катализатора в реакторе как результат его истирания и уноса с компенсирующей подпиткой свежего катализатора.
Катализаторы – Bi-Mo-O, U-Sb-O, Fe-Sb-O, Sn-Sb-O
Промышленные катализаторы на территории СНГ (псевдоожиженный слой)
С-41 (Саратов, Нитрон) – Bi-Mo-Fe-Ni-Co-Na-P-O/SiO2
(SOHIO)
A-112 (Новополоцк, Полимир) – Bi-Mo-O/SiO2
(ASAHI Chemical)
Приготовление катализатора методом распылительной сушки.
  1 C3
H3
N 1 C3
H3
N
 C3
H6
3 C3
H6
3
2 CH3
CN, HCN, CO, CO2
,H2
O


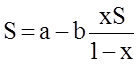
Псевдоожиженный слой по двухфазной модели характеризуется коэффициентом массообмена между фазами b и безразмерным параметром j=(k1
+k2
)/ b.


Если активность катализатора ниже стандартной в 2 раза, например, вместо k=k1
+k2
=1сек-1
получили образец с k=0,5сек-1
, то для t=1сек, b=0,2сек-1
(т.е. при j=5) конверсия уменьшается с 0,965 до 0,943.
Если доокисляющая способность выше стандартной в два раза, например, b вместо 0,01 равно 0,02, то выход уменьшается с 0,79 до 0,65.
Механизм реакции по данным меченых атомов и кинетическому изотопному эффекту.
Дейтерирование пропилена показало, что лимитирует скорость реакции отрыв метильного водорода. Эти же эксперименты, а также эксперименты с изотопами углерода, показали, что образующееся на поверхности соединение – симметричное. Распределение дейтерия в продуктах показывает, что образуется p-, а не d-комплекс.
Результаты опытов с изотопами кислорода над висмут-молибденовыми катализаторами.
Окислительное хлорирование этилена.
С2
H4
+ 2HCl + 0,5O2
= C2
H4
Cl2
+ H2
O
2 C2
H4
Cl2
= C2
H3
Cl + HCl
С2
H4
+ Cl2
= C2
H4
Cl2
2 С2
H4
+ Cl2
+ 0,5O2
= 2C2
H3
Cl + H2
O
Катализатор – CuCl2
/Al2
O3
Температура 220-2700
С.
Давление 3,5-4,5 атм.
Состав смеси на входе в реактор
HCl – 30%
С2
H4
- 15,5%
O2
– 11%.
Остальное – азот («воздушный» процесс) или азот + диоксид углерода («кислородный» процесс).
Преимущества (уменьшение выбросов дихлорэтана и потерь этилена) и недостатки (затраты на разделение воздуха и на циркуляцию смеси) «кислородного» процесса.
Механизм процесса по данным стационарных и нестационарных кинетических измерений.
Окисление этилена в окись этилена. Основные направления развития «кислородного» процесса. Механизм влияния соединений хлора на селективность и активность.
C2
H4
+ 0,5O2
= C2
H4
O + 27 ккал/моль
C2
H4
+ 3O2
= 2CO2
+ 2H2
O + 330 ккал/моль
Температура 220-2700
С
Давление 20 и более атмосфер.
Катализатор – 11-13% Ag с добавками/Al2
O3
(корунд)
Роль добавок и особенности приготовления катализаторов.
Состав смеси на входе в реактор
«воздушный» процесс
O2
– 7%
C2
H4
- 4% (конверсия этилена – 0,3)
CO2
– 7%
остальное – азот;
«кислородный» процесс
O2
– 7% (конверсия килорода – 0,3)
C2
H4
- выше 15%
CO2
– 7%
остальное – азот и (или) метан.
Влияние хлорсодержащих соединений на процесс.
Роль теплосъема, “runaway”, “decomp”.
Окисление бутана в малеиновый ангидрид. Окисление метанола в формальдегид на серебряных катализаторах.
Особенности процессов в реакторах с восходящим потоком и в условиях, когда реакция определяется внешним тепло- и массопереносом.
Окисление бутана в малеиновый ангидрид.
C4
H10
+ 3,5O2
= C4
H2
O3
+ 4H2
O
C4
H10
+ 5O2
= 3CO + CO2
+ 5H2
O
C4
H10
+ 3,5O2
= 2CO + 2CO2
+ H2
O
Катализатор – (VO)2
P2
O7
с добавками K, Cr или других металлов.
Особенности приготовления катализатора. Потери фосфора и компенсация этих потерь.
Температура – 380-4700
С.
Давление – до 4 атм.
Состав смеси на входе в реактор
- неподвижный слой
C4
H10
- 1,6%
воздух – остальное;
- псевдоожиженный слой
C4
H10
- 4,5%
O2
– 16%
азот – остальное.
Восходящий поток. Особенности процесса.
Механизм реакции по данным меченых атомов и изотопных эффектов.
Окисление метанола в формальдегид на серебряных катализаторах.
CH3
OH = CH2
O + H2
CH3
OH + 0,5O2
= CH2
O + H2
O
CH3
OH + nO2
= CO, CO2
, H2
O
CH2
O + mO2
= CO, CO2
, H2
O
Катализатор – Ag/пемза, мулит.
Температурный профили в адиабатическом реакторе для процесса, протекающего в области внешней диффузии.
Особенности процессов, протекающих во внешнедиффузионной области.
Реакции с участием СО, включая синтеза из СО и водорода, и синтез метанола.
Получение газов из углеводородного сырья на примере метана.
Очистка метана от сернистых соединений - деструктивное гидрирование на кобальт-молибденовых катализаторах до сероводорода (температура 350-4000
С, давление 10-40 атм) в адиабатическом реакторе, например,
С4
Н4
S + 4H2
= C4
H10
+ H2
S
и поглощение сероводорода с помощью ZnO
ZnO + H2
S = ZnS + H2
O
Паровая (порокислородная, углекислотная) конверсия метана -
CH4
+ H2
O = CO + 3H2
- 50 ккал/моль
CO + H2
O = CO2
+ H2
+ 10 ккал/моль
CH4
+ CO2
= 2CO + 2H2
- 60 ккал/моль
2CH4
+ O2
= 2CO + 4H2
+ 7 ккал/моль
Условия реакции - температура 800-8500
С, давление 10-40 атм, катализатор - никель на окиси алюминия, или магний-алюминиевой шпинели (магниевая соль алюминиевой кислоты). Почему высокое давление? Почему избыток пара? Мембранный реактор.
Синтез метанола.
CO2
+ 3H2
= CH3
OH + + H2
O 10 ккал/моль
CO + H2
O = CO2
+ H2
+ 10 ккал/моль
Условия реакции - температура 210-2800
С, давление 40-90 атм, катализатор - медь-цинк-алюминиевый.
Факториал (H2
- CO2
)/( CO2
+ CO) = 2,0 - 2,2 (для синтеза метанола), для синтеза высших спиртов и в оксосинтезе H2
/CO = 0,7 - 1,0, для синтеза углеводородов (процесс Фишера-Тропша) H2
/CO = 2,0 - 2,2.
Каталитические процессы в нефтепеработке.
Глубина переработки нефти.
Газы нефтепеработки: природный газ, попутный газ (растворен в нефти), газы процессов (например, каталитического крекинга).
Продукты нефтепеработки: моторные топлива, реактивные топлива, кокс, масла, асфальт, СК.
Октановые и цетановые числа.
Октановые числа:
н-гептан 0
2- метилгексан 41
2,2-диметилпентан 89
2,2,3-триметилбутан 113
метилциклогексан 104
толуол 124
Процессы нефтепеработки:
первичная перегонка,
гидроочистка ( обессеривание, деазотирование, деметаллирование), каталитический крекинг,
гидрокрекинг,
платформинг,
алкилирование,
олигомеризация
изомеризация.
|