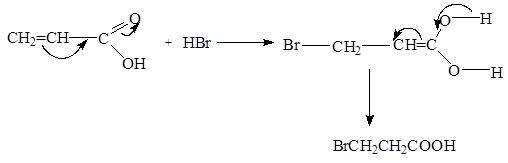Реферат: Функциональные производные карбоновых кислот
|
Название: Функциональные производные карбоновых кислот Раздел: Рефераты по химии Тип: реферат | ||||||||||||||||||
| Функциональные производные карбоновых кислот. Двухосновные карбоновые кислоты. a , b -Ненасыщенные кислоты Производные карбоновых кислот 1. Галогенангидриды . При действии галогенидов фосфора или хлористого тионила происходит образование галогенагидридов: CH 3 COOH + PCl 5 ® CH 3 COCl + POCl 3 + HCl Галоген в галогенангидридах обладает большой реакционной способностью. Сильный индукционный эффект определяет легкость замещения галогена другими нуклеофилами: - OH , - OR , - NH 2, - N 3, - CN и др.: CH3 COCl + CH3 COOAg ® (CH3 CO)2 O уксусный ангидрид + AgCl 1. Ангидриды. Ангидриды образуются при взаимодействии солей кислот с их галогенангидридами: CH 3 COONa + CH 3 COCl ® NaCl + ( CH 3 CO )2 O Ангидриды кислот обладают большой химической активностью и являются, как и галогенангидриды, хорошими ацилирующими агентами. 2. Амиды . Амиды получают через галогенангидриды CH3 COCl +2 NH3 ® CH3 CONH2 ацетамид + NH4 Cl или из аммонийных солей кислот, при сухой перегонке которых отщепляется вода и образуется амид кислоты. Также амиды кислот образуются как побочный продукт при гидролизе нитрилов. Процессы амидирования имеют важное значение в промышленности для производства ряда ценных соединений (N , N -диметилформамид, диметилацетамид, этаноламиды высших кислот). 4. Нитрилы . Важнейшими представителями нитрилов являются ацетонитрил CH 3 CN (применяется как полярный растворитель) и акрилонитрил CH 2 = CHCN (мономер для получения синтетического волокна нейрона и для производства дивинилнитрильного синтетического каучука, обладающего масло- и бензостойкостью). Основным способом получения нитрилов является дегидратация амидов на кислотных катализаторах:
CH 3 CONH 2 ® CH 3 C - CN + H 2 O 5. Сложные эфиры . Сложные эфиры карбоновых кислот имеют важное практическое значение в качестве растворителей, гидравлических жидкостей, смазочных масел, пластификаторов и мономеров. Их получают этерификацией спиртов кислотами, ангидридами и галогенангидридами или взаимодействием кислот и алкенов: CH3 -CH=CH2 + CH3 COOH ® CH3 COOCH(CH3 )2 Многие эфиры используются в качестве душистых веществ:
Двухосновные насыщенные кислоты Двухосновные предельные (насыщенные) кислоты имеют общую формулу Cn H 2 n ( COOH )2 . Из них важнейшими являются: НООС-СООН - щавелевая, этандикарбоновая кислота; НООС-СН2 -СООН - малоновая, пропандикарбоновая кислота; НООС-СН2 -СН2 -СООН - янтарная, бутандикарбоновая кислота; НООС-СН2 -СН2 -СН2 -СООН - глутаровая, пентандикарбоновая кислота. Способы получения Общие методы получения двухосновных кислот аналогичны способам получения одноосновных кислот (окисление гликолей, гидролиз динитрилов, синтез Кольбе - см. Лекцию№27). 1. Окисление оксикислот :
OH-CH2 CH2 COOH ® HOCCH2 COOH ® HOOC-CH2 -COOH 2. Окисление циклоалканов . Это промышленный способ получения адипиновой кислоты HOOC - CH 2 CH 2 CH 2 CH 2 - COOH из циклогексана.
Побочно образуются также янтарная и щавелевая кислоты. Адипиновая кислота применяется для синтеза волокна найлон 6,6 и пластификаторов. Химические свойства Двухосновные кислоты более сильные, чем одноосновные. Это объясняется взаимным влиянием карбоксильных групп, облегчающих диссоциацию:
В целом реакции дикарбоновых кислот и их монокарбоновых аналогов почти не различаются между собой. Механизм реакций образования диамидов, диэфиров и др. из карбоновых кислот тот же, что и для монокарбоновых кислот. Исключение составляют дикарбоновые кислоты, содержащие меньше четырех атомов углерода между карбоксильными группами. Такие кислоты, две карбоксильные группы которых способны реагировать с одной функциональной группой или друг с другом, обнаруживают необычное поведение в реакциях, протекающих с образованием пяти- или шестичленных замкнутых активированных комплексов или продуктов. Примером необычного поведения карбоновых кислот могут служить реакции, протекающие при нагревании. 1. Декарбоксилирование . При 150 о С щавелевая кислота разлагается на муравьиную кислоту и СО2 :
HOOC-COOH ® HCOOH + CO2 2. Циклодегидратация . При нагревании g -дикарбоновых кислот, у которых карбоксильные группы разделены атомами углерода, происходит циклодегидратация, в результате чего образуются циклические ангидриды:
3. Синтезы на основе малонового эфира . Двухосновные кислоты с двумя карбоксильными группами при одном углеродном атоме, т.е. малоновая кислота и ее моно- и дизамещенные гомологи, при нагревании несколько выше их температур плавления разлагаются (подвергаются декарбоксилированию ) с отщеплением одной карбоксильной группы и образованием уксусной кислоты или ее моно- и дизамещенных гомологов: HOOCCH2 COOH ® CH3 COOH + CO2 HOOCCH(CH3 )COOH ® CH3CH2COOH + CO2 HOOCC(CH3 )2 COOH ® (CH3)2 CHCOOH + CO2 Атомы водорода метиленовой группы, находящейся между ацильными группами диэтилового эфира малоновой кислоты (малоновый эфир ), обладают кислотными свойствами и дают натриевую соль с этилатом натрия. Эту соль – натрий-малоновый эфир – алкилируют по механизму нуклеофильного замещения SN 2 . На основе натрий-малонового эфира получают одно- и двухосновные кислоты: [CH(COOCH2 CH3 )2 ]- Na+ + RBr ® RCH(COOCH2 CH3 )2 + 2 H2 O ® R-CH(COOH)2 алкилмалоновая кислота ® R-CH2 COOH алкилуксусная кислота + CO2 4. Пиролиз кальциевых и бариевых солей . При пиролизе кальциевых или бариевых солей адипиновой (С6 ), пимелиновой (С7 ) и пробковой (С8 ) кислот происходит отщепление СО2 и образуются циклические кетоны:
Непредельные одноосновные карбоновые кислоты Непредельные одноосновные кислоты этиленового ряда имеют общую формулу Cn H 2 n -1 COOH , ацетиленового и диэтиленового рядов - Cn H 2 n -3 COOH . Примеры непредельных одноосновных кислот:
Непредельные одноосновные кислоты отличаются от предельных большими константами диссоциации. Ненасыщенные кислоты образуют все обычные производные кислот - соли, ангидриды, галогенангидриды, амиды, сложные эфиры и др. Но за счет кратных связей они вступают в реакции присоединения, окисления и полимеризации. Благодаря взаимному влиянию карбоксильной группы и кратной связи присоединение галогенводородов к a,b-непредельным кислотам происходит таким образом, что водород направляется к наименее гидрогенизированному атому углерода: CH 2 = CHCOOH + HBr ® BrCH 2 CH 2 COOH b -бромпропионовая кислота
Этиленовые кислоты типа акриловой кислоты и их эфиры значительно легче подвергаются полимеризации, чем соответствующие углеводороды. отдельные представители Акриловую кислоту получают из этилена (через хлоргидрин или оксид этилена), гидролизом акрилонитрила или окислением пропилена, что более эффективно. В технике используются производные акриловой кислоты - ее эфиры, особенно метиловый (метилакрилат ). Метилакрилат легко полимеризуется с образованием прозрачных стекловидных веществ, поэтому его применяют в производстве органического стекла и других ценных полимеров. Метакриловая кислота и ее эфиры получают в больших масштабах методами, сходными с методами синтеза акриловой кислоты и ее эфиров. Исходным продуктом является ацетон, из которого получают ацетонциангидрин, подвергают дегидратации и омылению с образованием метакриловой кислоты. Этерификацией метиловым спиртом получают метилметакрилат, который при полимеризации или сополимеризации образует стекловидные полимеры (органические стекла) с весьма ценными техническими свойствами. Двухосновные ненасыщенные кислоты Наиболее простые ненасыщенные двухосновные кислоты - фумаровая и малеиновая - имеют одну и ту же структурную формулу HOOCCH = CHCOOH , но разную пространственную конфигурацию: фумаровая - транс -, малеиновая - цис -. Малеиновая кислота (лабильная форма) под действием брома, йода, азотистой кислоты легко переходит в устойчивую (стабильную) форму - фумаровую кислоту. Обратный переход осуществляется под действием ультрафиолетовых лучей. Малеиновая кислота в технических масштабах получается каталитическим окислением бензола и нафталина кислородом воздуха. Обе кислоты способны образовывать соли, сложные эфиры, амиды и некоторые другие производные кислот. Однако, малеиновая кислота, в отличие от фумаровой, легко образует циклический ангидрид, так как обе карбоксильные группы расположены по одну сторону от двойной связи (цис -изомер). Малеиновый ангидрид служит характерным реактивом для обнаружения 1,3-диеновых соединений: он легко вступает в реакцию диенового синтеза и во многих случаях дает ценные продукты. Малеиновый ангидрид широко применяется при производстве полиэфирных смол и сополимеров со стиролом, акриловым и метакриловым эфирами. Гидратацией малеинового ангидрида получают яблочную кислоту, применяемую в пищевой промышленности. Монокарбоновые кислоты ароматического ряда Ароматическими карбоновыми кислотами называются производные бензола, содержащие карбоксильные группы, непосредственно связанные с ароматическим ядром. Кислоты, содержащие карбоксильные группы в боковой цепи, рассматриваются как жирноароматические . По количеству карбокисльных групп ароматические кислоты делятся на одно-, двухосновные и т.д. Название кислоты производится от ароматического углеводорода (бензойная кислота, п -толуиловая кислота). Способы получения 1. Окисление ароматических углеводородов . Для синтеза ароматических кислот наиболее подходят метильные гомологи бензола, радикально-цепное окисление которых протекает через стадии первичного гидропероксида и альдегида:
ArCH3 + O2 ® ArCH2 OOH ® ArCHO+ O2 ® ArCOOH Жидкофазным окислением метилбензолов кислородом воздуха в промышленности получают моно- и дикарбоновые ароматические кислоты. 2. Окисление спиртов, альдегидов и кетонов . Ароматические спирты, альдегиды и кетоны окисляются легче, чем углеводороды. Окисление обычно ведут с помощью гипохлоритов по схеме: C 6 H 5 - CO - CH 3 + 4 NaOCl ® C 6 H 5 - COOH + NaCl + H 2 O + CO 2
3. Гидролиз галогенпроизводных . Этот способ широко применяется в технике. C 6 H 5 CCl 3 + 2 H 2 O ® C 6 H 5 COOH + 3 HCl При хлорировании толуола получают три вида галогенпроизводных: хлористый бензил для производства бензилового спирта; хлористый бензилиден – для получения бензальдегида; бензотрихлорид перерабатывается на бензойную кислоту. 4. Синтез Гриньяра . C6 H5 Li + CO2 ® C6 H5 COOLi + LiBr Химические свойства В водных растворах монокарбоновые кислоты обнаруживают большую степень диссоциации, чем алифатические кислоты (Ка бензойная к-та =6,6×10-5 , Ка уксусная к-та =1,8×10-5 ). Большая степень диссоциации бензойной кислоты обусловлена электрофильным характером бензольного кольца:
Кислотность ароматических кислот почти не зависит от резонансных эффектов. Ароматические кислоты вступают во все те реакции, которые свойственны и кислотам жирного ряда. За счет карбоксильной группы образуются различные производные кислот: действием кислот на щелочи и карбонаты получаются соли , эфиры - нагреванием смеси кислоты и спирта в присутствии минеральной кислоты. Если заместителей в орто -положении нет, то этерификация карбоксильной группы происходит так же легко, как и в случае алифатических кислот. Если одно из орто -положений замещено, то скорость этерификации сильно уменьшается, а если заняты оба орто -положения, то этерификация не идет. Эфиры орто -замещенных бензойных кислот могут быть приготовлены при реакции серебряных солей с галогеналканами. Они с трудом подвергаются гидролизу. Такое явление носит название пространственных (стерических) затруднений. Группы, большие, чем водород, в такой степени заполняют пространство вокруг углеродного атома карбоксильной группы, что затрудняет переход в промежуточное состояние при образовании или омылении эфира. Хлорангидриды получаются действием на кислоты хлористого тионила или пятихлористого фосфора: C 6 H 5 COOH + SOCl 2 ® C 6 H 5 COCl + HCl + SO 2
Ангидриды получают перегонкой смеси кислоты с уксусным ангидридом или действием хлорангидридов на соли: C 6 H 5 COCl + NaOOCC 6 H 5 ® ( C 6 H 5 CO )2 O + 2 NaCl При сплавлении соли ароматической карбоновой кислоты со щелочью карбоксильная группа замещается на водород: C 6 H 5 COONa + NaOH ® ArH + Na 2 CO 3
Важнейшие представители 1. Бензойная кислота . Основными способами получения бензойной кислоты являются окисление толуола и декарбоксилирование фталевой кислоты. Применяется в качестве консерванта в пищевой промышленности вследствие сильного антисептического действия, а также в производстве красителей и душистых веществ. Очень важным производным бензойной кислоты является ее хлорангидрид - хлористый бензоил . Это жидкость с характерным запахом и сильным лакриматорным действием. 2. п-трет -Бутилбензойная кислота получается в промышленных масштабах окислением трет -бутилтолуола в присутствии растворимой соли кобальта в качестве катализатора. Применяется в производстве полиэфирных смол. Дикарбоновые ароматические кислоты Известно три бензолдикарбоновых кислоты: фталевая (о -изомер), изофталевая (м -изомер) и терефталевая (п -изомер). Терефталевая кислота является кристаллическим веществом (Т возг . 300о С), по сравнению с изомерными кислотами наименее растворима в воде и органических жидкостях. Терефталевая кислота и ее диметиловый эфир играют важную роль в производстве синтетического волокна лавсан (терилен ) - продукта их поликонденсации с этиленгликолем. Терефталевую кислоту получают окислением п -ксилола. Изофталевая кислота применяется для производства полиэфиров. Ее получают аналогично терефталевой кислоте - жидкофазным окислением м -ксилола. |