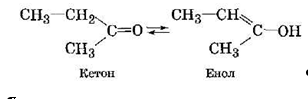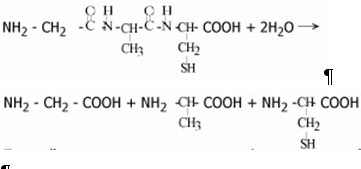Учебное пособие: Органическая химия
|
Название: Органическая химия Раздел: Рефераты по химии Тип: учебное пособие | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
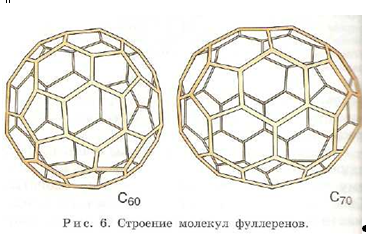
1. Определение понятия «Органическая химия»Из всего многообразия химических соединений большая часть (свыше четырех миллионов) содержит углерод. Почти все они относятся к органическим веществам. Органические соединения встречаются в природе, например углеводы, белки, витамины, они играют важную роль в жизнедеятельности животных и растений. Многие органическиё вещества и их смеси (пластмассы, каучук, нефть, природный газ и другие) имеют большое значение для развития народного хозяйства страны. Химия соединений углерода называется органической химией. Так определил предмет органической химии великий русский химик-органик А.М. Бутлеров. Однако не все соединения углерода принято относить к органическим. Такие простейшие вещества, как оксид углерода (II) СО, диоксид углерода СО2, угольная кислота Н2СО3 и ее соли, например, СаСО3, К2СО3, относят к неорганическим соединениям. В состав органических веществ кроме углерода могут входить и другие элементы. Наиболее часто - это водород, галогены, кислород, азот, сера и фосфор. Существуют также органическиё, вещества, содержащие другие элементы, в том числе металлы. 2. Строение атома углерода (С), структура его электронной оболочки2.1 Значение атома углерода (С) в химическом строении органических соединенийУГЛЕРОД (лат. Carboneum), С, химический элемент подгруппы IVa периодической системы; атомный номер 6, атомная масса 12,0107, относится к неметаллам. Природный углерод состоит из двух стабильных нук лидов - 12С (98,892% по массе) и 13С (1,108%) и одного нестабильного - С с периодом полураспада 5730 лет. Распространённость в природе. На долю углерода приходится 0,48% от массы земной коры, в которой он по содержанию занимает среди других элементов 17-е место. Основные углерод-содержащие породы - природные карбонаты (известняки и доломиты); количество углерода в них составляет около 9,610 т. В свободном состоянии углерод встречается в природе в виде горючих ископаемых, а также в виде минералов - алмаза и графита. Около 1013 т углерода сосредоточено в таких горючих ископаемых, как каменный и бурый уголь, торф, сланцы, битумы, образующих мощные скопления в недрах Земли, а также в природных горючих газах. Алмазы чрезвычайно редки. Даже алмазоносные породы (кимберлиты) содержат не более 9-10 % алмазов массой, как правило, не более 0,4 г. Найденным крупным алмазам обычно присваивают особое название. Самый большой алмаз «Куллинан» весом 621,2 г (3106 карат) был найден в Южной Африке (Трансвааль) в 1905 г., а самый большой русский алмаз «Орлов» весом 37,92 г (190 карат) -в Сибири в середине 17 в. Чёрно-серый непрозрачный жирный на ощупь с металлическим блеском графит представляет собой скопление плоских полимерных молекул из атомов углерода, непрочно наслоённых друг на друга. При этом атомы внутри слоя связаны между собой сильнее, чем атомы между слоями. Другое дело алмаз. В его бесцветном, прозрачном и сильно преломляющем свет кристалле каждый атом углерода связан химическими связями с четырьмя такими же атомами, расположенными в вершинах тетраэдра. Все связи одинаковы по длине и очень прочны. Они образуют в пространстве непрерывный трёхмерный каркас. Весь кристалл алмаза представляет собой как бы одну гигантскую полимерную молекулу, не имеющую «слабых» мест, т.к. прочность всех связей одинакова. Плотность алмаза при 20°С равна 3,51 г/см3 , графита - 2,26 г/см3 . Физические свойства алмаза (твёрдость, электропроводность, коэффициент термического расширения) практически одинаковы по всем направлениям; он является самым твёрдым из всех найденных в природе веществ. В графите же эти свойства по разным направлениям - перпендикулярному или параллельному слоям атомов углерода - сильно различаются: при небольших боковых усилиях параллельные слои графита сдвигаются друг относительно друга и он расслаивается на отдельные чешуйки, оставляющие след на бумаге. По электрическим свойствам алмаз - диэлектрик, графит же проводит электрический ток. Алмаз при нагревании без доступа воздуха выше 1000 °С превращается в графит. Графит при постоянном нагревании в тех же условиях не изменяется вплоть до 3000°С, когда он возгоняется без плавления. Прямой переход графита в алмаз происходит только при температуре выше 3000°С и огромном давлении - около 12 ГПа. Третья аллотропная модификация углерода -карбин - получена искусственно. Это мелкокристаллический чёрный порошок; в его структуре длинные цепочки атомов углерода расположены параллельно друг другу. Каждая цепочка имеет строение (-С=С)Л или (=С=С=)Л . Плотность карбина средняя между графитом и алмазом -2,68-3,30 г/см3 . Одна из важнейших особенностей карбина - его совместимость с тканями человеческого организма, что позволяет применять его, например, при изготовлении не-отторгаемых организмом искусственных кровеносных сосудов (рис. 1).
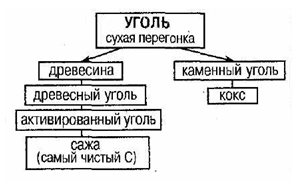
Рис. 1 Название своё фуллерены получили не в честь химика, а по имени американского архитектора Р. Фуллера, который предложил строить ангары и другие сооружения в виде куполов, поверхность которых образуют пяти- и шестиугольники (такой купол построен, например, московском парке «Сокольники»). Для углерода характерно также состояние с неупорядоченной структурой - это т. наз. аморфный углерод (сажа, кокс, древесный уголь) рис. 2. Получение углерода (С):
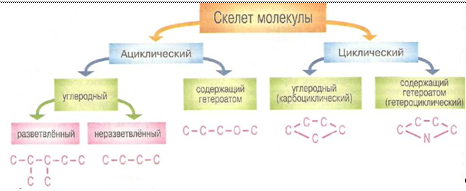
Рис. 2 2.2 Значение атома углерода (С) в химическом строении органических соединений Большинство окружающих нас веществ - органические соединения. Это ткани животных и растений, наша пища, лекарства, одежда (хлопчатобумажные, шерстяные и синтетические волокна), топливо (нефть и природный газ), резина и пластмассы, моющие средства. В настоящее время известно более 10 миллионов таких веществ, и число их каждый год значительно возрастает благодаря тому, что учёные выделяют неизвестные вещества из природных объектов и создают новые, не существующие в природе соединения. Такое многообразие органических соединений связано с уникальной особенностью атомов углерода образовывать прочные ковалентные связи, как между собой, так и с другими атомами. Атомы углерода, соединяясь друг с другом как простыми, так и кратными связями, могут образовывать цепочки практически любой длины и циклы. Большое разнообразие органических соединений связано также с существованием явления изомерии. Почти все органические соединения содержат также водород, часто в их состав входят атомы кислорода, азота, реже - серы, фосфора, галогенов. Соединения, содержащие атомы любых элементов (за исключением О, N, S и галогенов), непосредственно связанные с углеродом, объединены под названием элементоорганические соединения; основную группу таких соединений составляют металлоорганические соединения (рис. 3).
Рис. 3 Огромное число органических соединений требует их четкой классификации. Основу органического соединения составляет скелет молекулы. Скелет может иметь открытую (незамкнутую) структуру, тогда соединение называют ациклическим (алифатическим; алифатические соединения называют также соединениями жирного ряда, т.к. они впервые были выделены из жиров), и замкнутую структуру, тогда его называют циклическим. Скелет может быть углеродным (состоять только из атомов углерода) либо содержать другие, отличные от углерода атомы - т. наз. гетероатомы, чаще всего кислород, азот и серу. Циклические соединения подразделяют на карбоцикличе-ские (углеродные), которые могут быть ароматическими и алициклическими (содержащими один или несколько циклов), и гетероциклические. Атомы водорода и галогенов в скелет не входят, а гетероатомы входят в скелет лишь в том случае, если они имеют, по меньшей мере, две связи с углеродом. Так, в этиловом спирте СН3СН2ОН атом кислорода не включён в скелет молекулы, а в диметиловом эфире СН3ОСН3 включён в него. Кроме того, ациклический скелет может быть неразветвлённым (все атомы расположены в один ряд) и разветвлённым. Иногда неразветвлённый скелет называют линейным, однако следует помнить, что структурные формулы, которыми мы чаще всего пользуемся, передают лишь порядок связи, а не реальное расположение атомов. Так, «линейная» углеродная цепь имеет зигзагообразную форму и может закручиваться в пространстве различными способами. В скелете молекулы различают четыре типа атомов углерода. Принято атом углерода называть первичным, если он образует только одну связь с другим атомом углерода. Вторичный атом связан с двумя другими атомами углерода, третичный - с тремя, а четвертичный все свои четыре связи затрачивает на образование связей с атомами углерода. Следующим классификационным признаком является наличие кратных связей. Органические соединения, содержащие только простые связи, называются насыщенными (предельными). Соединения, содержащие двойные или тройные связи, называются ненасыщенными (непредельными). В их молекулах на один атом углерода приходится меньшее число атомов водорода, чем в предельных. Циклические ненасыщенные углеводороды ряда бензола выделяют в отдельный класс ароматических соединений. Третьим классификационным признаком является наличие функциональных групп-групп атомов, характерных для данного класса соединений и определяющих его химические свойства. По количеству функциональных групп органические соединения делятся на монофункциональные - содержат одну функциональную группу, полифункциональные - содержат несколько функциональных групп, например глицерин, и гетерофунк-циональные - в одной молекуле несколько различных групп, например аминокислоты. В зависимости от того, у какого атома углерода находится функциональная группа, соединения делятся на первичные, например этилхлорид СН3 СН2 С1, вторичные - изопропилхлорид (СНз)2СНС1 и третичные - бутилхлорид (СН8 )8 ССl. Функциональная группа определяет принадлежность органического соединения к тому или иному классу (см. таблицу). Органические соединения обладают самыми разнообразными свойствами. Как непохожи природный газ, сахар и, например, полиэтилен! Тем не менее, органические соединения имеют свои специфические особенности. Первая особенность связана с молекулярным строением этих веществ. По сравнению с ионными соединениями они имеют меньшие температуры плавления и кипения, их реакции часто протекают медленнее, чем у ионных соединений, и требуют применения катализатора. И второе, общее для большинства этих соединений свойство - способность к окислению, причем процесс окисления термодинамически выгоден. Большинство органических соединений окисляются в кислородсодержащей атмосфере с выделением большого количества энергии. Благодаря этим реакциям мы получаем энергию не только для обогрева наших домов и движения транспорта (дрова, уголь, нефть), но и для жизнедеятельности нашего организма (рис. 4).
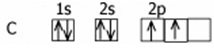
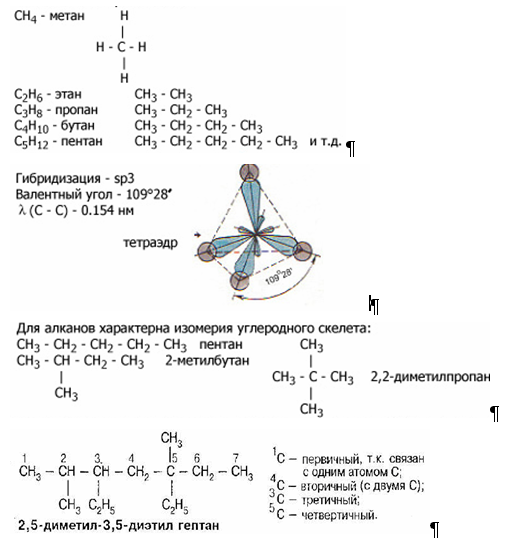
Рис. 4 2.3 Валентность атома углерода в органических соединениях Атомы углерода, входящие в состав органических соединений, всегда будут четырёхвалентны, имеют электронную конфигурацию 1s2s22p2 и могут находиться в трех валентных состояниях
Первое валентное состояние (на примере метана СН4). При образовании молекулы метана атом углерода переходит в возбужденное состояние:
Четыре неспаренных электрона (2s и 2р) участвуют в образовании четырех б - связей. При этом возникают гибридные орбитали. Гибридизация орбиталей - процесс выравнивания их по форме и энергии. Число гибридных орбиталей равно числу исходных орбиталей. В молекуле метана и во всех молекулах органических веществ по месту одинарной связи атомы углерода будут находиться в состоянии бр3 - гибридизации, т.е. у атома углерода гибридизации подверглись орбитали одного s - и трех р - электронов и образовались 4 одинаковые гибридные орбитали.
sp3 – гибридные облака располагаются под углом 109°28`. Второе валентное состояние атома углерода на примере этилена (C2H4) В молекуле этилена каждый атом углерода соеденён с тремя другими атомами, поэтому в гибридизацию вступают З орбитали: одна s и две р, т.е. происходит sр2 - гибридизация. Эти орбитали располагаются под углом 120° по отношению друг к другу.
Две негибридные орбитали перекрываются перпендикулярно плоскости и образуют – связь. Третье валентное состояние атома углерода (на примере ацетилена С2Н2). В молекуле ацетилена атом углерода соединен с двумя другими атомами, поэтому в гибридизацию вступают две орбитали: одна s и одна p, т.е. происходит sp-гибридизация.
Эти орбитали располагаются под углом 180º по отношению друг к другу.
Не вступившие в гибридизацию две p-отбитали при боковом перекрывании образуют две π-связи, расположенные во взаимно перпендикулярных плоскостях.
3. УглеводородыУГЛЕВОДОРОДЫ, органические соединения, молекулы которых состоят только из атомов углерода и водорода. Простейший представитель - метан СН4 . Углеводороды являются родоначальниками всех других органических соединений, огромное разнообразие которых может быть получено введением функциональных групп в молекулу углеводорода; поэтому органическую химию часто определяют как химию углеводородов и их производных. Углеводороды в зависимости от молекулярной массы могут быть газообразными, жидкими или твёрдыми (но пластичными) веществами. Соединения, содержащие в молекуле до четырёх атомов углерода, в обычных условиях - газы, например метан, этан, пропан, бутан, изобутан; эти углеводороды входят в состав горючего природного и попутного нефтяного газов. Жидкие углеводороды входят в состав нефти и нефтепродуктов; они, как правило, содержат до шестнадцати атомов углерода. В состав некоторых восков, парафина, асфальтов, битума, гудрона входят ещё более тяжёлые углеводороды; так, в состав парафина входят твёрдые углеводороды, содержащие от 16 до 30 атомов углерода. Углеводороды делятся на соединения с открытой цепью - алифатические, или нециклические, соединения с замкнутой циклической структурой - алициклические (не обладают свойством ароматичности) и ароматические (в их молекулах имеется бензольное кольцо или фрагменты, построенные из конденсированных бензольных колец). Ароматические углеводороды выделяют в отдельный класс, поскольку из-за наличия замкнутой сопряжённой системы гс-свя-зей они обладают специфическими свойствами. Нециклические углеводороды могут иметь не-разветвленную цепь углеродных атомов (молекулы нормального строения) и разветвлённую (молекулы изостроения), В зависимости от типа связей между атомами углерода как алифатические, так и циклические углеводороды делятся на насыщенные, содержащие только простые связи (алканы, циклоалканы), и ненасыщенные, содержащие наряду с простыми кратные связи (алкены, циклоалкены, диены, алкины, цикло-алкины). Классификация углеводородов отражена на схеме (см. стр. 590), где даны также примеры структур представителей каждого класса углеводородов. Углеводороды незаменимы в качестве источника энергии, поскольку основное общее свойство всех этих соединений - выделение значительного количества теплоты при горении (например, теплота сгорания метана составляет 890 кДж/моль). Смеси углеводородов используют как топливо на тепловых станциях и в котельных (природный газ, мазут, котельное топливо), как топливо для двигателей автомобилей, самолётов и других транспортных средств (бензин, керосин и дизельное топливо). При полном сгорании углеводородов образуются вода и углекислый газ. По реакционной способности различные классы углеводородов сильно отличаются друг от друга: насыщенные соединения относительно инертны, для ненасыщенных характерны реакции присоединения по кратным связям, для ароматических соединений - реакции замещения (например, нитрование, сульфирование). Углеводороды используют как исходные и промежуточные продукты в органическом синтезе. В химической и нефтехимической промышленности применяют не только углеводороды природного происхождения, но и синтетические. Способы получения последних основаны на переработке природного газа (производство и использование синтез-газа - смеси СО и Н2), нефти (крекинг), каменного угля (гидрогенизация), а в последнее время и биомассы, в частности отходов сельского хозяйства, переработки древесины и других производств. 3.1 Предельный углеводороды. Алканы CnH2n+2Особенности химического строения
Основные физические и химические свойства: СН4 газ без цвета и запаха, легче воздуха, нерастворим в воде С-С4 – газ; С5-С16- жидкость; С16 и больше – твердое вещество Примеры углеводородов, используемых в косметологии, их состав и свойства (парафин, вазелин). В косметике углеводороды используют для создания пленки, обеспечивающей скользящий эффект (например, в массажных кремах), и в качестве структурообразующих компонентов различных препаратов. Газообразные углеводороды Метон и этан являются составными частями природного газа. Пропан и бутан (в сжиженном виде) - горючее для транспорта. Жидкие углеводороды Бензин. Прозрачная, воспламеняющаяся жидкость с типичным запахом, легко растворимая в органических растворителях (спирте, эфире, четыреххлористом углероде). Смесь бензина и воздуха - сильное взрывчатое вещество. Специальный бензин иногда применяют для обезжиривания и очистки кожи, например, от остатков пластыря. Вазелиновое масло. Жидкий, вязкий углеводород с высокой точкой кипения и низкой вязкостью. В косметике применяется как масло для волос, масло для кожи, входит в состав кремов. Парафиновое масло. Прозрачное, бесцветное, не имеет ни цвета, ни запаха, густое, маслянистое вещество, высокой вязкости, нерастворимое в воде, почти нерастворимое в этаноле, растворимое в эфире и других органических растворителях. Твердые углеводороды Парафин. Смесь твердых углеводородов, получаемая при дистилляции парафиновой фракции нефти. Парафин представляет собой кристаллическую массу со специфическим запахом и нейтральной реакцией. Парафин применяется в термотерапии. Расплавленный парафин, обладающий высокой теплоемкостью, медленно остывает и, постепенно отдавая тепло, длительно поддерживает равномерное согревание тела. Остывая, парафин переходит из жидкого состояния в твердое и, уменьшаясь в объеме, сдавливает подлежащие ткани. Препятствуя гиперемии поверхностных сосудов, расплавленный парафин повышает температуру тканей и резко усиливает потоотделение. Показаниями к парафинотерапии являются себорея кожи лица, угревая сыпь, особенно индуративные угри, инфильтрированная хроническая экзема. Целесообразно после парафиновой маски назначать чистку кожи лица. Церезин. Смесь углеводородов, получаемая при переработке озокерита. Применяется в декоративной косметике в качестве загустителя, так кок хорошо смешивается с жирами. Вазелин – смесь углеводородов. Является хорошей основой для мазей, не разлагает лекарственные вещества, входящие в их состав, смешивается с маслами и жирами в любых количествах. Все углеводороды не омыляются, не могут проникать непосредственно через кожу, поэтому используются в косметике как поверхностное защитное средство. Все жидкие, полутвердые и твердые углеводороды не прогоркают (не подвергаются воздействию микроорганизмов). Рассмотренные углеводороды называются ацикличными. Им противопоставляют цикличные (имеющие в составе молекулы бензольное кольцо) углеводороды, которые получают при перегонке каменноугольной смолы - бензол (растворитель), нафталин, который раньше применялся кок средство против моли, антрацен и другие вещества. 3.2 Непредельные углеводородыАлкены (этиленовые углеводороды) – непредельные углеводороды, в молекулах которых имеется одна двойная связь
Особенности химического строения
С2 H4 этилен – бесцветный газ со слабым сладковатым запахом, легче воздуха, мало растворим в воде. Принципы составления названия углеводородов: Углеводороды, содержащие двойную связь, оканчиваются на –ен. Этан С2 H6 ®этен С2 H4
3.3 Циклические и ароматические углеводороды, принципы химического строения, примерыАрены (ароматические углеводороды), молекулы которых содержат устойчивые циклические структуры – бензольные ядра, с особым характером связей.
В молекуле бензола нет одинарных (С - О и двойных (С = С) связей. Все связи равноценны, их длины равны, Это особый вид связи - круговое р-сопряжение. Гибридизация - ;sр2 Валентный угол -120°
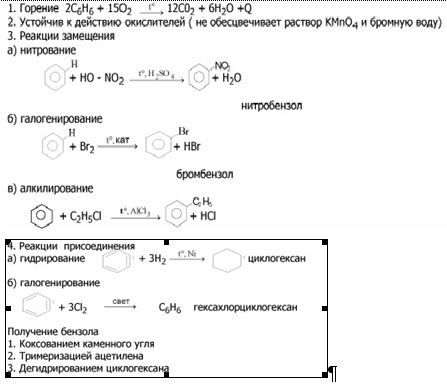
Шесть негибридных связей образуют единую p-электронную систему (ароматическое ядро), которое располагается перпендикулярно плоскости бензольного кольца. Химические свойства: Бензол занимает промежуточное положение между предельными и непредельными углеводородами, т.к. вступает в реакцию замещения (протекает легко) и присоединения (протекает трудно).
Азулен. Это циклический углеводород, получаемый синтетическим путем (природный аналог хамазулен получают из цветков ромашки и тысячелистника). Азулен обладает противоаллергическими и противовоспалительными свойствами, снимает спазм гладкой'мускулатуры, ускоряет процессы регенерации и заживления тканей. Применяется в косметике в концентрированном виде (жидкость темно-синего цвета) и в виде 25%-ного раствора в составе детских кремов, зубной пасты и декоративных средств, а также в смолах для биомеханической депиляции. 4. Спирты4.1 ОпределениеСпирты - это органические соединения, в которых один атом водорода (Н) заменен на гидроксильную группу (ОН). 4.2 Функциональные группы. Классификация спиртов на одноатомные и многоатомные спирты, примеры. Принципы составления названия спиртовВ соответствии с количеством ОН-групп различают одно- и многоатомные спирты. В зависимости от расположения ОН-группы спирты делятся на первичные, вторичные и третичные. В отличие от парафин-углеводородов они имеют относительно высокую точку кипения. Все многоатомные спирты обладают сладковатым привкусом. Спирты с короткими цепочками гидрофильны, т.е. смешиваются с водой и хорошо растворяют гидрофильные вещества, Одноатомные спирты с длинными цепочками почти или совершенно не растворяются в воде, т.е. гидрофобны. Спирты с большой массой молекул (жирные спирты) при комнатной температуре твердые (например, миристиловый или цетиловый спирт). Спирт, содержащий более 24 атомов углерода, называют вощеным спиртом. С увеличением числа гидроксильных групп усиливаются сладкий привкус и растворимость спирта в воде. Поэтому глицерин (3-атомный спирт), похожий на масло, хорошо растворяется в воде. Твердый 6-атомный спирт сорбит используется как заменитель сахара для диабетических больных. 4.3 Основные химические и физические свойства спиртов, их применение в косметологии (метанол, этанол, изопропанол, глицерин)Одноатомные спирты Метанол (метиловый спирт, древесный спирт) - прозрачная, бесцветная жидкость, легко смешиваемая с водой, спиртом и эфиром. Это крайне ядовитое вещество в косметике не применяется. Этанол (этиловый спирт, винный спирт, спирт пищевой) - прозрачная, бесцветная, летучая жидкость, может смешиваться с водой и органическими растворителями, значительно менее ядовит, чем метанол, широко применяется в медицине и косметике в качестве растворителя для биологически активных веществ (эфирных масел, смол, йода и т.д.). Получают этанол в результате брожения веществ, содержащих сахар и крахмал. Процесс брожения происходит за счет ферментов дрожжей. После брожения спирт выделяют путем перегонки. Затем производится очистка от нежелательных веществ-примесей (ректификация). Этанол поступает в аптеки в основном крепостью 96°. Другие смеси этанола с водой содержат 90, 80, 70, 40% спирта. Почти чистый спирт (с очень незначительными примесями воды) называют абсолютным спиртом. В зависимости от цели применения спирта его ароматизируют различными добавками (эфирными маслами, камфорой). Этанол способствует расширению подкожных капилляров, обладает дезинфицирующим действием. Туалетная вода для лица может содержать от 0 до 30% спирта, лосьон для волос - около 50%, одеколон - не менее 70%. В состав лавандовой воды входит около 3% эфирного масла. Духи содержат от 12 до 20% эфирных масел и фиксатор, одеколоны - около 9% эфирных масел и немного фиксатора. Изопропанол (изопропиловый спирт) - полноценный и недорогой заменитель этанола, относится к вторичным спиртам. Даже очищенный изопропиловый спирт имеет характерный запах, который не поддается устранению. Дезинфицирующие и обезжиривающие свойства изопропанола сильнее, чем у этилового спирта. Он применяется только наружно, в составе туалетной воды для волос, в фиксаторах и т.п. Водка не должна содержать изопропанол, а в спиртовой настойке на хвойных иголках (хвойный концентрат) допускается его незначительное количество. Многоатомные спирты Двухатомные спирты имеют стандартное окончание названия - гликоль. В косметических препаратах в качестве растворителя и увлажнителя применяют пропиленгликоль, обладающий невысокой токсичностью. Двухатомные спирты, или гликоли, по заместительной номенклатуре называют диолами. Трехатомный спирт - глицерин - широко используется в медицине и фарма-цее. По консистенции глицерин похож на сироп, почти без запаха, гигроскопичен, имеет сладкий привкус, растворим во всех других веществах, содержащих ОН-группу, нерастворим в эфире, бензине, хлороформе, в жирных и эфирных маслах. В торговлю поступает 86 - 88%-ный глицерин и обезвоженный 98%-ный глицерин. В разбавленном виде глицерин входит в состав кремов для кожи, туалетной воды для лица, зубных паст, мыла для бритья, геля для рук. Разбавленный в соответствующей пропорции, он смягчает кожу, делает ее эластичной, заменяя естественный фактор влажности кожи. В чистом виде в препаратах для ухода за кожей не применяется, поскольку пересушивает ее. Сорбит- разновидность виноградного сахара, в соединении с водой образует сладковатую вязкую жидкость, которая может быть использовано как заменитель глицерина. Сорбит обладает способностью сохранять влажность кожи, поэтому входит в состав увлажняющих кремов, кремов для бритья, зубных пост и других косметических препаратов. 5. Производные спиртов – эфиры и кетоны:КЕТОНЫ, органические соединения, в молекулах которых содержится карбонильная группа
Большинство кетонов - бесцветные жидкости с приятным запахом. Молекулы кетонов не способны образовывать водородные связи, поэтому температуры кипения и плавления кетонов значительно ниже, чем соответствующих вторичных спиртов. Низшие кетоны растворяются в воде. По химическим свойствам кетоны подобны альдегидам, но менее реакционноспособны. Двойная связь С=О в кетонах поляризована (электронная плотность смещена к атому кислорода в силу его большей электроотрицательности), поэтому для кетонов характерны реакции присоединения по карбонильной группе. Например, присоединяя водород, кетоны восстанавливаются в спирты по схеме:
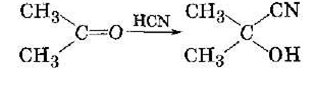
А реакция присоединения синильной кислоты, приводящая к нитрилам, имеет важное значение в органической химии, поскольку позволяет изменить углеродный скелет молекулы
Вследствие поляризации двойной связи в молекуле кетонов поляризуется и связь С-Н в ме-тиленовой группе СЩ, непосредственно связанной с карбонильной группой; подвижность протона метиленовой группы увеличивается. Результатом чего является способность кетонов к кето-енольной таутомерии, приводящей к равновесию кетон-енол, например:
Подвижность протонов определяет и возможность протекания реакций конденсации с участием кетонов. При окислении изопропанола образуется известный растворитель ацетон, он применяется при производстве лаков и смывки для ногтей. В косметике часто используют заменители кетона, так как он не обладает обезжиривающим эффектом. При окислении второго С-атома глицерина получают окисленный кетон (дигидроксиацетон): Дигидроксиацетон реагирует с белками и аминокислотами рогового слоя эпидермиса, вызывая окрашивание кожи, похожее на загар. Усиления образования пигмента меланина не происходит. Этот загар устойчив к воде и в полной мере соответствует натуральному загару. Он абсолютно не опасен! 5%-ный дигидроксиацетон (ДНА) вводится в масляные и водные эмульсии ДНА. Не может быть использован как средство от загара, так как не обладает фильтрующей способностью по отношению к ультрафиолетовым лучам. ЭФИРЫ Простые эфиры Это органические вещества, молекулы которых состоят из углеводородных радикалов, соединенных атомом кислорода R - О - R. Сложные эфиры Это вещества, имеющие общую формулу: О R - С - OR, где R и R'- углеводородные радикалы. Сложный эфир образуется из спирта или фенола и карбоновых кислот с выделением воды в присутствии серной кислоты. В название входит часть названия спирта и часть названия кислоты (например, сложный эфир уксусной кислоты и амилового спирта - амилацетат). Известный сложный эфир фенола - аспирин (фенол + ацетилсалициловая кислота). Простейшими эфира ми являются фруктовые эфиры, или эссенции, названные так из-за своего легкого фруктового запаха. Они используются для производства лака и жидкости для снятия лака, как растворители в технике и как ароматизаторы при производстве пищевых продуктов. Натуральные животные и растительные жиры представляют собой сложные эфиры трехатомного спирта глицерина с различными жирными кислотами. Например, кукурузное масло содержит триглицерид ненасыщенной линолевой кислоты (до 48%), масло какао - триглицериды насыщенных стеариновой (до 25%) и пальмитиновой (34%) кислот. Сложные эфиры жирных кислот и высокомолекулярных спиртов - полусинтетические жироподоб-ные вещества (изопропилмиристат, диизопропиладипат, бутилстеарат, изопропилпальмитат), которые легко эмульгируются, что позволяет получать маловязкие эмульсии. Они легко впитываются в кожу, не оставляя ощущения липкости и жирности. Используются для полной или частичной замены животных и растительных масел в средствах для ухода зо кожей и волосами, как растворители или смягчающие средства в лаках для ногтей. Другие сложные эфиры жирных кислот - известные эмульгаторы - драгил, цетиол, кремофор. Лецитин. Лецитин (фосфатидилхолин) - фосфолипид, сложный эфир глицерина с фосфорилилхолином и двумя остатками жирных кислот, из которых одна ненасыщенная. Содержится во всех клетках, преимущественно в биологических мембранах. Лецитин экстрагируют из соевых, бобов и арахиса. Много лецитина содержится в яичном желтке. Животный и растительный лецитин используют как добавки в кремы (в качестве эмульгатора) для кожи, в туалетную воду, лечебные препараты и аэрозоли для волос и т.д. Пурцелин. Это масляный или твердый, воскообразный сложный эфир, образованный вытяжкой жира из желез водоплавающих птиц. Он имеет высокую степень реагирования, хорошо переносится кожей, используется в косметических препаратах. 6. Органические кислотыКарбоновая кислота – представитель предельных одноосновных кислот. Карбоновыми кислотами называются органические вещества, в состав которых входит карбоксильная группа или в упрощенной записи - СООН. Карбоксильная группа состоит из соединенных карбонильной и гидроксильной групп, что определило ее название. В карбоновых кислотах карбоксильная группа соединена с углеводородным радикалом R, поэтому в общем виде формулу карбоновой кислоты можно записать так: R-СООН. В карбоновых кислотах карбоксильная группа может быть соединена с различными углеводородными радикалами ~- предельными, непредельными, ароматическими. В связи с этим выделяют предельные, непредельные и ароматические карбоновые кислоты, например:
В зависимости от числа карбоксильных групп, содержащихся в молекулах карбоновых кислот, различают одноосновные и двухосновные кислоты, например:
атом углерод кислота спирт липиды Одноосновные кислоты называют также монокарбоновыми, а двухосновные – дикарбоновыми кислотами. Общая формула членов гомологического ряда предельных одноосновных карболовых кислот СnН2n-1СООН, где п = 0, 1, 2, 3.. Номенклатура. Названия карбоновых кислот по заместительной номенклатуре строят из названия соответствующего алкана с добавлением окончания -овая и слова «кислота». Если углеродная цепь разветвленная, то в начале названия кислоты записывают заместитель с указанием его положения в цепи Нумерацию атомов углерода в цепи начинают с углерода карбоксильной группы. Примеры:
Некоторые предельные одноосновные кислоты:
Для некоторых членов гомологического ряда предельных карбоновых кислот применяют тривиальные названия, приведены формулы некоторых предельных одноосновных кислот и их названия по заместительной номенклатуре и тривиальные названия. Изомеры. Начиная с бутановой кислоты С3Н7СООН9 члены гомологического ряда предельных одноосновных кислот имеют изомеры. Их изомерия обусловлена разветвленностыо углеродной цепи углеводородных радикалов. Так, бутановая кислота имеет следующие два изомера (в скобках записано тривиальное название).
Формуле С4 Н9 СООН соответствуют четыре изомерные карбоновые кислоты:
Свойства, Кислоты гомологического ряда с нормальным -v строением от муравьиной до> С8 Н17 СООН (нонановой кислоты) при обычных условиях ~ бесцветные жидкости, имеющие резкий запах. Высшие члены ряда, начиная с С.9 Н19 СООН, - твердые вещества. Муравьиная, уксусная и продионовая кислоты хорошо растворимы в воде, смешиваются с ней в любых отношениях. Другие жидкие кислоты ограниченно растворимы в воде. Твердые кислоты в воде практически нерастворимы. Особенности химических свойств карбоновых кислот обусловлены сильным взаимным влиянием карбонильной С-О и гидроксильной О-Н групп. В карбоксильной группе связь между углеродом и карбонильным кислородом сильнополярна.. Однако положительный заряд на атоме углерода частично уменьшается в результате притяжения электронов атома кислорода гидроксильной группы. Поэтому в карбоновых кислотах карбонильный углерод менее склонён к взаимодействию с нуклеофильными частицами чем в альдегидах и кетонах. С другой стороны, под влиянием карбонильной группы усиливается полярность связи О-Н за счет смещения электронной плотности от кислорода к атому углерода. Все указанные особенности* карбоксильной группы -можно проиллюстрировать следующей схемой:
Рассмотренный характер электронного строения карбоксильной группы обусловливает относительную легкость отрыва водорода этой группы. Поэтому у карбоновых кислот хорошо выражены кислотные свойства. F безводном' состоянии и особенно в водных растворах карбоновые кислоты диссоциируют на ионы; Кислый характер растворов карбоновых кислот можно установить с помощью индикаторов. Карбоновые кислоты являются слабыми электролитами, причем сила карбоновых кислот уменьшается с увеличением молекулярной массы кислоты. Наиболее часто встречающиеся жирные кислоты: · пальмитиновая CH3 (CH2 )14COOH, · стеариновая СН3 (СН2 )16СООН, · олеиновая СН3 (СН2 )7 СН=СН(СН2 )7СООН, · линолевая СНз(СН2)4 (СН=СНСН2)2(СН2)6 СООН, · линоленовая СН3 СН2 (СН=СНСН2 )3(СН2)6СООН, · арахидоноваяСН3 (СН2 )4(СН=СНСН2 )4(СН2)2СООН, · арахиновая СН3 (СН2 )18СООН и некоторые другие кислоты. Муравьиная кислота. Это легкоподвижная, бесцветная жидкость с исключительно резким запахом, которая смешивается с водой в любых пропорциях, очень едкая, вызывающая волдыри на коже. Она применяется в качестве консерванта. Уксусная кислота. Обладает теми же свойствами, что и муравьиная. Концентрированная уксусная кислота затвердевает при 17°С, превращаясь в массу, похожую на лед. Ее используют при изготовлении уксусно-кислого глинозема, в качестве добавки в лосьон для бритья, а также при производстве ароматических веществ и растворителей (смывка для лака - амилацетат). Бензойная кислота. Имеет кристаллические иголочки без цвета и запаха. Она плохо растворяется в воде и легко - в этаноле и эфире. Это известное средство для консервации. Обычно применяется в виде натриевой соли как противомикробное и фунгицидное средство. Молочная кислота. В концентрированном виде обладает кератолитическим действием. В увлажняющих кремах используют натриевую соль молочной кислоты, которая благодаря своим гигроскопическим свойствам оказывает хорошее увлажняющее воздействие, а также отбеливает кожу. Винная кислота. Состоит из бесцветных прозрачных кристаллов или представляет собой кристаллический порошок с приятным кислым вкусом. Она легко растворяется в воде и этаноле. Ее используют в соли для ванн, а также в ополаскивателях для волос после применения лака. Тиомолочная кислота. Это молочная кислота, в которой один атом кислорода замещен атомом серы. Масляная кислота. Это жидкость без цвета и запаха, растворимая только в органических растворителях (бензине, бензоле, тетрахлоруглероде). В свободном виде масляная кислота в косметике не употребляется, она является составляющим элементом мыла и шампуней. Сорбиновая кислота. Эта твердая, белая, многократно ненасыщенная жирная кислота, трудно растворимая в холодной воде и легка растворимая в спирте или эфире. Ее соли и эфиры абсолютно нетоксичны, они используются как консерванты в продуктах питания и косметических средствах. Линолевая, линоленовая, арахидоновая кислаты. Эссенциальные (незаменимые) ненасыщенные жирные кислоты, которые не синтезируются в организме. Комплекс этих кислот называют витамином Г. Их физиалогическая роль заключается в следующем: - нормализация уровня холестерина в крови; - участие в синтезе простангландинов; - оптимизация функций биологических мембран; - участие в липидном обмене кожи. Они входят в состав эпидермальных липидов, образуя строго организованные липидные структуры (пласты) в роговом слое эпидермиса, которые обеспечивают его барьерные функции. При недостатке незаменимых жирных кислот происходит их замена на насыщенные. Например, замена линолевой кислоты на пальмитинавую приводит к дезорганизаци липидных пластов, в эпидермисе образуются участки, лишенные липидов и, следовательно, проницаемые для микраарганизмов и химических агентов. Эссенциальные жирные кислоты содержатся в масле семян кукурузы, пщеницы, сои, льна, кунжуга, арахиса, миндаля, подсолнечника. 7. МылаМЫЛА, соли высших жирных кислот с числом углеродных атомов от 12 до 18, обладающие поверхностно-активными свойствами. Различают мыла растворимые в воде и нерастворимые. Растворимые мыла содержат катион щелочного металла: натрия, реже калия. Поэтому их называют щелочными мылами. Эти мыла получают щелочным гидролизом жиров, например:
Водорастворимые мыла обладают наиболее сильным моющим действием и получили наибольшее распространение. Мыла с катионами кальция, магния, алюминия и др. в воде не растворяются; называют их «металлическими» мылами. Эти мыла получают обычно по реакции обмена между щелочными мылами и солями соответствующих металлов. Металлические мыла используют как загустители пластических смазок, ускорители высыхания лакокрасочных материалов и пр. В промышленности в качестве исходных веществ для получения натриевого щелочного мыла применяют животные жиры (сало низких сортов), растительные масла (хлопковое, пальмовое, кокосовое и др.), гидрогенизированные жиры, а также жирозаменители (например, синтетические жирные кислоты, канифоль). При нагревании сырья с гидроксидом натрия образуется густой раствор - «мыльный клей», содержащий глицерин и соли жирных кислот. При охлаждении раствор затвердевает и превращается в т. наз. клеевое мыло, используемое для хозяйственных и технических нужд (содержание основного вещества - 40-55%). Мыла получают также, используя высшие углеводороды нефти - парафин. Парафин окисляют до карбоновых кислот (смесь), выделяют из смеси нужные кислоты и действием соды Na2CO3 переводят их в натриевую соль. Как соли сильных оснований и слабых кислот, мыла в водных растворах подвергаются гидролизу, например:
поэтому растворы мыла имеют щелочную реакцию. Мыла обладают особыми поверхностно-активными свойствами, поэтому в растворах они проявляют моющее действие. В жесткой воде моющее действие мыла слабое. Это обусловлено взаимодействием их с ионами кальция, приводящим к образованию малорастворимых солей: В кислой среде мыла разлагаются с образованием высших карбоновых кислот. Мыла применяются не только как моющие средства. Они являются компонентами смазок, реагентами для флотации. Мыла плохо моют в жесткой воде. Поэтому развивается производство синтетических моющих средств (СМС). СМС – соли кислых сложных эфиров высших спиртов и серной кислоты:
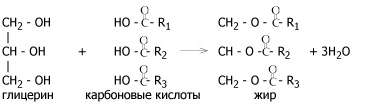
Жёсткость воды обычно определяют титрованием щелочным раствором комплексного соединения трилона Б. По количественному содержанию ионов Са2+ и Mg2+ природную воду различают как очень мягкую (концентрация этих ионов до 30 мг/л), мягкую (30-80 мг/л), средней жёсткости (80-150 мг/л), жёсткую (150-250 мг/л) и очень жёсткую (свыше 250 мг/л). Особенно большой жёсткостью отличается вода морей и океанов. В океанах средняя концентрация в воде ионов кальция 450 мг/л, магния -1290 мг/л и общая - 1740 мг/л. Напротив, многие воды северных рек и рек, имеющих ледниковое питание, очень мягки. Вода для хозяйственных нужд и для питья - водопроводная вода - имеет концентрацию ионов Са и Mg не более 170 мг/л. В жёсткой воде растворённые в ней соли при нагревании и испарении воды образуют в паровых котлах, отопительных приборах и на стенках металлической посуды слой накипи, который плохо проводит теплоту. Для удаления накипи приходится применять специальные вещества - антинакипины- гл. обр. органические кислоты, например адипиновую НООС(СН2 )4СООН и щавелевую НООССООН, растворяющие накипь. При стирке или мытье в жёсткой воде требуется повышенный расход мыла, поскольку часть мыла (а это калиевая соль стеариновой кислоты С47Н35СООК) расходуется на связывание ионов Са2+ и Mg2+ и осаждается в виде нерастворимых солей: 2С17 Н35 СОО + Са2+ - (С17 Н35 СОО)2Са 2С17 Н35 СОСГ + Mg2 + = (C17 H35 COO)2Mg Мыльная пена образуется лишь после полного осаждения этих ионов. В воде с высокой кальциевой жёсткостью плохо развариваются овощи и мясо, т. к. катионы Са2 + с белками пищевых продуктов образуют нерастворимые соединения. Большая магниевая жёсткость (как в морской воде) придаёт воде горький привкус и оказывает послабляющее действие на кишечник. Очень жёсткую воду перед употреблением умягчают, обрабатывая её, например, смесью гашёной извести и соды. При этом известь устраняет карбонатную жёсткость: Са(НСО3 )2 + Са(ОН)2 = 2СаСО3 + 2Н2 О Mg(HCO3)2 + 2Са(ОН)2 = Mg(OH)2 + 2СаСО3 + 2Н2 О, а сода - некарбонатную жёсткость, например: CaSO4 + Na2 CO3 = CaCO3 + Na2 SO4 Кроме мыла разработаны другие моющие средства -синтетические моющие средства. Их производят без использования такого важного пищевого сырья, как жиры. Использование мыла Мыла - типичные поверхностно-активные вещества, и все их полезные для человека качества - следствие их поверхностной активности. Грязь удерживается на ткани тонким слоем жиров и масел, которые должны быть удалены. Мыла обладают моющими свойствами, посколь ку способны эмульгировать жиры и масла, т. е. переводить их в мельчайшие капельки, которые смачиваются водой. Эмульгирующие свойства моющих веществ связаны с наличием в их молекулах одновременно гидрофильных (имеющих сродство к воде) и гидрофобных (имеющих сродство к неполярной фазе, например к липидам -жирам и маслам) групп. Гидрофильными свойствами обладает полярный фрагмент СОО~, а углеводородная цепь является гидрофобной группой. При мытье загрязнённой ткани молекулы мыла окружают капли жира или масла, так что гидрофобные группы оказываются «растворёнными» в масле, а гидрофильные - в воде. Образуется мицелла, которая уносится с током воды (рисунок). Поскольку поверхности всех мицелл заряжены отрицательно, мицеллы не слипаются. 8. Липиды (жиры)8.1 Определение, особенности химического строенияЛИПИДЫ, большая группа природных органических соединений, практически нерастворим! в воде, но хорошо растворимых в неполярных органических растворителях (например, х форме, эфире, бензоле). С помощью таких растворителей липиды извлекают из клеток животных, растений и микроорганизмов. Назван происходит от греч. слова липос - жир, т.к жиры являются наиболее известными и самыми распространёнными в природе липидами. Структурное многообразие липидов обусловлено наличием в их составе остатков жирных кислот, причём жирные кислоты липидов высших растений и животных, как правило, имеют чётное число углеродных атомов - 16, 18 или 20. Получают жиры реакцией этерификации:
  8.2 Химические свойства жиров 8.2 Химические свойства жиров
определяются принадлежностью их к классу сложных эфиров. Поэтому наиболее характерна для них рекция гидролиза:
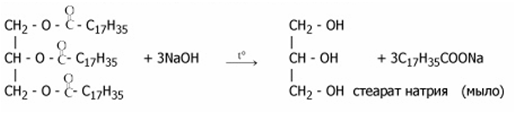
Гидролиз жиров в щелочной среде называется омылением:
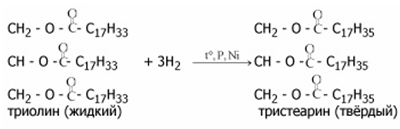
Жиры подвергаются гидрированию:
Связующим звеном между гидрофильным и гидрофобным участками обычно являются остатки многоатомных алифатических спиртов, содержащих две или три гидроксильные группы. Например, более половины липидов, встречающихся в природе, - производные трёхатомного спирта глицерина. Согласно одной из возможных классификаций, все липиды делят на простые липиды, сложные липиды и производные липидов. К первым относят эфиры жирных кислот и спиртов, например жиры и воски. В молекулу липидов второй группы, кроме остатков жирных кислот и спиртов, входят и другие фрагменты. Например, в фосфолипидах, служащих главными структурными компонентами биологических мембран, один из остатков жирной кислоты замещён на фосфатную группу. К третьей группе относят все соединения, которые нельзя отнести к первым двум, например стероиды, витамины липидной природы и пр. В живых организмах встречаются также вещества, в молекулах которых липиды связаны с соединениями других классов, например с белками (т. наз. липопротеины), углеводами (гликолипиды) и пр. Структурное разнообразие липидов, а также широкий диапазон специфических функций, выполняемых ими в организме, служат одной из основ многообразия природных систем. 8.3 Значение жиров для человеческого организмаЭтому классу соединений принадлежит важная роль в процессах жизнедеятельности. Они служат энергетическим резервом клеток, выполняют роль защитных барьеров, предохраняющих живые организмы от термического, электрического и физического воздействий, вход в состав оболочек, защищающих от инфекций и излишней потери или накопления воды, moj быть предшественниками в биосинтезе друг важных соединений, являются активными компонентами биологических мембран. Некоторые витамины и гормоны также относятся к классу липидов. 8.4 Источники липидов, масла и твердые жиры. Применение липидов в косметологииЖИРЫ И МАСЛА РАСТИТЕЛЬНОГО И ЖИВОТНОГО ПРОИСХОЖДЕНИЯ Все жиры и масла растительного и животного происхождения образуются из элементов С, Н и О. Они представляют собой сложные эфиры глицерина, растворяются только в органических растворителях (бензине, бензоле, тетрахлоруглероде, три-и перхлорэтилене), не распадаются при нагревании до 250°С. Под воздействием света, воздуха, воды жиры могут распадаться на жирные кислоты и глицерин, изменяя при этом цвет и запах. Прогорклые жиры не могут быть использованы в косметике. Все жиры, масла и мази легче воды, их плотность между 0,8 и 0,94. Растительные жиры содержатся в основном в семенах и плодах. Животные жиры получают главным образом путем вытапливания или вытяжек, растительные - путем отжима или вытяжки. Первый отжим считается самым лучшим, его называют также холодным отжимом. При вытяжке можно получить большее количество масла. При этом масло экстрагируется растворителями; бензином, бензолом и проч. Во всех растительных и животных жирах присутствуют липоиды, так называемые попутчики жиров. Липоиды Это вещества, которые по своему химическому строению, а также физическим и физиологическим свойством сходны с жирами. Кроме того, они являются эмульгаторами, как, например, холестерин, эргостерин, лецитин и т.д. Растительные жиры и масла Растительные жиры и масла находят в косметике все более широкое применение. Ценные растительные масла входят в состав высококачественных эмульсий и жировых композиций для смягчения кожи. Растительные жиры играют важную роль в диетологии. Заслугой д-ра Феликса Гранделя является создание «диеты красоты», в которую включаются масла зародышей зерна. В них содержатся витамины, фитогормоны и жизненно необходимые (эссенци-альные) ненасыщенные жирные кислоты. Масло авокадо. Высококачественное масло, получаемое из плодов авокадо, произрастающих в Мексике и Гватемале. Оно желтоватого цвета, не усыхает, долго хранится и хорошо проникает в кожу. Содержит лецитин, а также витамин А и провитамин Д, микроэлементы. Может быть использовано во всех высококачественных средствах для ухода за кожей. Масло календулы. Получают из свежих цветков календулы методом масляной экстракции. Для вытяжки применяется любое растительное масло. Масло календулы имеет желто-красный цвет с резким ароматом. Содержит высокую концентрацию каратиноидов (каротин, ликопин, флавохром), органические кислоты, эфирные масле!. Обладает высокими противовоспалительными и антиоксидантными свойствами. Его вводят в препараты для ухода за потрескавшейся, грубой, обветренной и чувствительной кожей. Масло земляного ореха, или арахиса. Получают из земляного ореха в результате отжима. Оно содержит 40 - 80% триглице-ридов. Желтое, неусыхающее, с мягким привкусом. В косметической промышленности применяется в эмульсиях, мылах, в средствах по уходу за кожей тела и лица. Японский воск. По своему химическому составу чистый жир, так как в основном содержит триглицериды. Его получают в Японии при вываривании или отжиме плодов сумах. Применяется как заменитель пчелиного воска. Масло зверобоя. Получают из цветков зверобоя путем масляной экстракции. Свежие цветы сначала раздавливают, затем помещают в оливковое масло. Смесь в стеклянной емкости несколько недель выдерживают на солнце, пока масло не станет темно-красного цвета. Масло зверобоя имеет типичный запах и вводится в специальные кремы для сверхчувствительной, аллергической кожи. Повышает чувствительность кожи к ультрафиолету. Масло какао. Получают из семян плодов какао, предварительно обжаренных и очищенных от скорлупы. Оно представляет собой твердый жир, от желтоватого до белого цвета, с приятным запахом, который становится мягче уже при температуре тела. Применяется в губной помаде, мазях и кремах, в жирных масках для лица, а также в композициях для особо чувствительной кожи как средство защиты ее от неблагоприятных погодных воздействий. Масло моркови. Создается на базе масляного экстракта моркови. Оно содержит каротин - провитамин А, вводится в препараты для ухода за сухой, шелушащейся кожей. Кокосовое масло. Получают из съедобной ткани кокосового ореха, плода кокосовой пальмы. Кокосовое масло в твердом виде применяется в основном в мылах. Льняное масло- Получают из семени льна. Оно богато ненасыщенными жирными кислотами - линолевой и линоленовой. После хорошей очистки удаляют оболочку семени и дробят его. Затем производят отжим масла при температуре 65 - 70°С Полученное масло-сырец очищают, фильтруют и осветляют. После холодной прессовки льняное масло имеет золотисто-желтый цвет, мягкий, приятный вкус и запах. После горячей прессовки - цвет от янтарного светлого до коричневатого, резкий запах. Под воздействием кислорода льняное масло быстро высыхает. В косметике употребляется только льняное масло после холодной прессовки, в основном, в средствах для ухода за телом и волосами. Миндальное масло. Получают из кисло-сладкого миндаля. Оно светло-желтого цвета, без запаха, имеет нежный, мягкий вкус, может быстро прогоркнуть. Считается одним из лучших масел для косметических целей. Оно не обладает подсушивающим эффектом, используется в медицинских и косметических мазях и кремах. Из выжимок после прессования получают миндальные отруби. Оливковое масло. Получают в результате холодной прессовки мякоти плодов оливкового дерева, в них содержится до 50% оливкового масла. Оно светло-желтого или зеленоватого цвета с типичным привкусом и запахом, мутнеет при температуре +10° и затвердевает при температуре ниже +]0°, не прогоркает. Его применяют в основном в масляных композициях, масляных ванночках для кожи, для массажа чувствительной кожи, для производства мыла и для изготовления масляно-водных и водно-масляных эмульсий. Масло из зародышей риса. Это масло получают из ядер семян риса. Ядра семян риса содержат до 25% масла, рисовые отруби - до 14%. Это зеленовато-желтое или коричневатое, приятно пахнущее масло. Быстро прогоркает. Применяется так же, как масло из зародышей пшеницы, кроме того, при производстве высококачественных сортов мыла. Рисовое масло. Получают из семян риса, в которых его содержится до 60%. Оно почти бесцветное, со слабым запахом и привкусом, растворяется до прозрачности в чистом спирте и уксусной кислоте, в эфире и бензине - с трудом. Это тягучее, не высыхающее масло, может долго сохраняться. Содержащаяся в нем рисовая масляная кислота действует как антиоксидант. Благодаря хорошей растворимости в холодном спирте, оно использовалось ранее как составная часть туалетной воды для волос. Способствует росту волос и поэтому находит применение в средствах по уходу за ресницами и бровями. Масло из зародышей ржи. Это масло содержится в ядрах семян ржи. В них присутствует около 8 -10% масла. Полученный продукт сходен с маслом из семян пшеницы. Это масло желто-коричневого или светло-желтого цвета, густое, имеет легкий запах свежего хлеба. Применяется так же, как и масло пшеницы, но имеет более низкий процент содержания витаминов. Кунжутное масло. Получают из очищенных и раздробленных семян кунжута. Родина кунжута Индия, но его культивируют и в других тропических и субтропических странах, например в Италии. Семена содержат до 50% масла. Кунжутное масло имеет светло-желтый цвет, приятный вкус, почти без запаха, при температуре 20° превращается в мазь. Долго не прогоркает и поэтому может успешно применяться в препаратах с длительным сроком хранения. Оно играет особую роль как экстрагирующее масло при производстве ароматических веществ. Масло ши. Экстракт из растущего в Африке ореха ши. Используется для замены масла какао в кондитерской промышленности при изготовлении шоколада и как жир в средствах для ухода за телом. Масло ши защищает кожу от температурных влияний и солнца, В косметике оно находит применение как концентрат неомыляющейся добавки. Масло грецкого ореха - Жирное масло, получаемое в результате прессования грецких орехов. Совершенно не имеет запаха, цвета и является одним из лучших масел в косметике. Масло из зародышей пшеницы. Получают из зародышей (ядра) пшеницы при холодном прессовании и последующей очистке. Ядра пшеницы содержат 6 - 10% масла. Оно имеет желтый цвет и слабый, оригинальный запах. Содержит провитамин А, витамин Е, полиненасыщенные жирные кислоты и фитогормоны, а также фитостерин и лецитин. Его перерабатывают в высококачественный продукт для использования в средствах по уходу за кожей и в пищевой промышленности. Масло огуречной гравы (бурачника). Содержит слизистые вещества, витамины, линолевой кислоты до 24%. Обладает противовоспалительными, смягчающими и увлажняющими свойствами. Масло из семян малины. Содержит высокую концентрацию линолевой, леноленовой и арахнаидоновой кислот. Нормализует липидный обмен в коже, восстанавливает ее барьерные функции, устраняет шелушение и раздражение. Применяют в средствах для ухода за кожей и волосами. Облепиховое масло. Это масляный экстракт плодов облепихи. Содержит каратиноиды (до 60 мг%), витамины С, группы В, дубильные вещества, органические кислоты. Уменьшает воспалительные процессы. Масло шиповника. Представляет собой масляный экстракт плодов шиповника. Содержит высокую концентрацию каратинои-дов, витамина С, органических кислот, микроэлементов. Способствует заживлению ран, уменьшает воспалительные процессы Масло вечерней примулы. Масляный экстракт цветов, содержит высокую концентрацию полиненасыщенных жирных кислот, способствует нормализации липидного обмена в коже, восстанавливает ее барьерные функции. РАСТИТЕЛЬНЫЕ ВОСКИ Воски - это сложные эфиры жирных кислот и длинноцепочечных (высокомолекулярных) спиртов. Масло (воск) жожоба. Жожоба - кустарниковое растение, принадлежащее к семейству буковых, произрастает в Центральной Америке. Куст жожоба - это вечнозеленое, медленно растущее растение с глубоко уходящими в землю корнями. Дикорастущие кусты достигают возраста 100 - 150 лет. Плод заключен в скорлупу и имеет вес от 0,5 до 0,8 кг. Ядро плода содержит от 44% до 59% масла жожоба. Хотя жожоба обычно называют маслом, это жидкий воск. Масло жожоба использовалось в Индии как средство для ухода за волосами и кожей, а также как масло для бороды и усов. Жожоба имеет исключительную устойчивость к прогорклости. На коже обнаруживает очень хорошую степень реагирования. Новые исследования показали, что масло жожоба способно глубоко проникать в кожу. Воск карнауба. Самый твердый растительный воск, он образуется на листьях бразильской восковой пальмы (до 7 грамм на каждом листе}. В процессе высушивания листья скручиваются, и отделяется воск. Его перетапливают, очищают и по возможности осветляют. Применяемый в косметике воск должен быть светлого, желтоватого цвета. Он плавится при температуре около 85°С. Широко применяется в декоративной косметике (тушь для ресниц, губная помада и пр.). Придает косметическим препаратам нужную консистенцию и термостойкость. Канделилльский воск. По свойствам и прочности напоминает карнаубский. Получают из кактусов, произрастающих в штатах Техас, Аризона и в Мексике. При нагревании появляется легкий запах бензойной кислоты. ЖИВОТНЫЕ ЖИРЫ И МАСЛА (триглицериды) Яичное масло. Вырабатывается из желтка свежего яйца птицы. Желток нагревают и после его свертывания выдавливают масло под прессом. Это густое масло от желтоватого до красно-желтого цвета с мягким запахом. Яичный желток содержит лецитин, холестерин, провитамин А, свободные жирные кислоты, пальмитиновую и стеариновую кислоты, применяется в кремах и шампунях. Лебертан. Получают преимущественно из печени рыб тресковых пород. Он содержит витамин А, Д, Е, насыщенные и ненасыщенные жирные кислоты, железо, бром, холестерин, в небольшом количестве йод и соединения фосфора. Он оказывает легкое антисептическое воздействие и смягчает роговой слой кожи. Его применяют в лечебных мазях. Так кок лебертан имеет специфический запах, в косметике вместо него часто используют насыщенное витамином А масло зверобоя. Масло сурка. Масло получают из подкожного жира сурка. Этот дорогостоящий препарат хорошо переносится кожей, впитывается, не оставляя жирного блеска, нормализует липидный обмен в коже. Пока не находит широкого применения в косметологии. Жир крупного рогатого скота. Белый плотный жир, может иметь желтоватый оттенок. Состоит из триглицеридов масляной, пальмитиновой, стеариновой, ланолиновой кислот. Приятный на вкус и запах, но может быстро прогоркнуть. Применяется преимущественно для производства ядрового мыла. Свиное масло. Получают из жира свиней. По консистенции похоже на мазь; тонко плавления 35 - 40°С. Так как свиное сало может быстро прогоркнуть, то для препаратов длительного использования оно применяется только в консервированном виде. Свиное сало очень хорошо переносится кожей, однако не имеет широкого применения в медицине и косметологии. Черепаховое масло. Получают из жира черепах. Это высококачественное масло желтого цвета по консистенции напоминает мазь. Содержит витамины A, D, К, Н и ненасыщенные жирные кислоты. Используется в увлажняющих кремах, маслах и дорогих препаратах против морщин. Оно способствует проникновению через кожу биологически активных веществ. Норковый жир. Получают из внутреннего жира норки. По свойствам приближается к жиру сурка. Хорошо впитывается в кожу, не создает ощущения липкости и жирности благодаря триглицеридам ненасыщенных жирных кислот. Содержит жирорастворимые витамины. Снимает ощущение сухости и шелушения, активизирует липидный обмен в коже. Стеарин. Смесь стеариновой и пальмитиновой кислот, получаемых из разных животных жиров. Имеет твердую консистенцию. Применяемый в косметике материал чисто белый, почти без запаха, ненасыщенный жирами. Он легко омыляется, поэтому в соединении с кокосовым жиром используется в производстве мыла для бритья, в водно-масляных и масляно-водных эмульсиях, а также для приготовления грима, например губной помады. Пурцелиновое масло. Это жировая прослойка водоплавающих птиц (масло внутренних желез). Пурцелиновое масло - светлая жидкость, без запаха, хорошо разбрызгивается. Устойчива к окислению и к энзимам. Использование пурцелинового мосла облегчает равномерное распределение эмульсий на поверхности кожи. Оно делает кожу мягкой и гладкой. Синтетический вариант пурцелинового масла по качеству соответствует натуральному. ЖИВОТНЫЕ ВОСКИ Воск и жиры схожи внешне и характером воздействия на кожу. По химическому строению воск представляет собой сложные эфиры высокомолекулярных спиртов, жиры - сложные эфиры глицерина. В отличие от жиров и масел воск не может прогоркнуть. Ланолин. Очень часто в косметике применяется шерстяной воск, или ланолин, получаемый из шерсти овцы. Шерсть-сырец овцы содержит около 5-10% воска. После очистки получают чистый, обезвоженный шерстяной воск. Он желтоватого цвета, твердой консистенции, имеет слабый запах, не прогоркает. Применяемый в косметике ланолин светло-желтого цвета, вязкий, почти без запаха, имеет консистенцию мази. Ланолин - это идеальная основа для кремов, особенно таких, которые представляют собой водно-масляную эмульсию, так как ланолин обладает способностью на 100% поглощать воду без добавления эмульгаторов. В кремы ланолин вводится с водой, маслами и другими биологически активными веществами. Он содержит холестерин и эргостерин - провитамин Д, хорошо впитывается и максимально заменяет жир кожи. Аллергическая реакция на ланолин наблюдается крайне редко. При добавлении кислот висмута и ртути ланолин используют в отбеливающих кремах. Эйцерин. Смесь спиртов шерстяного воска и парафина. Обладает способностью удерживать значительное количество воды и одновременно составляет нераздражающую основу для кремов. Его широко используют медицине и косметике, так как он обладает способностью мягко влиять на кожу. Пчелиный воск. Продукт, выделяемый пчелами для построения сот. Холодный пчелиный воск - это пористое вещество, мелкозернистое на изломе, со специфическим медовым запахом, хорошо эмульгируется. Близок по составу к воскам кожи. Необработанный пчелиный воск имеет коричневатый цвет. Путем осветления получают белый пчелиный воск, который применяется в косметике. Пчелиный воск образует на поверхности кожи легкую пленку; используется при изготовлении кремов и губной помады, кроме того, в композициях для лица (восковых композициях), а также как воск для депиляторов. 9. Углеводы9.1 ОпределениеУглеводы, или сахариды - соединения, содержащие атомы углерода, водорода и кислорода. Состав углеводов обычно выражается формулой Сх(Н2О), где параметры х и у больше или равны трем. Название «углеводы» говорит о том, что водород и кислород присутствуют в молекулах этих веществ в том же соотношении, что и в молекуле воды. Все углеводы являются либо альдегидами, либо кетонами, их молекулы содержат несколько гидроксильных групп, которые определяют химические свойства вещества. Углеводы присутствуют во всех живых организмах в свободном виде или в комплексах с белками и липидами, являются одним из важнейших источников энергии. 9.2 Классификация, примеры простых сахаров, дисахаридов и полисахаридовУглеводы подразделяют на 3 основных класса: моно-, ди- и полисахариды. Моносахариды - это простые сахара. В зависимости от количества атомов углерода их подразделяют на: тириозы (С3) - например, дигидрооксиацетон; тетрозы (С4) - встречаются у бактерий; пентозы (С5) - например, рибоза; гексозы (С6) - например, глюкоза, фруктоза, галактоза и др. Важнейшие углеводы, используемые при изготовлении косметических препаратов - это глюкоза и фруктоза. Эти сахара имеют одну и ту же суммарную формулу: С6Н12О6. Они отличаются лишь пространственным расположением молекулярных групп. В зависимости от числа атомов углерода в молекуле углевода различают триозы, тетрозы, пентозы, гексозы и т. д. Приведем примеры таких моносахаридов:
Глюкоза представляет собой альдогексозу состава C6H12О6. Она встречается в растительных и животных организмах. Так, ее много в соке винограда, поэтому ее называют виноградным сахаром. Она содержится также и в других фруктах и ягодах, в меде, в крови человека. Глюкоза - бесцветное кристаллическое вещество, растворимое в воде. Изучение химического строения и свойств этого моносахарида показало, что он может существовать в различных формах: альдегидной и двух циклических, которые одновременно сосуществуют и могут переходить друг в друга:
Дисахориды образуются в результате реакции конденсации между двумя моносахарами. Среди дисахаридов наиболее широко распространены: · мальтоза (глюкоза + глюкоза); · лактоза (глюкоза + галактоза); · сахароза (глюкоза + фруктоза). Мальтоза содержится в пророщенных семенах и в организме животных. Лактоза находится только в молоке. Сахароза - как правило, в растениях. Полисахариды - это полимеры моносахаров. Используются растениями и животными в качестве строительного материала (целлюлоза), а также резерва пищи и энергии (гликоген, крахмал). Крахмал. Это полимер глюкозы. Запасается в растительных клетках в виде зерен. В животных организмах не синтезируется. В организме человека крахмал расщепляется на солодовый сахар (мальтозу) и виноградный сахар (глюкозу). Гликоген. Это резервный полисахарид из остатков глюкозы, синтезируемый в животном организме. У позвоночных содержится главным образом в печени и в мышцах. Целлюлоза. Полимер глюкозы - строительный полисахарид, содержится в растениях. Целлюлоза не расщепляется, а выделяется организмом в неизмененном виде. Целлюлозные сложные эфиры вводятся как конденсаторы (сгустители), вспомогательные эмульгаторы и гелеобразующие компоненты в зубные пасты, лаки для ногтей, компактные пудры, губную помаду, а также применяются для изготовления обезжиренных косметических продуктов. Все полисахариды имеют обволакивающий эффект, как слизистые вещества. Они улучшают скольжение препарата по коже, обладают способностью на некоторое время удерживать воду, например, в масках и композициях, причем растворимые в воде биологически активные вещества с помощью полисахаридов лучше проникают через кожу. Гуар. Берет название от семян дерева гуар, произрастающего в Индии. Этот полисахарид образует тягучую жидкость. Степень сгущения равна 8 (больше, чем у крахмала). Он используется в качестве сгустителя в кремах, шампунях, масках и композициях для уходо за кожей лица, а также как основа в «Роллон - дезодорантах». Трагонт. Полисахарид, получаемый из коры тропического дерева астрагалуса, 5%-ный раствор его в воде образует гель.
Агар-агар. Полисахарид из морских водорослей. Используется как вспомогательный эмульгатор и сгуститель. Из агар-агара изготовляют также желе. Инулин. Полимер фруктозы. Играет роль резервного полисахарида в корнях и клубнях растений семейства Compositae (георгины, топинамбур). Соединения, близкие к полисахаридам Мукополисахариды. Эти вещество построены из повторяющихся остатков, в которых один из двух Сахаров представляет собой аминосахар, например глюкозамин. Имеют большое биологическое значение. Хитин- по своей структуре близок к целлюлозе. Встречается у членистоногих в составе наружного скелета. В косметике используется как влагоудерживающее вещество. Гиалуроновая кислота - построена из чередующихся остатков сахарной кислоты и аминосахара. Основной компонент соединительной ткани позвоночных. Содержится в синовиальной жидкости, выполняющей функцию смазки в суставах, в стекловидном теле и в матриксе дермы. В косметике используется в качестве увлажнителя, гелеобразователя и загустителя. Хондроитинсульфат- близок по составу к гиалуроновой кислоте. Основной компонент хрящей, костной и другой соединительной ткани. Пектины. Эти вещества содержатся в матриксе клеточной стенки у растений, состоят из галактозы и галактуроновой кислоты (производное галактозы). Образуют плотные гели. Используются как желирующие добавки. Камеди и слизи. Состоят из Сахаров (арабиноза, галактоза, ксилоза) и сахарных кислот (глюкуроновая и галактуроновая). Образуются в ответ на повреждение в виде плотных блестящих экссудатов (например, гуммиарабик у акации или каучук у каучукового дерева). В воде набухают, образуя гели или клейкие растворители. Используются в косметике в качестве загустителя. Все полисахариды и выжимки растительного происхождения требуют добавления консервантов для защиты от бактерий. 10. Белки10.1 Определение белковБелки – высокомолекулярные природные полимеры, молекулы которых построены из остатков аминокислот, соединенных амидной (пептидной) связью. Белки выполняют различные биологические функции: · каталитические (ферменты); · регуляторные (гормоны); · структурные, двигательные, транспортные (гемоглобин); · защитные и др. Различают несколько структур белковой молекулы. 10.2 Образование пептидных связей
Первичная структура – последовательность соединения аминокислотных остатков в полипептидной цепи.
Вторичная структура – пространственная конфигурация, которую принимает полипептидная цепь. Поддерживается благодаря водородным связям между группами – СО- и –NH-, расположенными на соседних витках спирали.
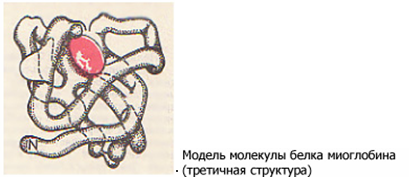
Третичная структура – это конфигурация, которую принимает в пространстве закрученная в спираль полипептидная цепь. Поддерживается взаимодействием между функциональными группами радикалов полипептидной цепи (-NH2, -OH, -COOH). Существует и четвертичная структура белка. Важное свойство белков – способность подвергаться гидролизу:
Под действием химическим веществ (кислот, щелочей, спиртов), при нагревании, действии радиации, солей тяжелых металлов происходит разрушение вторичной и третичной структур белка до первичной – денатурация. Белки горят с характерным запахом жженых перьев. Для распознавания белков используют цветные реакции: · ксантопротеиновую: · раствор белка +HNO3 (конц.) ® желтое окрашивание; · биуретовую: · раствор белка +Cu(OH)2 ® красно-фиолетовое окрашивание; Сложные белки: · Фосфопротеины - входят в состав казеина молока. · Гликопротеины - содержатся в плазме крови, слюне (муцин). · Нуклеопротеины - входят в состав хромосом. · Хромопротеины - входят в состав гемоглобина. · Липопротеины - входят в состав мембран, транспортная система крови. · Флавопротеины - компонент для переноса электронов при дыхании. 10.3 Свойства аминокислот, особенности химического строения, заменимые и незаменимые аминокислотыБольшинство встречающихся в природе аминокислот - а-аминокяслоты. В их общей формуле R - фрагмент различного состава и строения. В белках и тканях млекопитающих встречаются остатки около 30 различных а-ами-нокислот. Все эти аминокислоты выделены гидролизом белка и хорошо изучены. Структурные формулы, названия, принятые сокращённые обозначения некоторых наиболее важных сс-аминокислот приведены в таблице. В зависимости от строения боковой цепи выделяют алифатические (например, глицин, аланин, валин, лейцин), ароматические (фенилаланин, тирозин, триптофан), гидроксилсодержащие (серии, треонин), серосодержащие (цистеин, метионин), кислые (аспарагиновая кислота, глутаминовая кислота), основные аминокислоты (гистидин, лизин). Некоторые важнейшие аминокислоты:
10.4 Основные белки, применяемые в косметикеКоллаген (kollagen) является важнейшим белком соединительной ткани, сухожилий, хрящей, костей и в то же время - строительным белком всех животных клеток, обеспечивающим их прочность. Молекула коллагена образуется из трех перекрученных в спираль и тесно связанных друг с другом полипептидов. Молекулярная масса составляет около 360 000 углеродных единиц массы. Коллаген синтезируется фибробластами. По современной классификации существуют 7 типов этого белка. Наибольший интерес для косметолога представляют типы 1-й и 3-й. Тип] - опорный коллаген (его волокна имеют максимальный диаметр). Тип 3 - репарационный, при его недостатке образуются келлоидные рубцы, а также нарушается синтез коллагена 1-го типа. С возрастом количество коллагена 3-го типа значительно уменьшается. В тканях коллаген встречается в виде длинных нитей (фибрилл), в которых молекулы расположены пучками, направленными в одну сторону. Коллагеновые нити гибкие и упругие, отдельные макромолекулы в них соединены друг с другом химическими связями. По мере старения тканей увеличивается число связей между макромолекулами, это уменьшает упругость нитей. Коллаген рекомендуется для ухода за сухой и стареющей кожей. Проникновение гигантской молекулы коллагена в волосы или кожу затруднено, поэтому более широкое применение нашли коллагеновые гидролизаты, содержащие аминокислоты и пептиды. В настоящее время из фибробластов молодых животных выделено вещество, которое является активатором синтеза коллагена 3-го типа и входит в состав липосомальных комплексов. Элостин Это вещество, аналогичное коллагену. Образованные им нити более упруги и растяжимы. Входит в состав соединительной ткани, стенок кровеносных сосудов. Эластин и коллаген не растворимы в воде, их полипептидные цепи содержат большое количество аминокислот глицина, пролина, оксипролина. Эластин вводят в состав увлажняющих препаратов и средств для ухода за стареющей кожей. Кератин. Прочный, твердый белок. Не растворим в воде и жидкостях организма. Является идеальным покровным веществом. Входит в состав рогового слоя эпидермиса, ногтей и волос. Обладает способностью разбухать и размягчаться под действием воды. Одной из важных структурных частей молекулы кератина является серосодержащая аминокислота цистеин. Препараты на основе белков Восстановительный комплекс (Repair Complex) Вместе с коллагеном в косметических средствах применяется так называемый восстановительный комплекс - ненасыщенный раствор рибонуклеиновой кислоты и субстанций целлюлозы. Список литературы1. Глинка Н.Л.. Общая химия: Учебное пособие для вузов. – 22-е изд., испр. / Под ред. Рабиновича В.А. – Л.о. «Химия», 1982. 2. Кукрашева К.К.. Химия в таблицах и схемах. – М.: «Лист Нью». 2005. 3. Химия и физика в косметологии. Косметическое сырье, аппаратная косметология: Учебное пособие, том 5 / Под ред. к.м.н. А.П.Безуглого. – Издательство CosmeticForum, 1998. 4. Хомченко И.Г. Общая химия. Учебник. – 2-е изд., испр. и доп. – М.: ООО «Издательство Новая Волна»: Издатель Умеренников, 2005. 5. Химия: Школьная энциклопедия / Гл. ред. Ю.А. Золотов. – М.: Большая Российская энциклопедия, 2003. |