Министерство образования и науки Российской Федерации
Федеральное агентство по образованию
Государственное образовательное учреждение
Высшего профессионального образования
"Курский государственный университет"
Естественно-географический факультет
Кафедра химии
Курсовая работа
по теме:
"Диоксид серы в продуктах переработки плодов и овощей"
Выполнила: студентка 31 группы
специальность "химия"
Савкова Ольга.
Научный руководитель:
доцент химических наук
Дроздова С. Н.
Курск 2010 г
План
Введение
1. Классификация соков
2. Плодово-ягодное пюре и детское питание
3. Диоксид серы. Его использование и влияние на организм
3.1 Загрязнение диоксидом серы окружающей среды
3.2 Консервирование продуктов переработки плодов и овощей
4. Практическая работа
4.1 Качественный метод определения диоксида серы ГОСТ 25555.5-91
4.2 Йодиметрический метод определения свободного и связанного диоксида серы. ГОСТ 25555.5 – 91
Вывод
Литература
Введение
Роль серы для человеческого организма очень велика. Сера входит в состав всех клеток человеческого организма, но больше всего ее содержится в клеточных белках, где она является важнейшим элементом белковой структуры. Сера занимает пятое место в иерархии минеральных макроэлементов, необходимых для организма человека. Она необходима для синтеза органических соединений, играющих важнейшую роль в обеспечении здоровья человека. Основным источником серы для организма являются две аминокислоты: метионин
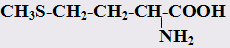
ицистеин
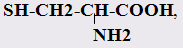
которые должны поступать из пищевых продуктов. Она входит в состав биологически активных веществ (гистамина, биотина, липоевой кислоты и др.) В активные центры молекул ряда ферментов входят SH - группы, участвующие во многих ферментативных реакциях, в том числе в создании и стабилизации нативной трехмерной структуры белков, а в некоторых случаях - непосредственно как каталитические центры ферментов.
Сера обеспечивает в клетке такой тонкий и сложный процесс, как передача энергии: переносит электроны, принимая на свободную орбиталь один из не спаренных электронов кислорода.
Этим объясняется высокая потребность организма в данном элементе.
Сера участвует в фиксации и транспорте метильных групп. Она является также частью различных коэнзимов, включая коэнзим А. Большая часть серы поступает в организм в составе аминокислот. Почти 75% попадающей в организм серы окисляетсясульфитоксидазами до сульфатов и выводится, в основном с мочой. Соединение с сульфатом способствует выведению из организма многих ненужных и вредных веществ (к примеру, никотина). Небольшое количество неорганических сульфатов вместе с натрием и калием присутствуют в крови и иных тканях. Много содержащих серу аминокислот содержится в кератине - белке, который входит в состав волос и ногтей, поэтому людям с более развитым волосяным покровом требуется и большее количество серы.
Медицина долгое время относилась к этому химическому элементу с опаской. Роль серы должным образом оценили лишь тогда, когда было установлено, что она входит в состав многих жизненно важных органических соединений. Сера, к примеру, содержится в глютаминовой кислоте, которая необходима для нормального функционирования нервной системы, мозга, для синтеза глицина - простейшей алифатической аминокислоты, участвующей в качестве посредника в активной деятельности мышц, а значит, совершенно необходимой при лечении больных рассеянным склерозом. Присутствует сера и в витамине В12 и в гепаритине - субстанции, понижающей кровяное давление и содержащейся во всех без исключения тканях, и в метионине - аминокислоте, которая присутствует в печени и необходима, в частности, больным СПИДом. Сера обеспечивает печени возможность осуществлять функцию детоксикации, поскольку действует в качестве фильтра, очищающего организм от ядов. (Не следует, однако, забывать, что в большом количестве сера и сама является чрезвычайно сильным ядом.) Практика доказала, что сера оказывает благотворное влияние на суставы, кожу и состояние волосяного покрова. Недостаток серы вызывает различные, иногда очень серьезные, расстройства.
Диоксид серы используют во многих продуктах из фруктов как промежуточный консервант. Его добавляют к сырью или полуфабрикатам и удаляют в процессе переработки нагреванием или вакуумированием.
Восстанавливающие и антиокислительные свойства диоксида серы имеют большое значение для многих отраслей пищевой промышленности. Добавлением SO2
, можно замедлить реакции ферментативного побурения (он подавляет активность ферментов или перехватывает ускоряющие процесс свободные радикалы). Диоксид серы тормозит также многие неферментативные реакции побурения, включая реакцию Майяра. Некоторые сульфиты в определённых условиях могут разрушать образующиеся в пищевых продуктах афлатоксины.
Однако использование значительно превышающих норму количеств диоксида серы очень вредно для человеческого организма. Вдыхание оксидов серы вызывает удушье, затруднение дыхания, возможен даже коллапс. Отравления меньшими дозами вызывают отек легких или воспаление бронхов. При длительном воздействии в малых концентрациях наблюдаются изменения со стороны органов пищеварения, имеют место функциональные нарушения щитовидной железы.
Особенно опасен диоксид серы для витаминов группы В, содержащихся в продуктах, в частности тиамина (В1), который разрушается под действием сернистой кислоты. Это действие проявляется при высокой концентрации двуокиси серы в сочетании с низким значением рН. Кроме того, продукты, богатые витамином В, вряд ли можно законсервировать сернистой кислотой, так как поглощение двуокиси серы тиамином снижает консервирующий эффект. Недостаток витаминов группы В может привести к нарушению работы нервной, сердечно - сосудистой и пищеварительной систем, а также к ломкости волос и ногтей и болезням зрения.
Из-за выдвинутых против двуокиси серы и сульфитов обвинений в токсичности им давно ищут замену. В числе прочих заменителей обсуждались: 5,6-сульфинил-6-аскорбиновая кислота, 2-фосфат аскорбиновой кислоты, сама аскорбиновая кислота, ингибиторы полифенолоксидаз и серосодержащие аминокислоты. Так же как и нитриты, двуокись серы — многофункциональное вещество. По некоторым свойствам она может быть заменена другими консервантами. Однако до сих пор не известно вещество, которое одновременно может проявлять такие функции диоксида серы, как ингибирование ферментов, восстанавливающее и антиокислительное действие.
Из вышесказанного можно сделать вывод, что содержание диоксида серы в продуктах должно строго нормироваться, для того, чтобы не допускать разрушительного для человеческого организма воздействия. В настоящее время участились случаи ненормированного применения консервантов, в том числе и диоксида серы. Целью данной работы является проверка соответствия содержания серы в продуктах переработки плодов и овощей установленному стандарту.
1. Классификация соков
питание диоксид сера йодиметрический консервирование
В сети общественного питания наряду со свежими плодами и овощами широко применяются продукты их переработки. К наиболее распространенным способам переработки относятся: сушка; консервирование высокими температурами в герметично укупоренной таре; квашение и соление, маринование; замораживание; консервирование сахаром и др.
В настоящее время в России производится порядка 950 млн. л сока в год (в 1999 году — 500 млн. л). Рост рынка происходит в основном за счет отечественных производителей. Если в 1998 г. импорт составлял 31 % всех потребляемых в России соков, то в 2000 г. — менее 5 %. Средний уровень потребления соков на одного человека в год в России составляет 4 л, в Москве — 21 л. Потребление соков в Центральной части России постепенно будет приближаться к московским показателям, т.к. в этом регионе уже сформировалась культура потребления соков и заботы о своем здоровье (за 2000-2001 гг. соковый рынок данного региона вырос на 40 %). В Сибири и на Дальнем Востоке соки пока воспринимаются только как заменители фруктов с ярко выраженным сезонным потреблением в весенний период, но и данный регион может стать перспективным в будущем. Таким образом, потенциальный рынок соков в России достаточно емкий.
Соки по цене и составу подразделяются на:
—"соки и напитки стоимостью до 21 рубля за литр" (сегмент "ММ" — торговые марки "Dr. Fresh", "Добрый сок", "Любимый сад", "Фруктовый сад", "Моя семья", "Троя";
—"соки и напитки стоимостью от 21 до 26 рублей за литр" (сегмент VFM) —брэнды "100 % Gold Premium", "Nico", "Depsona", "Амтел", "Иван Поддубный", "Очаков", "Привет", "Тонус", "Gutta";
—"соки и напитки стоимостью от 26 до 31 рубля за литр" (сегмент "ОМР") — торговые марки "J7", " Сокос", "Чемпион", "Sunpride", "Viko", "Чудо-Ягода", "Я";
—"соки и напитки стоимостью свыше 31 рубля за литр" (сегмент "premium") — брэнды "Santal", "Rio Grande".
Появляются на рынке новые марки соков, напитков, рассчитанные на менее состоятельных покупателей. Во-первых, концентрат, занимающий от 40 % до 60 % в себестоимости соков, стал закупаться по возможности ближе к его производителям. Во-вторых, по мере возможностей производители переключаются на работу с российским сырьем или на сырье из ближнего зарубежья, тем самым уходя от валютной составляющей. Кроме того, с целью удешевления продукции многие компании перешли на производство миксов, например, апельсиновый или банановый сок на яблочной основе.
В зависимости от состава соки разделяют на натуральные, состоящие из жидкой фазы плодов и ягод, и соки с теми или иными добавками: сахара, органических кислот, красящих, ароматических и консервирующих веществ. Натуральные соки могут быть из одного вида плодов или их смеси (купажированные).
К сокам с добавками относятся прежде всего соки с сахаром. Сахар добавляют в виде сахара-песка или сиропа с целью улучшить вкусовые свойства соков, что особенно необходимо для соков из высококислых плодов и ягод. Для соков из малокислых плодов и ягод в некоторых случаях можно добавлять органические кислоты, что практикуется в производстве соков с мякотью. В том случае, когда к сокам добавляют аскорбиновую кислоту как антиокислитель или для витаминизации продукта, сок остается в группе натуральных. К сокам с добавками относятся также соки, консервированные химическими консервантами (сорбиновая кислота, сернистый ангидрид, дегидроацетовая кислота и т. п.).
В зависимости от содержания мякоти различают соки осветленные, неосветленные и с мякотью. Осветленные соки, благодаря применению специальных способов, освобождены от взвешенных частиц мякоти и большей части коллоидных веществ, по внешнему виду прозрачные и более стойки в хранении, чем другие виды соков.
Неосветленные соки содержат все коллоидные вещества и некоторую часть тонкодисперсных частичек мякоти, по внешнему виду мутные, при хранении в них выпадает осадок, ухудшающий внешний вид и товарные качества сока. Однако вкус и аромат неосветленных соков более полный, чем осветленных соков. Они изготавливаются на ленточном прессе для переработки фруктов, например, фирмой "Молмаш" г. Москва.
Соки с мякотью содержат все коллоидные вещества и тонкоизмельченную мякоть плодов и ягод, по составу близки к исходному сырью, и поэтому их часто называют жидкими плодами. Соки с мякотью выпускают натуральные и с сахаром. Последние получили название нектаров.
В зависимости от способов производства соки могут быть разделены на соки одинарной крепости, концентрированные и газированные. В соках одинарной крепости содержание растворимых сухих веществ примерно такое же, как и в исходном сырье. В концентрированных соках путем удаления тем или иным способом воды концентрация сухих растворимых веществ увеличена в несколько раз. Газированные соки — это соки натуральные или с сахаром, насыщенные диоксидом углерода на конечной стадии производства.
По способу консервирования различают соки, обработанные теплом (пастеризованные, консервированные горячим розливом, асептическим способом), охлаждением или замораживанием, химическими консервантами. Пастеризованные соки получают путем розлива в тару, герметичной укупорки и нагревания по установленному режиму при температурах ниже 100 °C (пастеризация) или при 100 °C и выше (стерилизация). Консервирование горячим розливом осуществляют путем нагрева сока в потоке до 95...98 °C), розлива при этой температуре в горячую, подготовленную тару с немедленной укупоркой и последующей выдержкой в течение нескольких минут в горячем виде, затем охлаждения на воздухе или искусственным путем.
Асептическое консервирование включает кратковременный нагрев сока при температуре 115...125 °C, быстрое охлаждение до 35...40 °C и розлив охлажденного сока в стерильных условиях в стерильную тару. Охлаждение до 0... минус 2 °C) применяют при хранении соков-полуфабрикатов в крупных резервуарах в атмосфере диоксида углерода.
Замораживание при температуре не выше минус 18 °C) осуществляют преимущественно для сохранности концентрированных соков с целью избежать их потемнения и других нежелательных изменений при хранении.
Химическое консервирование путем внесения в сок консервирующих средств применяют для соков-полуфабрикатов. Спиртование путем добавления к сокам 16...18 % этилового спирта применяют при заготовке полуфабрикатов для безалкогольной промышленности.
В ассортимент данных консервов входят следующие группы: соки осветленные и неосветленные, соки из отдельных видов сырья, концентрированные соки, газированные соки, соки с мякотью.
Для разлива соков могут применяться комплекты оборудования фирмы "Фруктонад" г. Москва.
В России начинает активно формироваться сегмент сокосодержащих витамизированных напитков в упаковке большого объема, как картонной, так и полиэтиленовой. Это позволяет производителям устанавливать низкую на них цену, например, на данный момент ниже цены соков низшего ценового сегмента. Этот сегмент можно считать наиболее перспективным, учитывая все возрастающую склонность потребителей к маркам соков из низшего ценового сегмента. В этом сегменте присутствуют брэнды "Соковичок" (компания "Троя-Ультра"), "Да" — Нидан- Экофрукт, "Фрустайл" — ЭКЗ Лебедянский.
Технологическая схема получения соков из плодов и ягод подобна получению соков из овощей: вначале получают натуральный сок, часть из которого поступает в продажу, а остальная часть путем удаления воды тем или иным способом доводится до концентрированного состояния. Этот жидкий или порошкообразный концентрат доставляется в любой регион, где путем добавления воды и необходимых ингредиентов получают сок.
2. Плодово-ягодное пюре и детское питание
Широко распространенным продуктом на российском рынке также является плодово-ягодное пюре. Онопредставляет собой протертую мякоть плодов или ягод без кожицы, волокон, косточек, семян. В пюре из земляники, ежевики, малины, клюквы, черной и красной смородины, черники допускается наличие семян, а в пюре из айвы и груши — твердые включения. Цвет пюре и его вкус должны быть свойственными исходным плодам или ягодам. Яблочное пюре должно иметь цвет от светло-желтого до кремоватого, абрикосового и персикового — от светло-желтого до оранжевого. Допускается потемнение верхнего слоя пюре и отделение жесткой фазы слоем не более 5 мм. Пюре поставляется на предприятия в стеклянной таре вместимостью 3 и 10 л. Используют пюре для производства повидла, мороженого, кондитерских изделий. Хранят пюре при температуре от 0 до 20 °С и относительной влажности воздуха не выше 75 %. Для промышленной переработки плодово-ягодное пюре консервируют с применением диоксида серы, бензоата натрия или сорбиновой кислоты. Плодово-ягодное повидло. Повидло представляет собой уваренное с сахаром плодовое пюре с добавлением или без добавления пищевого пектина и пищевых кислот. Повидло вырабатывают из свежего или сульфитированного пюре. Для производства повидла используют абрикосы, алычу, айву, вишни, груши, кизил, персики, сливы, яблоки, а также смесь плодов и ягод. Консистенция повидла мажущаяся или плотная. Цвет должен соответствовать цвету плода. Вкус повидла кисло-сладкий, свойственный плодам, из которых изготовлено повидло, запах — с ароматом плодов. Не допускаются засахаривание повидла и наличие посторонних примесей. Содержание сухих веществ в стерилизованном повидле не менее 61 %, в нестерилизованном — 66 %. Содержание сахара в пересчете на инвертный, соответственно, не менее 55 и 60 %. Повидло мажущейся консистенции фасуют в бочки и банки, плотной консистенции — в ящики. Хранят в сухих, хорошо вентилируемых помещениях при температуре от 0 до 20 °С и относительной влажности воздуха 75-80 %. При этих условиях гарантийный срок хранения повидла в ящиках 6 мес, в бочках 9 мес. Количество сернистой кислоты в повидле составляет 0,01 % (в пересчете на сухое вещество), бензоата натрия — 0,07 (в пересчете на бензойную кислоту), сорбиновой кислоты — 0,05 %; общая кислотность (в пересчете на яблочную кислоту) — 0,2-1 %. В состав яблочного повидла входят(в %): вода — 32,9, углеводы — 65,3, клетчатка — 0,7, белки — 0,4, органические кислоты — 0,3, зола — 0,4.
Также внушительную часть плодово-ягодных консервов в продаже занимает детское питание, к которому нормы содержания вредных веществ, консистенции и др. показателей более высокие, чем для обычного плодово-ягодного пюре.
3. Диоксид серы. Его использование и влияние на организм
E220 Диоксид серы — Сернистый ангидрид при обычных условиях представляет собой бесцветный негорючий газ с резким запахом. Плотность сернистого газа в два с лишним раза выше, чем у воздуха; при —10°С он сгущается в жидкость. Диоксид серы попадает в продукты переработки плодов и овощей двумя путями –1) через загрязнение этим веществом окружающей среды и 2)вследствие консервирования им продуктов переработки.
3.1 Загрязнение диоксидом серы окружающей среды
При сжигании угля или нефти содержащаяся в них сера окисляется. При этом образуется два соединения: диоксид серы и триоксид серы. В процессе первоначального горения окисляется менее 3% серы. Остальная часть превращается в диоксид серы – первичную форму, в которой сера поступает в атмосферу. Здесь он окисляется кислородом воздуха до триоксида, который, реагируя с водяным паром образуя серную кислоту:
H2
O + SO3
= H2
SO4
Серная кислота присутствует в воздухе в виде легкого тумана, состоящего из крошечных капель.
Диоксид серы, образующийся при сжигании топлива, тоже вступает в реакцию с парами воды, образуя сернистую кислоту (H2
SO3
). Эта слабая кислота в свою очередь постепенно реагирует с кислородом воздуха, образуя серную кислоту: 2H2
SO3
+ O2
= 2H2
SO4
. Итак, серная кислота в воздухе образуется двумя путями. В сухом воздухе образуется главным образом триоксид серы и затем серная кислота; а при высокой влажности образуется в основном сернистая кислота, которая окисляется до серной.
При сжигании топлива образуются также оксиды кальция и железа. Они попадают в атмосферу в больших количествах при сжигании угля, но при сгорании нефти их образуется гораздо меньше. Попавшие в атмосферу оксиды вступают в реакцию с серной кислотой с образованием сульфатов кальция и железа: CaO + H2
SO4
= CaSO4
+ H2
O
FeO+H2
SO4
= FeSO4
+H2
O
Fe2
O3
+3H2
SO4
=Fe2
(SO4
)3
+3H2
O.
Количество содержащихся в городском воздухе частиц сульфатов и капелек серной кислоты может достигать от 5 до 20%. Полагают, что большая часть диоксида серы превращается в сульфаты и серную кислоту в течение нескольких дней после ее выброса в атмосферу. За это время ветры могут отнести эти загрязнения на сотни километров от места их выброса.
Из атмосферы сульфаты и серная кислота попадают в почву и воду посредством кислотных дождей, откуда в основном в связанном состоянии диоксид серы поступает в плоды и овощи.
Предельные концентрации SO2
в воздухе: при краткосрочном воздействии 0,4 мг/м3
, при длительном воздействии 0,14 мг/м3
.
3.2 Консервирование продуктов переработки плодов и овощей
Консервирование диоксидом серы плодов и овощей называется сульфитацией.
Сульфитация основана на антисептическом действии сернистой кислоты, подавляющей развитие микроорганизмов. Как антимикробное средство диоксид серы применяют для сохранения целых и дроблёных фруктов (используемых для дальнейшей переработки), сухофруктов, фруктовых соков (используемых как сырьё), концентратов фруктовых соков, фруктовых пульп и фруктовых пюре. Кроме антимикробной роли она почти всегда должна выполнять и другие функции защиты — от окислительных (ферментативных и неферментативных) реакций побурения, других реакций окрашивания, от разрушения витаминов. Необходимая в этих случаях концентрация сернистой кислоты часто выше концентрации, которая требуется для защиты от микроорганизмов. На практике (в зависимости от вида продукта) добавляют от 0,01 до 0,2% 502, а в отдельных случаях и более. Остаточное количество сернистого газа в конечном продукте редко превышает 0,01 %, чаще оно значительно ниже. Если такие концентрации и оказывают антимикробное действие, то незначительное, тем более что часть диоксида серы связана с компонентами пищевого продукта, например с сахаром.
Для человеческого организма сернистая кислота токсична. Поэтому сульфитированные плоды и ягоды используют только как полуфабрикаты для промышленной переработки. Перед использованием сульфитированные плоды десульфитируют, т. е. нагреванием удаляют из них диоксид серы. Полностью удалить диоксид серы при десульфитировании не удается, поэтому ее содержание строго нормируется в засульфитированных плодах (0,12-0,20% массы плодов), а в готовых изделиях, получаемых после дисульфитации,- не более 0,01 %.
При выработке компотов, а также всех видов консервов, предназначенных для детского питания, применение сульфитированных заготовок не допускается.
Сульфитация может проводится сухим или мокрым способом. При первом плоды окуривают SO2 в герметичных камерах, а при втором плоды закладывают в бочки и заливают раствором сернистой кислоты. Косточковые плоды сульфитируют мокрым способом, а семечковые - сухим.
Люди по-разному реагируют на двуокись серы. Некоторые безболезненно переносят до 4 г сульфита в день (т.е. примерно 50 мг на 1 кг массы тела), а другие уже после приема очень малых количеств жалуются на головные боли, тошноту, понос или ощущение тяжести в желудке. Для переносимости сернистой кислоты большое значение имеет кислотность желудочного сока, — люди, имеющие пониженную или повышенную кислотность, существенно более чувствительны, чем люди с нормальной кислотностью. Может вызывать фатальные аллергические реакции у астматиков, разрушает витамин В1.
Однако диоксид серы, некоторые сульфиты, бисульфиты и пиросульфиты разрешены практически во всех странах для консервирования многих продуктов питания (в основном растительных).
4. Практическая работа
Для анализа было взято три пробы соков и две пробы детского питания.
1) Детское питание "Бабушкино лукошко" Чернослив.
Изготовитель: ООО "Завод детского питания "Фауст" Россия, Московская область, пос. Белозерский
Дата изготовления:06.03.10
Срок годности: 30 месяцев
2) Детское питание "Агуша" яблоко-банан
Изготовитель: ОАО "Экспериментальный комбинат детского питания"
ОАО "ВБД" Россия, Курская область, Фатежский район, пос. Чермашной
Дата изготовления: 07.03.10
Срок годности: 24 месяца
3) Сок "Остров колибри" персик-яблоко
Изготовитель: ОАО "Лебедянский" Россия, Липецкая область, г. Лебедянь
Дата изготовления: 17.03.10.
Срок годности: 1 год
4) Сок с инулином мультифрукт "Здрайверы"
Изготовитель: ОАО "Вимм-Билль-Данн" Россия, Москва, Дмитровское шоссе
Дата изготовления:01.03.10
Срок годности: 1 год
5) Сок "Добрый" яблоко
Изготовитель: ЗАО "МУЛТОН", г. Санкт-Петербург, ул.Софийская д.14
Дата изготовления: 01.03.10
Срок годности: 1 год
4.1 Качественный метод определения диоксида серы ГОСТ 25555.5-91
Сущность метода
Метод основан на обесцвечивании йодкрахмальной бумаги диоксидом серы, вытесненным из продукта его подкисления. При определении связанного диоксида серы навеску продукта предварительно обрабатывают щелочью.
Метод применим для продуктов с массовой долей диоксида серы не менее 0,0002%.
Аппаратура, материалы, реактивы
Шкаф сушильный лабораторный с автоматическим регулированием температуры
Пипетки по НТД вместимостью 2 и 10 мл
Колба коническая по ГОСТ 25336 вместимостью 100 или 250 мл
Стаканчик для взвешивания по ГОСТ 25336
Бумага фильтровальная лабораторная по ГОСТ 12026
Бумага индикаторная универсальная для определения рН = 7-14
Крахмал растворимый по ГОСТ 10163, раствор массовой концентрации 5 г/л: при приготовлении раствора крахмал, разведенный водой, добавляют в кипящую воду и кипятят около 10 мин. Раствор пригоден в течение нескольких дней
Иодид калия по ГОСТ 4232, х.ч., раствор массовой концентрации 1 г/л
Йод по ГОСТ 4159, ч.д.а., раствор массовой концентрации 12 г/л; готовят, используя раствор иодида калия
Кислота ортофосфорная по ГОСТ 6552, ч.д.а., раствор с массовой долей 50%
Натрия гидроокись по ГОСТ 4328, ч.д.а., раствор массовой концентрации 40г/л
Вода дистиллированная по ГОСТ 6709
Подготовка к испытанию
Фильтровальную бумагу помещают в раствор крахмала и после пропитывания им высушивают в шкафу при температуре 300
С, операции повторяют трижды. Подготовленную крахмальную бумагу режут на полоски размером 2×5 см.
Проведение испытания
На полоску крахмальной бумаги наносят 2-3 капли раствора иодида калия и сразу же помещают на 5-10с в стаканчик для взвешивания с раствором йода, укрепляя полоску с помощью крышке в воздушном пространстве над раствором йода. На полоске должно появиться светло-синее окрашивание. Приготовленную таким способом полоску йодкрахмального индикатора следует использовать немедленно.
В коническую колбу помещают навеску подготовленной пробы продукта массой около 20г. В случае густых консервированных продуктов к пробе добавляют около 20 мл, а в случае сушеных фруктов и овощей – около 50мл горячей воды и содержимое колбы перемешивают. Затем вносят 2 мл раствора ортофосфорной кислоты и сразу же закрывают колбу пробкой, с помощью которой в воздушном пространстве над продуктом закрепляют полоску йодкрахмальной индикаторной бумаги. Колбу помещают на кипящую водяную баню.
При содержании в продукте свободного диоксида серы не менее чем 0,0002 % индикаторная бумага должна обесцветиться не более чем через 5 мин.
Если бумага не обесцветилась, то определяют наличие связанного диоксида серы. Для этого снова берут навеску продукта, как описано выше, и подщелачивают ее, добавляя раствор гидроокиси натрия в небольшом избытке (по индикаторной универсальной бумаге). Через 5 мин смесь подкисляют раствором ортофосфорной кислоты; объем раствора кислоты должен составлять не менее 10% объема раствора гидроокиси натрия, взятого для подщелачивания. Сразу же колбу закрывают пробкой, удерживающей полоску йодкрахмальной индикаторной бумаги, помещают колбу на кипящую водяную баню и через 5 мин оценивают обесцвечивание индикаторной бумаги.
Примечание. Метод не применим для продуктов, содержащих лук и чеснок (они выделяют вещества, обесцвечивающие йодкрахмальную бумагу при обработке гидроокисью натрия).
Результаты:
Таблица 1:Качественный анализ наличия свободного и связанного диоксида серы в пробах.
| № |
Свободный диоксид серы |
Связанный диоксид серы |
| 1 |
+ |
+ |
| 2 |
+ |
+ |
| 3 |
+ |
+ |
| 4 |
+ |
+ |
| 5 |
+ |
+ |
4.2 Йодиметрический метод определения свободного и связанного диоксида серы. ГОСТ 25555.5 – 91
Сущность метода
Метод основа на переводе свободного и связанного диоксида серы в соль сернистой кислоты, которую затем титруют в кислой среде йодом. Для учета расхода йода на другие вещества, реагирующие с ним, проводят параллельно йодометрическое титрование еще одной пробы продукта в присутствии формалина, связывающего диоксид серы.
Метод применяют для анализа плодовых и ягодных продуктов с содержанием диоксида серы не менее 0,001%.
Аппаратура, материалы, реактивы
Весы, бюретка
Пипетки по НТД с делениями вместимостью 5 и 10 мл; без делений вместимостью 10 и 20 мл
Колба мерная по ГОСТ 1770 вместимостью 250мл
Цилиндры или мензурки по ГОСТ 1770 вместимостью 50 или 250мл
Колба коническая по ГОСТ 25336 вместимостью 500мл
Мешалка электрическая
Часы и таймер
Натрия гидроокись по ГОСТ 4328, раствор с(NaOH)=4моль/л
Кислота серная по ГОСТ 4204, раствор с массовой долей 10%
Йод стандарт титр с(1/2 I2
)=0,1моль/л
Крахмал растворимый по ГОСТ 10163
Натрий хлористый по ГОСТ 4233
Формалин технический по ГОСТ 1625, раствор с массовой долей 37%
Вода дистиллированная по ГОСТ 6709
Примечания:
1.Квалификация всех применяемых реактивов должна быть не ниже ч.
2.Допускается применение других средств измерений с метрологическими характеристиками не ниже указанных и реактивов более высокой квалификации.
Подготовка к испытанию
Приготовление раствора крахмала
13 г крахмала перемешивают с небольшим количеством воды, вносят в 150 мл кипящей воды и кипятят 10 мин. Затем добавляют 50г хлористого натрия, перемешивают, охлаждают, переносят количественно в мерную колбу вместимостью 250 мл и доводят водой до метки. Раствор годен в течение двух недель.
Проведение испытаний
Определение свободного диоксида серы
Навеску пробы продукта массой 10 -100г количественно переносят в колбу для титрования с помощью 50 -100мл воды, добавляют 3 мл раствора серной кислоты, 1 мл раствора крахмала и сразу титруют раствором йода до появления голубовато-синей окраски, не исчезающей в течение 15с.
Определение связанного диоксида серы
Сразу же после титрования свободного диоксида серы в ту же колбу добавляют в мл раствора гидроокиси натрия, закрывают пробкой, перемешивают и оставляют на 5 мин. После этого добавляют 10 мл раствора серной кислоты и немедленно титруют раствором йода до появления голубовато-серой окраски, не исчезающей в течение 15 с.
Вновь добавляют 20мл раствора гидроокиси натрия, закрывают пробкой, перемешивают и оставляют на 5 мин. Затем добавляют 200 мл холодной воды, тщательно перемешивают, вносят 30 мл раствора серной кислоты и титруют раствором йода до появления голубовато-синей окраски, не исчезающей в течение 15 с.
Внесение поправки на вещества, окисляемые йодом
Навеску пробы продукта, масса которой точно равна массе навески, вносят в колбу для титрования, добавляют 5 мл формалина, колбу закрывают пробкой, тщательно перемешивают и оставляют на 30мин. Затем добавляют 3мл раствора серной кислоты, 1 мл раствора крахмала и титруют раствором йода до появления голубовато-синей окраски, не исчезающей в течение 15с.
Обработка результатов
Массовую долю свободного (х1
) и связанного (х2
) диоксида серы в процентах вычисляют по формулам:
х1
=(сМ(V1
– V4
)*0,1)/m
х2
=(cM(V1
+V2
+V3
-V4
)*0,1)/m
V1
–объем раствора йода, израсходованного на титрование свободного диоксида серы, мл
V2
и V3
– объемы раствора, израсходованного на титрование связанного диоксида серы, мл
V4
– объем раствора йода, израсходованного на титрование веществ, окисляемых йодом, мл
М – молярная масса, 32 г/моль
m-масса навески,г.
Результаты.
Приготовили раствор йода и установили его точную концентрацию по стандартному 0,1 н. раствору Na2
S2
O3.
V1
=14, 4 мл
V2
=14, 8 мл
V3
=15 мл
V4
=15 мл
Vср. = 14, 7 мл
C(Na2
S2
O3
)*V(Na2
S2
O3
) = C(I2
)*V(I2
)
0,0147*0,1 = 0,015* C(I2
)*
Сн
(I2
) = 0,098 моль.экв./л
С(I2
)=0,196 моль/л
Масса навески 15 г.
Таблица 2:Количественный анализ наличия свободного и связанного диоксида серы в пробах. (Массовая доля свободного и связанного диоксида серы не должна превышать 0,01%).
| № |
V1
,мл |
V2
,мл |
V3
,мл |
V4
,мл |
Массовая доля свободного диоксида серы, % |
Массовая доля связанного диоксида серы, % |
Общее содержание диоксида серы,% |
| 1 |
1,6
1,7
1,7
|
1,4
1,3
1,3
|
1
0,9
1
|
0,5 |
0,049
Δх=0,00355
|
0,143
Δх=0,00263
|
0,192
Δх=0,00618
|
| 2 |
1
0,9
1
|
0,5
0,4
0,4
|
0,3
0,3
0,3
|
0,1 |
0,036
Δх=0,00327
|
0,067
Δх=0,00448
|
0,103
Δх=0,00775
|
| 3 |
0,2
0,2
0,2
|
0,1
0,1
0,1
|
0,2
0,2
0,2
|
0,1 |
0,004 |
0,017 |
0,021 |
| 4 |
0,4
0,3
0,4
|
0,3
0,1
0,3
|
0,4
0,2
0,3
|
0,1 |
0,011
Δх=0,00327
|
0,031
Δх=0,0104
|
0,042
Δх=0,01367
|
| 5 |
0,3
0,1
0,2
|
0,2
0,2
0,2
|
0,3
0,2
0,2
|
0,1 |
0,003
Δх=0,00137
|
0,022
Δх=0,00263
|
0,025
Δх=0,004
|
Вывод
В ходе анализа было обнаружено, что в первой пробе массовая доля общего содержания серы составляет 0,192%, Δх=0,00618%, что примерно в 19,2 раза превышает норму.
Во второй пробе массовая доля общего содержания серы составляет 0,103%, Δх=0,00775% - в 10,3 раз превышает норму.
В третьей пробе диоксид серы содержится в количестве 0,021%, что в 2,1 раз выше нормы, в 4 пробе 0,042%,Δх=0,0136% - в 4,2 раза, в 5 пробе 0,025%,Δх=0,004 – в 2,5 раза.
Из данных опыта можно сделать вывод о том, что во всех взятых для анализа пробах повышенное содержание диоксида серы. Причем в детском питании оно выше в 19,2 и в 20 раз! Это неприемлемо для данных продуктов, и, следовательно нужно понизить содержание данного вещества в пробах
1) Детское питание "Бабушкино лукошко" Чернослив.
2) Детское питание "Агуша" яблоко-банан
Или использовать другой консервант.
Литература
1)Журнала "АПК-Информ: Овощи и фрукты",№6
2) Энциклопедический словарь-справочник "Окружающая среда",т.1,Москва, Издательская группа "ПРОГРЕСС",1999
3) П.Ревелль, Ч.Ревелль "Среда нашего обитания",Книга 2, Москва, "Мир", 1995
4) Семенов Д.А. "Технология производства диоксида серы" , Москва, "Мир", 1999
5) "Биологическая химия" под редакцией Ковалевской, Москва ACADEMA,2005
6) В.П. Комов, В.Н. Шведова "Биохимия", Москва, "Дрофа", 2004
7) Скальный А.В. "Химические элементы в физиологии и экологии человека: учебное пособие, рек. УМО", Москва, "Оникс 21 век", 2004
8) Филлипович Ю.Б. "Основы биохимии" 4-е издание, переработанное и дополненное, Москва, "Агар", 1999
9)Глотова С.Г. "Биохимия питания (вещества, их функции в организме, потребности, понятие об основных процессах)" - Курск "ГЕКБУС", 1998
10) Л.А. Сарафанова "Энциклопедия. Пищевые добавки.", Москва, " Мир", 2000
|