Отдел образования администрации Центрального района
Муниципальная гимназия № 1
реферат
По теме:
несимметричные сульфиды на основе
4 - ( g - хлорпропил ) - 2 - трет. - бутилфенола
Галанская галина,Евсюкова Ирина и Кривошапкин Иван,
ученики 11 «А» класса
научный руководитель: ст. преподаватель
кафедры органической химии НГПУ Марков Александр Федорович
Новосибирск – 2000
СОДЕРЖАНИЕ
1. Введение............................................................................................................................
2. Пространственно-затрудненные фенолы и стабилизация полимерных материалов...............................................................................................................................................
2.1. Старение полимеров.........................................................................................................
2.2. Пространственно-затрудненные фенолы, как ингибиторы радикальных процессов в полимерах.
3. Методы получения органических сульфидов.....................................................
4. Пути синтеза несимметричных сульфидов на основе 4-(g-хлорпропил)-2-трет.-бутилфенола..................................................................................................................
4.1. Получение 4-(g-хлорпропил)-2-трет.-бутилфенола (хлорид Ф-13)..............................
4.2. Синтез 4-(g-меркаптопропил)-2-трет.-бутилфенола....................................................
4.3. Синтез 2,2'– метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола]......................
4.4. Синтез несимметричных сульфидов алкилированием 4-(g-меркаптопропил)-2-трет.-бутилфенола и 2,2`метиленбис-[4-(g-меркаптопропил)-6-трет.- бутилфенол] алкилгалогенидами в щелочном виде..........................................................................................................................................
5. Практическая часть......................................................................................................
5.1. Наработка 4-(g-хлорпропил)-2-трет.-бутилфенола (хлорид Ф-13)...............................
5.2. Получение 4-(g-меркаптопропил)-2-трет.-бутилфенола..............................................
5.3. Получение 2,2'-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола].........................
5.4. Взаимодействие 2,2'-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола] с бромистым бутилом (н-C4
H9
Br) в щелочной среде.............................................................................................
5.5. Взаимодействие 2,2'-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола] с йодистым этилом (C2
H5
J) в щелочной среде.................................................................................................
5.6. Взаимодействие 4-(g-меркаптопропил)-2-трет.-бутилфенола с йодистым этилом (C2
H5
J) в щелочной среде................................................................................................................................
5.7. Взаимодействие 4-(g-меркаптопропил)-2-трет.-бутилфенола с бромистым бутилом (н-C4
H9
Br) в щелочной среде...............................................................................................................
6. Выводы............................................................................................................................
Полимерные вещества внедрились во все сферы человеческой деятельности – технику, здравоохранение, быт. Ежедневно мы сталкиваемся с различными пластмассами, резинами, синтетическими волокнами. Полимерные материалы обладают многими полезными свойствами: они высокоустойчивы в агрессивных средах, хорошие диэлектрики и теплоизоляторы. Некоторые полимеры обладают высокой стойкостью к низким температурам, другие - водоотталкивающими cвойствами и так далее.
Недостатками многих высокомолекулярных соединений является склонность к старению и, в частности, к деструкции – процессу уменьшению длины цепи и размеров молекул. Деструкция может быть вызвана механическими нагрузками, действий света, теплоты, воды и особенно кислорода и озона. Процесс уменьшения цепи идёт за счёт разрушения связей С-С и образования радикалов, которые в свою очередь, способствуют дальнейшему разрушению полимерных молекул.
Перед учёными стоит проблема продления срока службы полимерных изделий. Для предотвращения старения в полимерные материалы вводят различные добавки (стабилизаторы).
В качестве ловушек свободных радикалов, образующихся при деструкции полимерных материалов, используют фенольные стабилизаторы.
Фенольные стабилизаторы более эффективны, так как, улавливая свободные радикалы, образуют более устойчивые связи с ними, предотвращая дальнейшую деструкцию углеродной цепи. Кроме того, они обладают комплексным защитным действием (например, предотвращают разрушающее действие кислорода и высоких температур, или кислорода и радиации). Фенольные стабилизаторы выгодно отличаются от других добавок тем, что не изменяют цвет полимерных материалов, в состав которых вводятся.
В настоящее время в промышленном производстве полимеров требуются новые фенольные добавки с широким спектром стабилизирующих свойств и низкой себестоимостью. Несмотря на актуальность проблемы, исследований по разработке и получению фенольных стабилизаторов ведется мало. В связи с этим целью нашей работы был синтез новых серосодержащих пара-функционально-замещенных пространственно-затрудненных фенолов на основе 4-(g-хлорпропил)-2-трет.-бутилфенола и 2,2'-метиленбис-[4-(g-хлорпропил)-6-трет.-бутилфенола].
Основными задачами, которые требовалось решить в ходе исследования, являлись:
1. Изучить проблему старения полимеров и способов его предотвращения путем введения в материал фенольных стабилизаторов.
2. Ознакомиться с распространенными методами получения сульфидов.
3. Проверить возможности синтеза несимметричных сульфидов взаимодействием меркаптанов (4-(g-меркаптопропил)-2-трет.-бутилфенола и 2,2'-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола]) с алкилгалогенидами в этиловом спирте.
2.
Пространственно-затрудненные фенолы и стабилизация полимерных материалов
Полимерные материалы в значительной мере подвержены воздействию условий окружающей среды (свет, тепло, действие озона, радиация, механические нагрузки).Под влиянием этих факторов снижается эластичность, ухудшается электроизоляционные свойства и др. Эти явления, называемые в совокупности старением, приводят к необратимым изменениям свойств полимерных материалов и сокращают срок службы изделий из них. При эксплуатации большинство полимеров находится в контакте с кислородом воздуха, т.е. в окислительной среде. Реакции окислительной деструкции являются наиболее распространенными из реакций, протекающих при старении в естественных условиях, и представляют собой радикально-цепной окислительный процесс. Этот процесс активируется различными внешними воздействиями – тепловым, радиационным, механическим, химическим. Характерная особенность радикально-цепных окислительных процессов – возможность их резкого замедления путем введения небольшого количества ингибитора (стабилизатора).
Выделяют следующие типы стабилизаторов:
· антиоксиданты или антиокислители (защищающие полимерные вещества от разрушающего действия кислорода);
· антиозонаты (защищающие полимерные вещества от разрушающего действия озона);
· светостабилизаторы (защищающие полимерные вещества от разрушающего действия ультрафиолетовых лучей);
· термостабилизаторы (защищающие полимерные вещества от разрушающего действия высокой температуры);
· антирады (защищающие полимерные вещества от разрушающего действия радиационного излучения).
Как известно, основу макромолекулы большинства полимеров общего назначения составляет углеродная цепь типа:
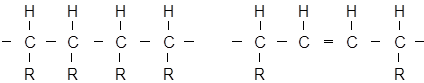
где: R = H, alk, ar.
В общем виде механизм ингибированного окисления углеводородов молекулярным кислородом может быть представлен следующей схемой:
Механизм ингибированного окисления углеводородов
(0) RH ® R•
(1) R• + O2
® ROO•
(2) ROO• + RH ® ROOH + R•
(3) ROOH ® RO• + HO•
(4) R• + R• ® R-R
(5) ROO• + R• ® ROOR
(6) ROO• + ROO• ® ROH + R"COR + O2
(7) ROO• + InH ® ROOH + In•
(8) In• + RH ® InH + R•
(9) In• + In• ® In-In
(10) In• + ROO• ® InOOR
В целом процесс окисления зависит от величины константы скорости реакции продолжения цепи (k2) и концентрации перекисных радикалов. Соответствующие гидроперекиси являются первичными продуктами окисления, дальнейший распад которых приводит к различным кислородсодержащим веществам и часто сопровождается разрывом углерод-углеродной цепи.
Присутствующий в окисляющейся системе ингибитор (InH), как правило, реагирует c радикалами ROO• (реакция 7), либо прерывая цепь окисления, либо уменьшая концентрацию этих радикалов, что приводит к снижению скорости окисления. Естественно, что чем менее активен получающийся из ингибитора радикал, тем меньше вероятность протекания реакции 8. Следовательно, тормозящее действие любого ингибитора окисления зависит, с одной стороны, от скорости реакции перекисных радикалов с ингибитором, а с другой – от активности получающегося из ингибиторов радикала. Малоактивные радикалы In• обычно не способны продолжать цепь (реакция 8) и рекомбинируют друг с другом (реакция 9). Таким образом, относительная активность радикала In• непосредственно в процессе окисления должна определяться отношением констант скоростей реакций k2/k7, которое характеризует максимальную возможность торможения процесса окисления при использовании данного ингибитора (сила ингибитора). Чем меньше это отношение, тем больше возможное тормозящее действие ингибитора.
2.
2. Пространственно-затрудненные фенолы, как ингибиторы радикальных процессов в полимерах.
В качестве стабилизаторов могут быть использованы различные органические сульфиды, в том числе пространственно-затруднённые фенолы типа:
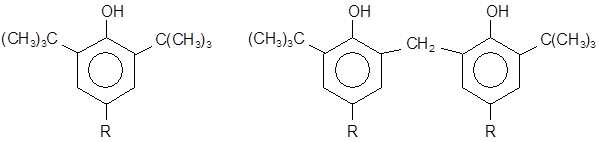
Пространственно-затрудненные фенолы (и получающиеся из них феноксильные радикалы) полностью удовлетворяют требованиям, предъявляемым к сильным антиоксидантам, и являются эффективными ингибиторами процессов окисления различных органических материалов. Подобные фенолы, как правило, реагируют с радикалами ROO•, прерывая цепь окисления.
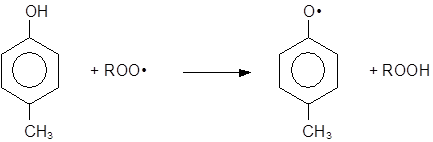
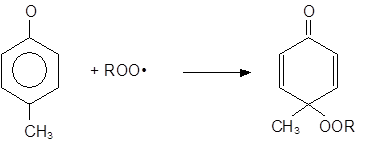
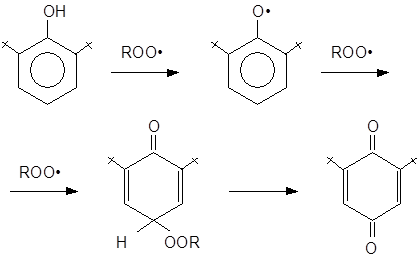
Эффективность пространственно-затрудненных фенолов как ингибиторов окисления существенно зависит от их структуры. Определяющим фактором в этом случае является строение о-алкильных групп и характер пара-заместителя. Ниже приведено соотношение k2/k7, характеризующее эффективность некоторых пространственно-затрудненных фенолов при ингибированном окислении тетралина при 50°С.
| k2/k7 |
| Фенол |
83 |
| о-крезол |
522 |
| 2-трет.-бутилфенол |
787 |
| 2,6-ди-трет.-бутилфенол |
967 |
| 2,4,6-три-трет.-бутилфенол |
1413 |
| 4-метил-2,6-ди-трет.-бутилфенол |
1990 |
Введение в пара-положение молекулы пространственно-затрудненного фенола электрондонорных заместителей увеличивает его антиокислительную активность, а электронакцепторных - уменьшает:
| Пара-заместитель: |
Относительная
эффективность: |
| - CH3
|
100 |
| - C2H5
|
125 |
| н-C4
H9
|
140 |
| - CH(CH3
)C2
H5
|
80 |
| - C(CH3
)3
|
36 |
Эффективность большинства стабилизаторов класса пространственно-затрудненных фенолов значительно повышается в композиции с веществами, разрушающими гидроперекиси и предотвращающими возможность вырожденного разветвления цепи окисления сульфидами, фосфитами, аминами, тиолами.
При использовании антиоксидантов помимо рассмотренных выше закономерностей, определяющих эффективность ингибитора, необходимо дополнительно учитывать следующие факторы: совместимость стабилизатора с защищаемым материалом, степень окрашивания полимера и особенности продукта его окисления, летучесть.
Как стабилизаторы могут использоваться симметричные и несимметричные сульфиды.
Наиболее распространённым способом получения симметричных органических сульфидов является взаимодействие алкилгалогенидов с сульфидом натрия Na2
S в органических растворителях. Более высокие выходы достигаются при использовании протонных (спирты: этиловый, изопропиловый и другие) или апротонных (диметилформамид) растворителях.
2 R–Hal + Na2
S ® R–S–R + 2 NaHal
Когда R = R’, то получаются симметричные сульфиды. Получение несимметричных сульфидов можно осуществить взаимодействием тиолов с алкилгалогенидами в присутствии щелочей. Сначала образуется тиолят-анион:
R – SH + OH` ® R – S` + H2
O
Далее возможны два варианта:
R – S` + R’ – Hal ® R – S – R’
или
R – Hal + R’ – S` ® R – S – R’
Выбор зависит от многих факторов.
Меркаптаны (алкантиолы), имеющие небольшую молекулярную массу, достаточно летучи (имеют отвратительный запах!), ядовиты и отсутствуют в продаже.
Для получения тиолов (меркаптанов) более эффективны и чаще используются в лабораторных условиях непрямые методы синтеза, с последующим разложением или восстановлением промежуточных продуктов. Из прямых синтезов наиболее доступным является нуклеофильного замещения атомов галогена на гидросульфид анион HS` . В лабораторных условиях из гидросульфидов с высоким выходом и хорошего качества получают гидросульфид аммония NH4
HS.
Получение соответствующих алкилгалогенидов из спиртов в лабораторных условиях не представляет особой сложности.
Одним из перспективных направлений производства отечественных антиоксидантов до настоящего времени остаётся синтез полифункциональных пространственно-затруднённых фенолов на основе 4-(g-хлорпропил)-2-трет.-бутилфенола (g-пропанола, разработка НИОХ СО РАН). Среди промышленных фенольных антиоксидантов неплохо зарекомендовали себя метиленбисфенолы.
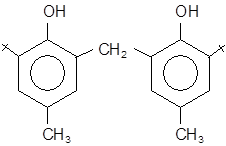
2,2’
-
метиленбис
-
[4
-
метил
-
6
-
трет.
-
бутилфенол]
Для получения метиленбисфенолов применяют конденсацию 2,4-диалкилфенолов с формальдегидом в кислой среде:
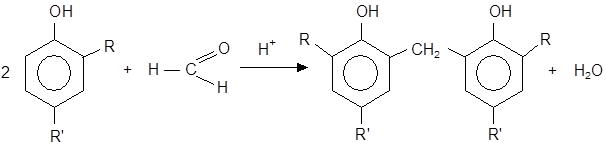
4.1. Получение 4
-(g-хлорпропил)-2-трет.-бутилфенола (хлорид Ф-13)
4-(g-хлорпропил)-2-трет.-бутилфенол удобнее получать деалкилированием 4 – (g-хлорпропил)-2,6-ди-трет.-бутилфенола, синтез которого хорошо отработан на кафедре химии НГПУ взаимодействием 4-(g-гидроксопропил)-2,6-ди-трет.-бутилфенола с хлорангидридами неорганических кислот: SOCl2
, POCl, POCl3
, PCl5
и COCl2
.
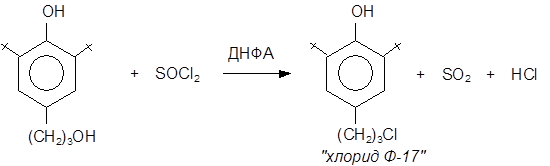
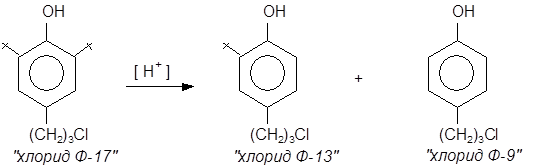
В качестве катализатора используют минеральные кислоты (H2
SO4
, HClO4
) или КУ-2 (катионно-обменная смола, Н-форма). Процесс ведут до почти полной конверсии исходного хлорида Ф-17, так как эффективного метода очистки целевого хлорида Ф-13 от остатков хлорида Ф-17 не существует. Хлорид Ф-9 хорошо растворяется в щелочах и его отмывают 5%-ным раствором гидроксида натрия NaOH. Продукт перегоняют под вакуумом (ост. давление 1-2 мм рт. ст.). Потери, за счёт протекания побочного процесса деалкилирования хлорида Ф-13 и образования хлорида Ф-9, составляют не менее 30%.Полученный хлорид Ф-13 (4-(g-хлорпропил)-2-трет.-бутилфенол) конденсируют с параформом в течении двух часов при 80°С (растворитель: уксусная кислота). Выход 70% от теоретического. Хлорид Ф-13 (4-(g-хлорпропил)-2-трет.-бутилфенол) используется как сырье при получении 4-(g-меркаптопропил)-2-трет.-бутилфенола и 2,2’метилен-бис-[4-(g-меркаптопропил)-6-трет.-бутилфенола].
4.2. Синтез 4
-(g-меркаптопропил)-2-трет.-бутилфенола
4-(g-меркаптопропил)-2-трет.-бутилфенол получали взаимодействием 4-(g-хлорпропил)-2-трет.-бутилфенола (хлорид Ф-13) с водноспиртовым раствором гидросульфида аммония при 120°С (16 часов, автоклав).
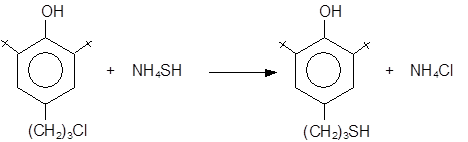
4.3. Синтез 2,2
'– метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола].
2,2’метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенол] получали аналогично 4-(g-меркаптопропил)-2-трет.-бутилфенолу.
Далее оба этих соединения используются в синтезе несимметричных сульфидов. Наиболее распространенным методом получения является алкилирование.
4.4. Синтез несимметричных сульфидов алкилированием 4
-(g-меркаптопропил)-2-трет.-бутилфенола и 2,2`метиленбис-[4-(g-меркаптопропил)-6-трет.- бутилфенол] алкилгалогенидами в щелочном виде.
При синтезе в качестве алкилирующих и конденсирующих агентов используют изобутилен, стирол, формальдегид, тиохлориды. Изобутилен выделяют из бутан-бутиленовой фракции газов пиролиза нефтепродуктов или получают дегидрированием изобутана. Изобутилен для производства индивидуальных стабилизаторов содержит 98,5-99% основного вещества.
Стирол получают каталитическим дегидрированием этилбензола. Для производства стабилизаторов используют стирол, предназначенный для получения полистирола. Гидрохинон, который вводят в стирол для ингибирования его полимеризации при ректификации и хранении, практически не влияет на процесс алкилирования стиролом в производстве стабилизаторов.
Формальдегид, получаемый окислением метанола, используют в виде водного раствора. Примесь метанола в формалине обычно не влияет на синтез стабилизаторов. В лабораторных условиях предпочтительнее применять параформ.
Получение сульфидов осуществляли в открытой системе при кипении растворителя ( этиловый спирт, 96°), в течение четырех часов, мольное соотношение тиол : галогенид : NaOH = 1 : 1,5 : 1,05 соответственно. Инертная среда - аргон. Экстрагент - бензол. Полученные продукты представляют собой вязкие, слабоокрашенные смолы.
5.1. Наработка 4
-(g-хлорпропил)-2-трет.-бутилфенола (хлорид Ф-13)
В четырёхгорлую круглодонную колбу ёмкостью 1000 мл, снабжённую мешалкой, термометром, насадкой Дина-Старка и керном с трубкой (для подачи инертного газа аргона) загрузили расплав 564,3 г (1,9352 моля) 4-(g-хлорпропил)-2,6-ди-трет.-бутилфенола (хлорид Ф-17), 115 г катионно-обменной смолы КУ-28 (Н-форма), 7 мл воды и нагрели, пропуская слабый ток аргона: 1 пузырек в секунду, на масляной бане (t°бани=180-190°) в течении 3,5 часов. Убрали нагрев, охладили реакционную смесь до 80-100°С и прилили 250 мл бензола, перемешали и отфильтровали катионно-обменную смолу. Катионно-обменную смолу промыли на фильтре несколько раз бензолом (объем 250 мл). Фильтрат перенесли в делительную воронку (емкостью 2 л) и промыли пять раз 5%-ным раствором гидроксида натрия NaOH (общий объём 1500 мл). Прилили 200-300 мл разбавленной соляной кислоты, встряхнули, слили водно-кислотный слой до нейтрального значения pH (универсальная индикаторная бумага pH 0-12), осушили над безводным сульфатом натрия Na2
SO4
, отфильтровали осушителем и отогнали бензол на ротационном вакуум-испарителе. Полученную смолу перегнали при остаточном давлении 1-2 мм рт. ст. и собрали основную фракцию от 120 до 125°С. Получили 219,4 г маслянистой бледно-желтой прозрачной жидкости (хлорид Ф-13). Выход 50% от теоретического.
5.2. Получение 4
-(g-меркаптопропил)-2-трет.-бутилфенола
В толстостенную стеклянную ампулу ёмкостью 100 мл загрузили 10 г хлорида Ф-13, 17 мл 20%-ого водного раствора гидросульфида аммония NH4
HS и 20 мл этилового спирта. Ампулу запаяли и нагрели при 125°С в течении 16 часов. После охлаждения ампулу отпаяли, содержимое перенесли в делительную воронку, прилили избыток разбавленной соляной кислоты, встряхнули и экстрагировали бензолом (объем 50-70 мл), промыли водой до нейтрального значения pH (универсальная индикаторная бумага pH 0-12), осушили над безводным сульфатом натрия Na2
SO4
, отфильтровали осушитель и отогнали бензол на ротационном вакуум-испарителе, получили 9,57г светло-жёлтой прозрачной вязкой смолы (4-(g-меркаптопропил)-2-трет.-бутилфенол), СОВ по данным ГЖХ 95%, выход 94,7% от теоретического.
5.3. Получение 2,2'
-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола]
В толстостенную стеклянную ампулу ёмкостью 100 мл загрузили 10 г хлорида Ф-27 (2,2'-метиленбис-[4-(g-хрорпропил)-6-трет.-бутилфенол]), 17 мл 20%-го водного раствора гидросульфида аммония NH4
HS и 20 мл этилового спирта. Ампулу запаяли и нагрели при 125°С в течении 16 часов. Выделение продукта провели аналогично выделению 4-(g-меркаптопропил)-2-трет.-бутилфенола. Получили 9,97 г светло-жёлтой прозрачной очень вязкой смолы (2,2'-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенол]) Выход 98,5% по данным ГЖХ от теоретического.
5.4
.Взаимодействие 2,2'-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола] с бромистым бутилом (н-C4
H9
Br) в щелочной среде
В четырехгорлую остродонную колбу емкостью 25 мл, снабженную мешалкой, обратным холодильником и керном для подачи аргона, загрузили 3 г (0,0065 моль) меркаптана Ф-27, 1,8 мл бромистого бутила, 0,65 г гидроксида натрия и 10 мл этилового спирта (96°). Нагрели до кипения и выдержали при постоянном перемешивании и слабом токе аргона в течении 4-х часов. После охлаждения нейтрализовали смесь раствором соляной кислоты. Содержимое колбы перенесли в делительную воронку, дважды провели экстракцию бензолом; объединённый бензольный экстракт отмыли дистиллированной водой и осушили над безводным сульфатом натрия Na2
SO4.
Осушитель отфильтровали, и отогнали бензол на ротационном вакуумном испарителе.
Получили вязкую тёмно-жёлто-зеленоватую смолу, массой 3,9 г.
5.5. Взаимодействие 2,2'
-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола] с йодистым этилом (C2
H5
J) в щелочной среде
В четырехгорлую остродонную колбу емкостью 25 мл, снабженную мешалкой, обратным холодильником и керном для подачи аргона, загрузили 3,72 г (0,0065 моль) меркаптана Ф-27, 2,2 мл йодистого этила, 0,65 г гидроксида натрия и 10 мл этилового спирта (96°). Нагрели до кипения и выдержали при постоянном перемешивании и слабом токе аргона в течении 4-х часов. После охлаждения нейтрализовали смесь раствором соляной кислоты. Содержимое колбы перенесли в делительную воронку, дважды провели экстракцию бензолом; объединённый бензольный экстракт отмыли дистиллированной водой и осушили над безводным сульфатом натрия Na2
SO4.
Осушитель отфильтровали, и отогнали бензол на ротационном вакуумном испарителе.
Получили вязкую жёлто-зеленоватую смолу, массой 3,86г.
5.6. Взаимодействие 4
-(g-меркаптопропил)-2-трет.-бутилфенола с йодистым этилом (C2
H5
J) в щелочной среде.
В четырехгорлую остродонную колбу емкостью 25 мл, снабженную мешалкой, обратным холодильником и керном для подачи аргона, загрузили 3 г (0,013 моль) меркаптана Ф-13, 1,6 мл йодистого этила, 0,55 г гидроксида натрия и 10 мл этилового спирта (96°).Нагрели до кипения и выдержали при постоянном перемешивании и слабом токе аргона в течении 4-х часов. После охлаждения нейтрализовали смесь раствором соляной кислоты. Содержимое колбы перенесли в делительную воронку, дважды провели экстракцию бензолом; объединённый бензольный экстракт отмыли дистиллированной водой и осушили над безводным сульфатом натрия Na2
SO4.
Осушитель отфильтровали, и отогнали бензол на ротационном вакуумном испарителе.
Получили вязкую светло-жёлтою смолу, массой 3,3г .
5.7. Взаимодействие 4
-(g-меркаптопропил)-2-трет.-бутилфенола с бромистым бутилом (н-C4
H9
Br) в щелочной среде.
В четырехгорлую остродонную колбу емкостью 25 мл, снабженную мешалкой, обратным холодильником и керном для подачи аргона, загрузили 3 ,2 (0,0138 моль) меркаптана Ф-13, 2,3 мл йодистого этила, 0,58 г гидроксида натрия и 10 мл этилового спирта (96°). Нагрели до кипения и выдержали при постоянном перемешивании и слабом токе аргона в течении 4-х часов. После охлаждения нейтрализовали смесь раствором соляной кислоты. Содержимое колбы перенесли в делительную воронку, дважды провели экстракцию бензолом; объединённый бензольный экстракт отмыли дистиллированной водой и осушили над безводным сульфатом натрия Na2
SO4.
Осушитель отфильтровали, и отогнали бензол на ротационном вакуумном испарителе.
Получили вязкую светло-жёлтою смолу, массой 4,7г.
· Освоена методика деалкилирования пространственно-затруднённых фенолов на катионно-обменной смоле КУ-28 и осуществлена наработка 200 г 4-(g-хлорпропил)-2-трет.-бутилфенола.
· Получен 4-(g-меркаптопропил)-2-трет.-бутилфенол взаимодействием 4-(g-хлорпропил)-2-трет.-бутилфенола с 20%-ным водным раствором гидросульфида аммония NH4
HS в закрытой системе.
· Получен 2,2’-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенол] взаимодействием 2,2’-метиленбис-[4-(g-хлорпропил)-6-трет.-бутилфенола] с 20%-ным водным раствором гидросульфида аммония в закрытой системе.
· Взаимодействием 4-(g-меркаптопропил)-2-трет.-бутилфенола в щелочной среде с йодистым этилом C2
H5
J и бромистым бутилом
н-C4
H9
Br получено два продукта, содержащих несимметричные сульфиды.
· Взаимодействием 2,2’-метиленбис-[4-(g-меркаптопропил)-6-трет.-бутилфенола] в щелочной среде с йодистым этилом C2
H5
J и бромистым бутилом н-C4
H9
Br получено два смолоподобных продукта, содержащих несимметричные сульфиды.
· Полученные несимметричные сульфиды на основе 4-(g-меркаптопропил)-2-трет.-бутилфенола являются теоретически возможными перспективными антиоксидантами, но их химические свойства ещё не изучены.
Список литературы
1. Адельшина Е.Б.
Синтез новых пространственно-затруднённых пара- функционально-замещённых метиленбисфенолов. Дипломная работа. – Новосибирск: НГПУ, 1996.
2. Берлин А.Я.
Техника лабораторных работ в органической химии. –
М.: Химия, 1973.
3. Горбунов Б.Н., Гурвич Я.А., Маслова И.П.
Химия и технологии стабилизаторов полимерных материалов. – М.: Химия,1981.
4. Ершов В.В., Никифоров Г.А., Володькин А.А.
Пространственно-затруднённые фенолы. – М.: Химия,1972.
5. Карякин Ю.В, Ангелов И.И.
Чистые химические вещества. – М.: Химия, 1974.
6. Общая органическая химия, том 5. – М.: Химия,1983.
7. Органикум. Практикум по органической химии, том 1. – М.:Мир,1973.
8. Птицына О.А. и др.
Лабораторные работы по органическому синтезу. –
М.: Просвещение, 1979.
9. Справочник химика, том 2. – Л.: Химия, 1971.
|