| Содержание: стр:
Введение……………………………………………………………2
1. Общий обзор методов определения витаминов…………………3
2. Хроматографические методы определения витаминов…………5
3. Электрохимические методы определения витаминов…………10
4. Инверсионно вольтамперометрический метод определения
водорасторимых витаминов B1
B2
в пищевых продуктах………..13
Заключение………………………………………………………...18
Введение
В настоящее время на рынке появилось огромное количество витаминизированных продуктов питания для человека и кормов для животных, представляющих собой сухие многокомпонентные смеси. Ассортимент таких продуктов представлен достаточно широко. Это, прежде всего, биологически активные добавки к пище, премиксы, комбикорма для животных и птиц, поливитаминные препараты. Критерием качества таких продуктов может являться их анализ на содержание витаминов и, особенно, таких жизненно необходимых, как водорастворимые и жирорастворимые витамины, количество которых регламентируется нормативными документами и санитарными нормами качества.
Для определения витаминов применяют различные методы. Широко используемые оптические методы анализа трудоемки, требуют больших затрат времени и дорогостоящих реактивов, применение хроматографических методов осложнено использованием дорогостоящего оборудования. С каждым годом расширяется ассортимент и увеличивается производство продуктов питания, совершенствуется рецептура детского питания. Это в свою очередь предъявляет повышенные требования к контролю за качеством выпускаемой продукции и совершенствованию методов определения витаминов. Медико-биологические требования и санитарные нормы качества продовольственного сырья и пищевых продуктов характеризуют пищевую ценность большинства видов и групп продуктов детского питания различного назначения.
1. Общий обзор методов определения витаминов
Почти все витамины легко подвергаются окислению, изомеризации и разрушаются под воздействием высокой температуры, света, кислорода воздуха, влаги и других факторов.
Из существующих методов определения витамина С (аскорбиновой кислоты) наиболее широко применяют метод визуального и потенциометрического титрования раствором 2,6-ди-хлорфенолиндофенола по ГОСТ 24556—81, основанный на редуцирующих свойствах аскорбиновой кислоты и ее способности восстанавливать 2,6-ДХФИФ. Темно-синяя окраска этого индикатора при добавлении аскорбиновой кислоты переходит в бесцветную. Важное значение имеет приготовление экстракта исследуемого продукта. Наилучшим экстрагентом является 6 %-ный раствор метафосфорной кислоты, который инактивирует аскорбинотоксидазу и осаждает белки.
Каротин в растительном сырье, концентратах и безалкогольных напитках контролируют физико-химическим методом по ГОСТ 8756.22—80. Метод основан на фотометрическом определении массовой доли каротина в растворе, полученном в процессе экстрагирования из продуктов органическим растворителем. Предварительно раствор очищают от сопутствующих красящих веществ с помощью колоночной хроматографии. Каротин легко растворяется в органических растворителях (эфир, бензин и др.) и придает им желтую окраску. Для количественного определения каротина используют адсорбционную хроматографию на колонках с окисью алюминия и магния. Такое определение пигментов на колонке зависит от активности адсорбента, количества пигментов, а также присутствия других компонентов в разделяемой смеси. Сухая смесь окиси алюминия задерживает каротин, а влажная пропускает в раствор другие красящие вещества.
Тиамин в основном находится в связанном состоянии в виде дифосфорного эфира — кокарбоксилазы, которая является активной группой ряда ферментов. С помощью кислотного гидролиза и под воздействием ферментов тиамин освобождается из связанного состояния. Этим способом определяют количество тиамина. Для расчета содержания витамина B1 используют флюрометрический метод, который применяют для определения тиамина в пищевых продуктах. Он основан на способности тиамина образовывать в щелочной среде с феррнцианндом калня тиохром, который дает интенсивную флюоресценцию в бутиловом спирте. Интенсивность процесса контролируют на флюорометре ЭФ-ЗМ.
В продуктах питания и напитках рибофлавин присутствует в связанном состоянии, т. е. в форме фосфорных эфиров, связанных с белком. Чтобы определить количество рибофлавина в продуктах, необходимо освободить его из связанного состояния путем кислотного гидролиза и обработки ферментными препаратами. Витамин B1 в безалкогольных напитках рассчитывают с помощью химического метода для определения количества легкогидролизуемых и прочно связанных форм рибофлавина в тканях. Метод основан на способности рибофлавина к флюоресценции до и после восстановления его гипосульфитом натрия. Определение общего содержания фенольных соединений. Для этого используют колориметрический метод Фолина — Дениса, который основан на образовании голубых комплексов при восстановлении вольфрамовой кислоты под действием полифенолов с реагентом в щелочной среде. Фенольные соединения определяют по хлорогеновой кислоте методом пламенной фотометрии на приборе ЕКФ-2.
2. Хроматографические методы определения витаминов
В последнее время за рубежом бурное развитие переживает метод высокоэффективной жидкостной хроматографии. Это связано, прежде всего, с появлением прецизионных жидкостных хроматографов, совершенствованием техники выполнения анализа. Широкое использование метода ВЭЖХ при определении витаминов нашло отражение и в числе публикаций. На сегодняшний день более половины всех опубликованных работ по анализу как водо- так и жирорастворимых витаминов посвящено применению этого метода.Широкое распространение при определении витаминов получили различные варианты хроматографии.
Для очистки токоферола от посторонних примесей используют метод тонкослойной хроматографии В сочетании со спектрофотометрическими и флуориметрическими методами этим способом проводят и количественное определение витамина Е. При разделении используют пластинки с силуфолом , кизельгелем
Метод газовой хроматографии рекомендован Государственной Фармакопеей (ГФ XI) для анализа масляных растворов а-токоферола ацетата. Этим способом определяют витамин Е в виде гептафторбутирильных производных и в пищевых продуктах.
Анализ изомеров токоферола в оливковом масле проводится методом газо-жидкостной хроматографии. Методики анализа ГХ и ГЖХ требуют получения летучих производных, что крайне затруднительно при анализе жирорастворимых витаминов. По этой причине данные способы определения не получили большого распространения. Определение витамина Е в пищевых продуктах, фармпрепаратах и биологических объектах проводят в градиентном и изократическом режимах как в нормально-фазовых, так и в обращенно-фазовых условиях. В качестве адсорбентов используют силикагель (СГ), кизельгур, силасорб , ODS-Гиперсил и другие носители. Для непрерывного контроля состава элюата в жидкостной хроматографии при анализе витаминов и увеличения чувствительности определения используют УФ (А,=292 нм), спектрофотометрический (Х=295нм), флуоресцентный (Х,=280/325нм), электрохимический, ПМР- [81] и масс-спектроскопический детекторы.
Большинство исследователей для разделения смесей всех восьми изомеров токоферолов и их ацетатов предпочитают использовать адсорбционную хроматографию. В этих случаях подвижной фазой обычно служат углеводороды, содержащие незначительные количества какого-либо простого эфира. Перечисленные методики определения витамина Е, как правило, не предусматривают предварительного омыления образцов, что существенно сокращает время выполнения анализа.
Разделение с одновременным количественным определением содержания жирорастворимых витаминов (А, Д, Е, К) при их совместном присутствии в поливитаминных препаратах проводят как на прямой, так и на обращенной фазах. При этом большинство исследователей предпочитают использовать обращенно-фазовый вариант ВЭЖХ. Метод ВЭЖХ позволяет анализировать водорастворимые витамины В1 и В2 как одновременно, так и отдельно. Для разделения витаминов используют обращенно-фазный, ион-парный и ионообменный варианты ВЭЖХ. Применяют как изократический, так и градиентный режимы хроматографирования. Предварительное отделение определяемых веществ от матрицы осуществляют путем ферментативного и кислотного гидролиза пробы.
Преимущества метода жидкостной хроматографии:
-Одновременное определение нескольких компонентов
-Устранение влияния мешающих компонентов
- Комплекс можно быстро перестроить на выполнение других анализов.
Состав и характеристика оборудования и программного обеспечения для жидкостного хроматографа "Хромос ЖХ-301":
Таблица 1
| Насос SSI серии III
|
Насос для подачи элюента имеет низкий уровень пульсаций
|
| Детектор спектрофотометрический СПФ-1
|
Детектор по измерению поглощения (длинна волны 254 - 455 нм)
|
| Кран-дозатор
|
Применяется шестипортовый двухходовой петлевой дозатор. Увеличение петли дозирования позволяет увеличить чувствительность анализа.
|
| Насос SSI серии III
|
Дополнительный насос может быть использован для создания градиента (необязателен)
|
| Колонки хроматографические
|
Аналитическая колонка Vydac 201SP54 250х4 мм или аналогичная.
|
| Вспомогательное оборудование для лаборатории жидкостной хроматографии
|
Вакуумный насос для дегазации элюента .
|
| Программа сбора и обработки хроматографической информации "Хромос 2.3."
|
Работа одного компьютера с несколькими хроматографами (количество зависит от конфигурации компьютера). Методы расчета хроматограмм: абсолютная калибровка, внутренний стандарт.
|
| Компьютер IBM-PC/AT с принтером
|
Celeron-366 (и выше), 32 Мб RAM. HDD-10G. FDD 1.44 (либо CD-ROM). клавиатура, мышь. монитор 15" SVGA, принтер.
|
|
Достоинства хроматографа "Хромос ЖХ-301":
-высокая стабильность и точность поддержания расхода элюента обеспечивается конструкцией насосов высокого давления.
-легкий доступ к колонкам обеспечивается конструкцией прибора.
-эффективность разделения обеспечивается применением высокоэффективных хроматографических колонок.
-широкий линейный диапазон измерительного сигнала детекторов без переключений предела измерения, что позволяет с высокой точностью измерять пики как большой, так и малой концентрации.
Хроматограмма анализа водорастворимых витаминов:
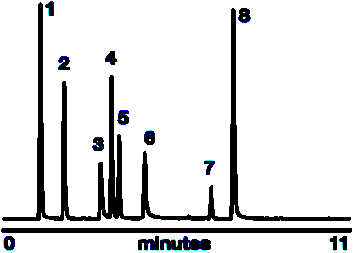 1 аскорбиновая кислота (C), 1 аскорбиновая кислота (C),
2 никотиновая кислота (Niacin),
3 пиридоксин (B6),
4 тиамин (B1),
5 никотинамид (B3),
6 фолиевая кислота (M),
7 цианокобаламин (B12),
8 рибофлавин (B2).
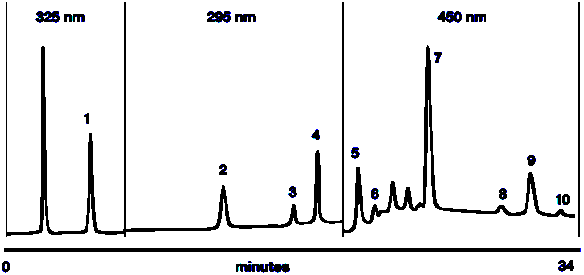
Хроматограмма анализа жирорастворимых витаминов:
1. Витамин А
2. токол
3. y -токоферол
4. a -токоферол (Витамин E)
5. лютеин
6. зеаксантин
7. криптоксантин
8. a -каротин
Несмотря на высокую чувствительность метода ВЭЖХ, высокая стоимость приборов, а также длительность анализа с учетом времени пробоподготовки существенно ограничивает его применение в аналитических лабораториях нашей страны.
3. Электрохимические методы определения витаминов
Электрохимические методы анализа широко используются в аналитической практике благодаря простоте, надежности, экспрессности, возможности определять практически все элементы периодической системы, разнообразные неорганические и органические соединения в широком диапазоне концентраций. Наибольшее развитие электрохимические методы получили в последние годы за счет использования электронной аппаратуры, компьютеров, разработке новых электродов и способов их очистки, позволяющих применять электрохимию на различных стадиях исследования. В настоящее время электрохимические методы анализа успешно применяются и для определения витаминов.
Публикации по определению витамина Е электрохимическими методами немногочисленны. Потенциометрическое и амперометрическое титрование хлорным золотом находит ограниченное применение из-за малой специфичности, т.к. хлорное золото не обладает способностью окислять эфиры токоферолов и другие производные. Для определения суммы токоферолов в их концентратах предложен метод амперометрического титрования в среде 1н. раствора серной кислоты в 75% этаноле раствором сульфата церия (IV) с помощью платинового электрода. Анализ токоферолов в этаноле и хлороформе с использованием ферроцианид иона в качестве медиатора проводили методом кулонометрии .
Также существует методика определения витамина Е в растительных маслах хронопотенциометрическим методом. Токоферолы окисляют при постоянном токе (4-10 мА) на стеклоуглеродном плоском дисковом электроде. Предел обнаружения и нижняя граница определяемых содержаний, достигнутые при определении витамина этим методом, составили соответственно 15 мг/дм3 и 20 мг/дм3.
Потенциометрическое определение витамина В1 применяют в нескольких вариантах. Потенциометрическое титрование тиамина бромида проводят в 0,05 М AgNC>3 на индикаторном серебряном электроде. В фармпрепаратах тиамин титруют вольфрамовофосфорной кислотой с использованием графитового электрода.
В основе амперометрического метода определения тиамина лежит его реакция с метавольфрамовой кислотой. Измерения проводят при Е=-0,65 В анализаторе Гейровского.
Полярографический метод получил достаточно широкое распространение при анализе органических веществ. Основой, позволяющей делать заключение о структуре вещества, является форма и характер поляризационной кривой, а также величина потенциала полуволны, которая характеризует не только функциональную группу, но и ее положение в молекуле. Токоферолы являются полярографически активными, способны окисляться, образуя в области положительных потенциалов анодную волну. Известен способ определения токоферолацетата, основанный на получении одноэлектронной волны его анодного окисления (Е1/2-1,33 В, относительно нас.к.э.) в растворе ацетонитрила на фоне перхлората лития. о-Токоферол в этих условиях образует анодную волну при потенциале Е,/2=0,68 В. Определение витамина Е полярографированием на катоде возможно в виде его окисленной формы - токоферилхинона. Восстановление проводят в 75% этаноле на фоне ацетатного буферного раствора (рН 6-7).
Методика количественного полярографического определения токоферолов в маслах и жирах в виде токоферилхинонов основан на том, что анализ ведут на ртутном капельном электроде в среде ацетатного буферного раствора, содержащем 75 % этилового спирта (рН 7). Пробоподготовка включает омыление пробы 2 н. раствором КОН на кипящей водяной бане, экстракцию неомыляемой фракции сернокислым эфиром, растворение полученного экстракта в 96% этиловом спирте. После осаждения стеринов, токоферолы окисляют до токоферилхинонов раствором комплексной соли аммонийнитрата церия. Полярографический метод анализа витамина Е находит ограниченное применение в аналитической практике. Использование ртутного капельного электрода нежелательно по требованиям техники безопасности в испытательных химических лабораториях. Много внимания в литературе уделено полярографическому методу определения водорастворимых витаминов. Витамин В вызывает образование каталитических волн в аммиачном растворе кобальтовой соли, которые обусловлены раскрытием тиазолового цикла и образованием SH-формы тиамина. В щелочных средах при рН>9 тиамин образует анодную волну при Е]/2= -0,4В, которая соответствует образованию соединения SH-формы тиамина со ртутью. Определение витамина B1 в поливитаминных препаратах проводили на фоне 0,1 М KCI при Е=-1,25 В. Минимально определяемая концентрация витамина в этих условиях равна 2,0 мг/л [174, 216]. Методом производной полярографии тиамин анализировали в кислых буферных растворах. При рН 1,3 - 3,07 обнаруживается две волны, а при рН 3,07-4,92 только одна волна восстановления витамина. Переменнотоковая полярография применялась при исследовании хлористоводородной соли тиамина в буферных растворах с рН 3-10 [174].
4. Инверсионно вольтамперометрический метод определения водорасторимых витаминов B1
B2
в пищевых продуктах.
Витамины B1
/тиамин; 4-метил-5- β -оксиэтил-N-/2-метил-4-амино-5-метилпиримидил/-тиазолий бромид /или хлорид/ / и B2
/рибофлавин; 6,7-диметил-9-/ в -1-рибитил/-изоаллоксазин/ необходимы для нормальной жизнедеятельности организма. Они входят в состав сложных биокатализаторов, выполняющих различные функции в процессе обмена веществ. Важнейшие вещества такого рода активны физиологически в малых дозах и поступают в организм человека вместе с пищей.
Для вольтамперометрического анализа часто допустимы более простые методики предварительного выделения соединений, чем флуориметрические или хроматографические. Предварительная подготовка проб также может быть существенно уменьшена из-за возможности проведения вольтамперометрических измерений в мутных и окрашенных растворах как в водных, так и в неводных средах.
Проводится гидролиз связанных форм витаминов и белка, осаждение водорастворимого белка из гидролизата с последующим инверсионно-вольтамперометрическим определением витаминов. Новым в способе является то, что проводят кислотный гидролиз (0,15-0,20) M раствором H2
SO4
или HCl на кипящей водяной бане в течение 30 40 минут, после охлаждения гидролизата проводят осаждение водорастворимого белка (0,4-0,5) г хлорида марганца 4-водным, затем 2-3 г хлорида калия с последующим инверсионно-вольтамперометрическим определением витаминов в безбелковом гидролизате путем регистрации катодных пиков витамина B1
при потенциалах (0,35-0,48)B (Eэ
-0,15 B), анодных пиков витамина B2
в диапазоне потенциалов (0,15-0,20)B и Eэ
-(0,50-0,60)B в режиме дробного дифференцирования.
В прототипе описано проведение гидролиза сначала 0,10M раствором HCl, затем протеолитическими и фосфатазными ферментами в течение более 16 20 часов. Для определения витаминов ИВ способом использование ферментов значительно снижает экспрессность анализа и делает невозможным проведение вольтамперометрического определения. Предлагаемые условия гидролиза (0,15-0,20) M H2
SO4
или HCl при кипячении в течение 30 40 минут позволяют селективно и экспрессно определять водорастворимые витамина B1
и В2
с хорошей воспроизводимостью. Относительное стандартное отклонение Sr не превышает 0,2 для концентрации определяемых веществ 0,1 мг/100 г. Тиамин и рибофлавин, вероятно, можно было бы определять методом ИВ и без их выделения из основы в отсутствии больших количеств белковых примесей. Присутствие значительных количеств белка в пищевых продуктах мешает ИВ определению витаминов, т.к. белки являются электрохимически активными, хорошо адсорбируются на электродных материалах и могут участвовать в редокс-превращениях , что затрудняет ИВ анализ и приводит к завышенным показателям содержания витаминов в пробах. Для устранения мешающего влияния белков, разрушения связанных форм витаминов и распада белков на более простые составные части в предлагаемом способе гидролиз проводят (0,15-0,20) М H2
SO4
или HCl. Концентрации кислот и время гидролиза /t/ (равное 30-40 минутам) подобраны экспериментально. Абсолютной новизной является экспериментально подобранный реагент H2
SO4
. Использование кислот с молярной концентрацией C<0,15 М ухудшает условия гидролиза, а при C>0,20 М ухудшаются условия ИВ определения из-за большого значения остаточного тока, связанные с выделением водорода на индикаторном стеклоуглеродном электроде. Оптимальным временем гидролиза является 30-40 минут. При t>40 минут снижается экспрессность анализа, а при t<30 минут ухудшаются условия проведения гидролиза.
Другим отличительным признаком являются установленные условия осаждения остаточных количеств растворимого белка из гидролизата (в прототипе осаждение не применяли). Необратимое осаждение белка проводили солями тяжелых металлов (Pb2+
, Cu2+
, Ag+
, Fe2+
, Mn2+
и др.). При этом вместе с белками выделялись и их комплексные соединения с фенольными веществами и сахаридами, что обеспечивало оптимальные условия проведения электродного процесса. В предлагаемом способе впервые в качестве осадителя выбрана соль MnCl2
· 4H2
O в количестве 0,40-0,50 г. Ранее для отделения белка соль MnCl2
-4H2
O не применялась. Использование больших количеств соли />0,5 г/ повышает растворимость белка, по-видимому, за счет протекания адсорбционной пептизации, и ухудшаются условия проведения электродного процесса, особенно при определении тиамина. При массе соли <0,45 г ухудшаются условия осаждения органических примесей. После отделения осадка центрифугированием проводили вторичное осаждение следов белка из центрифугата с помощью нейтральных солей KCl и (NH4
)2
SO4
(высаливание следов белковых примесей). Хлорид калия осаждал белки слабее, чем сульфат аммония, вследствие меньшей дегидратирующей способности, которая характеризуется положением ионов в ряду Гофмейстера. Однако применение сульфата аммония ухудшало воспроизводимость и точность электроанализа. Использование KCl способствовало стабилизации условий проведения электродного процесса, повышало точность и воспроизводимость КХА методом ИВ. Масса используемой соли KCl также установлена экспериментально. Использование больших количеств соли KCl />3 г/ понижало электрическую проводимость раствора и ухудшало условия проведения электродного процесса. Уменьшение концентрации соли /<2 г/ ухудшало условия осаждения. Осадок белка мог вновь частично раствориться при стоянии пробы или после разведения пробы водой.
Важным для определения водорастворимых витаминов методом ИВ является выбор фонового электролита. В предлагаемом способе применение дополнительного электролита в качестве фона не требуется. Анализируемый раствор после осаждения белков имеет оптимальное значение pH для ИВ определения, обладает хорошей электропроводностью и поэтому сразу подвергается вольтамперметрированию. Определение тиамина проводят методом катодной ИВ с использованием ртутно-пленочного индикаторного электрода, рибофлавина - адсорбционной ИВ на стеклоуглеродном электроде в режиме дробного дифференцирования. Вольтамперограммы регистрируют при максимальных значениях потенциала -(0,35-0,48)В и -(0,15-0,20)В соответственно для витаминов B1
и B2
. Метод ИВ для определения водорастворимых витаминов B1
и B2
в пищевых продуктах ранее не применялся. Массовую долю витамина в пробе вычисляют в мг/100 г по формуле:

где X1
содержание данного компонента в анализируемой пробе, мг/100 г;
Cд
концентрация аттестованной смеси /АС/ витамина, из которой делается добавка к анализируемой пробе, мг/см3
;
Vд
объем добавки АС витамина, см3
;
J1
величина максимального тока компонента в анализируемой пробе, А;
J2
величина максимального тока компонента в пробе с добавкой АС, А;
Vал
объем аликвоты пробы, взятой для анализа, см3
;
Vк
объем анализируемого раствора после гидролиза, см3
;
mпр.
масса анализируемого вещества, г.
Установленные условия анализа в предлагаемом способе впервые позволили экспрессно (за 1,5-2 часа) количественно определять витамины B1
и B2
в пищевых продуктах на уровне 0,01-0,02 мг/100 г в присутствии пигментов, в окрашенных средах без предварительного отделения других водорастворимых витаминов группы B, PP, аскорбиновой, фолиевой, никотиновой, лимонной кислот, триптофана, мочевины, цистина, цистеина, ионов PO3
4
-
Cl-
, F-
, Br-
, S2-
, SO2
4
-
Zn2+
, Cu2+
, Cd2+
, Fe2+
, Fe3+
и др.
Пример: 1.
Определение витамина B1
(тиамина) в детской молочной смеси "Семилко".
Навеску пробы массой 10 г переносят в мерную колбу вместимостью 250 см3
добавляют 92 см3
0,15 М HCl и нагревают с воздушным холодильником на кипящей водяной бане в течение 30 минут.Затем охлаждают до температуры -30o
C и добавляют 0,5 г MnCl2
·4H2
O, центрифугируют на лабораторной медицинской центрифуге в течение 20 минут со скоростью 3000 оборотов в минуту. Центрифугат сливают в стакан и добавляют 3 г KCl. Полученный осадок отфильтровывают через бумажный фильтр. Аликвоту фильтрата объемом 10 см3
помещают в электролизер и проводят вольтамперометрические измерения при условии: потенциал электролиза Eэ
=-0,10 В, время электролиза τэ
= 180 с, скорость развертки потенциала W=20 мВ/с. Катодный пик витамина регистрируют с использованием ртутно-пленочного электрода в диапазоне потенциалов -(0,45-0,48) B при чувствительности прибора 2·10-9
A/мм. Содержание вещества оценивают методом добавок аттестованных смесей. Время анализа одной пробы не превышает 2 часа.
Заключение
В современных физико – химических методах определения витаминов, при взаимодействии витаминов с рядом химических соединений наблюдаются характерные цветные реакции, интенсивность окраски которых пропорциональна концентрации витаминов в исследуемом растворе. Поэтому витамины можно определить фотоколориметрически, например витамин В1
– при помощи диазореак-тива и т.д. Эти методы позволяют судить как о наличии витаминов, так и о количественном содержании их в исследуемом пищевом продукте или органах и тканях животных и человека. Встречаются трудности при подборе специфического реактива для взаимодействия с определенным витамином. Некоторые витамины обладают способностью поглощать оптическое излучение только определенной части спектра. В частности, витамин А имеет специфичную полосу поглощения при 328-330 нм. Измеряя коэффициент поглощения спектро-фотометрически, можно достаточно точно определить количественное содержание витаминов в исследуемом объекте. Для определения витаминов В1
, В2
и других применяют флюорометрические методы. Используют и титриметрические методы - например, при определении витамина С применяют титрование раствором 2,6-дихлорфенолиндофенола.
Список использованной литературы:
1. ГОСТ 25999-83. Продукты переработки плодов и овощей.
2. Методы определения витаминов B1
и B2
. -М.Госкомитет СССР по стандартам, 1984, с.11.
3. Витамины. Под. ред. Смирнова В.Г. -М.: Медицина, 1974. - 496 с.
4. Березовский В.М. Химия витаминов. - М.: Пищепромиздат, 1959.
5. Степанова Е.Н., Сапожникова Г.А., Нефедова Р.С. Сравнительное изучение различных методов определения рибофлавина в пищевых продуктах. //Вопросы питания. - 1969. - Т.28, № 5. - С. 14-18.
6. Экспериментальная витаминология. Под. ред. Ю.М. Островского. — Минск, 1979. - С. 224 - 266.
7. Тутельян В.А., Суханов Б.П., Австриевских А.Н., Позняковский В.М. Биологически активные добавки в питании человека. - Томск: Изд-во НТЛ, 1999.-296 с.
8. Интернет – www.himik.ru; www.vitamin.ru;
|