| Министерство образования и науки Российской Федерации
Федеральное агентство по образованию
государственный технический университет
кафедра химической технологии
КУРСОВАЯ РАБОТА
по дисциплине «Общая химическая технология»
на тему: «Производство бутадиена-1,3»
2007 г.
1.
Содержание
1. Содержание
2.Задание
3.Введение
4.Синтез ХТС
4.1 Обоснование создания эффективной ХТС
4.2 Определение технологической топологии ХТС
4.3 Установление технологических и конструкционных параметров ХТС, технологических параметров режима и потоков
4.4 Изображение графических моделей ХТС (функциональной, структурной, операторной, технологической схемы с описанием)
5 Анализ ХТС.
5.1 Представление изучаемого объекта в виде иерархической структуры ХТС
5.2 Построение математической модели ХТС
5.3 Изучение свойств и эффективности функционирования ХТС
6 Заключение
7 Список использованной литературы
2. Задание
Какое количество бутана необходимо для получения 2т бутадиена-1,3, если известно, что бутан содержит 15% примесей, а степень превращения составляет 80%?
3. Введение
Производство бутадиена-1,3 очень актуально, т.к. бутадиен является сырьём для производства каучуков.
Бутадиеновые каучуки— продукт полимеризации бутадиена. При полимеризации молекулы бутадиена могут соединяться с участием любой из двух или обеих двойных связей, образуя полимеры с различной конфигурацией химических звеньев в макромолекуле:
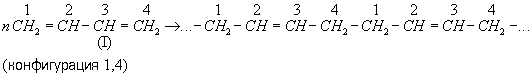
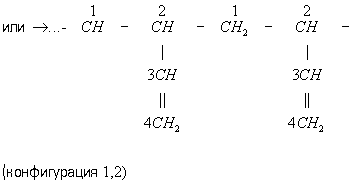
Для конфигурации 1, 4 возможны 2 изомера — цис (II) и транс (III)
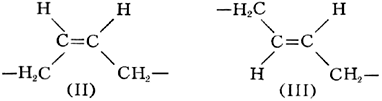
В зависимости от условий полимеризации и природы катализатора получают Б. к., различающиеся содержанием в их макромолекулах звеньев конфигурации 1, 4 (как цис-, так и транс-структуры) и звеньев конфигурации 1, 2.
Бутадиен является крупнотоннажным продуктом, который очень широко используется.
Бутадиеновые каучуки - каучуки общего назначения. Основная область применения каучуков с высоким содержанием звеньев 1,4-цис- изготовление протекторных и обкладочных (каркас, боковина) шинных резин. Эти каучуки используют также в производстве РТИ (например, конвейерных лент), низа обуви, изоляции кабеля, ударопрочного полистирола и др. Каучуки с высоким содержанием звеньев 1,2 (СКВ, СКДСР) используют в производстве антифрикционных асбестотехнических изделий, линолеума, абразивного инструмента, изделий бытового назначения и др.
По объему мирового производства бутадиеновые каучуки уступают лишь бутадиен-стирольным каучукам; выпуск бутадиеновых каучуков капиталистических странах в 1985 составил приблизительно 1,5 млн. т.
4.Синтез ХТС
4.1 Обоснование эффективной ХТС
Производство бутадиена
Впервые промышленное производство бутадиена из этилового спирта было осуществлено в СССР в 1933 г. по разработанному С. В. Лебедевым методу. В основе процесса лежат превращения этанола в присутствии бифункционального катализатора, обеспечивающего одновременное протекание реакций дегидрирования (ZnO) и дегидратации (А12
О3
, промотированный К2
О), при температуре не выше 400 "С:
2С2
Н5
ОН → СН2
=СН-СН=СН2
+ 2Н2
О + Н2
В настоящее время этот и другие методы практически полностью вытеснены одно- или двухстадийным дегидрированием насыщенных углеводородов.
Каталитическое дегидрирование насыщенных углеводородов стало основным источником производства не только бутадиена, но и таких крупнотоннажных продуктов как изопрен, изобутилен, стирол. На основе этих мономеров, получаемых в близких условиях, вырабатываются многочисленные виды синтетических каучуков, в том числе хлоропренового, нитрильного, бутадиенового, бутилкаучука, изопренового, бутадиен-стирольного, бутадиен-нитрильного и др. Спрос на бутадиен обусловлен также его использованием для производства адипонитрила и получением на его основе найлона.
Двухстадийный процесс
Большинство промышленных установок получения дивинила из бутана работает по двухстадийной схеме. Первая стадия дегидрирования бутана заключается в превращении его В бутилен, а вторая — это процесс получения дивинила из бутилена-
Дегидрирование бутана в бутилен на хромооксидном промотированном катализаторе, нанесенном на оксид алюминия, протекает по реакции
С3
Н10
↔С4
Н8
+Н2
; ΔН= 131 кДж
В промышленных реакторах протекают и побочные реакции: обратная реакция гидрирования бутилена, крекинг бутана и бутилена, изомеризация бутана и бутилена, реакции углеобразования. На советских промышленных установках по дегидрированию бутана применяют системы с кипящим слоем мелкозернистого алюмохромового катализатора марки К.-5.
В процессе дегидрирования бутана катализатор покрывается углеродистыми отложениями и изменяет свой химический состав. Активность катализатора при этом резко снижается. С целью реактивации катализатор непрерывно отводят из реактора и обжигают в токе воздуха в регенераторе с кипящим слоем. Углеродистые соединения при этом выгорают, а низшие оксиды хрома окисляются до Сг2
О3
.
Дегидрирование бутилена до дивинила протекает на хром-кальций-фосфатном катализаторе по реакции
С4
Н8
↔С4
Н6
+ Н2
, ΔН= 119 кДж
Бутадиен при повышенных температурах разлагается, поэтому для сохранения достаточно высокой селективности по бутадиену на практике приходится прибегать к снижению парциального давления реакционных газов за счет применения перегретого водяного пара или вакуума.
Оптимальная температура сырья на входе в реактор 860—910 К. Степень конверсии регулируется объемной скоростью, которая колеблется для разных катализаторов в пределах 150—600 ч™1
.
Двухстадийный процесс позволяет создать на каждой стадии оптимальные условия ее протекания, обеспечивающие максимальный выход продуктов и селективность.
Для проведения первой стадии широко используются аппараты кипящего слоя. Такие аппараты отличаются целым рядом преимуществ в сравнении с аппаратами, в которых катализатор неподвижно располагается на нескольких тарелках: 1) изотермичность слоя, которая достигается благодаря активному перемешиванию; 2) текучесть слоя, в результате которой появляется возможность транспортировки закоксованного катализатора из реактора в регенератор и обратно; 3) высокая поверхность межфазного обмена, обусловленная малым размером частиц катализатора, в результате — высокие скорость теплообмена и массопередачи; 4) низкое гидравлическое сопротивление слоя, обеспечивающее уменьшение энергозатрат и повышающее скорость процесса.
Таким образом, в конструкции реактора КС соблюдены все закономерности проведения гетерогенно-каталитических реакций. Процессы дегидрирования и регенерации осуществляются в разных аппаратах одинаковой конструкции.
В отличие от первой, вторая стадия протекает в адиабатических реакторах с неподвижным слоем катализатора. Необходимое для реакции тепло подводится с перегретым паром, смешиваемым с сырьем. Достоинство этих аппаратов — простота конструкции, недостатки — неравномерность распределения температуры в слое, высокое гидравлическое сопротивление аппарата, ухудшение показателей эффективности работы реактора по мере закоксовывания катализатора, периодичность работы аппарата, попеременно работающего то в режиме дегидрирования, то в режиме регенерации.
Стадия осуществляется при более высокой температуре и пониженном парциальном давлении, которое достигается при разбавлении бутенов водяным паром. Температура для разных типов катализатора колеблется от 580 до 677 "С, разбавление паром — в соотношении 20 : 1. Охлаждение контактного газа (закалка) осуществляется впрыскиванием водяного конденсата, дальнейшее охлаждение газа происходит в котле-утилизаторе, затем газ направляется на промывку в скруббер и далее на разделение.
Выход бутадиена от массы исходного бутена составляет 20— 35 %. Селективность колеблется от 73 до 94 %.
Одностадийное дегидрирование н-бутана
Одностадийный процесс дегидрирования н-бутана до бутадиена-1,3 может быть описан суммарным уравнением:
С4
Н10
↔ С4
Н6
+ 2Н2
+ 247 кДж
и складывается из двух последовательных реакций дегидрирования н-бутана до н-бутиленов и н-бутиленов до бутадиена-1,3 . В этом процессе н-бутилены не выводятся из сферы, реакции и в реакторе создается система «н-бутан — н-бутилены — бутадиен-1,3 — водород», равновесный состав которой зависит от температуры и давления.
Одностадийный процесс дегидрирования н-бутана осуществляется по регенеративному принципу, при котором затраты тепла на проведение эндотермической реакции дегидрирования в адиабатическом режиме возмещаются за счет тепла, уделяющегося на стадии регенерации катализатора при выжигании отложившегося на нем кокса. В этом процессе разогретый регенерированный катализатор используется как теплоноситель, а для повышения его способности аккумулировать тепло, к нему добавляется в отношении 1 : 3 инертный теплоноситель в виде гранул оксида алюминия, предварительно обожженных.
Жесткие условия чередующихся окислительно-восстановительных циклов дегидрирования и регенерации предъявляют к катализаторам повышенные требования. В одностадийном процессе используется алюмо-хромовый окисный катализатор ДВ-3М состава Сг2
О3
∙А12
Оз, активный при температуре около 6ОО°С, ускоряющий обе реакции дегидрирования, прочный и устойчивый в эксплуатации и хорошо регенерирующийся. Так как он отравляется парами воды, то понижение парциального давления углеводородного сырья в процессе достигается не введением в систему водяного пара, а проведением дегидрирования в вакууме.
Технологическая схема производства бутадиена-1,3 одностадийным дегидрированием н-бутана в вакууме включает операции:
—очистка сырья (бутановой фракции, попутного газа);
—каталитическое дегидрирование н-бутана;
—сжатие контактного газа и выделение из него фракции С4;
—выделение бутадиена-1,3 из фракции С4;
—отдувка углеводородов и регенерация катализатора.
Реакторный блок установки, включает два (или больше) аппаратов, работающих попеременно на дегидрирование сырья и регенерацию катализатора.
Сырьем для производства бутадиена методом дегидрирования служит бутановая фракция попутного газа или бутан-бутиленовая фракция газов каталитического крекинга или пиролиза.
 Реакция дегидрирования бутана относится к классу сложных последовательных сильно эндотермических реакций, протекающих с увеличением объема: Реакция дегидрирования бутана относится к классу сложных последовательных сильно эндотермических реакций, протекающих с увеличением объема:
Кроме целевой реакции в этой системе протекает большое количество побочных процессов: реакции циклизации, крекинга, изомеризации, ароматизации, коксообразования и др. Вследствие этого в результате дегидрирования образуется сложная смесь углеводородов, разделение которой связано с существенными затратами энергии и вспомогательных материалов.
Процесс дегидрирования осуществляется в присутствии катализатора. Высокие температуры синтеза и повышенная реакционная способность продуктов приводят к его быстрому закоксовыванию. В результате катализатор работает на дегидрирование только 15—20 мин, затем реактор переключается на регенерацию. Регенерация осуществляется с помощью выжигания кокса воздухом и длится 30 мин.
Сравнительная характеристика
Сопоставление технико-экономических данных показывает, что одностадийный процесс экономичнее двухстадийного ввиду отсутствия в нем промежуточной подсистемы разделения контактного газа после первой ступени и меньшей величины расходных коэффициентов по сырью и энергии.
Таблица 1. ТЭП производства бутадиена-1,3
| Методы производства
|
Капитальные затраты
|
Энергоёмкость
|
Себестоимость
|
| Одностадийное дегидрирование
|
47
|
34
|
39
|
| Двухстадийное дегидрирование
|
72
|
77
|
53
|
Достоинствами одностадийного процесса дегидрирования н-бутана до бутадиена-1,3 являются:
—значительное сокращение расхода технологического пара;
—использование теплоты регенерации катализатора и проведение реакции дегидрирования в адиабатическом режиме и, как следствие, простота конструкции реактора и отсутствие сложного теплообменного оборудования;
—исключение второй стадии дегидрирования и операций разделения бутан-бутиленой фракции.
За счет этого относительно невысокие выход бутадиена-1,3 (12—14%) и степень конверсии н-бутана (не превышающая 0,2) компенсируются меньшими капитальными затратами и энергоемкостью производства и, как следствие, более низкой, чем в двухстадийном методе, себестоимостью бутадиена-1,3.
4.2 Определение технологической топологии ХТС
При рассмотрении технологической схемы производства бутадиена-1,3 можно сказать, что между технологическими операторами данной ХТС существует последовательная (связь, когда поток, выходящий из одного элемента является входящим для следующего и все технологические потоки проходят через каждый элемент системы не более одного раза), параллельная (когда выходящий из элемента ХТС поток разбивается на несколько параллельных подпотоков) и обратная (характеризуется наличием рециркуляционного потока, связывающего выход последующего элемента ХТС с входом предыдущего) технологические связи.
4.3 Установление технологических и конструкционных параметров ХТС, технологических параметров режима и потоков
Бутадиен-1,3 (дивинил) C4
H6
представляет собой при обычных условиях бесцветный газ, конденсирующийся в жидкость при 268,7 К (-4,3°С), с температурой кипения -4,4°С, температурой плавления - 108,9°С и плотностью в жидком состоянии 0, 645 т/м3
(при 0°С). Не растворим в воде, плохо растворим в спиртах, хорошо — в бензоле, диэтиловом эфире, хлороформе; с некоторыми растворителями образует азеотропные смеси. Критическая температура бутадиена 152°С. С воздухом бутадиен образует взрывчатые смеси с пределами воспламеняемости 2,0 и 11,5% об. Температура вспышки бутадиена составляет -40°С, температура самовоспламенения 420"С.
Бутадиен легко полимеризуется. Полимеризация инициируется пероксидами, образующимися при контакте бутадиена с воздухом. Тепловой эффект полимеризации зависит температуры и составляет от 72, 8 до 125,6 кДж/моль. Вследствие этого бутадиен хранится в присутствии ингибиторов, например, п-оксидифениламина или п-трет-бутилпирокатехина, которые удаляются промывкой гидроксидом натрия перед полимеризацией. При радикально-цепной сополимеризации бутадиена со стиролом, а-метилстиролом или акрилонитрилом образуются сополимеры, в макромолекуле которых беспорядочно чередуются звенья исходных веществ
-СН2
-СН=СН-СН2
-СН2
-СН- -СН2
—СН -СН2
-СН
СН-СН2
С6
Н5
CN
причем бутадиен связывается в 1,4- или 1,2-положениях.
Бутадиен в высоких концентрациях обладает наркотическим действием; в малых концентрациях раздражает дыхательные пути и слизистую оболочку глаз. ПДК составляет 100 мг/м3
.
4.4 Модель рассматриваемой ХТС
Функциональная схема
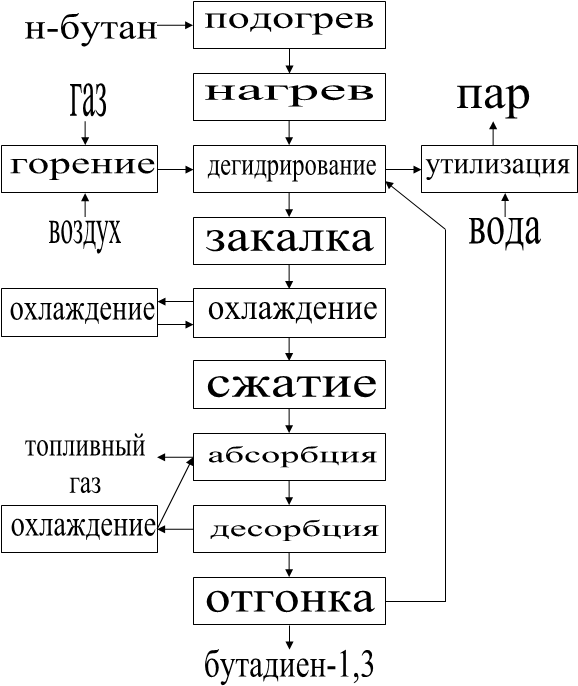
Структурная схема
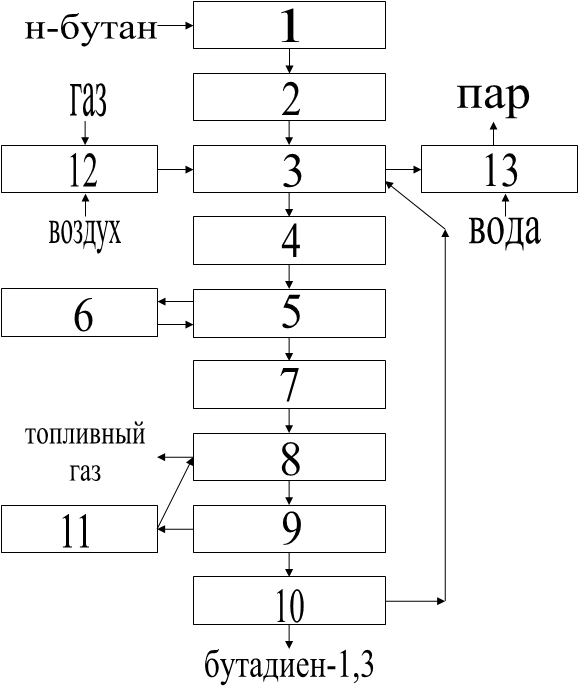
1 – нагреватель сырья;
2 – печь;
3 - реакторы;
4- “закалочный” аппарат;
5- скруббер;
6,11- холодильники;
7- турбокомпрессор;
8- абсорбер;
9- десорбер;
10- стабилизирующая колонна (депропанизатор);
12- топка;
13-.котёл-утилизатор
Операторная схема
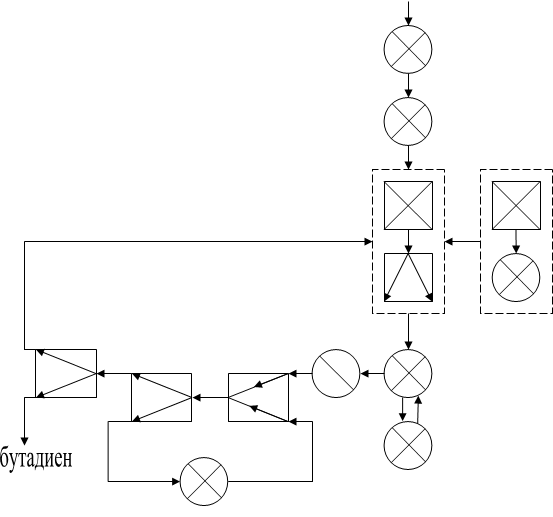
Технологическая схема
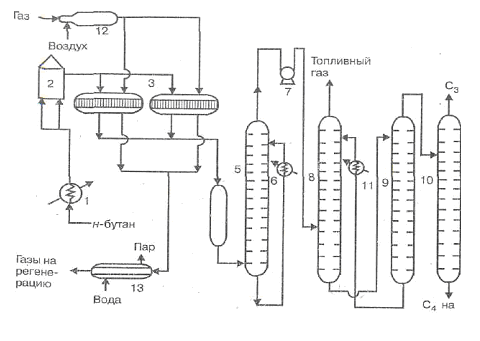
1 – нагреватель сырья;
2 – печь;
3 - реакторы;
4- “закалочный” аппарат;
5- скруббер;
6,11- холодильники;
7- турбокомпрессор;
8- абсорбер;
9- десорбер;
10- стабилизирующая колонна (депропанизатор);
12- топка;
13-.котёл-утилизатор
Описание технологической схемы
Через подогреватель 1 н-бутан поступает в печь 2, где нагревается до 600—620ºС и направляется в один из реакторов 3, который работает на дегидрирование. Из реактора контактный газ, пройдя для «закалки» аппарат 4, подается в скруббер 5, в котором охлаждается холодным маслом, циркулирующим через холодильник 6. Охлажденный в скруббере газ сжимается в турбокомпрессоре 7 до давления 1,3 МПа и направляется в абсорбер 8. Из верхней части абсорбера выходит водородсодержащий топливный газ, а раствор углеводородов в абсорбенте подается в десорбер 9. Ио верхней части десорбера отгоняется фракция С3
— С4
, а абсорбент через холодильник 11 возвращается на орошение абсорбера 8. В качестве абсорбента используется высококипящая углеводородная фракция С5
. Фракция С3 — C4 из верхней части десорбера 9 поступает в колонну 10 (депропанизатор), где из нее отгоняется пропан. Оставшаяся фракция С4 с содержанием бутадиена-1,3 от 11 до 13% массовых направляется на выделение бутадиена, а бутан-бутиленовая фракция возвращается в виде рецикла на дегидрирование, присоединяясь к свежему н-бутану. По окончании цикла дегидрирования поток углеводородного сырья переключается на другой реактор, а первый продувается сначала водяным паром для удаления сорбированных катализатором углеводородов, а затем для регенерации катализа-хора топочными газами с небольшим содержанием кислорода из топки 12. Теплота газообразных продуктов регенерации катализатора используется для выработки технологического пара в
котлеутилизаторе 13.
Основной аппарат технологической схемы — реактор дегидрирования (контактный аппарат). Это стальной цилиндр диаметром 6 м и длиной 12—14 м расположенный горизонтально и футерованный внутри огнеупорным материалом. Внутри реактора расположены решетки из керамических плит, на которых размещены слои катализатора.
5 Анализ ХТС
5.1 Представление изучаемого объекта в виде иерархической структуры ХТС
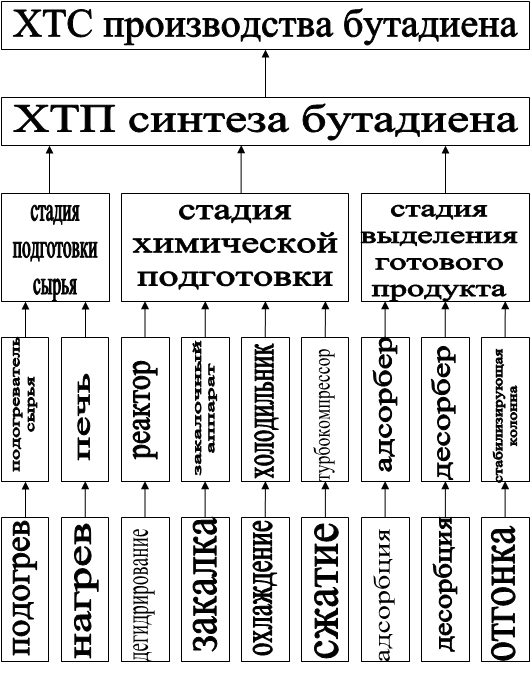
5.3 Изучение свойств и эффективности функционирования ХТС
Какое количество бутана необходимо для получения 2т бутадиена-1,3, если известно, что бутан содержит 15% примесей, а степень превращения составляет 80%?
Решение
Для решения поставленной задачи нам необходимо написать уравнение реакции получения бутадиена-1,3 из бутана.
С4
Н10
→ С4
Н6
+2Н2
m(С4
Н10
)=x т
Mr(С4
Н10
)=58 г/моль
m(С4
Н6
)=2 т
Mr(С4
Н6
)=54 г/моль
Составим пропорцию, чтобы найти массу бутадиена.
х/58=2/54 откуда х = 2,14 т.
Найдём массу бутана с учётом степени превращения (80%)
2,14 т – 80 %
y - 100%
Степень превращения – отношение количества превращённого исходного сырья в целевой продукт к общему количеству исходного сырья.
Составим пропорцию, чтобы найти массу бутадиена с учётом степени превращения.
2,14/y=80/100 откуда y = 2,675 т
Найдём массу бутана с учётом примесей (15%)
2,675 т – 85 %
z - 15%
z – масса примесей
Составим пропорцию, чтобы найти массу примесей.
2,675/z=85/15 откуда z = 0,472 т
Тогда масса бутана с примесями = 2,675+0,472=3,147 т
|