ЧЕРНИГОВСКИЙ АВТОРСКИЙ КОЛЛЕГИУМ
Реферат по учебной дисциплине химия на тему:
“Химическая связь ”
Выполнил: ученик 11-Д класса
Пономарёв Алексей
Чернигов 2002
ХИМИЧЕСКАЯ СВЯЗЬ, общее определение сил и различных типов взаимодействий, обусловливающих существование двух- и многоатомных соединений — молекул, ионов, радикалов, кристаллов. Главные отличитительные черты X. с.: 1) понижение полной энергии многоатомной системы по сравнению с энергией изолированных атомов или атомных фрагментов, из которых она образована; 2) существенное перераспределение электронной плотности в области X. с. по сравнению с простым наложением электронных плотностей несвязанных атомов или атомных фрагментов, сближенных на расстояние связи. Последняя особенность наиболее, точно отделяет X. с. от межмолекулярных взаимодействий, тогда как энергетический критерий является менее определенным.
Природа X. с. полностью определяется электрическим кулоновскими взаимодействием ядер и электронов, однако правильное описание распределения электронного заряда возможно лишь с учетом законов квантовой механики. Точные расчеты зависимостей полной энергии и ее компонент от межъядерного расстояния для простейшей структуры с X. с.— молекулярного иона Н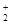 с одноэлектронной связью — показывают, что минимум полной энергии, который достигается при равновесном межъядерном расстоянии, равном 1,06 А,связан с резким понижением потенциальной энергии электрона вследствие концентрации и сжатия облака электронной плотности в межъядерной области. При этом кинетическая энергия электрона возрастает и наполовину компенсирует понижение потенциальной. Результирующий эффект (понижение энергии) превышает энергию расталкивания положительно заряженных ядер и обусловливает образование X. с. с энергией 255 кДж/моль. Такая интерпретация природы X. с., дополненная учетом эффектов межэлектронного отталкивания и электронной корреляции, в целом распространяется на описание связей в двух- и многоэлектронных молекулах. с одноэлектронной связью — показывают, что минимум полной энергии, который достигается при равновесном межъядерном расстоянии, равном 1,06 А,связан с резким понижением потенциальной энергии электрона вследствие концентрации и сжатия облака электронной плотности в межъядерной области. При этом кинетическая энергия электрона возрастает и наполовину компенсирует понижение потенциальной. Результирующий эффект (понижение энергии) превышает энергию расталкивания положительно заряженных ядер и обусловливает образование X. с. с энергией 255 кДж/моль. Такая интерпретация природы X. с., дополненная учетом эффектов межэлектронного отталкивания и электронной корреляции, в целом распространяется на описание связей в двух- и многоэлектронных молекулах.
Полагая движение электронов независимым от намного более медленных ядерных движений (адиабатическое приближение), можно вполне строго описать образование X. с. как результат действия кулоновских сил притяжения положительно заряженных атомных ядер к электронному облаку, сконцентрированному в межъядерном пространстве. Заряд этого облака стремится приблизить ядра друг к другу (связывающая область), тогда как электронный заряд вне межъядерного пространства (несвязывающая область) стремится ядра раздвинуть. В этом же направлении действуют и силы ядерного отталкивания. При сближении атомов на равновесное расстояние часть электронной плотности из несвязывающей области переходит в связывающую (см. рис.). Электронный заряд распределяется в обеих областях так, чтобы силы, стремящиеся сблизить и оттолкнуть ядра, были одинаковыми. Это достигается при некотором равновесном расстоянии, соответствующем длине связи.
Варианты классификации X. с. определяются различнымиее характеристиками или способами описания (в духе классической теории валентности или в рамках квантовохимических представлений; следует подчеркнуть, что между этими подходамине всегда могло 6ыть установлено однозначное соответствие). В теории валентности каждой связи между атомами соответствует одна электронная пара. В зависимости от способаее образования из электронов связываемых атомов можно выделить ковалентную связь и координационную связь. Если электронная пара X. с. полностью принадлежит одному из атомов, то образуется ионная связь. По степени смещения центра тяжести электронного облака связывающих; электронов X. с. делят на неполярные (равноудаленностьот обоих атомных центров) и полярные (промежуточныемежду неполярными и ионными). Ковалентные и координационные связи подразделяются по числу образующих их электронных пар на простые и кратные — двойные, тройные и четвертные.
При рассмотрении X. с., основанном на квантовомеханических расчетах волновых функций многоатомных молекул, ионов, кристаллов, понятие двухцентровой связи, используемое в классической теории валентности, не получает прямого эквивалента, вследствие делокализации электронных орбиталей по нескольким (нередко всем) атомным центрам. Переход к локализованным орбиталям часто сохраняет возможность анализировать X. с. в многоатомных молекулах в рамках традиционных представлений о связях, поделенных и неподеленных электронных парах. Типичные примеры соединений с локализованными двухцентровыми связями — насыщенные углеводороды (связи С—С, С—Н). В том случае, когда процедура локализации не позволяет однозначно выделить в молекуле локализованные двухцентровые орбитали, реализующиеся в ней X. с. относят к мпогоцентровым связям, характерным для ненасыщенных соединений с сопряженными связями. Предельныйслучай делокализации — металлическая связь, обусловленная перемещением валентных электронов металла во всем пространстве кристаллической решетки, образуемой его положительными ионами.
Основные характеристики X. с.— прочность, длина, полярность. Прочность X. с. определяется энергией связи. В двухатомной молекуле она равна теплоте диссоциации молекулы на отдельные атомы. Энергии X. с. в многоатомной молекуле соответствует энергия атомизации — разность между полной энергией молекулы и суммой энергий изолированных атомов и энергии нулевых колебаний молекулы. В расчете на одну связь энергии X. с. составляют от 10—20 кДж/модъ (связи в молекулах и ионах Сd2
, Н , связь С—С1 в радикале СОСl, слабые водородные связи) до > 1000 кДж/моль (тройные связи в молекулах N2
, СО). Для многоатомных молекул с хорошо локализованнымидвухцентровыми связями полная энергия X. с. достаточно точно оценивается как сумма энергий отдельных связей. , связь С—С1 в радикале СОСl, слабые водородные связи) до > 1000 кДж/моль (тройные связи в молекулах N2
, СО). Для многоатомных молекул с хорошо локализованнымидвухцентровыми связями полная энергия X. с. достаточно точно оценивается как сумма энергий отдельных связей.
Длина X. с. меньше суммы ван-дер-ваальсовых радиусов атомов, образующих связь. В зависимости от кратности связей, а также от характера ближайшего окружения она может изменяться в довольно широких пределах, напримердля углерод-углеродных связей — от 1,21 А (тройные связи в алкинах) до 1,7—1,8А (простые связи в напряженных углеводородах).
Полярность связи характеризуется ее дипольным моментом, который для большинства ковалентных связей составляет 0—3D, для координационных связей — обычно 2—7D. Дипольные моменты соединений с ионной связью существенно выше, например для молекулы КВг — 10, 4D (1D = 3,33564*
10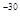 Кл*
м). Кл*
м).
|