Диоксины и безопасность продовольственного сырья и продуктов питания
|
|
Министерство сельского хозяйства Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего пРофессионального образования российский государственный аграрный университет – МСха имени К.А. Тимирязева |
Факультет почвоведения, агрохимии и экологии
Кафедра физической и органической химии
Курсовая работа на тему:
«Диоксины и безопасность продовольственного сырья и продуктов питания»
Выполнила:
магистр
Проверил:
Москва, 2015
СОДЕРЖАНИЕ
|
Стр |
||
|
Введение……………………………………………………………………... |
3 |
|
|
1. |
История развития проблемы диоксинов……………………………… |
4 |
|
2. |
Физико-химические свойства диоксинов………………….................. |
9 |
|
3. |
Источники диоксинов…………………………...................................... |
10 |
|
4. |
Взаимодействие диоксинов с биологическими системами………….. |
12 |
|
5. |
Медицинские аспекты интоксикации диоксинами ………...…..…… |
17 |
|
6. |
Определение диоксинов в объектах окружающей среды и контроль за их содержанием в продукции растениеводства ……….. |
19 |
|
Заключение…………………………………………………………………... |
25 |
|
|
Список литературы………………………………………………………….. |
27 |
Введение
В последние четверть века к обширному перечню экологических бед, угрожающих цивилизации, добавилась еще одна - опасность общепланетарного отравления среды нашего обитания диоксином и родственными соединениями.
Диоксин и многочисленная группа диоксиноподобных веществ - это чужеродные живым организмам вещества (ксенобиотики), поступающие в живую и неживую природу с продукцией или отходами многочисленных технологий. В отличие от множества других ксенобиотиков, например хлорорганических пестицидов, диоксины никогда не являлись целевой продукцией человеческой деятельности, а лишь сопутствовали ей в виде микропримесей. Поэтому негативные воздействия микропримесей диоксинов на живое вещество планеты на фоне действия тысяч и миллионов других техногенных выбросов многие десятилетия оставались незамеченными. Однако именно микропримеси диоксинов, характеризующихся комплексом необычных физико-химических свойств и уникальной биологической активностью, могут стать одним из источников опаснейшего долговременного заражения биосферы. И эта опасность несравненно более серьезна, чем заражение природы многими другими веществами, например хлорорганическими пестицидами.
Диоксин и родственные соединения непрерывно и во все возрастающих масштабах генерируются цивилизацией в последние полвека, выбрасываются в природную среду и накапливаются в ней. Этот процесс не знает ни пределов насыщения, ни национальных границ. В настоящее время ситуация такова, что концентрация диоксинов в гидросфере и литосфере может достичь критических значений и поражение живого вещества может принять необратимый характер.
1. История развития проблемы диоксинов
История "знакомства" человечества с диоксинами восходит к 30-м годам, когда развитие широкомасштабного производства и применения полихлорфенолов привело к появлению массовых профессиональных заболеваний хлоракне (рецидивирующее воспаление сальных желез) [163,164,169,170], хотя само это заболевание известно с 1899 г.
География распространения хлоракне значительно расширилась в 40-50-е годы в связи с созданием во многих странах крупнотоннажных производств 2,4,5-трихлорфенола (ТХФ), а также производств получаемых из него 2,4,5-трихлорфеноксиуксусной кислоты (2,4,5-Т), антибактериального препарата гексахлорфена (ГХФ) и т.д. Описаны многочисленные случаи острого отравления персонала этих производств в процессе эксплуатации, в том числе в результате аварий, первая из которых случилась в США еще в 1949 г. В последующем было показано, что рецидивы хлоракне у многих пораженных проявлялись даже спустя несколько десятилетий после отравления [1].
Источник этих поражений был установлен и описан в 1956-1957 г. одновременно несколькими группами исследователей. Им оказался 2,3,7,8-тетрахлордибензо-n-диоксин (2,3,7,8-ТХДД) (рис.1), образующийся в виде микропримеси при промышленном получении 2,4,5-ТХФ. Поступая с последним в технологические цепи и затем в конечную продукцию (гербициды, антибактериальные препараты и т.д.) и отходы, он приводил, как выяснилось в дальнейшем, не только к заболеваниям хлоракне, но и к другим поражениям, включая острые, подострые и хронические отравления.
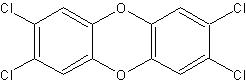
Рис. 1. 2,3,7,8-тетрахлордибензо-n-диоксин (2,3,7,8-ТХДД) [1]
Одновременно с диоксином (рис.1) в качестве хлоракнегенного фактора постулировался и 2,3,7,8-тетрахлордибензофуран (2,3,7,8-ТХДФ) (рис.2). Однако особое внимание к себе этот ксенобиотик привлек как микропримесь к полихлорбифенилам (ПХБ), широко используемым в качестве жидких диэлектриков, теплоносителей, гидравлических жидкостей и т.д. Обусловленные ксенобиотиоком (рис.2) массовые поражения людей (в 1968 г. в Японии и в 1979 г. на Тайване) были связаны с попаданием ПХБ в рисовое масло, что привело к так называемой болезни Юшо - Ю Ченг (острое поражение печени, сопровождающееся многочисленными побочными эффектами).
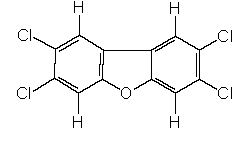
Рис.2. 2,3,7,8-тетрахлордибензофуран (2,3,7,8-ТХДФ) [1]
Было показано также, что 2,3,7,8-ТХДД и 2,3,7,8-ТХДФ, равно как и многие другие представители полихлорированных дибензо-n-диоксинов (ПХДД) и полихлорированных дибензофуранов (ПХДФ), имеют сходные токсикологические характеристики, если атомы хлора занимают четыре латеральных 2,3,7,8-положения. Всего же гомологов и изомеров, составляющих ряды ПХДД и ПХДФ, в принципе должно быть соответственно 75 и 135.
История овладения научным сообществом знаниями о диоксинах как экологической опасности общепланетарного масштаба богата событиями и по-своему драматична. После первых статей о 2,3,7,8-ТХДД, опубликованных в 1956-1957 гг. и содержавших главным образом медицинскую информацию, за отдельными исключениями, на эту проблему легла многолетняя завеса молчания. Объясняют этот феномен обычно соображениями секретности, связанными с такими токсикологическими характеристиками веществ типа 2,3,7,8-ТХДД и 2,3,7,8-ТХДФ, что их стали называть смертельными молекулами, суперядами и т.д. Соответственно, у определенных слоев общества возникал соблазн рассматривать диоксины как прямое средство ведения химической войны. Гербицидная война США во Вьетнаме, невольным участником которой стал высокотоксичный 2,3,7,8-ТХДД, подтверждает небеспочвенность этой мысли.
Однако с конца 60-х годов покров тайны, который окутывал диоксиновую проблему в странах Запада, был в значительной мере сброшен, причем в первую очередь именно в США. Опасность диоксинов, в том числе опасность долговременного заражения диоксинами живой и неживой природы, оказалась объектом внимания исследователей промышленно развитых стран. Еще задолго до окончания войны во Вьетнаме в научной печати появился ряд острых и очень доказательных предостережений о диоксиновой опасности.
Были опубликованы также многочисленные научные данные, касающиеся большинства важнейших аспектов диоксиновой проблемы. Стало известно, например, о содержании ПХДД в обращающихся на сельскохозяйственном рынке гербицидах и хлорфенолах, а также ПХДФ в коммерческих ПХБ. Были опубликованы данные о распределении и бионакоплении диоксина в водных экосистемах, об их подвижности и устойчивости в почве, о фоторазложении диоксинов в природных условиях и вообще об их устойчивости при различных воздействиях, об их образовании при пиролитических процессах. Появились и первые сообщения о взаимоотношении диоксинов с живыми организмами, в том числе с растительными и животными, а также о токсикологии диоксинов и механизме их токсического действия [2].
В начале 70-х годов достоянием научного сообщества стали первые результаты анализа промышленных аварий на хлорфенольных производствах США, Великобритании, Германии, бывшей Чехословакии и Нидерландов с однозначным указанием на их диоксиновую природу. Были опубликованы данные изучения заболеваний людей (хлоракне) и домашних животных в связи с их диоксиновым происхождением, а также об опасных для здоровья людей количествах диоксина, найденных в коммерческом ГХФ, применяемом в фармацевтических целях [2,3].
Наконец появились многочисленные публикации, характеризующие стандартные химические данные об этих веществах - о методах синтеза диоксиновых ксенобиотиков и о методах определения диоксинов в различного рода объектах. Стали известны физико-химические характеристики 2,3,7,8-ТХДД и октахлордибензо-n-диоксина (ОХДД), а также данные дифрактометрии и спектроскопии ЯМР 13С, относящиеся ко многим диоксиновым производным [1].
Следует еще раз подчеркнуть, что все эти данные были опубликованы в 1968-1974 гг., т.е. задолго до окончания войны во Вьетнаме (1975 г.), причем часть материалов была обнародована до окончания химического этапа этой войны, завершившегося в 1971 г. В последующие годы поток сообщений по диоксиновой проблематике приобрел лавинообразный характер. Таким он остается до наших дней.
Первый симпозиум по проблеме "Хлордиоксины - их источники и судьба" был организован в США в рамках 162-й ежегодной конференции Американского химического общества, по существу, одновременно с прекращением гербицидной войны США во Вьетнаме (Вашингтон, сентябрь 1971 г.). Во второй половине 70-х годов стало ясно, что опасность диоксинов как веществ, относящихся к разряду суперэкотоксикантов, приобрела общепланетарные масштабы. Как следствие в эти годы в химической экологии возник совершенно иной - хемосферный - подход к проблеме. Он рассматривает живые организмы главным образом в аспекте их взаимодействия со всей совокупностью непрерывно влияющих на них химичеcких веществ. В рамках этого подхода оформилась и специальная дисциплина - экотоксикология.
В целом, однако, диоксиновая проблема в силу своей сложности и многообразия сложилась как проблема сугубо междисциплинарная, новые грани которой могут возникать с самой неожиданной стороны. Одно из проявлений именно этого аспекта диоксиновой проблемы - обнаружение диоксинов (1977-1978 гг.) в выбросах МСП [4].
Это и ряд других обстоятельств подтолкнули западные страны к организации серьезных исследований на международной основе. В последнее же десятилетие актив международного сообщества ученых пополнился двумя принципиальными достижениями, связанными с многоликостью опасности диоксинов. Одно из них - это обоснование идеи суммирования токсических эффектов различных веществ с помощью единого показателя (так называемого диоксинового эквивалента, ДЭ), за основу которого взят 2,3,7,8-ТХДД. Второе достижение - это разработка и широкое внедрение в аналитическую практику целостной методологии определения микроколичеств диоксиновых соединений на фоне большой макрокомпоненты органических веществ, обращающихся в живой и неживой природе.
Помимо указанных событий, получивших общепланетарную известность, произошло также много других, менее известных широкой публике случаев массовых поражений людей и заражения территорий. Например, в штате Миссури (США) было распылено на компактной территории от 20 до 40 кг 2,3,7,8-ТХДД. Аналогичные события происходили в других районах США, а также в Германии, Нидерландах, Швеции, Финляндии и т.д. В последнее время начали появляться соответствующие данные, относящиеся к России.
Все эти явления раскрыли ужасающие перспективы отдаленных последствий глобального заражения биосферы высокотоксичными диоксинами. И они не могли не оказать психологического давления на человечество. Так возникло повышенное внимание промышленно развитых стран к диоксинам как к источнику возможного экологического бедствия, источнику, принципиально более серьезному и неизмеримо опасному по сравнению с многотоннажными выбросами многих других загрязнителей [5].
2. Физико-химические свойства диоксинов
Диоксины обладают комплексом традиционных для галогенорганических веществ, а также необычных химических свойств. В свою очередь последние определяют поведение диоксинов в объектах живой и неживой природы, а также стратегию борьбы с ними.
Для ПХДД и ПХДФ известны реакции электрофильного замещения - хлорирования, бромирования, нитрования. Первые могут быть использованы для синтеза самих диоксинов, последняя - для получения различного рода производных [1,5].
Реакционная способность альфа- и бета-положений диоксинового скелета различна: замещение идет главным образом в латеральные, а не в апикальные положения. Соответственно 2,3,7,8-ТХДД оказывается в этих реакциях наименее реакционноспособным.
Известны также способность диоксинов к нуклеофильному замещению и гидролизу в сильнощелочных спиртовых растворах при нагревании. Это может серьезно исказить данные анализа. Отметим, что гидролиз - это, по существу, основной путь метаболизма этих веществ в живых организмах.
К числу наиболее важных химических характеристик диоксинов следует отнести их поведение в условиях экстремальных химических воздействий. Как оказалось, они обнаруживают чрезвычайную стабильность в сильнокислых и щелочных растворах, а также высокую устойчивость к окислителям в некаталитических условиях.
Все эти химические свойства определяют высокую стабильность диоксинов в объектах окружающей среды. В частности, в почве период полураспада наиболее токсичного 2,3,7,8-ТХДД превышает 10 лет (доходит до 20), а в воде и донных отложениях он может достигать 2 лет [3,6].
Стабильность диоксинов по отношению к различным физическим воздействиям может существенно различаться.
В истинных растворах хлорорганические ксенобиотики ПХДД и ПХДФ и их броморганические аналоги сравнительно легко дехлорируются при УФ-облучении. Последовательное удаление атомов хлора облегчается наличием протонов в среде. Легче всего поэтому дехлорирование проходит в органических растворителях. Роль в их распаде фотолиза на поверхности, а также биодеградации ничтожна.
Гамма-радиация разрушает 2,3,7,8-ТХДД в органических растворителях. Представления об условиях термического образования и распада диоксинов претерпели значительную эволюцию. Первоначально считалось, что необратимое термическое разложение хлорорганических диоксинов происходит при температурах, несколько превышающих 750oС. В дальнейшем, однако, было показано, что даже при температурах до 1200oС их терморазложение - процесс обратимый. Только выдерживание в течение 4-7 с при 1200oС и выше приводит к необратимой фрагментации диоксинов. В настоящее время считается надежно установленным, что при температурах от 750 до 900оС идет главным образом образование 2,3,7,8-ТХДД, тогда как его эффективное разрушение происходит лишь в температурном диапазоне 1200-1400оС. Эти результаты позволили сформулировать требования к режимам работы МСП).
Термическая устойчивость характерна также для броморганических диоксинов ПБДД и ПБДФ: при 800oС более эффективно их образование, а не разрушение [1].
3. Источники диоксинов
Источники возникновения диоксинов и пути проникновения их в неживую и живую природу весьма разнообразны. Известны попытки объяснить картину появления диоксинов в биосфере только лишь лесными и степными пожарами. Это оказалось, однако, упрощением, хотя сама по себе идея возникновения диоксинов в процессах горения весьма плодотворна. Серьезных доказательств накопления каких-либо существенных количеств этих ксенобиотиков в донных отложениях рек и озер, образовавшихся до 1940 г., т.е. до начала масштабного производства гербицидов на основе феноксиуксусных кислот 2,4,5-Т и 2,4-Д, не найдено. Не обнаружено и серьезных доказательств биогенного образования диоксинов или их предшественников непосредственно в живой природе.
В настоящее время считается строго доказанным, что диоксины имеют исключительно техногенное происхождение, хотя и не являются целью ни одной из существующих технологий. Их появление в окружающей среде обусловлено развитием разнообразных технологий, и в основном связано с производством и использованием хлорорганических соединений и утилизацией их отходов. Во всяком случае ни в тканях эскимосов, замерзших 400 лет назад, ни в тканях чилийских индейцев, мумифицированных 2800 лет назад, диоксины не обнаружены даже в следовых количествах [1,6].
По хозяйственно-территориальным признакам источники диоксинов удобно подразделять на локальные и диффузные (пространственно распределенные), а по темпам накопления в окружающей среде и объектах живой природы - на регулярные и экстремально-залповые.
Диффузные источники диоксинов с точки зрения загрязнения окружающей среды диоксинами представляются особенно опасными.
Это обусловлено двумя причинами - во-первых, изомерно-гомологическим разнообразием поступающих в окружающую среду ксенобиотиков, а во-вторых, чрезвычайной трудностью обнаружения опасности до того, как она себя проявит [1].
Типов пространственно распределенных источников чрезвычайно много. Перечислим некоторые из тех, что принципиально возможны и уже попали в поле зрения специалистов:
- лесные пожары (леса, обработанные хлорфенольными пестицидами);
- хлорирование питьевой воды; - выхлопы автомобилей;
- работа домашних печей, использующих "техногенную" древесину (пропитанную пестицидами и иными галогенорганическими веществами);
- обработка сельскохозяйственных угодий диоксинсодержащими гербицидами или гербицидами, способными превращаться в диоксины непосредственно в живой и неживой природе и т.д.
Что касается источников, способствующих основным поступлениям диоксинов в живую и неживую природу, то можно выделить три основные группы:
1. Функционирование несовершенных, экологически небезопасных технологий производства продукции химической, целлюлозно-бумажной, металлургической и иной промышленности. Для всех них характерны диоксинсодержащие отходы и сточные воды в период регулярной деятельности, а также большие дополнительные выбросы диоксинов в случае аварийной обстановки.
2. Использование химической и иной продукции, содержащей примеси диоксинов (или их предшественников) и/или образующей их в процессе использования или же в случае аварий.
3. Несовершенство и небезопасность технологий уничтожения, захоронения или же утилизации бытового мусора, отходов химических и иных производств.
Подчеркнем, что эта классификация приводится исключительно из соображений удобства обсуждения. Что касается механизмов образования рассматриваемых микропримесей, то предлагаемая классификация столь же уязвима, как и всякая иная. Во всяком случае такой многоликий механизм образования диоксинов, как термические процессы, следует рассматривать при обсуждении всех трех групп источников.
Нельзя, кроме того, забывать и о субъективных моментах. Пути проникновения диоксинов в сферу быта могут зависеть и от подхода к обеспечению экологической безопасности, культивируемого тем или иным государством. Другими словами, в одних странах диоксины могут быть опасны при контакте всего населения с продукцией, а в других, где применяются более интенсивные очистные операции,- лишь при контакте с отходами производства [1,4].
4. Взаимодействие диоксинов с биологическими системами
Взаимодействие диоксинов с живым веществом планеты многообразно. В ряде случаев оно cтоль специфично, что отдельные представители этого класса веществ квалифицируют в качестве суперэкотоксикантов, суперкумулянтов и т.д [1,2].
Многие свойства диоксинов, в первую очередь их токсикологические особенности, связывают с высокой липофильностью и исключительной стабильностью в живых организмах и объектах окружающей среды.
Липофильная природа диоксинов способствует кумуляции их в органической фазе биосферы и биоконцентрированию в живых организмах. В представителях фауны диоксины эффективно накапливаются главным образом в жировых тканях (примерно на 9/10). В больших количествах они накапливаются также в печени, коже, тимусе, кроветворных органах. В жировой ткани и в крови их уровень коррелирует с содержанием липидов.
Биоконцентрирование осуществляется главным образом по пищевым цепям. Оно происходит также путем межфазных переходов из любых сред, в том числе из воздуха, воды и почв (даже в случае их ничтожного содержания в этих средах). Другими словами, большинство ПХДД и ПХДФ легко поглощается живыми организмами и через желудочно-кишечный тракт, и через кожные покровы. Механизм их проникновения в клетки пока не очень ясен [2].
Предполагается, что коэффициент биоконцентрирования (КБК) непосредственно связан с коэффициентом распределения в системе октанол-вода простой зависимостью, например: lg КБК = 0,76 Кow - 0,23.
В организме рыб, в частности, значение КБК изменяется от 2000 до 6000. Это расхождение объясняется существенным влиянием биохимических особенностей аккумулирующих организмов на степень поглощения и удерживающую способность в отношении диоксинов. Кроме того, свойства чистых диоксинов существенно отличаются от свойств их реальных аддуктов с органическими веществами, принимающими участие в биопереносе [2].
Диоксины чрезвычайно стабильны в живых оргaнизмах, следствием чего является их длительное сохранение в биосфере. Токсикокинетические исследования последних лет показали, что они очень медленно выводятся из живых организмов, а из организма человека практически не выводятся. В частности, период полувыведения высокотоксичного диоксина 2,3,7,8-ТХДД из живых организмов составляет (в днях): мышь, хомячок - 15; крыса – 30; морская свинка - от 30 до 94; обезьяна – 455; человек - 2120 (5-7 лет).
Высокохлорированные ПХДД имеют сопоставимое время полувыведения из организма человека - порядка 3-6 лет.
При оральном поступлении диоксина в организм человека более 87% его всасывается в желудочно-кишечный тракт. Накапливается он преимущественно в жировой ткани, коже и печени. Ниже приведены данные по эффективности накопления диоксина в органах, тканях и выделениях человека в сравнении с кровью (даны коэффициенты распределения по результатам работ): жировая ткань – 300; почки – 7; кожа – 30; мышцы – 4; печень – 25; фекалии - 0,6; грудное молоко – 13; желчь - 0,5; стенки кишечника – 10; плацента (кровь плода) - 0,1; моча - 0,00005; органы с интенсивным кровообращением (мозг, селезенка, щитовидная железа) – 10
Токсичность ПХДД и ПХДФ (табл.1) вызывается в основном действием не разрушенных живыми организмами молекулами этих ксенобиотиков. В связи с этим важно понимание путей метаболизма диоксинов, в том числе наиболее токсичных. Эта проблема рассмотрена довольно подробно, что вполне естественно, поскольку именно с этим связаны важнейшие вопросы устойчивости и динамики биологической активности диоксинов во времени. В частности, от направления и скорости метаболизма диоксинов зависят продолжительность их токсического действия и направление изменений при биотрансформации. Характерно, что, как правило, метаболиты наблюдаются в экспериментах in vivo. Для млекопитающих идентифицированы в основном два метаболита ТХДД. Изучение метаболизма серии ПХДД, содержащих в их скелете от одного до четырех атомов хлора, позволило выяснить, что замещаются на гидроксил и один и два атома хлора, причем в латеральном положении. Это означает, что нуклеофильное замещение (гидроксилирование) должно сопровождаться детоксификацией диоксинов. И действительно было показано, что токсичность гидроксилированных метаболитов 2,3,7,8-ТХДД по крайней мере на 2 порядка ниже, чем в самом диоксине. Важно также, что для метаболитов 2,3,7,8-ТХДД не характерна биоаккумуляция, и они после образования комплексов с глюкуроновой кислотой легко выводятся из организма с желчью или мочой [2].
Таблица 1
Острая токсичность некоторых диоксинов [2]
|
Соединение |
LD5, мкг/кг |
|||
|
морская свинка |
обезьяна |
мышь |
крыса |
|
|
III (ПХДД) |
||||
|
2,3-Cl2-ДД |
- |
- |
- |
>1000000 |
|
2,7-Cl2-ДД |
- |
- |
>2000000 |
>1000000 |
|
2,8-Cl2-ДД |
>300000 |
- |
874000 |
>5000000 |
|
1,3,7-Cl3-ДД |
- |
- |
>15000000 |
>5000000 |
|
2,3,7-Cl3-ДД |
29444- |
- |
>3000 |
>1000000 |
|
1,2,3,4-Cl4-ДД |
- |
- |
- |
1000000 |
|
1,3,6,8-Cl4-ДД |
>15000000 |
- |
>2987000 |
>1000000 |
|
2,3,7,8-Cl4-ДД |
0,6-2,0 |
70 |
114-284 |
22-45 |
|
1,2,3,7,8-Cl5-ДД |
3,1 |
- |
337,5 |
- |
|
1,2,4,7,8-Cl5-ДД |
1125 |
- |
>5000 |
- |
|
1,2,3,4,7,8-Cl6-ДД |
72,5 |
- |
825 |
- |
|
1,2,3,7,8,9-Cl6-ДД |
60-100 |
- |
>1440 |
- |
|
1,2,3,6,7,8-Cl6-ДД |
70-100 |
- |
1250 |
- |
|
1,2,3,4,6,7,8-Cl7-ДД |
>600 |
- |
- |
- |
|
Cl8-ДД |
- |
- |
>4000000 |
>1000000 |
|
IV (ПХДФ) |
||||
|
2,8-Cl2-ДФ |
- |
- |
>15000000 |
>15000000 |
|
2,4,8-Cl3-ДФ |
- |
- |
>15000000 |
>5000000 |
|
2,3,7,8-Cl4-ДФ |
5-10 |
1000 |
>6000 |
>1000 |
|
2,3,4,7,8-Cl5-ДФ |
3-10 |
- |
- |
916 |
|
2,3,4,6,7,8-Cl6-ДФ |
120 |
- |
- |
- |
|
V (ПБДД) |
||||
|
2,3,7,8-Br4-ДД |
- |
- |
- |
<1000 |
|
VI (ПБДФ) |
||||
|
2,3,7,8-Br4-ДФ |
<15 |
- |
- |
- |
Реальные процессы, однако, много сложнее. В частности, найдены признаки увеличения иммунодепрессивного действия метаболита.
Среди других особенностей взаимодействия 2,3,7,8-ТХДД и 2,3,7,8-ТХДФ с живыми организмами следует отметить, что скорость и направление метаболизма могут зависеть от биологических особенностей организма [5].
Важно, однако, иметь в виду, что, помимо нуклеофильного замещения, диоксиновые производные могут превращаться в живых организмах и по иным механизмам, например по механизму восстановительного дехлорирования. Так, при введении в организм лабораторных животных ОХДД, многие годы считавшегося совершенно нетоксичным, признаки, характерные для поражения диоксином, были обнаружены, однако не сразу, а лишь через 13 недель. Таким образом, за счет восстановительного дехлорирования Cl5-Cl8-производные диоксина могут преобразовываться в живых организмах в более токсичные изомеры.
Биологическая активность диоксинов обычно выражается концентрацией субстрата, вызывающей 50%-ное повышение активности цитохрома Р-448 от максимально возможного. Разработан ряд других способов оценки токсических свойств диоксинов - по индукции бензпирен-гидроксилазы (7-этоксирезоруфин-О-деэтилазы) в микросомах печени, по потере веса тела (увеличению отношения веса печени и всего тела), по степени атрофии тимуса [2].
По-видимому, первые сообщения об острой токсичности именно диоксина, в частности 2,3,7,8-Hal4-ДД, относятся к 1957 г. Люди, осуществлявшие синтез 2,3,7,8-ТХДД [281] и 2,3,7,8-ТБДД [285], получили поражение и были госпитализированы. Позднее сообщалось и о других случаях острого поражения исследователей от диоксина.
После получения первых данных о высокой острой токсичности некоторых диоксинов и их бромсодержащих аналогов появились многочисленные работы, посвященные систематическому изучению токсикологических особенностей веществ, в том числе их острой, подострой и хронической токсичности [2,3].
Данные об острой токсичности диоксинов получены на животных. Хроническое действие исследовано как на животных, так и на людях, оказавшихся пораженными по тем или иным причинам - при авариях, при прямом контакте с гербицидами на сельскохозяйственных работах или же в период военных действий и т.д [1,2].
5. Медицинские аспекты интоксикации диоксинами
Клинические признаки острого и хронического поражения диоксинами проявляются с задержкой, выражены не явно и не всегда адекватны степени отравления.
Первым признаком и легкого и тяжелого отравления хлорорганическими соединениями часто является заболевание хлоракне - тяжелая форма профессиональных угрей (в случае поражения броморганическими соединениями - бромакне). Помимо поражения кожи, в клинической картине наблюдаются поражения печени, желудочно-кишечного тракта и нервной системы.
Хлоракне характеризуется комедонами в виде черных точек, закупоривающих устья фолликулов, и роговыми кистами до 10 мм в диаметре. Проявляются на 10-14-й день, а часто и много позже. Хлоракне - это признак не только местного, кожного, но и системного поражения организма. Средняя продолжительность наблюдения хлоракне составляет 26 лет [2].
Во всех случаях диоксиновых отравлений обнаруживаются порфирии - нарушение порфиринового обмена. При поздней кожной порфирии кожа становится более ранимой, наблюдаются эритематозные и буллезные высыпания, гиперпигментация кожи, гипертрихоз. При сильном отравлении наблюдается быстрое, прогрессирующее исхудание пораженных, происходит также инволюция тимуса (атрофия вилочковой железы) [2].
Возможно наблюдение при клинико-лабораторном обследовании в крови - панцитопения, а в моче - порфиринурия (ее цвет становится темным, оранжево-красным). Летальные случаи при отравлении ПХДД и ПХДФ пока не известны. Поражения диоксинами зависят от видовых особенностей живого организма. В частности, хлоракне и сходные поражения кожи наблюдались не только у человека, но и у подопытных обезьян. Однако они не наблюдаются практически у всех остальных лабораторных животных. У морских свинок, вида, наиболее чувствительного ктоксическому действию 2,3,7,8-ТХДД, его однократное введение приводит к индукции микросомных ферментов, резкой потере массы, иммунодефициту, снижению количества жира в организме и, наконец, к смерти.
Таблица 2 дает представление о специфичности различных диоксиновых поражений в зависимости от особенностей пораженных теплокровных (данные о человеке, как уже упоминалось, пока ограничены).
В работах многих ученых были обобщены многочисленные клинические проявления, связанные с поражением человека диоксинами.
Степень выраженности и преобладание в клинической картине поражения тех или иных симптомов зависят от многих факторов - дозы диоксина, длительности его воздействия, индивидуальных особенностей организма и т.д.
В одном из последних изданий ВОЗ клинические проявления диоксинового отравления обобщены в следующем виде:
- Кожные проявления: - хлоракне; - гиперкератоз;
- гиперпигментация; - гирсутизм; - эластоз.
- Неврологические эффекты: - половая дисфункция (отсутствие
либидо, импотенция); - головная боль; - невропатия; - расстройство зрения; - изменение вкуса, обоняния, слуха.
- Психиатрические эффекты: - расстройство сна; - депрессия;
- потеря активности; - нехарактерные приступы гнева.
- Системные эффекты: - слабовыраженный фиброз печени.
- повышение активности трансаминаз в сыворотке крови;
- гиперхолестеринемия; - гипертриглицеридемия; - потеря аппетита, потеря массы тела; - нарушения пищеварения (непереносимость алкоголя и жирной пищи, тошнота, рвота, метеоризм, диарея); - боли в мышцах, суставах, слабость в нижних конечностях; - увеличение лимфатических узлов; - нарушения со стороны сердечно-сосудистой системы, мочевого
тракта, дыхательных путей, поджелудочной железы.
Таблица 2
Проявления диоксиновых поражений в зависимости от особенностей теплокровных [2]
|
Эффект |
Организмы |
|||||
|
человек |
обезьяна |
морская свинка |
мышь |
цыпленок |
крыса |
|
|
Хлоракне и аналогичные поражения кожи |
+ |
+ |
- |
- * |
- |
- |
|
Потеря веса |
- |
+ |
+ |
+ |
+ |
+ |
|
Развитие токсичности |
+ |
+ |
- |
+ |
+ |
+ |
|
Поражение печени |
- |
+ |
- |
+ |
+ |
+ |
|
Отек |
- |
+ |
- |
+ |
+ |
+ |
|
Атрофия тимуса |
- |
+ |
+ |
+ |
+ |
+ |
|
* Наблюдается в одном из видов |
В настоящее время предположение об интоксикации какой-либо группы населения именно диоксинами, как правило, уже основывается на множественности признаков интоксикации и эпидемического характера заболевания. Тем не менее основной клинический признак интоксикации - заболевание хлоракне - должен надежно отличаться от других видов акне [2].
6. Определение диоксинов в объектах окружающей среды и контроль за их содержанием в продукции растениеводства
В пищевые продукты диоксины могут попадать при использовании территорий, загрязненными диоксинами, для сельскохозяйственной деятельности (бывшие территории свалок, территории расположенные рядом с ними, рядом с крупными городами, а также объектами металлургической, нефтеперерабатывающей и химической промышленности) [2].
Диоксины также могут попадать в пищевые продукты при использовании диоксин-содержащих сырья (кормов), полученных промышленным способом. Так, в 2011 году, в Германии ряд продуктов животноводства был загрязнен диоксинами вследствие использования в составе кормов жирных кислот (содержали диоксин), образовавшихся в процессе вырабатывания биотоплива.
Для человека основным источником диоксинов (на 98-99%) являются пищевые продукты. Наиболее опасные с точки зрения высокого содержания диоксинов являются мясо, молочные продукты и рыба (речь преимущественно идет о продуктах с высоким содержанием жира). Так, диоксины способны накапливаться в коровьем молоке (с точки зрения химии молоко это эмульсия жира в воде, в жировых каплях и содержатся диоксины), где их содержание в 40-200 раз выше, чем в других тканях животного.
Другими источниками диоксинов могут быть различные корнеплоды (картофель, морковь и др.), так диоксины преимущественно кумулируются в корневых системах растений (в надземных частях около 10%) [2,6].
Допустимая суточная доза диоксинов для человека составляет 10 нг/кг. В основных пищевых продуктах установлен норматив для диоксинов на уровне от 0,75 до 4 нг/кг (в пересчете на жир). В ряде продуктов их содержание не допускается (в пределах обнаружения существующих методов).
Избежать воздействия диоксинами очень сложно, т.к. нет определенных признаков, благодаря которым можно выделить продукцию, явно загрязненную диоксинами. Основным фактором, снижающим риски отравления диоксинами может являться тщательный выбор производителей пищевых продуктов из мест удаленных от бывших и существующих производств хлорсодержащих компонентов: Дзержинск (Нижегородская обл.), Чапаевск (Самарская обл.), Новомосковск (Тульская обл.), Щелково, Серпухов (Московская обл.), Новочебоксарск (Чувашия), Уфа (Башкортостан), а так же крупных производств целлюлозно-бумажной и нефтехимической промышленности. Крупными загрязнителями диоксинами также являются мусорные полигоны и мусоросжигательные заводы [5,6].
Контроль за содержанием диоксинов в пищевых продуктах очень сложен. Это связано с их многочисленностью и малым содержанием в пищевых продуктах. В РФ есть всего несколько центров, которые проводят подобное исследование.
При всем разнообразии методов определения диоксинов ПХДД и ПХДФ они включают ряд обязательных этапов: отбор и подготовку пробы, выделение искомых веществ из любой пробы, их очистку и концентрирование и, наконец, собственно качественное и количественное определение.
Анализ образца может включать несколько подходов. Один из них - это определение в очищенном экстракте отдельных групп диоксиновых веществ ПХДД и ПХДФ, например, всех 17 соединений, содержащих фрагмент 2,3,7,8-Cl4, всех изомеров ТХДД или ТХДФ, всех изомеров ПнХДД, ГкХДД и т.д. Другой подход - это раздельное определение каждого компонента смеси, в первую очередь наиболее токсичных. Это достигается последовательным использованием методов хроматографии и количественной масс-спектрометрии, в том числе высокого разрешения. Иногда их прямо комбинируют, например, путем подсоединения колонки хроматографа непосредственно к ионному источнику масс-спектрометра.
К настоящему времени благодаря широкому международному сотрудничеству создано много методик определения следовых количеств ПХДД и ПХДФ, в том числе и наиболее токсичных. Они предполагают применение высокоэффективной очистки диоксинов от многочисленных фоновых веществ и включают экстракционное извлечение, хроматографическое разделение и масс-спектрометрическое определение. Этот прогресс обеспечен как улучшением аналитических возможностей инструментальной техники, так и развитием и стандартизацией методов пробоотбора и пробоподготовки.
Сформировалось два подхода к определению диоксинов:
- одновременное определение всех гомологов и изомеров в одной фракции путем обогащения по измеряемым компонентам (отделение от матрицы);
- определение отдельных изомеров, в особенности наиболее тосичных 2,3,7,8-ТХДД и 2,3,7,8-ТХДФ [2].
Оба подхода находят применение для общего ориентирования в экологической обстановке, хотя первый более пригоден для программ мониторинга. Если же поставленная цель - оценка диоксиновои опасности объектов и регионов, то аналитические приемы должны быть токсикологически ориентированными (т.е. нацеленными на определение 17 наиболее токсичных изомеров ПХДД и ПХДФ из 210) и экспрессными (тут могут оказаться эффективными биологические методы определения.
Знание физико-химических, структурных и токсикологических особенностей диоксинов, в первую очередь ПХДД и ПХДФ, позволило сформулировать требования, которым должна удовлетворять любая методика их определения в объектах окружающей среды и в биологических образцах. Она должна обеспечивать: 1. высокую чувствительность; 2. высокую селективность; 3. высокую избирательность; 4. высокую воспроизводимость результатов [6].
Первое, второе и четвертое требования вполне удовлетворительно обеспечиваются с помощью масс-спектрометрии высокого разрешения. Дифференциация отдельных изомеров в смесях достигается с помощью высокого разрешения.
Работа по анализу диоксинов сопряжена с большими трудностями - методическими и техническими. Даже в рамках уже устоявшейся системы, т.е., по существу, на потоке, эти анализы чрезвычайно дороги, трудоемки и продолжительны (как правило, они занимают много дней). Для получения надежных результатов необходимо, чтобы поддерживалась высокая чистота лабораторных помещений, по крайней мере на уровне, требуемом при проведении работ по генной инженерии[5].
Сложность рассматриваемых анализов состоит в том, что для обеспечения их успешного проведения потребовалось создание специальной химической инфраструктуры. Необходимо, в частности, применение специальных высокочистых органических растворителей, неорганических кислот, адсорбентов и других химически чистых реактивов и материалов.
Наиболее трудный этап работы - отбор и подготовка проб, вследствие чего подавляющее число диоксиновых анализов проводится в настоящее время в лабораторных условиях. С другой стороны, важными представляются аналитические работы в реальном масштабе времени. В связи с этим ведутся работы по созданию аналитической техники, приспособленной к измерениям непосредственно в полевых условиях. В Германии, например, создан передвижной масс-спектрометр, способный определять непосредственно в полевых условиях диоксины в субнанограммовых количествах, а также некоторые другие высокотоксичные вещества [5].
Развиваются новые подходы к анализу диоксинов. Они связаны как с трудоемкостью определения диоксинов в рамках традиционных методов, так и с необходимостью получения экспресс-информации о конкретной эпидемиологической ситуации.
Сделаны попытки разработать биологические, в частности иммунные методы определения и оперативного тестирования образцов. Для биотестирования предложено использовать несколько биологических субстратов, способных к специфической чувствительной реакций на высокотоксичный ТХДД и родственные диоксины (эмбрионы птиц, некоторые клетки крыс и овец и т.д.). Для биотестирования может быть использовано также избирательное поглощение ПХДД и ПХДФ из окружающей среды некоторыми представителями флоры (листвой и еловым иглами) и фауны. Для определения ПХДД в рыбе разработан радиоиммунный метод.
В частности, в случае, если в качестве биоиндикатора загрязненности атмосферного воздуха ПХДД и ПХДФ используют хвою, отбирают лишь однолетние иглы и сохраняют их в алюминиевой фольге при 20°С. С помощью хвои удалось установить наличие диоксинов в некоторых местностях Германии.
Особенно перспективным представляется использование для иммуно-определения диоксинов моноклональных антител, обеспечивающих по сравнению с поликлональными антителами, устойчивую специфичность и возможность значительного снижения предела обнаружения. Авторами выделен набор антител, обеспечивающих специфическую реакцию с высокотоксичными тетра- и пентахлорированными диоксинами рядов ПХДД и ПХДФ с латеральным 2,3,7,8-расположением: атомов хлора. С обычными веществами матрицы (фенолами, гербицидами, в том числе 2,4,5-Т, ПХБ и т.д.) эти антитела не реагируют. Определение диоксинов в матрицах различных типов (летучей золе, моторных маслах, кубовых остатках и т.д.) привело к удовлетворительным результатам (подтверждено корреляцией между данными иммуноопределения и нормальными данными ГХ-МС). Метод позволяет детектировать 0,5 нг диоксина ТХДД с перспективой снижения предела обнаружения до пикограммного уровня.
По-видимому, это направление анализа, несмотря на ряд ограничений, может обеспечить резкое снижение денежных и временных затрат на определение образцов различных типов и заложить основу для мониторинга ТХДД в реальном масштабе времени [2,5].
Заключение
Проблема защиты окружающей среды от опасностей, тесно связанных с антропогенной деятельностью, приобрела исключительную значимость по мере ускорения темпов технического прогресса. Стало очевидным, что в результате преобразующей деятельности человека возникли новые противоречия между его биологическими особенностями и созданными им факторами среды. В настоящее время они уже соизмеримы с действиями природных факторов, что приводит к качественному изменению соотношения сил между обществом и природой.
Человек стал главной силой, изменяющей процессы в биосфере. Образованный таким способом новый вид обмена имеет уже техногенный характер, являясь, по существу, антропогенным обменом веществ.
На современном этапе осознание проблемы охраны и оздоровления окружающей среды способствовало разработке методологических основ медико-экологического мониторинга токсикантов на уровне локальных территорий, обеспечивающих возможность выявления фактического загрязнения, проведения оценки реальной опасности и управления ситуацией.
Глобальный план на 21 век принят ООН в 1992 году. Он предусматривает сильнейшее совершенствование природоохранных мер, направленное на поддержание и усиление эколгической безопасности. В нем были одобрены и предложены следующие рекомендации:
Для улучшения аналитической методологии необходимо:
- проведение межлабораторных и "круговых" (round-robin) исследований с использованием стандартизованных гарантий качества и процедур контроля качества. Следует оптимизировать и стандартизовать стратегию отбора проб, методики анализа и интерпретации данных до проведения исследований.
- Необходимо дальнейшее накопление данных по мониторингу, включая динамику во времени, идентификацию состава изомеров, содержания ПХДД и ПХДФ в объектах окружающей среды, особенно в пищевых продуктах, атмосферном воздухе и донных отложениях.
- Необходимо получить данные о влиянии ПХДД и ПХДФ на биосоставляющую окружающей среды.
- Требуется больше информации о биодоступности ПХДД и ПХДФ из различных носителей в окружающей среде и из продуктов питания; воздействие из этих источников следует соотносить с практикой ведения сельского хозяйства и промышленными процессами.
- Следует разработать и обосновать более простые и менее дорогостоящие методы скрининга.
- Должны быть исследованы механизмы токсичности ПХДД и ПХДФ, чтобы объяснить межвидовые различия в чувствительности и осуществить экстраполяцию данных, полученных в эксперименте, на человека.
- Важны дополнительные исследования иммунотоксичности, включая цитотоксическую функцию Т-лимфоцитов. Особую важность представляют исследования последствий перинатального воздействия и продолжительности воздействия на иммунную систему.
- Следует провести исследования отдаленных последствий, включая исследования репродуктивной функции на нескольких поколениях у различных видов, с тремя наиболее распространенными ПХДД и ПХДФ, а именно 2,3,4,7,8-пентаХДФ, 1,2,3,7,8-пентаХДД и октаХДД.
- Поскольку население подвергается воздействию сложных смесей ПХДД и ПХДФ, то для оценки токсического действия этих соединений и других смесей следует разработать и обосновать тест-системы, включая методики, пригодные для оценки тканей человека.
Список литературы
- Александров В.Д., Емельянов В.И. Отравляющие вещества. М.: Воениздат, 1990.
- Косарев В.В., Жестков А.В., ЛотковВ.С. Влияние диоксинов на иммунную систему человека // Экология человека, 1999.-№2.-С. 30-32
- Новиков Ю.В., Минин Г.Д.,Сайфутдинов М.М. Проблема диоксинов в окружающей среде // Токсикологическийвестник, 1994. -№1.-С. 2-6.
- Толстиков Г.А., Шаванов С.С. // Успехи химии. 1991. .60, N 3. .620-626.
- Giffi F., Reginato R., Benfenati E., Fanelli R. // Chemosphere. 1982. Vol.11, P.577-583.
- Stehr-Green P.A., Naylor P.H., Hoffman R.E. // J. Toxicol. Environ. Health. 1989. Vol.28. P.285-295.
