Содержание токсичных элементов (Pb, Cd, Hg, As) в речной рыбе Приамурья
СОДЕРЖАНИЕ
|
ВВЕДЕНИЕ.....................................................................................................................
|
3
|
|
ГЛАВА I. ТЯЖЕЛЫЕ МЕТАЛЛЫ И ИХ СВОЙСТВА.............................................
|
5
|
|
1.1. Биогеохимические свойства тяжелых металлов..................................................
|
6
|
|
1.2. Биологическая роль металлов................................................................................
|
7
|
|
ГЛАВА II. РАЙОН РАБОТ. МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ....
|
23
|
|
2.1. Климатические и природные особенности ЕАО.................................................
|
23
|
|
2.2. Гидрологическая сеть и источники загрязнения вод ЕАО.................................
|
23
|
|
2.3. Отбор проб...............................................................................................................
|
25
|
|
2.4. Методика определения содержания тяжелых металлов в рыбе.........................
|
31
|
|
ГЛАВА III. СОДЕРЖАНИЕ ТОКСИЧНЫХ ЭЛЕМЕНТОВ В РЫБЕ ПОВЕРХНОСТНЫХ ВОДОТОКОВ БИРОБИДЖАНСКОГО РАЙОНА ЕАО.......
|
39
|
|
ВЫВОДЫ........................................................................................................................
|
48
|
|
СПИСОК ЛИТЕРАТУРЫ.............................................................................................
|
50
|
ВВЕДЕНИЕ
В течение последнего столетия в результате технического прогресса баланс тяжелых металлов в окружающей среде был нарушен и произошло глобальное загрязнение природы тяжелыми металлами. Наиболее распространены ртуть, свинец, кадмий, мышьяк, медь и другие. В результате, попадая в водоемы со сточными водами промышленных предприятий, они взаимодействуют с растительным и животным миром водоемов. Вследствие таких взаимодействий тяжелые металлы могут накапливаться в водных организмах, приводя к гибели или нарушениям жизнедеятельности, и передаваться по трофическим цепям, в том числе к человеку, приводя к различным заболеваниям.
На территории Еврейской автономной области было выявлено и разведано более 20 видов полезных ископаемых, в том числе крупные месторождения железа, марганца, олова, золота, графита, брусита, магнезитов, цеолитов, имеются целебные минеральные источники. По насыщенности месторождений и рудопроявлений, концентрации полезных ископаемых область является одной из богатейших территорий России (Миркин, Наумова, 1995). Однако потенциал её природных ресурсов до конца не изучен и не разведан. К тому же подавляющая часть продукции минерально-сырьевого комплекса вывозится и перерабатывается металлургическими предприятиями крайне мало. Таким образом, загрязнение водных объектов Еврейской автономной области тяжелыми металлами обусловлено преимущественно природными особенностями территории.
По результатам наблюдений ГУ «Хабаровский центр по гидрометеорологии и мониторингу окружающей среды с функциями регионального специализированного центра всемирной службы погоды» установлено, что реки Еврейской автономной области относятся к 4-му «а» (грязные) и 3-му (очень загрязненные) классам опасности. Основными веществами, загрязняющими эти реки, являются соединения железа и свинца. Появление металлов в водных объектах, в основном, обусловлено физико-географическими условиями области.
В связи с этим цель исследования – определить содержание токсичных элементов (Pb, Cd, Hg, As) в речной рыбе Приамурья.
Для достижения поставленной цели необходимо было решить следующие задачи:
- Изучить и проанализировать литературные источники по теме «Содержание токсичных элементов в рыбе поверхностных водотоков ЕАО».
- Установить уровни содержания свинца, кадмия, ртути и мышьяка в речной рыбе и сравнить с санитарно-гигиеническими нормативами.
- Проследить динамику содержания тяжелых металлов в речной рыбе, обитающей в поверхностных водотоках ЕАО за 2010-2015 гг.
- Выявить пищевую пригодность рыбы, из поверхностных водотоков Биробиджанского района ЕАО, к употреблению в пищу.
В работе применялись следующие методы исследования: описательный, аналитический, атомно-абсорбционный. Работа выполнена в рамках санитарно-эпидемиологического надзора, осуществляемого ФБУЗ «Центр гигиены и эпидемиологии в ЕАО» на территории области.
ГЛАВА I. ТЯЖЕЛЫЕ МЕТАЛЛЫ И ИХ СВОЙСТВА
Тяжёлые металлы - это элементы периодической системы химических элементов Д. И. Менделеева, с молекулярной массой свыше 50 атомных единиц. Известно около сорока различных определений термина тяжелые металлы, и невозможно указать на одно из них, как наиболее принятое. Соответственно, список тяжелых металлов согласно разным определениям будет включать разные элементы. Используемым критерием может быть атомный вес свыше 50, и тогда в список попадают все металлы, начиная с ванадия, независимо от плотности. Другим часто используемым критерием является плотность, примерно равная или большая плотности железа (8 г/см3), тогда в список попадают такие элементы как свинец, ртуть, медь, кадмий, кобальт, а, например, более легкое олово выпадает из списка. Существуют классификации, основанные и на других значениях пороговой плотности или атомного веса. Некоторые классификации делают исключения для благородных и редких металлов, не относя их к тяжелым, некоторые исключают не цветные металлы (железо, марганец) (электронный ресурс http://www.o8ode.ru/article/ planetwa/mere/heavy.htm).
Термин тяжелые металлы чаще всего рассматривается не с химической, а с медицинской и природоохранной точек зрения и, таким, образом, при включении в эту категорию учитываются не только химические и физические свойства элемента, но и его биологическая активность и токсичность, а также объем использования в хозяйственной деятельности (Ягодина, 1989; Даффус, 2002).
В результате, чего в последнее время термины «тяжелые металлы» и «токсичные металлы» стали синонимами.
Таким образом, к тяжелым металлам относят более 40 химических элементов с относительной плотностью более 6. Число же опасных загрязнителей, если учитывать токсичность, стойкость и способность накапливаться во внешней среде, а также масштабы распространения указанных металлов, значительно меньше (Ильин, 2001).
Прежде всего представляют интерес те металлы, которые наиболее широко и в значительных объемах используются в производственной деятельности и в результате накопления во внешней среде представляют серьезную опасность с точки зрения их биологической активности и токсических свойств. К ним относят свинец, ртуть, кадмий, цинк, висмут, кобальт, никель, медь, олово, сурьму, ванадий, марганец, хром, молибден и мышьяк (электронный ресурс http://www.o8ode.ru/article/planetwa/mere/heavy.htm).
1.1. Биогеохимические свойства тяжелых металлов
Формы нахождения тяжелых металлов в окружающей среде:
- В атмосферном воздухе тяжелые металлы присутствуют в форме органических и неорганических соединений в виде пыли и аэрозолей, а также в газообразной элементной форме (ртуть). При этом аэрозоли свинца, кадмия, меди и цинка состоят преимущественно их субмикронных частиц диаметром 0,5-1 мкм, а аэрозоли никеля и кобальта - из крупнодисперсных частиц (более 1 мкм), которые образуются в основном при сжигании дизельного топлива.
- В водных средах металлы присутствуют в трех формах: взвешенные частицы, коллоидные частицы и растворенные соединения. Последние представлены свободными ионами и растворимыми комплексными соединениями с органическими (гуминовые и фульвокислоты) и неорганическими (галогениды, сульфаты, фосфаты, карбонаты) лигандами. Большое влияние на содержание этих элементов в воде оказывает гидролиз, во многом определяющий форму нахождения элемента в водных средах. Значительная часть тяжелых металлов переносится поверхностными водами во взвешенном состоянии.
Сорбция тяжелых металлов донными отложениями зависит от особенностей состава последних и содержания органических веществ. В конечном итоге тяжелые металлы в водных экосистемах концентрируются в донных отложениях и биоте.
- В почвах тяжелые металлы содержатся в водорастворимой, ионообменной и непрочно адсорбированной формах. Водорастворимые формы, как правило, представлены хлоридами, нитратами, сульфатами и органическим комплексными соединениями. Кроме того, ионы тяжелых металлов могут быть связаны с минералами как часть кристаллической решетки (Майстренко, Хамитов, 1996).
В табл. 1.1 представлены биогеохимические свойства некоторых металлов.
Таблица 1.1
Биогеохимические свойства тяжелых металлов
|
Свойство
|
Тяжелые металлы
|
|
|
Cd
|
Co
|
Cu
|
Hg
|
Ni
|
Pb
|
Zn
|
|
Биохимическая активность
|
В
|
В
|
В
|
В
|
В
|
В
|
В
|
|
Токсичность
|
В
|
У
|
У
|
В
|
У
|
В
|
У
|
|
Канцерогенность
|
-
|
B
|
-
|
-
|
B
|
-
|
-
|
|
Обогащение аэрозолей
|
B
|
H
|
B
|
B
|
H
|
B
|
B
|
|
Минеральная форма распространения
|
B
|
B
|
H
|
B
|
H
|
B
|
H
|
|
Органическая форма распространения
|
B
|
B
|
B
|
B
|
B
|
B
|
B
|
|
Подвижность
|
B
|
H
|
У
|
В
|
Н
|
В
|
У
|
|
Тенденция к биоконцентрированию
|
В
|
В
|
У
|
В
|
В
|
В
|
У
|
|
Эффективность накопления
|
В
|
У
|
В
|
В
|
У
|
В
|
В
|
|
Комплексообразующая способность
|
У
|
Н
|
В
|
У
|
Н
|
Н
|
В
|
|
Склонность к гидролизу
|
У
|
Н
|
В
|
У
|
У
|
У
|
В
|
|
Растворимость соединений
|
В
|
Н
|
В
|
В
|
Н
|
В
|
В
|
|
Время жизни
|
В
|
В
|
В
|
Н
|
В
|
Н
|
В
|
В данной таблице были оценены биогеохимические свойства тяжелых металлов по трем параметрам: В - высокая, У - умеренная, Н - низкая.
Все тяжелые металлы имеют разные биогеохимические свойства такие, как токсичность, канцерогенность, растворимость и другие свойства, которые в них выражены по-разному. Среди всех критериев выделяются два биохимическая активность и органическая форма распространения, именно они определяют опасность для организма человека и животных в зависимости от концентрации.
1.2. Биологическая роль металлов
В последние годы все сильнее подтверждается важная биологическая роль большинства металлов. Многочисленными исследованиями установлено, что влияние металлов весьма разнообразно и зависит от содержания в окружающей среде и степени нуждаемости в них микроорганизмов, растений, животных и человека (Уильямс, 1975).
Фитотоксичное действие тяжелых металлов проявляется, как правило, при высоком уровне техногенного загрязнения ими почв и во многом зависит от свойств и особенностей поведения конкретного металла. Однако в природе ионы металлов редко встречаются изолированно друг от друга. Поэтому разнообразные комбинативные сочетания и концентрации разных металлов в среде приводят к изменениям свойств отдельных элементов в результате их синергического или антагонистического воздействия на живые организмы. Например, смесь цинка и меди в пять раз токсичнее, чем арифметически полученная сумма их токсичности, что обусловлено синергизмом при совместном влиянии этих элементов. Подобным образом действует и смесь цинка с никелем. Цинк, который является типичным элементом для морских сред, при добавлении кадмия в водоем увеличивает темп роста диатомовых водорослей, особенно при низкой концентрации CO2 в воде. Очевидны проявления синергизма и антагонизма металлов и в их многокомпонентых смесях. Поэтому суммарный токсикологический эффект от загрязнения среды тяжелыми металлами зависит не только от набора и уровня содержания конкретных элементов, но и особенностей их взаимного воздействия на биоту (Лэне, Морель, 1999; Зайцева, 1999).
Таким образом, влияние тяжелых металлов на живые организмы весьма разнообразно. Это обусловлено, во-первых, химическими особенностями металлов, во-вторых, отношением к ним организмов и, в-третьих, условиями окружающей среды (Кеннет, Фальчук, 1993; Ершов, Попов, 1994).
ГЛАВА II. РАЙОН РАБОТ. МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
2.1. Климатические и природные особенности ЕАО
Климат и природа Еврейской автономной области относится к одним из благоприятных условий Дальнего Востока России. Её территория представлена двумя типами рельефа – горным и равнинным. Горные области – южная часть обширной Хингано-Буреинской горной системы, занимающая примерно половину всей площади. Равнинная часть, простирающаяся на юге и востоке, представляет западную окраину Средне-Амурской низменности. Климат – умеренный муссонный; средняя температура января – от -21 % до -26 %, средняя температура июля - от +18 % до +21 %; количество осадков – около 500-800 мм в год. На территории области распространены бурые лесные, лугово-болотные и аллювиальные почвы. Растительность: хвойные (ель, пихта, кедр) и смешанные (лиственница, дуб, береза) леса.
С юго-запада, юга и юго-востока на протяжении 584 км территория области омывается водами одной из величайших рек Евразии – Амура. Ширина русла у западных границ области – 1,5 км, у восточных – 2,5 км.
К бассейну Амура принадлежит ряд крупных (длиной более 10 км) и 1146 малых (длиной менее 10 км) рек. Это Бира, Биджан, Биракан, Ин, Урми, Икура и другие. Общая протяжённость речной сети составляет 8231 км. Верховья рек Бира и Биджан служат нерестилищем для дальневосточной кеты. Благодаря малой антропогенной нагрузке (кроме Амура) в водоемах области обитает более 73 видов рыб, в том числе белый и черный амур, верхогляд, желтощек, калуга, кета, ленок, амурский лещ, осетр, сазан, налим, таймень, толстолоб, хариус, щука, и другие. Для воспроизводства дальневосточного стада лососёвых рыб в области действует два рыборазводных завода мощностью закладки 64,5 млн икринок в год (Медведев, 1998).
Такие обширные и богатые растительным и животным миром территории создают хорошие условия для промыслового вида деятельности такого, как рыболовство и охота.
2.2. Гидрологическая сеть и источники загрязнения вод ЕАО
На территории Еврейской автономной области формируют полностью или частично сток более пяти тысяч водотоков. Гидрографическая сеть хорошо развита. В горных и предгорных районах густота речной сети достигает 0,7 – 0,8 км/км2, на остальной территории – 0,12 – 0,13 км/км2, в среднем по области – 0,5 км/км2. Более 55 % водотоков формируется на территории Облученского муниципального района.
Основное питание рек территории – дождевое, на его долю приходится до 50 – 70 % общего годового стока, на снеговое питание приходится 10 – 20 %, на подземное – 10 – 30 % стока.
Речной сток области в средний по водности год составляет 236,4 км3, из них 221 км3 приходится на реку Амур и 15,4 км3 – на реки Бира, Биджан и Тунгуска. Характеристики важнейших по водохозяйственному значению рек области приведены в табл. 2.1.
Таблица 2.1
Перечень основных водотоков ЕАО
|
Наименования рек
|
Площадь бассейна, км2
|
Длина водотока, км
|
|
Большая Бира
|
9580
|
261
|
|
Сутара
|
1750
|
123
|
|
Кульдур
|
1110
|
64
|
|
Икура
|
409
|
120
|
|
Хинган
|
1230
|
59
|
|
Самара
|
1550
|
105
|
|
Добрая
|
1770
|
58
|
|
Амур
|
864000
|
2824
|
|
Вертопрашиха
|
281
|
42
|
|
Малая Бира
|
1810
|
150
|
|
Тунгуска
|
30200
|
86
|
|
Урми
|
15000
|
458
|
|
Ин
|
2640
|
258
|
|
Аур
|
359
|
74
|
|
Биджан
|
7940
|
274
|
Наиболее распространённые химические загрязняющие вещества поверхностных вод: легко окисляемые органические вещества (БПК5), азот аммонийный, железо общее, марганец, медь.
Появление нефтепродуктов обусловлено поступлением сточных вод с промышленных предприятий, селитебных территорий вместе с неочищенными ливневыми стоками, стоками с дорог.
Присутствие фенолов в водных объектах носит как природный, так и антропогенный характер.
Водородный показатель (рН) на водотоках и водоемах Еврейской автономной области варьируется в пределах от 4,65 до 9,3 (реакция от нейтральной до щелочной).
Кислородный режим водотоков в целом по области удовлетворительный.
2.3. Отбор проб
Пробы отбирались в Биробиджанском районе ЕАО на реках Урми и Ин в 2010 – 2012 гг , река Бира в районе поселка Тукалевский и река Малая Бира с. Надежденское 2014- 2015 гг..
Урми – река, большая часть которой находится в Хабаровском крае, но часть её заходит на границу Еврейской автономной области, правая составляющая р. Тунгуска (приток Амура). Длина – 458 км, площадь бассейна – 15 тыс. км. В бассейне Урми около 1040 озер общей площадью свыше 32 км. Она берёт начало на южном склоне Баджальского хребта, течёт вдоль Бурсинского хребта, низовья – на Нижнеамурской низменности. Сливаясь с рекой Кур, дает начало левому притоку Амура реке Тунгуске, для которой является правой составляющей. Питание преимущественно дождевое. Средний расход воды в 204 км от устья 170 м3/сек. Замерзает в ноябре, вскрывается в конце апреля – начале мая. Сплавная (260 км). Есть катерное судоходство. В верховьях Урми расположено крупнейшее в России оловорудное месторождение (Медведев, 1998).
Река Ин находится в Еврейской автономной области и является одним из притоков р. Большой Ин. Длина – 53 км, водосборная площадь – 213 км2. Глинянка, Баста, Большой и Малый Сореннак образуют основную водную подпитку реки. Ин располагается на болотистой равнине и имеет большое количество озер и стариц. Он имеет спокойное течение и только в сезоны дождей сильно разливается и становится более быстрым. В результате чего популяции рыб в озерах постоянно обновляются и пополняются. Для Ина характерны те же виды рыб, что и для Большой Биры, только здесь видов еще больше. По рыбным запасам близки к Большой Бире и такие большие реки Дальнего Востока, как Хор, Иман и Бикин.
Бира — река в Еврейской Автономной Области России, левый приток Амура. Протекает на территории Еврейской Автономной Области. Длина реки — 424 км, площадь бассейна — 9580 км. Образуется слиянием рек Сутар и Кульдур, стекающих с Сутарского хребта и хребта Малый Хинган. Течёт в основном по низменной равнине. Питание преимущественно дождевое; летом дожди вызывают резкие колебания уровня реки. На реке Бира расположен город Биробиджан, название которого обязано реке своим первым компонентом. Из подрусловых вод Биры осуществляется водозабор для производственных и бытовых нужд города.
На содержание тяжелых металлов анализировалась речная рыба, выловленная в период осень 2010-2012, декабрь 2014 и апрель 2015 года Отбор проб проводился в соответствии с ГОСТ 26929–94 «Сырье и продукты пищевые. Подготовка проб. Минерализация для определения содержания токсичных элементов».
Для проведения анализа вылов рыбы осуществлялся в пяти местах:
- Среднее течение р. Урми
- Низовье р. Урми
- Верховье р. Ин
- Устье р. Ин
- р. Бира р-он поселка Тукалевский,
- р. Малая Бира с. Надежденское
В результате были выловлены:
Серебряный карась (ранее лат. Carassius auratus gibelio (Bloch, 1782), с 2003 года принято биноминальное название лат. Carassius gibelio) – пресноводная рыба из рода карасей семейства карповых отличается от золотого более крупной и светлой чешуей и меньшей высотой тела. Как правило, окрас чешуй серебристо-серый или зеленовато-серый, но изредка встречаются экземпляры с золотистым и даже розовато-оранжевым окрасом. Соотношение высоты тела к длине может значительно меняться в зависимости от условий обитания. Серебряный карась достигает 40 см длины и массы до 2 кг. Отдельные экземпляры живут до 10–12 лет.
Изначально серебряный карась обитал в бассейне реки Амур и прилегающих водоёмах. Искусственно расселен в 60-х годах XX века во многие водоёмы Сибири и Европы. Сейчас завезен в Северную Америку, Индию и другие регионы. При этом в европейских и сибирских водоёмах произошло постепенное вытеснение серебряным карасём карася обыкновенного (золотого), вплоть до полного исчезновения последнего. Серебряный карась предпочитает крупные проточные озера, часто встречается в реках, но течения избегает. Он нетребователен к содержанию в воде кислорода и могут жить там, где другие рыбы погибают (Жуков, 1988; Попов, 2001).
Амурский хариус – род лососёвых рыб. Хариуса (лат. Thymallus arcticus grubii) – легко отличить по огромному спинному плавнику, который в сложенном состоянии достигает языковидного жирового плавника.
По своему цвету хариус – одна из самых пёстрых и красивых рыб России. Спина его серо-зелёная, усеянная более или менее многочисленными и ясными чёрными пятнышками, бока туловища светло-серые с продольными полосками. Парные плавники обыкновенно грязно-оранжевые, а непарные – фиолетовые с тёмными полосками или пятнышками. По Сабанееву вес хариуса достигает 500 граммов, но в реках Приполярного и Полярного Урала довольно часто встречаются особи более полутора килограммов весом, а иногда и больше (Решетников, Котляр, 1989).
Хариус живет в гористых местностях и вместе с форелью составляет главное рыбье население холодных и быстро текущих речек почти всей Европы, северной и северовосточной России и всей Сибири. Хариус живет предпочтительно в чистой воде.
Ленок – (лат. Brachymystax) пресноводная рыба семейства лососёвых.
Первоначально род содержал один вид Brachymystax lenok с двумя ярко выраженными формами – остромордой и тупомордой. Позже таксономия была пересмотрена и формы были выделены в отдельные виды:
- Brachymystax lenok – ленок; остромордый,
- Brachymystax savinovi – ускуч; тупомордый,
Распространен в реках и горных озёрах Сибири и Дальнего Востока, Китая Монголии, а также в Западной Корее, западнее Урала не встречается. Предпочитает быстрые холодные реки, главным образом их верховья. Держится небольшими стайками, крупные – в одиночку . Достигает длины около 70 см и массы 6 кг. Описаны случай поимки рыб весом до 8 кг и метровой длины. Темп роста невысокий. По форме тела ленок похож на сигов. Тело брусковатое, прогонистое, рот маленький с небольшими острыми зубами, чешуя мелкая, плотная. Окраска тела зависит от условий обитания, тёмно-бурое, на спине и боках с обилием тёмных округлых пятнышек и золотистым налётом, светлое в брюшной части, в нерестовую пору на боках выступают красные пятна, верхний, жировой и хвостовой плавники в пятнышках. Ленок, обитающий на перекатах, имеет серебристую окраску с тёмно-серой спинкой, плавники с желтоватым отливом. Половой зрелости ленок достигает на пятом-восьмом году жизни при длине 38 см и массе 600-800 г. Самки обычно созревают на год позже самцов. Нерест происходит в мае-июне, на глубине 0,5-1,5 м. Диаметр икры 4-4,5 мм, масса 50-60 мг. Продолжительность жизни ленка обычно не превышает 15 лет. Хищная рыба. Молодь ленка в раннем возрасте питается зоопланктоном, по мере роста переходит на потребление донных организмов – личинок насекомых (личинки веснянок, подёнок, ручейников, стрекоз, кузнечиков и других насекомых, гаммариды, водоросли), бокоплавов, мелких моллюсков, дождевых червей, икру и молодь других видов рыб (гольян, пескарь, елец, подкаменщик, окунь и хариус) (Паллас, 1773).
Крупные ленки иногда заглатывают мышей, землероек, лягушек. Питается ленок в любое время суток, особенно активно утром и вечером. Любит реки с быстрым течением и предпочитает жить в чистой воде.
Русское – ленок, эвенкийское – майгун, якутское – лимба, тюркское – ускуч, а ещё литературное – сибирская форель.
Щука – род пресноводных рыб, единственный в семействе щуковых (Esocidae). Типовой вид рода – Esox lucius (щука обыкновенная). Распространена в Европе, Сибири, Северной Америке.
Щуки (лат. Esox) могут достигать 1,8 м в длину и 67 кг веса, хотя встречаются и более крупные экземпляры. Продолжительность жизни отдельных особей может доходить до 30 лет. Тело щуки имеет вытянутую форму и напоминает торпеду. Остроконечная голова и острые зубы, типичные для хищных рыб. Окрас щуки – серо-зелёный в крапинку. Спинной и анальный плавники оттянуты далеко назад, и расположены около хвостового плавника, что помогает ей делать стремительные броски.
Щуки – чрезвычайно прожорливые хищники. Питаются они в основном рыбой (плотвой, окунями, гольянами). Для щуки характерен каннибализм: около 20 % ее рациона составляют более мелкие особи её собственного вида. Помимо этого, щуки питаются земноводными и рептилиями, крупными насекомыми и различными отбросами. Их добычей могут стать и мелкие млекопитающие, например, мыши или кроты, попавшие в воду. Щука охотится и на мелких водоплавающих птиц и их птенцов. Этот хищник нападает на животных, достигающих 1/3 от его собственных размеров. Обычно держится в прибрежной зоне среди зарослей водной растительности, где подкарауливает добычу. Типичный хищник-засадчик. Увидев добычу, медленно, работая одними брюшными и грудными плавниками поворачивается в её сторону и затем делает молниеносный рывок, на расстояние до нескольких длин своего тела. Щука может жить в реках с быстрым течением и в соленой воде (с концентрацией солей до 1%). Хорошо выдерживает кислую реакцию воды, может комфортно жить в водоемах с рН 4,75, но крайне чувствительна к различным загрязнителям (Берг, 1948; Клейменов, 1952).
Змееголов – пресноводная рыба семейства змееголовые. Первоначальный ареал обитания змееголова (лат. Channa argus) – реки Дальнего Востока от Янцзы на юге до бассейна реки Амур на севере, в том числе в Приморском крае в реках Уссури, Раздольная и в озёрах Хасан и Ханка.
В начале 1960-х годов было завезено менее ста годовиков змееголова из Московского зоопарка в рыбхоз «Калган-Чирчик» (ныне «Балыкчи»), где они быстро размножились, попали в Сырдарью, вместе с расселением прудовых карпов. Рыбы расселились по равнинным водоемам бассейнов всех рек Узбекистана и юга Казахстана и Туркменистана.
Крупная рыба длиной до 1 м и более, массой до 10 кг и более. Держится сильно заросших участков водоёмов на мелководьях.
Легко переносит дефицит кислорода, может обитать практически в заморных водоёмах. Обильно выделяется слизь, покрывающая тело, есть специальные наджаберные органы для дыхания атмосферным воздухом. Змееголову необходимо дыхание атмосферным воздухом, если доступ атмосферного воздуха будет прегражден для змееголова, то он гибнет даже в свежей воде. Легко переносит высокую минерализацию. В высохших водоёмах он зарывается в вырытую им камеру в иле глубиной до 60 см и смазанную слизью и находится там до следующего дождливого сезона или до повышения уровня воды. Может жить без воды до пяти суток. Легко переползает между водоёмами на значительные расстояния.
Половозрелости достигает в двухгодовалом возрасте при длине тела 30-35 см. Нерест в июне-июле при температуре воды 20-26°C. Плодовитость 20-120 тысяч икринок. Строит гнездо диаметром до 1 м из растений.
Икринки имеют жировую каплю, поэтому слегка всплывают и развиваются в толще воды. Оба родителя охраняют гнездо, плавниками создавая ток воды для нормального аэрирования развивающихся икринок. Охраняют и личинок и мальков.
Промысловый вид. Потенциально перспективная рыба для прудового разведения. Ведёт активное расселение. В ряде стран признан вредным видом в виду быстрого заселения водоема и истребления так называемой «белой» рыбы. Змееголов живет обычно в небольших сильно заросших и прогреваемых (иногда до 35—40°С) водоемах с низким содержанием кислорода в воде и может жить без воды во влажном месте до 5 суток. И неприхотлив к различным изменениям в окружающей среде (Никольский, 1956; Весёлов, 1997).
Чебак, или сибирская плотва (лат. Rutilus rutilus lacustris) — подвид плотвы, лучепёрой рыбы из семейства карповых, распространённый в Сибири и на Урале.
Чебак широко распространён в реках: Тоболе, Иртыше и озёрах Сибири, Урала, Дальнего Востока. Присутствует в больших количествах в реках Якутии, в основном это реки Индигирка и Колыма, а также в реках Забайкальского края (Хилок, Чикой).
Из всех пресноводных подвидов плотвы только чебак, при его достаточном количестве в водоёмах, добывается в промышленных масштабах (как сопутствующий основному промыслу), ввиду быстрого роста и размножения этого подвида. Максимальный вес до 3 кг.
Чебак, как и другая жилая плотва, встречается как в небольших речках, в прудах, так и в больших реках, озёрах, водохранилищах и довольно часто в каждом из этих водоёмов занимает по численности одно из первых мест среди других видов. Большую часть пищи этого подвида составляют водоросли, высшие растения, личинки различных насекомых, моллюски, другие организмы. Клюет чебак на тесто, на червя, на опарыша, в некоторых водоёмах на кукурузу. В сибирских деревнях чебак употребляется в пищу обычно жареным или вяленым, мелкий идёт на корм кошкам и курицам.
2.4. Методика определения содержания тяжелых металлов в рыбе
В санитарно-гигиенической лаборатории Россанэпиднадзора используется способ минерализации проб пищевых продуктов и продовольственного сырья с использованием аналитических автоклавов для последую�щего определения содержания токсичных элементов (меди, цинка, свинца, кадмия, мышьяка, ртути, олова, никеля, железа, хрома, селена, кобальта) методами атомной спектрометрии (атомно-абсорбционной спектрометрией с атомизацией в пламени, в графито�вой печи и с использованием техники генерации гидридов, атомно-эмиссионной спектрометрией с индуктивно-связанной плазмой) и инверсионно-вольтамперометрическим методом. Исследования по безопасности пищевых продуктов проводятся в соответствии с СанПиН 2.3.2.1078-01 «Гигиенические требования к безопасности и пищевой ценности пищевых продуктов».
2.3.1. Автоклавная минерализация
Пробоподготовка рыбы проводилась на автоклавном комплексе МКП–04
2.3.1.1. Подготовка проб рыбы к анализу
Отбор и подготовку проб пищевых продуктов и сырья к испытанию проводят в соответствии с нормативной документацией на исследуемый вид продукции.
В связи с использованием для разложения малых навесок образца (1–4 г) особое внимание следует уделить обеспечению представительности навески.
При сложном составе проб, представляющих смесь белков, углеводов, клетчатки, жиров, особенно при их неравномерном распределении в пробе (мясные, рыбные консервы, кондитерские изделия и т.д.), пробу перед анализом усредняют путем ее тщательного измельчения (гомогенизации) и перемешивания.
Масса навески пробы для минерализации не должна пре�вышать величину, рекомендованную для данного вида продукции.
Залитые реактивами навески образца выдерживают при комнатной температуре в течение 30-40 минут.
При подготовке лабораторной пробы не допускается использование инструментов и оборудования, загрязняющих пробу определяемыми элементами.
2.3.1.2.Автоклавный метод минерализации
Метод основан на полной минерализации пробы смесью азотной кислоты и пероксида водорода в герметично замкнутом объеме аналитического автоклава при воздействии повышенной температуры и давления.
Навеску пробы помещают в реакционную емкость, добав�ляют смесь реактивов и, если необходимо, выдерживают при ком�натной температуре.
Для контрольного («холостого») определения в реакци�онную емкость помещают только смесь реактивов без добавления испытуемой пробы.
Реакционную емкость закрывают крышкой и герметизируют в металлическом корпусе автоклава.
Сборку (герметизацию) автоклава (рис.1) осуществляют в сле�дующем порядке:
в реакционную емкость 1 загружают пробу исследуемого об�разца и реактивы, накрывают крышкой 2;
в корпус 3 вставляют донышко 4 и помещают загруженную реакционную камеру, на крышку реакционной камеры устанавли�вают тарелку 9; в которую вкладывают пружину 10; выкручивают шток 8 так, чтобы торец штока 8 и ползуна 6 были в одной плоскости внутри крышки 5;
крышку 5 без усилия надевают на корпус 3 и поворачивают вокруг оси по часовой стрелке до упора в штифт 11, при этом байонетные выступы на корпусе 3 должны полностью совпасть с байонетом крышки 5. Вворачивают шток 8 вручную до касания нижнего торца штока 8 с пружиной 10;
устанавливают автоклав в приспособление для сборки-раз�борки, фиксируя его от осевого вращения;
• ключом поворачивают шток 8 по часовой стрелке до упора, при этом происходит взвод пружины и герметизация реакционной камеры.
Автоклав загерметизирован и готов к установке в термостат.
Автоклав помещают в холодный термостат, устанавливают на пульте управления температуру первой стадии нагрева и нагревают автоклавы в соответствии с температурной программой, выдерживая на каждой стадии ступенчатого нагрева в течение времени, указанного в таблице 2.2.
Примечание. Указанное в таблице время выдерживания на первой ста�дии нагрева не включает в себя время выхода на стационарный режим, а отсчитывается с момента достижения заданной температуры, о чем свиде�тельствует установка стрелки индикатора на нулевую отметку.
По окончании минерализации с помощью приспособления для переноса извлекают автоклавы из термостата, помещают в устройство для охлаждения и охлаждают до комнатной температуры (30—60 мин в зависимости от типа образца и величины навески).
Рис. 1. Автоклав аналитический.
1 - реакционная емкость, 2 - крышка реакционной емкости, 3 - корпус, 4 - донышко, 5 - крышка корпуса, 6 - ползун, 7 - срезной винт, 8 - шток, 9 - тарелка, 10 - пружина, 11 - штифт.
Разборку (разгерметизацию) автоклава осуществляют в соответствии с правилами, изложенными в техпаспорте.
Разгерметизацию автоклава и последующие операции по подготовке минерализата к анализу проводят в вытяжном шкафу в резиновых перчатках во избежание попадания паров азотной кис�лоты на кожу рук.
Извлекают реакционную камеру, открывают крышку, раствор количественно переносят в кварцевую или фарфоровую чашку, обмывая внутреннюю полость и крышку автоклава небольшими порциями (2–3 см3) бидистиллированной воды.
Если указанная в таблице 2.2 навеска образца недостаточна для получения необходимой чувствительности определения аналита, возможно объединение растворов-минерализатов из двух реакционных емкостей с навесками одной и той же пробы в одну чашку. Объединенный минерализат подготавливают для анализа, как указано в методике; при расчете результата анализа навески суммируют. При этом контрольный («холостой») опыт проводят в тех же условиях.
2.3.2. Подготовка минерализата к определению токсичных элементов
Подготовку полученного в результате автоклавного разложения минерализата к анализу проводят в соответствии с требованиями методики анализа.
2.3.2.1. Подготовка минерализата к анализу с использованием электрохимических методов
При определении токсичных элементов электрохимическими методами (полярография, инверсионная вольтамперометрия) большое значение для получения правильных результатов играет полнота разложения органических соединений образца. В ряде случаев при использовании указанных в таблице температурно-временных па�раметров не удается обеспечить полное разложение органических соединений, о чем свидетельствует желтая окраска минерализата различной интенсивности, в зависимости от количества оставшейся в растворе органики. В этом случае необходимо провести ее доокисление как указано ниже.
Полученный минерализат упаривают на водяной бане досуха. Если сухой остаток имеет желтый или коричневый цвет, его обрабатывают небольшим количеством азотной кислоты (0,3– 0,5 см3) и несколькими каплями пероксида водорода и снова нагре�вают на водяной бане досуха. Если сухой остаток снова окрашен, обработку повторяют до полного удаления органических соединений и получения белого остатка. Полученный остаток переводят в раствор в соответствии с требованиями методики анализа.
2.3.2.2. Подготовка минерализата к анализу с использованием методов атомной спектрометрии
Подготовку минерализата для определения токсичных элементов методами атомной спектрометрии (атомно-абсорбционной спектро�метрии, пламенной фотометрии, атомно-эмиссионной спектрометрии с индуктивно-связанной плазмой) проводят в соответствии с требо�ваниями методики анализа.
2.3.3. Подготовка автоклавов к анализу
2.3.3.1. Подготовка к работе металлического кожуха автоклава
После удаления реакционной камеры с минерализатом детали металлического кожуха автоклава промывают горячей проточной водой с мылом (винты не выворачивать!) и просушивают.
2.3.3.2. Подготовка новой реакционной камеры к работе
2.3.3.2.1. Новую фторопластовую реакционную камеру (крышку, реакционную емкость) моют горячей проточной водой с мылом, ополаскивают детали камеры дистиллированной водой.
2.3.3.2.2. Дважды обрабатывают реакционную камеру азотной ки�слотой в автоклавном режиме: в реакционную емкость заливают 40 см3 азотной кислоты, закрывают крышкой, герметизируют в ме�таллическом кожухе, помещают в термостат, нагревают при 160 °С в течение 4 ч. После охлаждения извлекают камеру из кожуха, сли�вают азотную кислоту и ополаскивают детали камеры бидистилли�рованной водой.
2.3.3.2.3. Загружают реакционную камеру реактивами в соответст�вии с конкретной методикой анализа, проводят нагрев автоклава в соответствии с температурной программой, указанной в таблице. Полученный минерализат контрольного опыта анализируют на со�держание определяемого элемента.
Примечание. Для контроля чистоты реакционной камеры необходимо сравнить минерализат, проведенный через процедуру автоклавирования, с контрольным («холостым») раствором, приученным добавлением всех реактивов, но без автоклавирования для учета содержания определяемого элемента в реактивах.
2.3.3.2.4. Повторяют проверку минерализата до отсутствия обнаруживаемой концентрации определяемых элементов в контрольном опыте.
2.3.3.2.5. Хранят реакционную камеру в собранном виде, запол�ненную бидистиллированной водой.
2.3.3.3. Подготовка реакционной камеры к проведению анализа
2.3.3.3.1. Не рекомендуется оставлять минерализат в реакционной камере после разложения на длительное время.
2.3.3.3.2. После удаления минерализата реакционную камеру опо�ласкивают бидистиллированной водой, заливают в нее 6–10 см3 концентрированной азотной кислоты и после герметизации авто�клав помещают в термостат. Устанавливают температуру 180–200 °С и выдерживают при этой температуре 40–60 мин. После охлажде�ния автоклава сливают азотную кислоту, ополаскивают детали ка�меры бидистиллированной водой.
2.3.3.3.3. Хранят реакционную камеру в собранном виде, запол�ненную бидистиллированной водой.
2.3.4. Требования безопасности
2.3.4.1. Все операции с автоклавом, связанные с использованием исследуемых веществ и химических реактивов, выполняют только в вытяжном шкафу при включенной вытяжной вентиляции в условиях, исключающих попадание химических веществ на обслуживающий персонал или в атмосферу помещения в концентрациях, превышаю�щих нормы, установленные ГН 2.2.4.686–98 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны».
2.3.4.2. Помещение лаборатории должно соответствовать требова�ниям пожарной безопасности по ГОСТ 12.1.004-91 «Пожарная безопасность. Общие требования» и иметь средства пожаротушения по ГОСТ 12.4.009 – 83 «Пожарная техника для зашиты объектов. Основные виды. Размещение и обслуживание».
2.3.4.3. При работе с автоклавом не допускается:
эксплуатировать автоклав при обнаружении следов механи�ческих повреждений деталей: деформации, трещин, задиров и т. п.;
использовать в автоклаве реакционные камеры с полностью выработанной линией уплотнения; использовать для разложения химические вещества и реактивы, не указанные в методике анализа, в частности хлорную кислоту;
использовать массы навесок проб и объемы реагентов боль�ше указанных в таблице;
использовать перегрев автоклава выше рабочей температуры, указанной в методике анализа, для форсирования процесса разло�жения исследуемых веществ;
открывать автоклав, не охладив его до комнатной темпера�туры в устройстве для охлаждения автоклавов;
опускать автоклавы в термостат, температура которого пре�вышает комнатную температуру;
продолжать разложение пробы после срабатывания предо�хранительного клапана; при этом клапан будет расположен выше верхней плоскости крышки металлического кожуха автоклава, а момент срабатывания может сопровождаться характерным хлопком.
Примечание. В случае срабатывания предохранительного клапана в лю�бом из автоклавов следует прекратить дальнейшую тепловую обработку автоклавов в термостате:
• выключить прибор регулирования температуры (отжать кнопки НАГРЕВ и СЕТЬ), вынуть вилку сетевого кабеля прибора регулирования из розетки электропитания;
• снять с термостата защитную крышку;
извлечь автоклав, у которого сработал предохранительный клапан, и остальные автоклавы с помощью сервисного приспособления для переноса и охладить их до комнатной температуры в охлаждающем устройстве;
автоклав, у которого сработал предохранительный клапан, разобрать, все детали промыть водой с мылом и протереть насухо. Для сокращения вре�мени контакта кожуха автоклава с кислотой эти операции должны выпол�няться как можно быстрее.
После остывания термостата до комнатной температуры следует:
промыть внутреннюю поверхность защитной крышки водой с мылом и протереть насухо;
протереть влажной тряпкой крышку корпуса термостата и ячейки для автоклавов, вытереть насухо.
2.3.4.4. Перед началом работы с комплексом следует убедиться в отсутствии повреждения изоляции питающих кабелей.
2.3.4.5. При проведении профилактических работ и технического обслуживания необходимо отключить комплекс от сети.
2.3.4.6. Для подключения комплекса необходимо использовать ро�зетки, имеющие заземляющие контакты, которые должны быть под�соединены к заземляющему контуру.
Таблица 2.2
Условия минерализации проб рыбы в автоклаве НПВФ «АНКОН–АТ–2» с реакционной камерой, вместимостью 150 см3
|
Наименование объекта
|
Масса
навески, г
|
Объем реак�тивов, см3
|
Экспозиция (комнатная темпе�ратура)
|
Температура и время нагрева, ч
|
Примечание
|
|
Рыба живая,
охлажденная,
мороженная
|
3,00
|
HNO3-6
Н2О2- 1
|
30—40 мин
|
160°С - 1 ч 180°С – 2 ч 200°С - 1 ч
|
Для жирных сортов – заливают на ночь HNО3, утром добав�ляют Н2О2
|
ГЛАВА III. СОДЕРЖАНИЕ ТОКСИЧНЫХ ЭЛЕМЕНТОВ В РЫБЕ ПОВЕРХНОСТНЫХ ВОДОТОКОВ БИРОБИДЖАНСКОГО РАЙОНА ЕАО
Значения концентраций металлов в пробах сравнивали с принятыми в России допустимыми остаточными концентрациями (ДОК) этих элементов в свежих рыбопродуктах. Они описаны в санитарных правилах и нормах (СанПиН) 2.3.2.1078-01 «Гигиенические требования безопасности и пищевой ценности пищевых продуктов».
Допустимые уровни данных элементов для рыбы:
Pb - 1 мг/кг; Cd - 0,2 мг/кг; Hg: - Нехищные - 0,3 мг/кг, - Хищники - 0,6 мг/кг,
- Морские - 0,5 мг/кг; As - 1 мг/кг.
В результате данной работы было проанализировано 17 проб рыбы, что составляет 68 элемент-определения. Подготовка одной пробы рыбы занимает примерно 20 мин. Разложение рыбы в автоклаве занимает 4 ч. Анализ 6 проб рыбы атомно-абсорбционным методом по одному металлу занимает примерно 1 ч.
По содержанию в 2010 году в организме промысловых рыб токсичные элементы располагаются в следующие ранжированные ряды (токсичные элементы, имеющие концентрацию меньше предела обнаружения, не сравнивались между собой):
Хариус амурский – Hg > As, Cd, Pb Карась серебряный – Hg > As, Pb, Cd Ленок – Hg > As, Pb, Cd Щука – Hg > Pb > As, Cd Змееголов – Hg > Cd > As, Pb Ленок (пятнистый) – Hg > Cd > Pb > As
Распределение металлов по уменьшению величин их концентрации по организму специфично для каждой пробы рыб, однако имеются некоторые общие черты. В целом в организме рыб реки Урми и Ин преобладает ртуть. Мышьяк, свинец и кадмий, по допустимым остаточным концентрациям этих элементов в свежемороженых рыбопродуктах, находятся, либо в минимальных концентрациях, либо в концентрациях ниже предела обнаружения.
Изменение концентраций по разным токсичным элементам в речной рыбе поверхностных водотоков Биробиджанского района ЕАО, можно наблюдать на рис. 2, 3, 4.
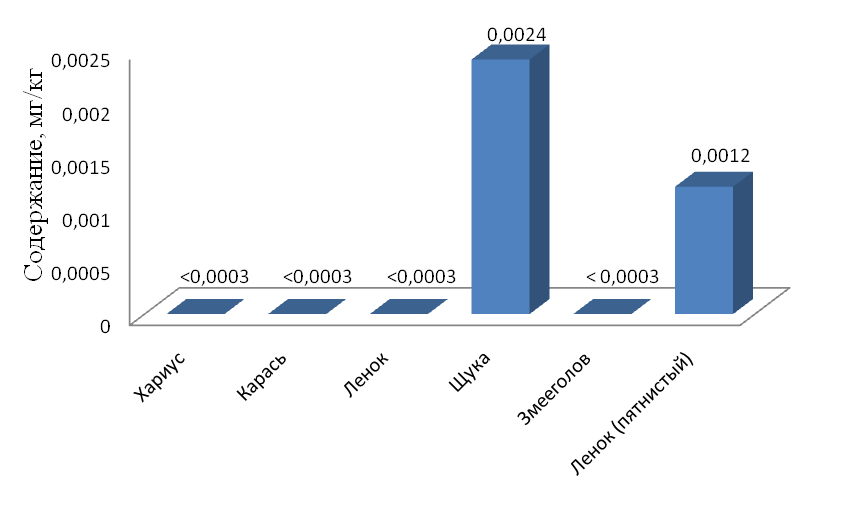
Рис. 2. Содержание свинца в рыбе, октябрь – декабрь 2010г.
Содержание свинца в речной рыбе поверхностных водотоков Биробиджанского района ЕАО не превышает допустимую остаточную концентрацию. В щуке концентрация свинца равна 0,24% от ДОК.
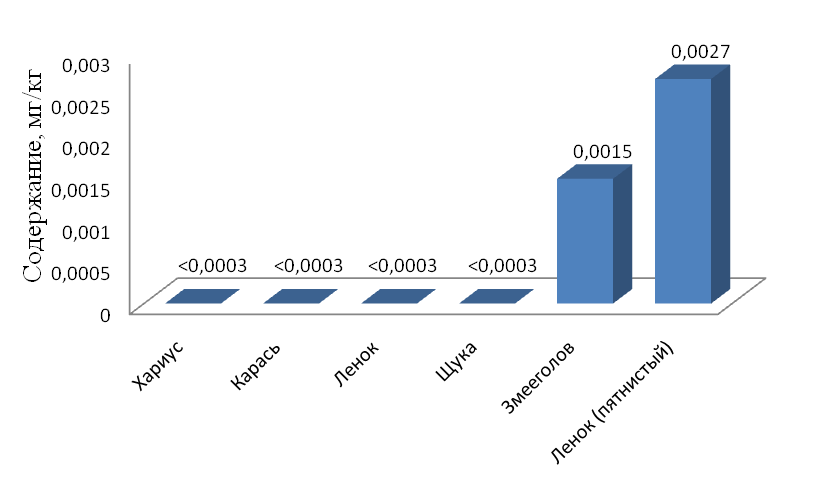
Рис. 3. Содержание кадмия в рыбе, октябрь – декабрь 2010г.
Содержание кадмия в речной рыбе поверхностных водотоков Биробиджанского района ЕАО также не превышает допустимую остаточную концентрацию. Максимальная концентрация кадмия в пробах речной рыбы наблюдается в ленке (пятнистый) и она составляет 1,35% от ДОК.
Низкая концентрация мышьяка, свинца и кадмия в промысловой рыбе поверхностных водотоков Биробиджанского района ЕАО может быть связана, как с природными особенностями районов, так и с физиологическими процессами (дыхание, кроветворение, накопление жировой прослойки, выделение и др.). А неодинаковое накопление токсичных элементов между разными видами рыб может быть обусловлено различными районами вылова рыб, особенностями предпочтения различными видами рыб находится в чистой или загрязненной зоне, возрастом рыбы и характером питания. Это хорошо видно на рис. 2, 3, 4.
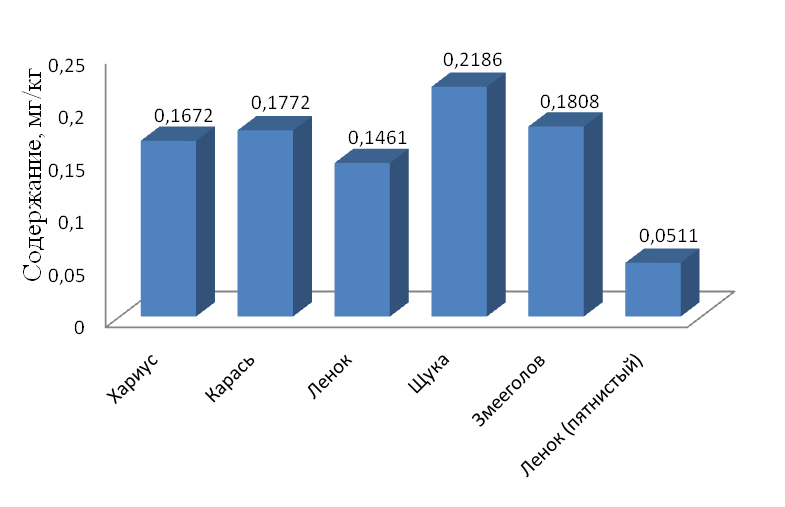
Рис. 4. Содержание ртути в рыбе, октябрь – декабрь 2010г.
Содержание ртути в речной рыбе поверхностных водотоков Биробиджанского района ЕАО хоть и не превышает допустимую остаточную концентрацию, но по сравнению с другими элементами имеет характерную выраженность, как в концентрации, так и в колебаниях между видами рыб. Поступление ртути в организм речной рыбы может быть связан с природными особенностями ЕАО (залеганием минералов-концентратов, к числу которых относят сфалерит). Заметное превалирование ртути над мышьяком, свинцом и кадмием в организме рыб связано с высоким сродством ртути с белком, которая накапливается преимущественно в мышечной ткани (Лукьяненко, 1983; Петухов, Морозов, 1983; Богдановский, 1994). Этот металл является чрезвычайно опасным для жизнедеятельности гидробионтов. Он накапливается в разных звеньях трофических цепей за счет способности живых организмов аккумулировать этот металл до концентраций, в сотни и тысячи раз превосходящих его содержание в окружающей среде. Содержание ртути в пище и окружающих средах определяет его уровень в гидробионтах. Так, характер питания беспозвоночных практически не влияет на содержание ртути в их теле, и лишь хищные гидробионты, находящиеся в конце пищевой цепи, накапливают более высокие концентрации ртути (Никаноров, Жулидов, 1991).
Содержание мышьяка в речной рыбе поверхностных водотоков Биробиджанского района ЕАО ниже предела обнаружения.
Таким образом, для рыб щука, карась, обитающих в р. Ин, характерно наличие в тканях и органах Pb и Hg, а для рыб змееголов, ленок, обитающих в р. Урми, – кадмия.
По содержанию в организме промысловых рыб токсичные элементы располагаются в следующие ранжированные ряды (токсичные элементы, имеющие концентрацию меньше предела обнаружения, не сравнивались между собой):
Хариус амурский – Hg > Cd > As > Pb Ленок – Hg > Pb > Cd > As Змееголов – Hg > Cd > As, Pb Карась серебряный – Hg > Cd > As > Pb Хариус амурский – Hg > Cd > As, Pb Ленок – Hg > As > Cd > Pb
Расположение токсичных элементов, в ранжированных рядах, по сравнению с результатами исследований речной рыбы в 2010 году практически не изменились. Так же наблюдается преобладание ртути над другими элементами. Небольшое изменение в содержании мышьяка, свинца и кадмия. В некоторых образцах они поднялись до уровня обнаружения данным методом, но также не превышают допустимые уровни.
Рассмотрим токсичные элементы в речной рыбе в сравнении с 2010 г. Изменение концентраций по разным токсичным элементам в речной рыбе поверхностных водотоков Биробиджанского района ЕАО по сравнению с 2010 годом, можно наблюдать на рис. 5, 6 , 7.
Рис. 5. Содержание мышьяка в рыбе, 2010 – 2012 гг.
Содержание мышьяка в речной рыбе 2012 года по сравнению с 2010 возросло до уровня обнаружения её в пробах. Но в некоторых пробах рыбы, концентрация мышьяка остается также ниже предела обнаружения, в сравнении с 2010 г. Максимальная концентрация мышьяка наблюдается в пробах ленка (0,0226 мг/кг) за 2012 год, она составляет 2,26% от допустимого уровня мышьяка в речной рыбе (ПДКAs – 1 мг/кг).
Рис. 6. Содержание кадмия в рыбе, 2010 – 2012 гг.
Содержание кадмия в речной рыбе поверхностных водотоков Биробиджанского района ЕАО по сравнению с 2010 годом возросло. Самые большие концентрации наблюдаются у хариуса (0,018 мг/кг) и серебряного карася (0,018 мг/кг), что составляет 9% от ДОК.
Рис. 7. Содержание ртути в рыбе, 2010 – 2012 гг.
Содержание ртути в речной рыбе поверхностных водотоков Биробиджанского района ЕАО сильно не изменились. Однако наблюдается небольшое уменьшение ртути в хариусе, ленке, серебряном карасе и небольшое увеличение у змееголова. В среднем концентрация ртути в хариусе, ленке и серебряном карасе за 2012 год уменьшилось в 1,5 – 2 раза по сравнению с показателями за 2010г.
Содержание свинца в речной рыбе поверхностных водотоков Биробиджанского района ЕАО практически во всех пробах ниже предела обнаружения. Но небольшая концентрация свинца наблюдается у одной из проб ленка, также как и в 2010г. В 2010 она составляла 0,0012 мг/кг, а в 2012 она составила 0,036 мг/кг. Что в 30 раз превышает концентрацию свинца в пробе ленка за 2010г.
Таким образом, содержание мышьяка, кадмия и свинца в речной рыбе поверхностных водотоков Биробиджанского района ЕАО по сравнению с 2010 годом возросло, но также не превышает предельно допустимые концентрации токсичных элементов. Сильных изменений в содержании ртути не обнаружено.
Было установлено, что максимальная концентрация токсичных элементов в речной рыбе поверхностных водотоков Биробиджанского района ЕАО за 2010 – 2012 гг. в отобранных пробах составила:
- свинец – 0,036 мг/кг (ПДК – 1 мг/кг);
- кадмий – 0,018 мг/кг (ПДК – 0,2 мг/кг);
- ртуть – 0,2369 мг/кг (ПДК – от 0,3 до 0,6 мг/кг);
- мышьяк – 0,0226 мг/кг (ПДК – 1 мг/кг),
что не превышает допустимую остаточную концентрацию по данным элементам.
По содержанию в организме промысловых рыб токсичные элементы располагаются в следующие ранжированные ряды (токсичные элементы, имеющие концентрацию меньше предела обнаружения, не сравнивались между собой).
Рассмотрим токсичные элементы в речной рыбе в сравнении с 2010- 2015 гг. Изменение концентраций по разным токсичным элементам в речной рыбе поверхностных водотоков Биробиджанского района ЕАО по сравнению с 2010-2012 годом, можно наблюдать на рис. 8, 9 , 10.
Рис. 8. Содержание мышьяка в рыбе, 2010 – 2015 гг.
Содержание мышьяка в речной рыбе 2015 года по сравнению с 2010 стало ниже уровня обнаружения её в пробах. Максимальная концентрация мышьяка наблюдается в пробах ленка (0,0226 мг/кг) за 2012 год, она составляет 2,26% от допустимого уровня мышьяка в речной рыбе (ПДК As – 1 мг/кг).
Рис. 9. Содержание ртути в рыбе, 2010 – 2015 гг.
Содержание ртути в речной рыбе поверхностных водотоков Биробиджанского района ЕАО стало значительно меньше, концентрация которой выявленная на 2015 год составляет менее 0,0005мг/кг
Рис. 10 . Содержание свинца в рыбе 2010-2015 гг.
Содержание свинца в речной рыбе поверхностных водотоков Биробиджанского района ЕАО практически во всех пробах ниже предела обнаружения. Но небольшая концентрация свинца наблюдается у одной из проб ленка, также как и в 2010г. В 2010 она составляла 0,0012 мг/кг, а в 2012 она составила 0,036 мг/кг. Что в 30 раз превышает концентрацию свинца в пробе ленка за 2010г. В 2015 г. содержание составляет менее 0,01. Что говорит об уменьшении концентрации по сравнению с 2012 годом.
Таким образом, содержание мышьяка, кадмия и свинца в речной рыбе поверхностных водотоков Биробиджанского района ЕАО по сравнению с 2010 годом уменьшилось и не превышает предельно допустимые концентрации токсичных элементов. Сильных изменений в содержании ртути не обнаружено.
В результате данной работы было выявлено, что речная рыба поверхностных водотоков Биробиджанского района ЕАО по концентрации свинца, кадмия, мышьяка и ртути не превышают допустимые остаточные концентрации (ДОК) этих элементов в свежих рыбопродуктах, по санитарным правилам и нормам, описанных в (СанПиН) 2.3.2.1078-01 «Гигиенические требования к безопасности и пищевой ценности пищевых продуктов». Вследствие этого можно говорить, что речная рыба поверхностных водотоков Биробиджанского района ЕАО пригодна к употреблению в пищу.
ВЫВОДЫ
- Подготовлен информационно-аналитический обзор по теме «Содержание токсичных элементов в рыбе поверхностных водотоках ЕАО».
- Установлено, что максимальная концентрация токсичных элементов в речной рыбе поверхностных водотоков Биробиджанского района ЕАО за 2010 – 2015 гг. в отобранных пробах составила: свинец – 0,036 мг/кг (ПДК – 1 мг/кг); кадмий – 0,018 мг/кг (ПДК – 0,2 мг/кг); ртуть – 0,2369 мг/кг (ПДК – от 0,3 до 0,6 мг/кг); мышьяк – 0,0226 мг/кг (ПДК – 1 мг/кг), что не превышает допустимую остаточную концентрацию по данным элементам.
- Динамика по содержанию тяжелых металлов в речной рыбе, обитающей в поверхностных водотоках Биробиджанского района ЕАО за 2010-2012 гг.
- Содержание мышьяка в речной рыбе 2012 года по сравнению с 2010 возросло до уровня обнаружения её в пробах. Но в некоторых пробах рыбы, концентрация мышьяка остается также ниже предела обнаружения, в сравнении с 2010 г. Максимальная концентрация мышьяка наблюдается в пробах ленка (0,0226 мг/кг) за 2012 год, она составляет 2,26% от допустимого уровня мышьяка в речной рыбе (ПДКAs – 1 мг/кг).
- Содержание кадмия в речной рыбе поверхностных водотоков Биробиджанского района ЕАО по сравнению с 2010 годом возросло. Самые большие концентрации наблюдаются у хариуса (0,018 мг/кг) и серебряного карася (0,018 мг/кг), что составляет 9% от ДОК.
- Содержание ртути в речной рыбе поверхностных водотоков Биробиджанского района ЕАО сильно не изменились. Однако наблюдается небольшое уменьшение ртути в хариусе, ленке, серебряном карасе и небольшое увеличение у змееголова. В среднем концентрация ртути в хариусе, ленке и серебряном карасе за 2012 год уменьшилось в 1,5 – 2 раза по сравнению с показателями за 2010г.
- Содержание свинца в речной рыбе поверхностных водотоков Биробиджанского района ЕАО практически во всех пробах ниже предела обнаружения. Но небольшая концентрация свинца наблюдается у одной из проб ленка, также как и в 2010г. В 2010 она составляла 0,0012 мг/кг, а в 2012 она составила 0,036 мг/кг. Что в 30 раз превышает концентрацию свинца в пробе ленка за 2010г.
Таким образом, содержание мышьяка, кадмия и свинца в речной рыбе поверхностных водотоков Биробиджанского района ЕАО по сравнению с 2010 годом возросло, но также не превышает предельно допустимые концентрации токсичных элементов. Сильных изменений в содержании ртути не обнаружено.
- В результате данной работы было выявлено, что речная рыба поверхностных водотоков Биробиджанского района ЕАО по концентрации свинца, кадмия, мышьяка и ртути не превышают допустимые остаточные концентрации (ДОК) этих элементов в свежих рыбопродуктах, по санитарным правилам и нормам, описанных в (СанПиН) 2.3.2.1078-01 «Гигиенические требования безопасности и пищевой ценности пищевых продуктов». Вследствие этого можно говорить, что речная рыба поверхностных водотоков Биробиджанского района ЕАО пригодна к употреблению в пищу.
СПИСОК ЛИТЕРАТУРЫ
- Берг Л.С. Рыбы пресных вод СССР. М.: Наука, 1948. 466 с.
- Беспамятнов Г.П., Кротов Ю.А. Предельно допустимые концентрации химических веществ в окружающей среде. Справочник. Л.: Химия, 1985. 675 с.
- Богдановский Г.А. Химическая экология: учебное пособие. М.: МГУ, 1994. 237 с.
- Большая советская энциклопедия: В 30 т. М.: "Советская энциклопедия", 1969-1978.
- Будников Г.К. Тяжелые металлы в экологическом мониторинге водных систем. Соросовский образовательный журнал. № 5 1998. 23-29 с.
- Васильева Е.Д. Рыбы. М.: Астрель, 1999. 640 с.
- Весёлов Е.А. Определитель пресноводных рыб. М.: Просвещение, 1997. 238 с.
- ГН 2.2.4.686–98 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны».
- ГОСТ 12.1.004-91 «Пожарная безопасность. Общие требования».
- ГОСТ 12.4.009 – 83 «Пожарная техника для зашиты объектов. Основные виды. Размещение и обслуживание».
- ГОСТ 26929–94 «Сырье и продукты пищевые. Подготовка проб. Минерализация для определения содержания токсичных элементов».
- Даффус Дж.Х. «Тяжелые металлы». Vol. 74, № 5, 2002. 793-807 с.
- Доклад об экологической ситуации в Еврейской автономной области в 2011 году. Биробиджан: УПР по ЕАО, 2011. 46 с.
- Евтушенко Н.Ю., Сытник Ю.М., Шаповал Т.Н., Кукля И.Г. Тяжелые металлы в рыбах среднего Дуная // Водные ресурсы. Т. 20. № 5. 1993. 605-614 с.
- Ершов Ю.А., Попков В.А., Берлянд А.С., Книжник А.З. Кадмий экологические аспекты. М.: Медицина, 1994. 165 с.
- Жуков П.И. Справочник по экологии пресноводных рыб. М.: Наука и техника, 1988. 208-214 с.
- Зайцева И.И. Экспериментальное изучение влияния тяжелых металлов на планктонные водоросли // Ботанический журнал. №8, 1999. 33-39 с.
- Ильин В.Б. Микроэлементы и тяжёлые металлы в почвах и растениях Новосибирской области. Н.: СО РАН, 2001. 229 с.
- Кабата-Пендиас А., Пендиас X. Микроэлементы в почвах и растениях. М.: Мир, 1989. 439 с.
- Кеннет Г., Фальчук И. Нарушения метаболизма микроэлементов // Внутренние болезни. Кн. 2. М.: Медицина, 1993. 451-457 с.
- Клейменов И.Я. Химический и весовой состав основных промысловых рыб. М., 1952. 58 с.
- Кнунянц И.Л. Химическая энциклопедия. М.: Советская энциклопедия, 1995. 639 с.
- Криксунов Е.А. Экологи. М.: Дрофа, 1995. 240 с.
- Лужников Е.А., Суходолова Г.Н. Острые отравления у взрослых и детей. М.: ЭКСМО, 2009. 556 с.
- Лукьяненко В.И. Общая ихтиотоксикология. М.: Легкая и пищевая пром-сть, 1983. 320 с.
- Лэне Т.В., Морель М.М. Биологическая функция для кадмия в морских диатомовых водорослях. 1999. 97 с.
- Майстренко В.Н., Хамитов Р.З., Будников Г.К. Экологический мониторинг суперэкотоксикантов. М.: Химия, 1996. 320 с.
- Материалы конференций по анализу природных и сточных вод в России за последние 5-10 лет.
- Медведев В.Е. Курганы Приамурья. Новосибирск: ИАиЭ СО РАН, 1998. 144 с.
- Мелихов А. Биробиджан — Земля обетованная. История одной грёзы «Октябрь» № 12, 2006. 16-45 с.
- Миркин Б.М., Наумова Л.Г. Экология России. 1995. 232 с.
- Миркин Б.М., Наумова Л.Г. Экология России. Учебник из Федерального комплекта для 9 - 11 классов общеобразовательной школы. Изд. 2-е, перераб. И доп. - М.: АО МДС, 1996. 272 с.
- Мур Дж.В., Рамамурти С. Тяжелые металлы в природных водах. М.: Мир, 1987. 286 с.
- Никаноров А.М., Жулидов А.В. Биомониторинг металлов в пресноводных экосистемах. Л.: Гидрометеоиздат, 1991. 312 с.
- Никольский Г.В. Рыбы бассейна Амура. М.: Изд-во АН СССР, 1956. 551 с.
Содержание токсичных элементов (Pb, Cd, Hg, As) в речной рыбе Приамурья