Окислительно - восстановительные реакции (ОВР)
Окислительно - восстановительные реакции (ОВР)
Реакции, протекающие с изменением степени окисления, называются окислительно – восстановительными.
Степень окисления – условный заряд атома в соединении, вычисленный из предположения, что оно состоит только из ионов.
- «» степень окисления имеют атомы, которые приняли электроны от других атомов или в их сторону смещены связующие электронные облака.
- «+» степень окисления имеют атомы, которые отдали свои электроны другим атомам.
- «0» степень окисления имеют атомы в молекулах простых веществ.
Правила определения степени окисления
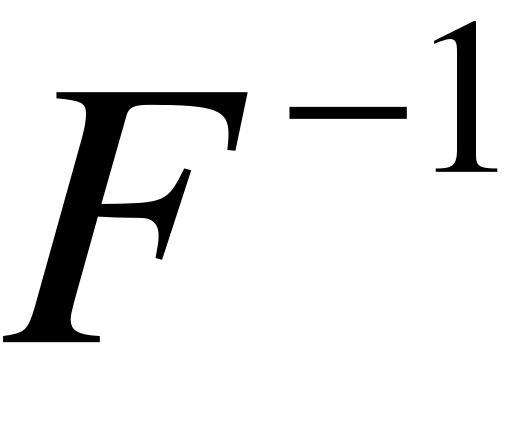
самый электроотрицательный элемент, во всех соединениях -1.
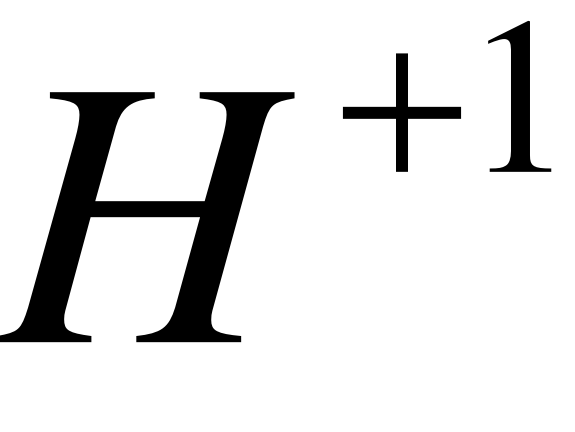
- за исключением гидридов металлов
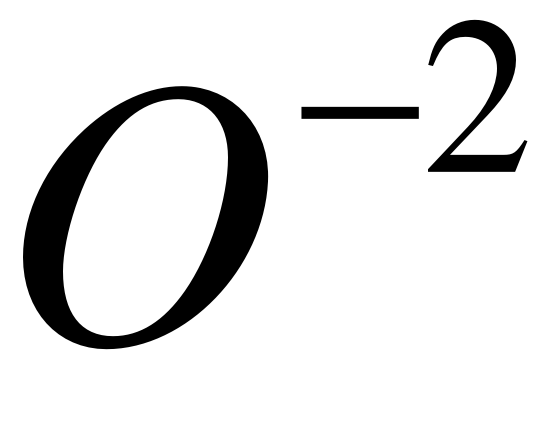
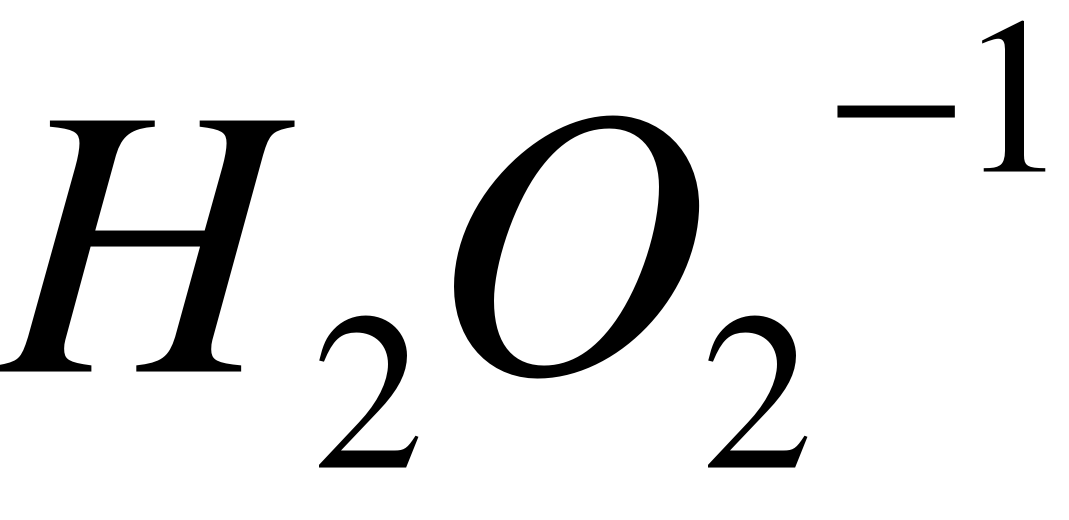
постоянная степень окисления –2, за исключением:
пероксида водорода
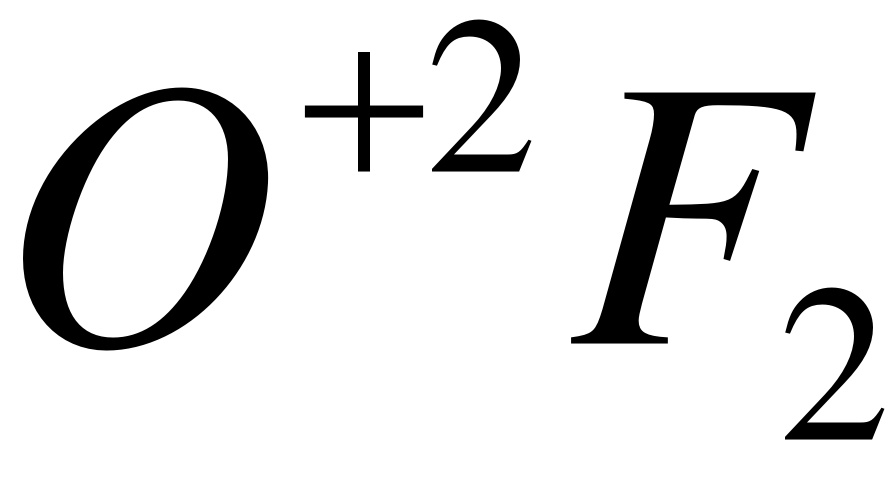
фторида кислорода
- В пероксидах и дисульфидах содержатся двухатомные мостики [-O-O-], [-S-S-] - степени окисления атомов O и S этих соединениях равна 1.
- Атомы элементов I-III групп ПС, отдающие свои электроны, имеют постоянную «+» степень окисления, равную номеру группы.
Исключение: Cu (+1,+2),
Au (+1,+3),
Hg (+1,+2).
- Атомы элементов главных подгрупп IV-VI групп могут проявлять несколько степеней окисления.
- Высшую «+», равную номеру группы
- Промежуточную, на 2 единицы меньше, чем высшая,
- Низшую «», равную разности между номером группы и число 8
Исключение: N (+1,+2,+3,+4,+5, -3)
- Атомы металлов могут иметь только «+» степень окисления.
- Атомы элементов VII группы, главной подгруппы –галогены (кроме фтора) могут иметь в соединениях все нечетные степени окисления от 1 до +7 (1, +1, +3,+5,+7)
- Алгебраическая сумма степеней окисления в соединение равна 0, а в сложном ионе – заряду иона.
Окислители и восстановители
- Окислением называется процесс отдачи электронов, степень окисления атома при этом повышается:
Al0 - 3 Al+3
S2 - 8 S+6
- Восстановлением называется процесс присоединения электронов, степень окисления при этом понижается:
S0 + 2 S2
Al+3 + 3 Al0
- Вещества, атомы которых присоединяют электроны, называются окислителями.
В процессе реакции окислители восстанавливаются.
- Вещества, атомы которых отдают электроны, называются восстановителями.
В реакции восстановители окисляются.
Окислителями могут быть:
Неметаллы в свободном состоянии;
Неметаллы и металлы в высшей степени окисления;
Восстановителями могут быть:
Металлы и водород в свободном состоянии;
Металлы и неметаллы в низшей степени окисления.
Вещества, в состав которых входит элемент в промежуточной степени окисления, проявляют окислительно – восстановительную двойственность: по отношению к окислителю они являются восстановителями, а по отношению к восстановителям – окислителями.
ОВР - это единство 2 противоположных процессов – окисления и восстановления. Число электронов, которое отдает восстановитель, равно числу электронов, которое присоединяет окислитель.
Классификация ОВР
1. Реакции межмолекулярного и межатомного окисления-восстановления (атомы повышающие и понижающие степень окисления входят в состав разных молекул):
2 KI + Cl20 2 KCl + I20
2. Реакции внутримолекулярного окисления-восстановления (атомы, изменяющие степени окисления входят в состав одной молекулы):
2 Na N+5O32 2 NaN+3O2 + O20
3.Реакции диспропорционирования (повышает и понижает степень окисления атом одного и того же элемента):
Cl20 + KOH KCl+O + KCl +Н2О
Реакции межмолекулярного и межатомного окисления-восстановления уравниваются слева направо.
Реакции внутримолекулярного окисления-восстановления и диспропорционирования – справа налево.
Составление уравнений ОВР методом электронного баланса
Пример 1. MnS +HNO3 MnSO4 + NO + H2O
1. Определяют степени окисления всех атомов и атомы, изменившие степень окисления:
Mn+2S2 + H+N+5O32
Mn+2S+6O42 + N+2O2 + H2+O2
2. Составляют схемы процессов окисления и восстановления.
3. Записывается число отданных и число принятых электронов, для этих чисел находится наименьшее общее кратное, разделив которое на число отданных и принятых электронов, получаем коэффициенты перед MnS и HNO3:
S2 - 8 S+6 8 24 3 - окисление
N+5 + 3 N+2 3 8 – восстановление
MnS – восстановитель; HNO3 – окислитель.
4. Найденные коэффициенты (основные коэффициенты) проставляются в левую часть уравнения (межмолекулярная ОВР), затем уравнивают элементы изменившие степень окисления в правой части уравнения:
3 MnS +8 HNO3 3 MnSO4 + 8 NO + H2O
5. В последнюю очередь уравнивают атомы Н.
3 MnS +8 HNO3 2 MnSO4 + 8 NO + 4 H2O
6. Для проверки - подсчитывают число атомов кислорода в левой и правой частях уравнения.
В левой части уравнения 24 атома кислорода, в правой части – то же 24 атома кислорода.
Последовательность:
- Основные коэффициенты;
- Металлы;
- Неметаллы;
- Н;
- Проверка по О.
Пример 2. При составлении полуреакций окисления и восстановления следует исходить из общего числа атомов, изменивших степень окисления.
Sn+2Cl2 + K2Cr2+6O7 + HCl Sn+4Cl4 + Cr+3Cl3 + KCl + H2O
В левой части уравнения 2 атома хрома, поэтому число принятых электронов рассчитывается с учетом этого.
Sn+2 - 2 Sn+4 2 6 3 - окисление
2Cr+6 + 23 2Cr+3 6 1 - восстановление
SnCl2 – восстановитель;
K2Cr2O7 – окислитель.
Найденные коэффициенты проставляются в левую часть уравнения, т.к. ОВР является межмолекулярной.
3Sn+2Cl2 + 1K2Cr2+6O7 + 14HCl
3Sn+4Cl4 + 2Cr+3Cl3 + 2KCl + 7H2O
Пример 3. Если число атомов, изменивших степень окисления больше 2, то коэффициенты определяют по сумме отданных и принятых электронов:
As2S3 + HClO3 + Н2О H3AsO4 + H2SO4 + HCl
As2+3S32 + HCl+5O3 + Н2О
H3As+5O4 +H2S+6O4 + HCl
Степень окисления изменяют 3 атома :
S, As, Cl.
2As+3 - 2•2 2 As+5 4 28 84 3 – ок-ие
3S2 - 3•8 3S+6 24
Cl+5 + 6 Cl 6 6 14 - вос-ие
3As2S3 + 14HClO3 + 18Н2О 6H3AsO4 +
9 H2SO4 + 14HCl
As2S3 – восстановитель;
HClO3 – окислитель.
Основы электрохимии
Если погрузить Ме в водный раствор его соли, то «+» ионы, находящиеся на поверхности металла, гидратируются и некоторое количество ионов переходит в раствор. В результате на пластине образуется избыток электронов, она заряжается «-»
Между металлом и раствором устанавливается равновесие:
МТВ + nН2О - z М(Н2О)nz+
Катионы, притягиваясь к отрицательно заряженной пластине, концентрируются вблизи нее. Анионы отталкиваются от пластины и их концентрация вблизи электрода будет понижена.
Раствор вблизи поверхности Ме приобретает заряд, противоположный по знаку заряду металла – образуется двойной электрический слой и возникает определенный скачок потенциала, который принято называть электродным потенциалом().
Значение электродного потенциала зависит:
1.От природы металла – чем большей химической активностью обладает металл, тем легче он растворяется, тем отрицательней потенциал;
2. От концентрации ионов металла в растворе – с увеличением концентрации катионов в растворе потенциал становится более положительным;
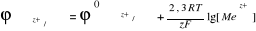
3. От температуры – с повышением температуры потенциал становится более положительным.
Уравнение Нернста
0 – стандартный электродный потенциал металла при стандартных условиях (Т=298 К, [Mez+]=1моль/л) характеризует химическую активность металла, чем активнее металл, тем отрицательней его стандартный электродный потенциал;
R – универсальная газовая постоянная, R=8,314 Дж/(моль К);
Т- абсолютная температура, К;
z – число электронов, участвующих в электродном процессе;
F –число Фарадея, F= 96500 Кл;
[Mez+] – молярная концентрация ионов металла в растворе, моль/л.
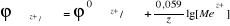
R=8,314 Дж/(моль К)
Т = 298 К
Измерение электродных потенциалов.
Стандартный водородный электрод
Измерить абсолютную величину электродного потенциала невозможно. Относительные значения измеряют в сравнении с некоторыми эталонными электродами - стандартными или электродами сравнения.
Стандартный водородный электрод
Платиновая пластина, покрытая для увеличения поверхности электрода платиновой чернью, и погруженная в водный раствор серной кислоты с [H+]= 1 моль/л. Через раствор пропускается газообразный водород.
Часть поглощенного платиной водорода переходит в атомарное состояние и в поверхностном слое платины устанавливается равновесие:
Н2 2Н
На границе Pt – H2SO4 устанавливается равновесие:
Н(Г) Н+ +
Водородный электрод ведет себя подобно металлу, погруженному в раствор своей соли. Металлическая платина выполняет роль носителя атомов водорода и проводника электронов, к раствору она безразлична.
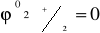
2Н+ + 2 Н2 - эталонный процесс для создания численной шкалы электродных потенциалов.
Не стандартные условия:
2Н+/Н2 = 0,059 lg[H+] = -0,059рН
Электрохимический ряд напряжений металлов
По отношению к стандартному водородному электроду выражают потенциалы всех других электродов - собирают гальванический элемент из стандартного водородного электрода и металла, потенциал которого измеряют.
Измеренная ЭДС равна стандартному электродному потенциалу металла, если концентрация его катионов равна 1 моль/л.
Расположив все металлы в порядке возрастания значений стандартных электродных потенциалов получают электрохимический ряд напряжений металлов:
|
Ме
|
K
|
Mg
|
Al
|
Zn
|
Fe
|
Ni
|
Sn
|
Pb
|
H
|
Cu
|
Ag
|
Pt
|
|
0,В
|
-2,92
|
-2,38
|
-1,66
|
-0,76
|
-0,44
|
-0,23
|
-0,14
|
-0,13
|
0
|
0,34
|
0,8
|
1,2
|
Положение металла в Ряду характеризует его способность к окислительно - восстановительному взаимодействию в водных растворах при стандартных условиях.
Из ряда напряжений следует:
- Восстановительная активность свободных металлов убывает слева направо;
- Восстановительная активность катионов металлов возрастает слева направо;
- Каждый металл вытесняет из растворов солей все другие металлы, стоящие в Ряду правее него;
- Первые члены Ряда (до Mg включительно) вытесняет водород из воды;
- Металлы, стоящие в Ряду от Mg до Н, вытесняют водород из разбавленных растворов кислот (за исключением HNO3);
- Металлы, стоящие в Ряду после водорода, не способны вытеснять водород из раствора кислот;
- Самопроизвольно могут протекать те реакции, в которых восстановитель имеет более отрицательный потенциал, чем окислитель;
Гальванические элементы
ОВР связаны с переносом электронов, поэтому их можно использовать для получения электрического тока.
Приборы, преобразующие химическую энергию в электрическую, называются гальваническими элементами(ГЭ) или химическими источниками электрической энергии (ХИЭЭ).
ХИЭЭ:
- Гальванические элементы;
- Аккумуляторы;
- Топливные элементы.
ГЭ – система, в которой происходит самопроизвольная ОВР (G<0), энергия которой превращается в электрическую.
ГЭ - электрохимическая система, из 2 электродов, растворы которых между собой соединены с помощью солевого мостика – стеклянной трубки, заполненной раствором соли (KCl или NaCl).
Солевой мостик (электрохимический ключ) препятствует смешиванию растворов, проводит электрический ток.
I ZnSO4 II CuSO4
Медно-цинковый гальванический элемент (элемент Якоби-Даниэля)
Если электрическая цепь замкнута, то в области I происходит окисление цинка, на поверхности пластины атомы Zn превращаются в ионы и переходят в раствор, цинковая пластина постепенно растворяется.
Электрод, на котором протекает процесс окисления, называется анодом.
Zn0 Zn+2 + 2 – анодный процесс
Образовавшиеся при этом свободные электроны движутся по внешней цепи к медному электроду.
В области II, на медном электроде, происходит восстановление ионов меди.
Электроны, переходящие по внешней цепи от цинкового электрода, соединяются с катионами меди из раствора, образуется атомы меди – масса медной пластины увеличивается.
Электрод, на котором протекают процессы восстановления, называется катодом.
Cu+2 + 2 Cu0 – катодный процесс
Суммарное уравнение токообразующей реакции:
Cu+2 + Zn0 Cu0 + Zn+2
CuSO4 + Zn0 Cu0 + Zn SO4
При работе ГЭ область II обедняется катионами меди, область I обогащается катионами цинка. Раствор в области II заряжается «-», а в области I – «+».
Создается электрическое поле, в котором катионы движутся к медному электроду, а анионы (SO42—) – к цинковому электроду по солевому мостику.
В итоге растворы в областях I и II остаются электронейтральными.
При схематической записи ГЭ вертикальными линиями разделяют те фазы, на границе раздела которых возникают скачки потенциалов, две вертикальные линии- солевой мостик:
Zn | ZnSO4 || CuSO4 | Cu
Максимальное значение напряжения ГЭ, соответствующее обратимому проведению процесса, называется электродвижущей силой (ЭДС) гальванического элемента (Е, В).
Е = UMAX
Е= (катода) – (анода)
Если соблюдаются стандартные условия, ЭДС элемента называется стандартной (Е0, В):
Е0= 0(катода) – 0(анода)
Электролиз
Электролиз - окислительно-восстановительные процессы, которые протекают под действием постоянного электрического тока, проходящего через раствор или расплав электролита.
Электролиз – процесс, противоположный работе ГЭ, он протекает с поглощением энергии.
Электролиз расплава хлорида магния
MgCl2 Mg2+ + 2Cl—
«-« Катод: Mg2+ + 2 Mg0
«+» Анод: 2Cl— - 2 Cl20
Суммарная реакция электролиза расплава хлорида магния:
MgCl2 Mg0 + Cl20
Электрод, на котором происходит восстановление, называется катодом, но в электролизе он заряжен «-».
Электрод, на котором протекает окисление, называется анодом, заряжен он «+».
Электролиз водных растворов электролитов
- На катоде будут восстанавливаться окисленные формы тех систем, которые имеют наибольшее значение электродного потенциала.
- На аноде будут окисляться те системы, которые имеют наименьшее значение электродного потенциала.
Катодные процессы
При рассмотрении этих процессов необходимо учитывать потенциал процесса восстановления водорода 2Н+ + 2 Н2:
2Н+/Н2 = 0,059 lg[H+] = -0,059рН
Нейтральная среда (рН=7):
2Н+/Н2 = -0,059•7= - 0,41В
- Металлы, стоящие в ряду напряжений до Al (Ti) включительно не восстанавливаются при электролизе водных растворов, т.к. их потенциал меньше, чем — 0,41В. В этих случаях на катоде образуется водород:
Среда нейтральная (рН=7):
2Н2О + 2 Н2 +2ОН—
Среда кислая (рН<7):
2Н+ + 2 Н2
- Металлы, стоящие в Ряду от Sn до конца , имеют 0 > - 0,41В, и из нейтральных растворов электролитов они будут восстанавливаться на катоде.
- Для металлов средней части Ряда, у которых 0 ~ — 0,41В, необходимо учитывать условия проведения электролиза (концентрацию, температуру).
-
Анодные процессы
Различают электролиз с активным (растворимым) и электролиз с инертным (материал, которого не претерпевает изменений в ходе электролиза) анодами.
Инертные аноды: угольные, графитовые, платиновые аноды, аноды из нержавеющей стали.
Анионы образуют собственный ряд напряжений, в котором слева направо увеличивается значение стандартного электродного потенциала:
Cl— S—2 I— Br— OH— (Н2О) SO42— NO3— NO2— F—0
- При электролизе водных растворов щелочей, кислородсодержащих кислот и их солей, фтороводорода и фторидов происходит электрохимическое выделение кислорода.
Щелочная среда (рН>7):
4ОН— О2 + 2Н2О + 4
Нейтральная среда (рН>7):
2Н2О О2 + 4Н+ + 4
- При электролизе водных растворов безкислородных кислот и их солей у анода будут разряжаться анионы этих кислот.
- Анод растворимый - в число конкурирующих процессов включают окисление материала анода.
Будет протекать тот процесс, который характеризуется наименьшим значением электродного потенциала.
Электролиз раствора CuCl2 с инертным анодом
Катод «-»
1) Cu2+ + 2 Cu0 ; 01=0,34В
2) 2Н2О+2Н2+2ОН—; 02=- 0,41в
01 > 02 – на катоде будет протекать восстановление меди.
Анод «+»
2Cl— - 2 Cl20 ;
2Н2О - 4 О2 + 4Н+ ;
на аноде будут разряжаться хлорид-ионы.
Суммарное уравнение электролиза:
CuCl2 + Н2О Cu0 + Cl20 + Н2О
Электролиз раствора CuCl2 с медным анодом
Катод «-»
1) Cu2+ + 2 Cu0 ; 01=0,34В
2) 2Н2О+2Н2+2ОН—; 02=- 0,41в
01 > 02 – на катоде будет протекать восстановление меди.
Анод (Cu) «+»
1)2Cl— - 2 Cl20 ; 01
2)2Н2О - 4 О2 + 4Н+; 02
3) Cu0 - 2 Cu2+ ; 03= 0,34В
03 < 01 < 02 - будет окисляться материал анода.
Суммарное уравнение электролиза:
Cu0 + CuCl2+ Н2О Cu0 + CuCl2+ Н2О
Электролиз сводится к переносу меди с анода на катод, такие процессы применяются для очистки (рафинирования) металлов.
Законы электролиза
С количественной стороны процесс электролиза был впервые изучен в 30-х гг. 19 века английским физиком Майклом Фарадеем (1791 г. - 1867 г.)
Первый закон Фарадея:
Масса вещества, выделившегося при электролизе, пропорциональна количеству электричества, прошедшего через электролит.
Второй закон Фарадея:
Одинаковые количества электричества выделяют на электродах эквивалентные массы различных веществ.
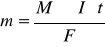
Для выделения на электроде 1 эквивалента любого вещества необходимо через электролит пропустить 96500 Кл электричества.
МЭ – эквивалентная масса, г/моль;
I - сила тока, А;
t – время проведения процесса, с;
F = 96500 Кл - число Фарадея .
1 F = 96500 Кл = 96500 А•с= 26,8 А•час
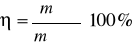
1Фарадей – это заряд, который несет на себе 1 моль электронов или 1 моль однозарядных ионов. Количественной характеристикой полноты использования тока является выход по току ():
Применение электролиза
- Получение металлов – выделение в чистом виде алюминия и щелочных, щелочноземельных металлов производится электролизом расплавов, а остальных металлов – электролизом водных растворов.
- Очистка металлов – электролиз проводят с активным (растворимым) анодом.
- Получение различных химических веществ
- Зарядка аккумулятора – при разрядке аккумулятор работает как гальванический элемент, а зарядка -это процесс электролиза.
- Получение металлических покрытий – в декоративных целях, для защиты от коррозии, повышения твердости и электропроводности производят осаждение металла электролизом водного раствора соли, покрываемое изделие выполняет роль катода.
- Защита от коррозии – защита основана на электролизе, при котором защищаемый объект играет роль катода, на котором происходит восстановление воды.
Коррозия металлов
Коррозия - разрушение металлов под воздействием окружающей среды.
Коррозия металлов - процесс окисления:
Ме - z Меz+
Коррозия – процесс самопроизвольный (G<0) и не может быть полностью предотвращен, однако существует ряд методов, позволяющих ее замедлить.
По механизму коррозия делится на химическую и электрохимическую.
Химическая коррозия – разрушение металлов в результате химического взаимодействия с окружающей средой.
Химическая коррозия делится:
- газовая (протекает при высоких температурах на воздухе, в присутствии газов-галогенов);
- коррозия в агрессивных средах – неэлектролитах (сернистая нефть).
При нагревании стальных изделий на воздухе их поверхность покрывается темным слоем окалины – продуктов окисления (оксида или гидраксида), которые препятствуют дальнейшей диффузии окислителя к металлу и замедляет коррозию.
Пример:
Предметы из меди и ее сплавов при длительном хранении покрываются зеленым налетом основной соли:
2Cu + O2 + H2O + CO2 = (CuOH)2CO3
Скорость химической коррозии зависит от свойств пленки и окислителя, и температуры.
Сплошную оксидную пленку, предотвращающую дальнейшую коррозию, дают такие металлы как Al, Zn, Cr.
Если пленка рыхлая, то замедляется процесс отвода тепла от металла, металл разогревается - скорость коррозии увеличивается.
Электрохимическая коррозия – разрушение металла под действием окружающей среды в результате возникновения гальванических пар.
Характерна для сред, проводящих электрический ток - протекает в электролитах, в атмосфере влажного газа, в почве.
Чаще всего причиной электрохимической коррозии является вода и растворенный в ней кислород, электродный потенциал этой системы равен 0,815 В, и она может окислять многие металлы.
Электрохимическая коррозия – разрушение металла под действием окружающей среды в результате возникновения гальванических пар.
Характерна для сред, проводящих электрический ток - протекает в электролитах, в атмосфере влажного газа, в почве.
Чаще всего причиной электрохимической коррозии является вода и растворенный в ней кислород, электродный потенциал этой системы равен 0,815 В, и она может окислять многие металлы.
Закономерности электрохимической коррозии:
- разрушается более активный металл;
- в кислой среде на поверхности менее активного металла выделяется водород;
- в нейтральной и щелочной средах на менее активном металле происходит восстановление молекулярного кислорода с образованием гидроксид - ионов.
Используемые в технике металлы, как правило, химически неоднородны, содержат примеси других металлов. Это является причиной возникновения микроГЭ, и следовательно, электрохимической коррозии.
Железо – активный металл и по отношению ко многим примесям (Sn, Pb, Ni, Cu и др.) выступает в роли анода.
Пример: коррозии железа в контакте с медью в кислой среде.
Образуется ГЭ: (-) Fe | HCl | Cu (+).
Железо более сильный восстановитель, чем медь, оно будет окисляться. Электроны переходят от железа к меди, перемещаются к поверхности меди, где будут восстанавливаться ионы водорода
Анод: Fe - 2 Fe2+
Катод: 2Н+ + 2 Н2 ( на поверхности меди)
Fe + 2Н+ Н2+ Fe2+
Пример: коррозия (ржавление) железа в нейтральной среде
Анод: Fe - 2 Fe2+
Катод: О2 + 2 Н2О +4 4 ОН—
Fe2+ + 2ОН— Fe(ОН)2
4Fe(ОН)2 + О2 + 2Н2О 4Fe(ОН)3
2Fe(ОН)3 Fe2О3 • Н2О + 2Н2О
Методы защиты от коррозии:
- Окраска металлических изделий, покрытие полимерными пленками (полиэфирными, эпоксидными);
- Оксидирование – получение на металлической поверхности плотного оксидного слоя (анодирование алюминия);
- Нанесение металлических покрытий – катодные покрытия - покрытие менее активным металлом, для железа используют покрытия оловом, никелем, медью;
- анодные покрытия - покрытие более активным металлом, который при нарушении целостности покрытия будет разрушаться, а основной металл останется невредимым;
- Протекторная защита – для защиты подземных трубопроводов, паровых котлов, корпусов кораблей – на некотором расстоянии от защищаемого металла устанавливается анод из более активного металла – искусственно создается ГЭ, в котором окисляться будет более активный металл, а защищаемое изделие останется невредимым.
Эффективный метод, металлическое изделие сохраняется в течение многих лет
- Электрозащита (катодная защита) – защищаемый объект присоединяют к «-» полюсу источника постоянного тока, «+» полюс присоединяют к расположенному вблизи куску металла – используется процесс электролиза;
- Применение ингибиторов коррозии – веществ, которые, адсорбируясь на поверхности металла, делают потенциал более положительным, тем самым замедляя коррозию.
Окислительно - восстановительные реакции (ОВР)