Синтез азокрасителя
Содержание
Введение
I Общие сведения об азокрасителях
1.1 Общая характеристика
1.2 Деление азокрасителей по группам
1.3 Классификация азокрасителей
1.3.1 Классификация по способу применения
1.3.2 Классификация по химической структуре
1.3.3 Классификация Степанова Б. И
II Синтез азокрасителя
2.1 Условия получения азокрасителя в лабораторных условиях
2.2 Диазотирование
2.3 Азосочетание
2.3.1 Механизм реакции
2.3.2 Условия проведения реакции
2.4 Выделение красителя
2.5 Синтез ализаринового жёлтого
Заключение
Список литературы
Введение
Области применения органических красителей очень многочисленны и разнообразны. Их применяют для окрашивания пряжи и ткани самого различного вида: льняных, шерстяных, хлопчатобумажных, шёлковых, из искусственных и синтетических волокон. Органическими красителями окрашивают кожу, мех, дерево, бумагу, различные виды пластмасс, резину, пищевые продукты и т.д. Отрасль химической промышленности, производящая органические красители и промежуточные продукты, необходимые для их производства, называется анилинокрасочной промышленностью. Название это сложилось исторически, так как первые синтетические красители были получены из анилина.
I. Общие сведения об азокрасителях
1.1 Общая характеристика
Красители — химические соединения, обладающие способностью интенсивно поглощать и преобразовывать энергию электромагнитного излучения в видимой и в ближних ультрафиолетовой и инфракрасной областях спектра и применяемые для придания этой способности другим телам..
Отличительная особенность красителя — способность пропитывать окрашиваемый материал (например, текстиль, бумагу, мех, волосы, кожу, древесину, пищу) и давать цвет по всему его объёму.
Азокрасители — органические соединения, содержащие одну или несколько азогрупп, например конго красный, метиловый оранжевый, -нафтолоранж и другие. Органические красители, в молекулах которых содержится одна или несколько азогрупп —N=N—, связывающих ароматические радикалы. Обычно азокрасители в ароматическом ядре содержат замещенные или незамещённые группы NH2 и OH, а также NO2, Cl, S03H, COOH и др. Кислотные группы обусловливают растворимость А. в воде.
Синтез азокрасителей основан на сочетании ароматических диазосоединений ArN2Cl с фенолами, ароматическими аминами или их производными, например:
1.2 Деление азокрасителей по группам
В зависимости от растворимости, химической природы и особенностей взаимодействия с окрашиваемыми материалами азокрасители делят на следующие группы:
1. Пигменты (азопигменты. Как правило, молекулы пигментов содержат NO2, Cl, CH3, CH3O, (C2H5)2NSO2 и др. заместители. Иногда пигменты наносят на минеральные субстраты, напр. Аl(ОН)3, BaSO4, мел, часто с добавками минеральных наполнителей для понижения интенсивности окраски.
2. Жиро-, спирто- и ацетонорастворимые азокрасители по химическому строению аналогичны пигментам; не растворимы в воде, хорошо растворимы в органических растворителях, моторных топливах, жирах, маслах и т.п.
3. Дисперсные азокрасители - обычно моноазокрасители; плохо растворимы в воде, растворимые в органических растворителях и полимерах.
4. Основные и катионные азокрасители содержат в молекуле основные или ониевые группы, например красный азокраситель (IX); растворимый в воде с образованием цветных катионов.
5. Кислотные азокрасители- чаще всего моноазокрасители и дисазокрасители, содержащие одну или несколько групп SO3H; растворяются в воде с образованием цветных анионов.
6. Лаки (азолаки) - не растворимые в воде соли (обычно Ва или Са) некоторых кислотных азокрасителей. Применяются для тех же целей, что и пигменты.
7. Хромовые (протравные) азокрасители характеризуются наличием групп SO3H (реже СООН), придающих растворимость в воде, и в орто-орто'-положениях к азогруппе - групп ОН, NH2 или СООН, которые при крашении могут образовывать с Сr3+ внутрикомплексные соединения, например - хромовый сине-черный .
8. Прямые азокрасители - в основном дис- и полиазокрасители., например прямой ярко-оранжевый. Обладают сродством к целлюлозным волокнам благодаря ван-дер-ваальсовому взаимодействию и водородным связям между группами красителя (ОН и NH2, атомы N гетероциклов и особенно NH—СО) и группами ОН целлюлозы.
9. Активные азокрасители обычно растворимы в воде; содержат группировки, которые при крашении вступают в химическую реакцию с молекулами субстрата, с образованием ковалентных связей, благодаря чему окраски устойчивы к мокрым обработкам и трению.
10. Азогены – нерастворимые азокрасители, образующиеся непосредственно на волокне сочетанием диазосоединений с азосоставляющими.
11. Металлсодержащие азокрасители - внутрикомплексные соединения азокрасителя с Сu2+ , Сr3+ , Со3+, реже с Ni2 + и Fe2+. По свойствам и способам применения относятся к кислотным, дисперсным, активным и прямым красителям. Окраски отличаются повышенной светостойкостью и другими ценными свойствами.
1.3 Классификация азокрасителей
Краситель - это вещество, которое – по крайней мере на какой-то стадии обработки - обладает внутренним сродством к окрашиваемому материалу.
Пигмент - это вещество, применяемое для придания окраски поверхности ткани. Пигменты могут быть как органическими, так и неорганическими веществами.
Красители можно классифицировать как по способу применения, так и по химической структуре.
1.3.1 Классификация по способу применения
В текстильной промышленности обычно используются красители восьми основных классов. Первые пять классов красителей (прямые, сернистые, реактивные и т.д.) используются в основном для крашения целлюлозных волокон, например хлопковых и вискозных. Последние три класса красителей (кислотные, основные и дисперсные) применяются для крашения других натуральных и синтетических волокон.
Прямые красители. Эти анионные водорастворимые красители называются так потому, что обладают высоким сродством к целлюлозным волокнам и могут применяться без вспомогательных химических средств. Прямые красители широко используются для крашения хлопковых и вискозных тканей. Их наибольшее достоинство – простота применения, а недостаток в том, что в ряде случаев они неустойчивы к мокрым обработкам. Сернистые красители - это органические соединения, получаемые нагревом соединений из группы аминов или фенолов в присутствии серы. В процессе обработки сернистыми красителями используются химические реакции восстановления и окисления. Наибольшее достоинство сернистых красителей – низкая стоимость. К недостаткам относятся невысокая яркость и, в некоторых применениях, низкая устойчивость к мокрым обработкам и воздействию света.
Реактивные красители. Реактивные красители, иногда называемые активными или волоконно-реактивными, разработаны в 1950-х годах. Реактивные красители образуют химическое соединение с волокном и становятся его частью. Поскольку связь между красителем и волокном прочна, реактивные красители очень устойчивы к мокрым обработкам, что является их основным достоинством. Реактивные красители, как правило, дороже прямых, сернистых и азоидных. Устойчивость реактивных красителей к воздействию хлора и других отбеливателей иногда бывает невысокой.
Кислотные красители. Кислотные красители называются так потому, что содержат в своей структуре кислотные группы. Кислотные группы красителя реагируют с основными группами белковых (шерсть и шелк) и полиамидных (найлон) волокон с образованием связей между красителем и волокном через органические солевые группы. Эти связи прочны и придают окраске высокую устойчивость к мокрым обработкам.
Основные красители. Эти красители иногда называют катионными, потому что молекула красителя содержит положительный заряд. Недостаток основных красителей – низкая устойчивость окраски к свету, особенно для белковых волокон.
Дисперсные красители. Дисперсные красители используются в основном для крашения полиэфирных, полиамидных и ацетилцеллюлозных волокон, хотя они могут окрашивать и другие волокна. Дисперсные красители почти нерастворимы в воде и должны быть диспергированы в ней для образования красильной ванны.
1.3.2 Классификация по химической структуре
В молекулах красителей присутствуют разнообразные структурные группы. Однако свыше половины всех красителей можно классифицировать как азокрасители или антрахиноновые красители.
Азокрасители. Азогруппы, т.е. два атома азота, соединенные двойной связью, обусловливают цвет свыше половины всех промышленно производимых красителей. Азогруппа -N=N- является сильным хромогеном, и поэтому азокрасители обычно обладают высокой красящей способностью. Молекулы азокрасителей могут содержать от одной до четырех, а иногда и больше азогрупп. Все азокрасители – синтетические соединения, не имеющие натуральных аналогов. Число теоретически возможных молекул с азогруппами чрезвычайно велико.  Получают азокрасители способам, общими для всех азосоединений, главным образом азосочетанием:
Получают азокрасители способам, общими для всех азосоединений, главным образом азосочетанием:
1.3.3 Классификация Б.И. Степанова
Б. И. Степановым разработана новая классификация красителей, опирающаяся на признаки общности хромофорных систем красителей, а порядок чередования классов определяется последовательным усложнением хромофорных систем. По сходству строения красителей, их химических свойств и методов применения все синтетические красители разделены на следующие классы:
Нитро- и нитрозокрасители.
Полиметиновые красители.
Арилметановые красители.
Хинониминовые красители.
Азокрасители.
Азометиновые красители.
Антрахиноновые красители.
Антрапиридиновые красители.
Кубовые красители.
Индигоидные и тиоиндигоидные красители.
Антрахиноновые и другие кубовые красители.
Периноновые красители.
Полициклохиноновые красители.
Сернистые красители.
Фталоцианиновые красители.
Флуоресцентные (оптические) отбеливатели.
II. Синтез азокрасителя
2.1 Условия получения азокрасителей в лабораторных условиях
В настоящее время группа азокрасителей включает самый большой и самый разнообразный ассортимент искусственных органических красителей. Основные условия получения азокрасителей в лабораторных условиях
1. Применение чистых исходных веществ.
2. Точное соблюдение относительных количеств реагирующих веществ.
3. Энергичное и постоянное перемешивание или встряхивание при проведении реакций диазотирования и сочетания.
4. Защита диазосоединений от нагревания и света. Применение диазосоединений непосредственно после их получения.
2.2 Диазотирование
Диазотирование протекает по уравнению:
Одна свободная сульфогруппа замещает моль соляной кислоты например:
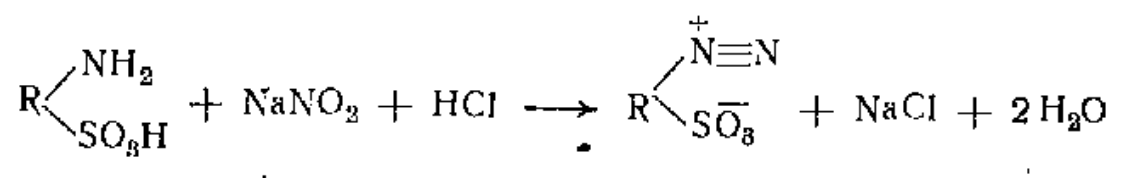
2.3 Азосочетание
Взаимодействие диазосоединений с ароматическими аминами и фенолами, сопровождающееся образованием веществ, содержащих азогруппу —N = N—, связанную с двумя ароматическими радикалами, называют азосочетанием.
Диазосоединения получили название диазосоставляющих реакции азосочетания, а амины или фенолы — азосоставляющей.
2.3.1 Механизм реакции
Установлено, что реакция азосочетания протекает по механизму электрофильного замещения, в котором атакующим агентом выступает ион диазония (Аг—N=N),а субстратом — ароматические системы, содержащие в п- или о-положении заместители NH2, NHAlk, NHAr, N(Alk)2, NHSO3H, NHNO2, ОН и в некоторых случаях OAlk:
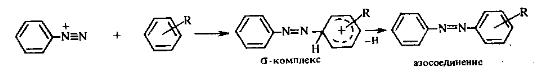
2.3.2 Условия проведения реакций
Для осуществления реакции азосочетания готовят два компонента: диазосоединение и азосоставляющий реагент. Чрезвычайно важным фактором является рН среды.
Как правило, для получения азосоединений охлажденный раствор соли диазония постепенно, при энергичном перемешивании, прибавляют к охлажденному раствору азокомпонента. Если диазосоединение нестабильно, порядок прибавления реагентов обратный.
Азосочетание часто проводят без охлаждения компонентов, особенно в тех случая, когда диазосоединение является стабильным и мало реакционноспособным, как, например, диазосоединения нафталина.
Для повышения скорости реакции сочетания на практике прибегают также к увеличению концентрации реагентов.
Реакцию сочетания осуществляют с таким расчетом, чтобы в реакционной смеси всегда был избыток азосоставляющей. Ее проводят следующим образом: на фильтровальную бумагу наносят каплю реакционной массы, к которой добавляют раствор натриевой соли 2-нафтол-3,6-дисульфокислоты (R-соль). Отсутствие окраски (образования красителя) указывает на то, что условия сочетания выдержаны.
2.4 Выделение азокрасителей
Если краситель мелкодисперсный, то прибегают к высаливанию: в реакционную смесь добавляют хлорид натрия из расчета 200 г на 1 л раствора. Этот способ используется также и в том случае, когда краситель хорошо растворим. При наличии в азосоединениях солеобразных групп, придающих продукту хорошую растворимость в воде, для выделения красителя в реакционную смесь добавляют кислоту.
2.5 Синтез ализаринового (протравного) жёлтого
Реактивы для синтеза: м-нитроанилин — 2,5 г., соляная кислота ( —1,19 г/см')— 10.1 г (8,5 мл); нитрит натрия— 1,5 г; салициловая кислота —2.5 г. ,карбонат натрия — 7,5 г; хлорид натрия, 10%-ный раствор.
Посуда и оборудование: стакан вместимостью 100 мл; стакан фарфоровый вместимостью 200 мл; воронка капельная; мешалка; термометр; баня ледяная.
В стакане растворили 2,5 м-нитроанилина в разбавленной соляной кислоте (8,5 мл концентрированной НС1 в 40 мл воды). Для полного растворения содержимое слегка нагревали. Охладив полученную смесь до 0°С, ее диазотировали, добавляя по каплям из капельной воронки раствор 1,5 г нитрита натрия в 5 мл воды. Следили за тем, чтобы температура не поднималась выше 5°С. Диазораствор при хорошем размешивании приливали к находящемуся в фарфоровом стакане при 0°С раствору 2,5 г салициловой кислоты и 7,5 г карбоната натрия в 40 мл воды. Жёлтый осадок красителя отфильтровали, слегка промыли 10%-ным раствором хлорида натрия и сушили при 40-50°С.
Химизм процесса состоит в следующем:
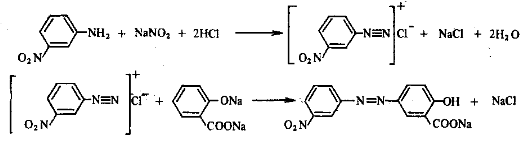
(C13H8N3Na05 ).
Выход 3,6 г (около 64% от теоретического).
Полученный нами краситель – ализариновый (протравный) жёлтый (З-карбокси-З'-нитро-гидроксиазобензол) — жёлтый азокраситель, в виде натриевой соли хорошо растворим в воде. Малорастворим в воде и 95 % спирте, легко растворим при нагревании.
Переход окраски раствора от светло-желтой к красно-оранжевой в интервале рН 10,0—12,0.
Раствор индикатора – это 0,1 % раствор.
Приготавливают его путём растворения 0,1 г индикатора в 100 мл воды. Растворение проводят при нагревании на водяной бане.
Заключение
Синтетические красители заняли в мире современного человека пусть не самое важное, но значимое место. Ведь большинство изготовленных человеком предметов, которые мы – люди используем в повседневной жизни, или которые просто украшают наш интерьер, будут более приятны в эксплуатации, если им придать определённую окраску. Примерно за 150 лет были изучены их свойства, отработаны различные способы их получения, предложены интересные теории, объясняющие способность красителя нести и передавать свою неповторимую окраску.
На тему синтетических красителей сегодня имеется масса научной литературы, где можно найти всё: от истории развития до поставленных методик получения, причём объём той литературы постоянно пополняется; масса предприятий занимается выпуском красителей и крашением текстильных и других материалов, создавая столь необходимые на сегодняшний день рабочие места для наших современников и для нас.
Список литературы
1. Бородкин В. Ф. Химия красителей .—М.: Химия, 1981. — 248 с.
2. Г. Э. Фирц-Давид, Л. Бланже. Основные процессы синтеза красителей. —М.: Изд-во иностр. Литературы, 1957. —382 с.
3. Чекалин М. А., Пассет Б. В., Иоффе Б. А.Технология органических красителей и промежуточных продуктов: Учебное пособие для техникумов.— 2-е изд., перераб. —Л.: Химия, 1980. 472 с, ил.
4. Мельников Б. Н. Виноградова Г. И. Применение красителей. Учеб. для вузов — М.: Химия, 1986.— 240 с.
5. Ч. Дж. Овербергер, Ж-П. Анселм, Дж. Г. Ломбардино. Органические соединения со связями «азот —азот». — Л.:, Химия, 1970. — 128 с.
6. Орлова О. В., Фомичева Т. Н. Технология лаков и красок: Учебник для техникумов. — М., Химия, 1990.— 384 с; ил.
7. www.roshimprom.ru
Синтез азокрасителя