Реабилитация больных после эндопротезирования межпозвоночного диска
ПОЯСНИТЕЛЬНАЯ ЗАПИСКА
ПензГТУ ___________________ПЗ
(шифр документа)
к выпускной квалификационной работе на тему:
Реабилитация больных после эндопротезирования межпозвоночного диска
Выпускную квалификационную работу разработал
студент группы _________М. А. Ганич___________________________________________
(подпись, дата)
Пояснительная записка и все материалы ВКР проверены
Руководитель А. И. Сафронов
Оценка руководителя – «________________________» _________________________________
(подпись, дата)
Выпускную квалификационную работу допустить к защите в ГАК
Заведующий кафедрой ____________________________________
Дата защиты ____________________2015 г.
Декан факультета ________________________________________
Выпускная квалификационная работа защищена с оценкой «_________________________»
протокол № _________ от «______» _______________________ 2015 г.
Секретарь ГАК _________________
г. Пенза
МИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
«Пензенский государственный технологический университет»
(ПензГТУ)
|
|
“УТВЕРЖДАЮ”
Заведующий кафедрой “_____________________________________”
“ __10__ ” _____марта____________2015 г.
|
ЗАДАНИЕ
на выпускную квалификационную работу
1. Студент группы гр.11ПБ1б факультета _________ФБПТС________ специальности (направления подготовки) ___Информационные технологии и менеджмент в медицинских и биотехнических системах
______ Ганич Максим Андреевич _ ____ _______
(фамилия, имя, отчество)
- Руководитель дипломного проекта Сафронов Алексей Иванович___ ___ (фамилия, имя, отчество, ученая степень, ученое звание, должность, место работы полностью)
Время выполнения дипломного проекта с 16 марта 2015 г. по 05 июля 2015 г._____________________
Место преддипломной практики ФГБОУ ВПО ПензГТУ,кафедра ИТММБС________________________________
Тема дипломного проекта
_ _ _________ Реабилитация больных после эндопротезирования межпозвоночного диска _
Тема утверждена приказом проректора по учебной работе от “ 10 ” марта 2015 г. № 23/05-04-04-08 .
|
6. Техническое задание на выполнение ВКР.
|
|
Изучить лечебно-диагностический процесс у больных после эндопротезирования межпозвоночного диска и предложить аппаратное обеспечение мониторинга реабилитационного периода у этой категории больных;
|
- Изучить общие проблемы эндопротезирования межпозвоночного диска.
|
- Проанализировать реабилитационный период у больных после эндопротезирования межпозвоночного диска.
|
- Предложить вариант аппаратного мониторинга критических параметров в период реабилитации
|
7. Цель ВКР выявление особенностей применения аппаратного мониторинга параметров реабилитации________________________________________________________________________
8. Основные требования к работе дать определение основным понятиям и терминам, привести примеры заболеваний, связанных эндопротезирование межпозвоночного диска, изучить общие проблемы эндопротезирования межпозвоночного диска, предложить вариант аппаратного мониторинга критических параметров в период реабилитации ________________________________________________________
9. Объем и содержание основной части дипломного проекта
9.1 Содержание пояснительной записки (перечень вопросов, подлежащих разработке, расчетов, обоснований, описаний)
ВВЕДЕНИЕ
1 ФИЗИОЛОГИЧЕСКИЕ ОСНОВЫ ВЕНТИЛЯЦИИ ЛЕГКИХ;
- Некоторые аспекты физиологии дыхания
- Вентиляция легких
- Обобщенная схема классификации систем замещения утраченных функций пациента
- Примеры заболеваний при которых используются СЗУФ
- Гипповентиляция
- Нормовентиляция
- Брадикардия
- Тахикардия
- Почечная недостаточность
- Нарушение двигательных функций, связанные с патологией концевой пластинки и моторных нервов
- Нарушение двигательных функций, связанные с нарушением функций спинного мозга
- Приборы и средства оценки СЗУФ
- Историческая справка
- Приборы для замещения утраченных функций пациента
- Средства оценки ЗУФ
2 АЛГОРИТМ РАБОТЫ АППАРАТА ИВЛ НА ПРИМЕРЕ ПРИБОРА А-ИВЛ/ВВЛ-ТМ
2.1 Технические характеристики аппарата
2.2 Подготовка к работе аппарата ИВЛ
2.3 Порядок работы аппарата ИВЛ
2.4 Обслуживание аппарата ИВЛ
2.4.1 Техническое обслуживане и ремонт аппарата ИВЛ
2.4.2 Правила хранения и расконсервации
2.5 Современные аппараты искусственной вентиляции легких
3 РАЗРАБОТКА ПРИНЦИПИАЛЬНОЙ ЭЛЕКТРИЧЕСКОЙ СХЕМЫ АППАРАТА ИВЛ
3.1 Структурная схема аппарата ИВЛ
3.2 Разработка процессорного модуля аппарата ИВЛ
3.2.1 Работа с портами
3.2.2 Разработка подсистемы памяти
3.2.3 Актуальность выбора микроконтроллера КР1816ВЕ51
3.3 Перспективы развития аппаратов ИВЛ
ЗАКЛЮЧЕНИЕ
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
ПРИЛОЖЕНИЯ
|
9.2. Графическая часть (перечень и содержание чертежей, плакатов)
|
|
|
1 Цели и задачи ВКР
|
1л формата А4
|
|
2 Анализ объекта исследования
|
1л формата А4
|
|
3 Классификация приборов для ЗУФ пациента
|
1л формата А4
|
|
4 Классификация средств для ЗУФ пациента
|
1л формата А4
|
|
5 Алгоритм работы аппарата ИВЛ
|
1л формата А4
|
|
6 Структурная схема электрического блока
|
1л формата А4
|
|
7 Принципиальная электрическая схема процессорного модуля аппарата ИВЛ
|
1л формата А4
|
|
8 Монтажная схема процессорного модуля аппарата ИВЛ
|
1л формата А4
|
10. Календарный график работ по выполнению дипломного проекта.
|
Наименование этапов работ
|
Объем
работы, %
|
Срок
выполнения
|
Подпись
руководителя
|
|
Изучение теоретических данных о СЗУФ пациента
|
10%
|
16.04.2015 г.
|
|
|
Анализ заболеваний, связанных с применением СЗУФ
|
10%
|
20.04.2015 г.
|
|
|
Обзор приборов для замещения утраченных функций пациента на примере аппаратов ИВЛ
|
10%
|
27.04.2015 г.
|
|
|
Анализ стандартных этапов работы аппарата ИВЛ
|
10%
|
05.05.2015 г.
|
|
|
Разработка принципиальной электрической схемы процессорного модуля аппарата ИВЛ
|
20%
|
15.05.2015 г.
|
|
|
Подбор элементной базы для процессорного модуля аппарата ИВЛ
|
10%
|
20.05.2015 г.
|
|
|
Оформление графической части
|
15%
|
25.05.2015 г.
|
|
|
Оформление ПЗ
|
15%
|
30.05.2015 г.
|
|
Примечание: задание по п.10 должно быть согласовано с руководителем дипломного проекта.
Дата выдачи задания “______” _____________________________ 2015 г.
Руководитель выпускной квалификационной работы _ Сафронов А.И..
(подпись) Инициалы, фамилия
Задание к исполнению принял “_______” __________________________2015 г. _______________________________________________________________________Ганич М.А.
(подпись) (Инициалы, фамилия студента)
АННОТАЦИЯ
Выпускная квалификационная работа на тему «Реабилитация больных после эндопротезирования межпозвоночного диска» состоит из пояснительной записки и графической части.
Основная часть пояснительной записки к выпускной квалификационной работе посвящена: рассмотрению основных заболеваний, связанных с применением эндопротезирования межпозвоночных дисков, изучить лечебно-диагностический процесс у больных после эндопротезирования межпозвоночного диска, предложить аппаратное обеспечение мониторинга реабилитационного периода у этой категории больных.
Графическая часть выпускной квалификационной работы выполнена на 10 листах формата А4.
Результаты исследований предназначены для применения в учебном процессе специальности «Биотехнические и медицинские аппараты и системы».
Выпускная квалификационная работа выполнена в соответствии с требованиями технического задания на исследование реабилитации больных после эндопротезирования межпозвонковых дисков.
РЕФЕРАТ
Пояснительная записка к дипломной работе на тему «Реабилитация больных после эндопротезирования межпозвоночного диска» объёмом 57 листов, содержит 16 рисунков,1 таблицу, 24 использованных источников.
Объектом исследования являются межпозвоночные диски, мониторинг реабилитационного периода.
Целью дипломного проектирования является предложение аппаратного обеспечения мониторинга реабилитационного периода после эндопротезирования межпозвонковых дисков.
Назначение и область применения разработки: аппаратного обеспечения мониторинга реабилитационного периода может быть применено в медицинских учреждениях, осуществляющих эндопротезирование.
СОДЕРЖАНИЕ
|
ВВЕДЕНИЕ
|
4
|
|
1 ПРОБЛЕМЫ ЭНДОПРОТЕЗИРОВАНИЯ
|
5
|
|
1.1 мЕЖПОЗВОНОЧНЫЕ ДИСКИ
|
7
|
|
1.2 ВИДЫ ЭНДОПРОТЕЗОВ
|
11
|
|
1.3 КОНЦЕПЦИЯ СФЕРИЧЕСКИХ ПРОТЕЗОВ МЕЖПОЗВОНКОВОГО ДИСКА
|
13
|
|
1.4 КОНЦЕПЦИЯ МЕХАНИЧЕСКИХ ПРОТЕЗОВ МЕЖПОЗВОНКОВОГО ДИСКА
|
15
|
|
1.5 КОНЦЕПЦИЯ ФИЗИОЛОГИЧЕСКИХ ПРОТЕЗОВ МПЖПОЗВОНКОВЫХ ДИСКОВ
|
16
|
|
1.6 ТОТАЛЬНЫЕ ПРОТЕЗЫ МЕЖПОЗВОНКОВОГО ДИСКА
|
17
|
|
1.6.1 «SBChariteArtificialDisc»
|
17
|
|
1.6.2 «ProDisc»
|
20
|
|
1.7 ЭНДОПРОТЕЗ МЕЖПОЗВОНКОВОГО ДИСКА «эНДОКАРБОН»
|
26
|
|
2 РЕАБИЛИТАЦИЯ ПОСЛЕ ОПЕРАЦИЙ НА ГРЫЖУ МЕЖПОЗВОНОЧНОГО ДИСКА
|
33
|
|
2.1 вОЗМОЖНЫЕ ОСЛОЖНЕНИЯ ПОСЛЕ УДАЛЕНИЯ МЕЖПОЗВОНОЧНОЙ ГРЫЖИ
|
44
|
|
2.2 РЕАБИЛИТАЦИОННЫЙ ПЕРИОД ПОСЛЕ ОПЕРАЦИИ НА ГРЫЖУ ПОЗВОНОЧНИКА
|
46
|
|
2.3 ИНТЕНСИВНАЯ РЕАБИЛИТАЦИЯ В ПОСЛЕОПЕРАЦИОННЫЙ ПЕРИОД
|
48
|
|
3 ВАРИАНТ АППАРАТНОГО МОНИТОРИНГА КРИТИЧЕСКИХ ПАРАМЕТРОВ В ПЕРИОД РЕАБИЛИТАЦИИ
|
50
|
|
ЗАКЛЮЧЕНИЕ
|
52
|
|
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
|
|
|
ГРАФИЧЕСКАЯ ЧАСТЬ
|
|
ВВЕДЕНИЕ
Реабилитация больных после операции эндопротезирования межпозвоночного диска должна выполняться под строгим наблюдением и контролем специалиста-реабилитолога в течение длительного времени. После эндопротезирования межпозвоночного диска этот период может продолжаться более полугода [2, 3, 4, 8, 10, 11]. Госпитализация пациентов на столь длительные сроки для восстановительного лечения нереальна, прежде всего, по экономическим соображениям (как у нас, так и за рубежом). В этой связи, как правило, больные вынуждены самостоятельно заниматься реабилитацией, руководствуясь лишь рекомендациями лечащего врача при выписке из стационара. По-видимому, это является основной причиной относительно большого числа неудовлетворительных результатов эндопротезирования межпозвоночного диска – по данным литературы процент неудач достигает 8-10% [2, 4, 6, 10]. Неполноценно проведённые реабилитационные мероприятия отрицательно сказываются на результатах высокотехнологического и дорогостоящего эндопротезирования межпозвоночного диска, существенно снижают качество жизни, как пациентов, так и лиц, обеспечивающих уход за ними.
Задачи по реабилитации больных после эндопротезирования межпозвоночного диска до сих пор являются предметом дискуссий как среди нейрохирургов, так и среди специалистов по реабилитологии.
1 ПРОБЛЕМЫ ЭНДОПРОТЕЗИРОВАНИЯ
Основная функция межпозвоночных дисков – рессорная. Благодаря им позвоночник может изгибаться вперёд, назад, в стороны, вращаться вдоль вертикальной оси, при этом спинной мозг не испытывает нагрузку и может полноценно функционировать. Грыжа диска – это выпячивание фиброзного кольца межпозвоночного диска вплоть до полного его разрыва с перемещением пульпозного ядра от центра в сторону выпячивания и выпадение его содержимого в спинномозговой канал. В итоге сдавливается спинной мозг, человек чувствует боль, нарушается работа внутренних органов. Грыжа может образовываться в любом из межпозвоночных дисков, однако чаще всего она бывает в поясничном и шейном отделах позвоночника.
Ведущая причина грыжи межпозвоночного диска – дегенеративные изменения диска на фоне нестабильности позвоночно-двигательного сегмента. По статистике специалистов Федерального Центра нейрохирургии: к 30 годам грыжа имеется у 80% населения; после 40 лет – у 90%; 19% больных с грыжами межпозвоночных дисков нуждаются в оперативном лечении.
В отечественной клинической практике эндопротезирование межпозвоночных дисков используется относительно недавно. Наиболее популярный за рубежом искусственный межпозвонковый диск М6 (шейный и поясничный) производства американской компании «Спайнал Кинетикс» зарегистрирован в России и разрешен к применению. В 2013 г. прошел клиническую апробацию эндопротез межпозвонкового диска «Эндокарбон» производства российского производителя – Пензенской компании «МедИнж».
Несмотря на постоянное совершенствование конструкции протезов межпозвоночного диска результаты хирургического лечения грыжи нельзя признать идеальными. В российском здравоохранении, а также за рубежом отсутствует обоснованный, строго индивидуальный и технологически обеспеченный подход к реабилитации этой сложной категории пациентов [2, 10]. Основная проблема заключается в том, что проведение полноценной реабилитации возможно лишь в условиях длительного пребывания больного в реабилитационном стационаре, оснащенном высокотехнологичным оборудованием. После эндопротезирования межпозвоночного диска этот период может продолжаться более полугода [2, 3, 4, 8, 10, 11]. В этой связи, как правило, больные вынуждены самостоятельно заниматься реабилитацией, руководствуясь лишь рекомендациями лечащего врача при выписке из стационара. По-видимому, это является основной причиной относительно большого числа неудовлетворительных результатов эндопротезирования межпозвоночного диска – по данным литературы процент неудач достигает 8-10% [2, 4, 6, 10].
В настоящее время послеоперационная реабилитация ортопедических больных базируется, в основном, на оптимизации двигательного режима, на индивидуальном подборе физических упражнений, массаже, физиотерапии [3, 6, 8, 9, 10]. При этом врач, как правило, ориентируется по самочувствию пациента и ряду других субъективных данных. Тем не менее, существует зарекомендовавший себя способ объективизации способности пациента поддерживать вертикальную позу на основе компьютерной стабилографии [1, 3, 5, 6, 7].
У больных, которым показана операция эндопротезирования межпозвоночного диска, имеются выраженные отклонения стабилограммы, которые при правильно проводимой реабилитации могут восстанавливаться [1, 2, 3, 5, 6, 7, 8]. Таким образом, используя объективные данные, можно создавать индивидуальную программу реабилитационных мероприятий для каждого больного и контролировать процесс реабилитации по критичным параметрам через Интернет. Больной при этом находится дома и самостоятельно выполняет все рекомендации врача-специалиста. Для этой цели больному выдается мобильный комплекс «ВебМультиМедик» (Патент на полезную модель № 122009), в состав которого входит стабилограф, электроэнцефалограф, электрокардиограф и электромиограф [1, 5, 6, 7]. Комплекс на протяжении 2012 г. прошел доклиническую апробацию в СарНИИТО. При помощи этого комплекса пациент ежедневно проходит процедуру контроля и передает сведения через Интернет своему врачу. Врач-реабилитолог анализирует параметры и оперативно проводит коррекцию реабилитационных мероприятий.
1.1 МЕЖПОЗВОНКОВЫЕ ДИСКИ
Следует помнить о том, что знания о межпозвонковых дисках имеют большую историю. Еще в 1655 году Везалий впервые описал строение межпозвонковых дисков, и только два столетия спустя Доменико Котугно (1764) привел описание ишиаса, как заболевания. Первая иллюстрация, на которой была изображена задняя протрузия студенистого ядра межпозвонкового диска, появилась в 1824 году в книге Чарлея Велла, изданной в Лондоне, а полное описание межпозвонкового диска сделал в последующем Вирхов в 1837 году (цит. по А. Дзяк, 1981).
Межпозвонковые диски (их всего 23) являются отдельной структурной частью межпозвонковых суставов. Соединяя тела позвонков, они одновременно выполняют амортизационную защиту позвоночника от сил тяжести тела и других вертикальных нагрузок. При этом сила, которая давит на межпозвонковый диск, уравновешивается, равной по величине, но противоположной по направлению, упругостью фиброзного кольца и пульпозного ядра. Дегенеративно-деструктивные изменения в межпозвонковых дисках занимают первое место среди причин возникновения вертеброгенных заболеваний. В этой связи необходимо рассмотреть последовательность развития анатомо-морфологических изменений в межпозвонковых дисках с тем, чтобы в дальнейшем иметь правильное представление о патогенезе заболевания и механизме действия ручных способов лечения. Межпозвонковые диски составляют в молодом возрасте у здорового человека 1/4 длины всего позвоночника. Они имеют разную высоту: в шейном отделе приблизительно 4 мм, в грудном 5-7 мм, а в поясничном около 10 мм. Диски имеют несколько больший диаметр, чем сами тела позвонков, благодаря чему позвоночник приобретает форму бамбуковой палки. В шейном отделе диски составляют 40%, в грудном 20%, а в поясничном 30% высоты позвоночника (Г.С. Юмашев, М.Е Фурман, 1984). Одни авторы относят межпозвонковые диски к хрящевым образованиям непрерывного костного скелета и, следовательно, не считают их суставами в обычном понимании, другие же — относят их к симфизам, т.е. прерывающимся соединениям костных структур, по крайней мере, начиная с 8-ми летнего возраста человеческого организма. Межпозвонковый диск состоит из студенистого ядраи фиброзной капсулы. Сверху и снизу он ограничивается от примыкающих тел позвонков покровными (замыкательными) пластинами, которые представляют собой не кальцинированный суставной хрящ. Эти пластины достаточно прочны и выдерживают большое напряжение при всех видах нагрузок на позвоночник. Г С. Юмашев и М.Е. Фурман (1984) сравнивают замыкательные пластины, покрытые гиалиновым хрящем, с суставными концами; студенистое ядро, содержащее жидкость типа синовиальной, уподобляют полости сустава, а фиброзное кольцо рассматривают как капсулу сустава и его связочный аппарат. А. Хем и Д. Кормак (1983) относят межпозвонковый диск к симфизам, так как он является соединением, в котором отдельные позвонки удерживаются вместе с помощью комбинации гиалинового и волокнистого хряща. Это обстоятельство позволило И.З. Пуринып (1978) назвать межпозвонковое соединение амфиартротическим сочленением. Межпозвонковые диски, как и другие хрящевые структуры, относятся к брадитрофным тканям, и у взрослого человека они не содержат ни кровеносных сосудов, ни нервов. Студенистое ядро составляет около 50-60% объема межпозвонкового диска и располагается в капсуле диска несколько асимметрично — ближе к заднему краю позвонка. Оно имеет консистенцию полузастывшего желе, на вид белого, блестящего, просвечивающегося тела. Орман Бидлл (Beadle Ormond, 1931) в обзоре об исследованиях Шморля по структуре и анатомии межпозвонковых дисков указывает на то, что «... только в детском возрасте пульпозное ядро настолько морфологически отличается от фиброзного кольца, что его можно легко вылущить». Детальное исследование микроскопической структуры студенистого ядра впервые осуществил Б. Сюльвен (В. Sylven, 1951). Им, в частности, было отмечено, что молодое и свежее ядро, при увеличении в 10 тыс. раз, представляет собой решетку из тонких фибрилл толщиной около 50 мл микрон, окутанную бесструктурным веществом, близким по химическому составу к межклеточному веществу самих фибрилл. Краниально и каудально фибриллы прикрепляются под острым углом к покровным (замыкательным) пластинам. По периферии ядра количество фибрилл увеличивается, и они располагаются более системно в виде узкой полоски волокнистого хряща, которая без четкой границы переходит в фиброзное кольцо. Студенистое ядро составляет наиболее специализированный и важный в функциональном отношении элемент межпозвонкового диска. Оно не абсолютно несжимаемо, как считают некоторые исследователи: так, в результате потери воды, под действием сильного сжатия, оно незначительно уменьшает свою форму и объем. Студенистое ядро выполняет три функции: является точкой опоры для вышележащего позвонка, утрата этого качества может послужить началом целой цепи патологических состояний позвоночника; выполняет роль амортизатора при действии сил растяжения и сжатия и распределяет эти силы равномерно во все стороны: по периметру фиброзного кольца и на хрящевые пластины тел позвонков; является посредником в обмене жидкостей между фиброзным кольцом и телами позвонков. Тела позвонков как будто катаются на своего рода «подшипнике» из гелеобразного ядра. Во время вентральной флексии ядро сдавливается в его вентральной части, во время дорзальной флексии (гиперэкстензии) позвоночника — в дорзальной. Во время таких движений суставные отростки дуг только поддерживают тела позвонков. Рост ядра осуществляется за счет разрастания его волокнистых элементов. К двенадцати годам жизни оно почти полностью состоит из хрящевой и фиброзной ткани. Студенистое ядро при рождении человека содержит 88% воды, в возрасте 18 лет — 80%, а в 77 лет его гидратация снижается до уровня 69%; в то время как фиброзное кольцо содержит в начале 78% воды, к 30 годам — 70% и на таком уровне степень его гидратации удерживается до глубокой старости. Но оказывается, что содержание воды в ядре может также изменяться от вариации силы нагрузки на позвоночник. На основании своих исследований Армстронг (Armstrong, 1965) приводит интересные данные о механизме гидратации студенистого ядра. Например, в условиях нормы сила всасывания воды уравновешивает силу сжатия ядра при его нормальной гидратации. По мере возрастания силы сжатия ядра наступает момент, когда давление извне превышает силу всасывания и происходит вытеснение жидкости из межпозвонкового диска. В результате потери жидкости возрастает сила всасывания воды и происходит восстановление равновесия. По мере уменьшения силы сжатия ядра временно преобладают силы всасывания, в итоге происходит увеличение содержания жидкости в ядре. Повышение гидратации, в свою очередь, ведет к уменьшению силы всасывания и к возвращению первоначального состояния равновесия. Ключом к пониманию данного механизма может послужить доказанный Харлеем (цит. по А. Дзяк, 1981) феномен всасывания воды студенистым ядром вопреки действия на него сил сжатия. Такое свойство студенистого ядра объясняется содержанием в его фибриллах и межфибриллярном веществе протеинов, гиалуроновой кислоты и полярных (ОН) групп мукополисахаридов, обладающих высокой имбибиционной и гидрофильной способностью. Большинство ученых сходятся во мнении о том, что нарушение гидратации студенистого ядра дает начало цепи сложных последовательных изменений, приводящих в итоге к повреждению межпозвонкового диска, которое становится отправным пунктом в развитии синдромов ВЗНС. Теоретически, как об этом уже упоминалось, позвоночник мог бы выдержать неограниченную силу сжатия, но после превышения его компенсаторного предела наступает прогибание замыкательных пластин и, как следствие этого, вдавливание части диска в вещество тела позвонка — образуются, так называемые, грыжи Шморля. В стареющем организме способность студенистого ядра удерживать воду в условиях сжатия резко снижается и такой позвоночник способен выдерживать воздействие сил лишь средней интенсивности. Хрящевые пластины покрывают центральную часть тел позвонков, при этом спереди и с боков они граничат с эпифизарным костным кольцом, а сзади достигают самого края тела позвонка. Отсюда берут начало волокна фиброзного кольца и студенистого ядра. Со стороны студенистого ядра пластины покрыты тонким слоем волокнистого хряща, а со стороны кости (тела позвонка) — плотно сращены с тонким слоем обызвествленного хряща. Функциональное значение покровных пластин заключается в том, что они представляют собой зоны роста для тел позвонков, фиксируют межпозвонковый диск между телами смежных позвонков и выполняют роль барьера между студенистым ядром и телами позвонков.
1.2 ВИДЫ ЭНДОПРОТЕЗОВ
Новый тотальный эндопротез межпозвонкового диска Slide-Disc® восстанавливал объём движений сегмента до интактного состояния. Удаление задней продольной связки после имплантации эндопротеза приводило к статистически значимому нарастанию объёма движений во всех плоскостях. Имплантация эндопротеза приводила к увеличению лордоза в сегменте в среднем на 3°, удаление задней продольной связки частично нивелировало этот эффект. Эндопротез Slide-Disc® сохранял близкую к интактной траекторию центра ротации сегмента при флексии/экстензии. Этот эффект наблюдался как до, так и после удаления задней продольной связки. В условиях физиологической нагрузки не произошло миграции компонентов эндопротеза и/или перелома краевых пластин. По сравнению с эндопротезом SB Charite III, эндопротез Slide-Disc® обеспечивал более физиологичный объём движений, ближе соответствующий интактному сегменту. Это отличие наблюдалось как до, так и после удаления задней продольной связки.
Инъецируемый силиконовый имплант PNR® восстанавливал объём движений и высоту сегмента до интактного уровня, в отдельных случаях он дополнительно уменьшил объём движений в сегменте относительно интактного уровня. После приложения длительной циклической нагрузки, объём движений и высота сегмента оставались в пределах интактного уровня. Длительная циклическая нагрузка не приводила к смещению и/или повреждению силиконового ядра и других компонентов эндопротеза. Наличие заднего дефекта фиброзного кольца после интерламинарной микродискэктомии не приводило к миграции силиконового ядра через данный дефект под действием длительной циклической нагрузки.
Эндопротез пульпозного ядра из гидрогеля заданной формы HydraflexТМ восстанавливал объём движений в сегменте до интактного уровня, данный эффект не зависел от состояния эндопротеза (сухое или гидратированное) при имплантации. Под действием длительной циклической нагрузки объём движений в сегменте возрос до такового при удалённом пульпозном ядре, данный эффект также не зависел от гидратации импланта. Высота препаратов после имплантации гидратированных имплантов соответствовала интактному уровню или превышала его, тогда как для дегидратированных имплантов была в основном меньше интактного уровня. Под действием циклическая нагрузки высота препаратов снижалась до уровня удалённого пульпозного ядра при гидратированном импланте и вдвое ниже данного уровня при дегидратированном импланте. При этом, наблюдались лишь незначительные смещения импланта как в гидратированном, так и в сухом состоянии. Не наблюдалось ни одного случая миграции импланта через имплантационный дефект в фиброзном кольце. Циклическая нагрузка ни в одном случае не приводила к повреждению имплантом краевых пластин или его миграции в тела позвонков.
Эндопротез пульпозного ядра из коллагена I типа в одном из шести препаратов был полностью выдавлен за пределы фиброзного кольца вместе с обтуратором имплантационного канала после первых 20 тысяч циклов длительного нагрузочного теста. Таким образом, сочетание пункционного доступа и обтуратора дефекта фиброзного кольца не позволило предотвратить миграцию импланта через имплантационный канал под действием длительной циклической нагрузки. В 5 препаратах без миграции импланта, коллагеновый эндопротез восстанавливал объём движений препарата до интактного уровня после удаления пульпозного ядра. Под действием длительной физической нагрузки наступала выраженная дестабилизация всех препаратов во всех плоскостях. В 5 препаратах без миграции импланта, коллагеновый эндопротез восстанавливал высоту препарата до интактного уровня после удаления пульпозного ядра. Под действием длительной физической нагрузки высота препаратов снизилась вдвое относительно высоты препаратов при первичном удалении ядра.
1.3 КОНЦЕПЦИЯ СФЕРИЧЕСКИХ ПРОТЕЗОВ МЕЖПОЗВОНКОВОГО ДИСКА
Сферическая форма протеза явилась толчком развития этого направления. Впервые импланты появились уже к концу 1950-х годов. Сферическая модель имеет очень простое строение и представляет собой шар, который после дискэктомии помещается в полость пульпозного ядра. Фиброзное кольцо сшивается, а имплантированный шар протезирует функцию пульпозного ядра.
Для проведения биомеханических и динамических экспериментов д-р Alf Nachemson вводил в диск заранее заготовленный силикон. Однако при нагрузках, превышающих 400-500 N, резина распадалась на части. В начале 1960-х в Южной Африке некоторое количество таких устройств было имплантировано пациентам с заболеваниями шейного отдела позвоночника. Впоследствии некоторые были удалены, но до сих пор точно неизвестно ни количество имплантированных устройств, ни результаты тех операций.
В 1966 году д-р Ulf Fernstrom установил 191 сферический протез 125 пациентам. Первоначально, через 2,5 года результаты были многообещающими. Только 27% (34 пациента) сообщили о возобновлении боли. В контрольной группе болевой синдром возобновился у 74%. Однако через 4-7 лет более 88% (168 имплантов) потеряли первоначльную высоту, просев в тела позвонков.
Во времена имплантаций д-ра Fernstrom’а, в Калифорнии д-ра PaulHarmon и AllenMcKenzie в Канаде также экспериментировали с металлическими шарами. В 1995 году д-р McKenzie представил ретроспективный отчет о проделанной им работе. За 18 лет им были имплантированы протезы 67 пациентам. Он указывает на то, что 95% пациентов вернулись к работе и у 83% пациентов были получены хорошие и отличные результаты. Однако в начале 1970-х он отказался от этих операций из-за возникновения ряда осложнений.
Интересным историческим фактом является то, что президент JohnF. Kennedy страдал хроническими болями в позвоночнике и ему был имплантирован «шар Fernstrom’а». Операция была выполнена в конце 1950-х д-м Harmon’м.
В настоящий момент изучением сферических протезов занимается д-р RobertBiscup. В начале 1997 года он имплантировал 8 протезов пятерым
своим пациентам. Они были изготовлены компанией «AcroMedCorp.» из карбонового волокна. Он утверждал, что использование именно этого материала позволит избежать эффекта проседания импланта в тела позвонков. В среднем, через 20 месяцев все пациенты вернулись к нормальному образу жизни, занятиям спортом и.т.д. Ни у одного пациента какого-либо смещения выявлено не было. Однако у всех пациентов было выявлено проседание разной степени выраженности, но тем не менее движения в оперированных сегментах были сохранены. По данным визуализационных методов обследования дегенеративные изменения оставались на прежнем уровне или становились более выраженными, но клинически это никак не проявлялось.
1.4 КОНЦЕПЦИЯ МЕХАНИЧЕСКИХ ПРОТЕЗОВ МЕЖПОЗВОНКОВОГО ДИСКА
Доказано, что механическая модель дольше всех продержалась на рынке имплантов этого вида. Механическая модель – это тотальный протез, предназначенный для восстановления движений в позвоночном сегменте. Такие устройства представляют собой металлические замыкательные пластинки, которые напрямую, или через вспомогательное устройство, крепятся к телам позвонков. Эти протезы функционируют также как и протезы других суставов (напр. коленного сустава).
Было разработано большое количество механических протезов - одни имели очень сложное, другие, наоборот, очень простое строение.
За последние 20 лет было имплантировано довольно большое количество таких протезов. Д-р Urbaniak в 1973 году имплантировал 8 таких протезов четырем взрослым шимпанзе. Однако, впоследствии из-за осложнений, связанных с инфицированием, плохой биосовместимостью и недостаточным хирургическим навыкам, результаты оказались очень плохими.
Д-р CaseyLee разработал тотальный трехкомпонентный протез диска, состоящий из центрального ядра, сделанного из относительно мягкого полимера, окруженного более жестким кольцевым полимером и замыкательных пластин. Слои ядра и кольца компенсировали 60% общей высоты, а замыкательные пластины - 40%. Было проведено исследование на собаках (invitro) и биомеханическое тестирование. Они показали, что производство таких протеза слишком трудоемко, а качество конечного продукта непостоянно.
Единственным примером механической модели, дошедшей до маркетинговой стадии, является продукт компании «Charite» (более 3.000 имплантаций во всем мире) и «ProDisc» (более 250 имплантаций в мире). Оба протеза производятся за пределами США, но прошли там клинические испытания.
1.5 КОНЦЕПЦИЯ ФИЗИОЛОГИЧЕСКИХ ПРОТЕЗОВ МЕЖПОЗВОНКОВЫХ ДИСКОВ
Как правило, в этих устройствах используется ядро из гидрогеля или полиуритана. Их задача - восстановить функцию диска посредством поглощения и отдачи жидкости в межпозвонковом пространстве, а также распределять возникающие нагрузки, то есть протезировать «рессорную» функцию диска. Такое устройство может быть имплантировано для борьбы с дискогенной болью, для восстановления высоты и нормальной кинематики диска.
1.6 ТОТАЛЬНЫЕ ПРОТЕЗЫ МЕЖПОЗВОНКОВОГО ДИСКА
- Link Spine Group, Charite
- Spine Solutions, ProDisc
- DePuy AcroMed, AcroFlex
- Medtronic Sofamor Danek, lubar disc
- Tensegra, NUDISC
- Disc Replacement Technologies, BI-CAD DISC
- Spinal Dynamics, Bryan Disc
- Medtronic Sofamor Danek, Bristol Disc
- Scient’x, cervical disc
- Pearsalls Limited, cervical disc
- Biorthex, Spiral Disc
1.6.1 «SBChariteArtificialDisc»
Устройство протеза
«SBChariteArtificialDisc» – это тотальный протез, имитирующий суставную функцию диска и восстанавливающий его нормальное физиологическое движение. Это естественный протез, позволяющий осуществлять сгибательные, разгибательные, наклонные и ротационные движения.
Первое поколение. Первый протез был создан в Берлине в 1982 году докторами Buttner-Janz и Schellnack’м. Первая имплантация была выполнена в 1984 году. Протез первого поколения состоял из двух маленьких циркулярных, стальных замыкательных пластин, каждая из которых имела по 11 зубцов и центрального полиэтиленового ядра. Цемент для имплантации не применялся. Замыкательные пластины были симметричными и делались из отполированной стали толщиной 1 мм. С внутренней стороны они охватывали вогнутую центральную часть, а с внешней стороны на них находились фланцы с заостренными краями. Полиэтиленовое ядро имело двояковогнутую форму и делалось из листа «Chirulen», прошедшего предварительную термическую обработку, после чего оно шарнирно соединялось с замыкательными пластинами. С целью последующей рентгенографической идентификации скользящее ядро оборудовалось металлическим кольцом. Позднее, протез модифицировался путем уменьшения числа зубцов, вместо 11 их стало 5.
Второе поколение. Годом позже была произведена частичное усовершенствование протеза, которое заключалась в повышении его стабильности путем изменения толщины замыкательных пластин - вместо 1 мм стальных пластин были сделаны более толстые пластины из медицинской нержавеющей стали, оснащенные 3 вентральными и 2 дорзальными крепежными зубцами и двухсторонними крыльями. Также был встроен рентген - позитивный маркер для послеоперационного контроля. Для того, чтобы сохранить вогнутость тел позвонков, замыкательные пластины выполнялись слегка выпуклыми. Необходимо указать на то, что эта версия имела три стандартных размера.
Два первых поколения, из-за недостатков материала, из которого они были сделаны, в клиническом применении потерпели неудачу.
Третье поколение. Данная версия протеза, «SBChariteIII», была разработана в 1987 году.
Протез «SBChariteArtificialDisc» – это трехкомпонентный модульный имплант. Протез состоит из двух замыкательных пластин, сделанных из кобальт – хром - молибдена и двояковыпуклого ядра, выполненного из высокомолекулярного полиэтилена (UHMWPE).
Каждая замыкательная платина имеет вогнутую поверхность, предназначенную для шарнирного соединения с ядром и по 3 острых зубца с каждой стороны длиной 3 мм и толщиной 1 мм. Интервалы между зубцами варьируют от 2 до 3 мм. Замыкательные пластины крепятся к телам позвонков. Замыкательные пластины обработаны пористым титаном и гидроксиапатитом.
Инструментарий и методика имплантации.
Установка протеза осуществляется по частям, начиная с замыкательных пластин и заканчивая ядром. Операция производится из переднего ретроперитонеального доступа с использованием расширителей и специального установочного инструмента. Ключевым моментом является выбор размера протеза. Сама операция занимает не более 90 минут.
- Подготовка - ретракторы Hohmann вбиты тела позвонков.
- Надрез – для открытия фиброзного кольца производится эксцентричный надрез.
- Дискэктомия – при помощи кюреток и кусачек производится удаление материала диска. Расширитель смещается латерально и осуществляется удаление задних отделов диска.
- Калибровка – применяется для определения размера и расположения замыкательных пластин.
- Установка замыкательных пластин – вводятся при помощи расширителя и специальных щипцов, имеющих ограничитель.
- Расширение – при помощи дополнительного расширителя осуществляется дистракция. Для достижения максимальной дистракции потребуются несколько дополнительных расширителей.
- Примерка – дополнительный расширитель удаляется. Для определения размера ядра используется примерочный вариант.
- Установка – используется установочный инструмент, применяется техника постукивания.
- Фиксация – для фиксации положения, после удаления расширителя и щипцов для введения, используется поддерживающий инструмент.
- Закрытие – фиброзное кольцо закрывается и на него накладываются швы.
SBChariteIII сегодня
Протез «SBCharite» на сегодняшний день является самым часто имплантируемым протезом в мире. Всего имплантировано более 3.000, из них только в 2000 году было имплантировано 600 протезов. Есть пациенты, у которых период наблюдения превышает 10 лет. Сегодня протезы продаются более, чем в 20 странах мира. Наиболее охвачен рынок Франции, Германии и Англии. Эти страны закупают около 60-70% всех производимых протезов. В США, под патронажем FDA, проводится клиническое исследование, в котором участвуют около 400 пациентов.
1.6.2 «ProDisc»
Устройство протеза
«ProDisc»- это 3-х компонентный протез, состоящий из двух кобальт-хром-молибденовых пластин и ядра, сделанного из высокомолекулярного полиэтилена. Строение протеза основано на физиологической форме и функции здорового позвоночного сегмента. Кинематика и морфология импланта повторяет как биомеханические, так и анатомические характеристики здорового позвоночника.
Высокомолекулярное полиэтиленовое ядро куполообразной формы фиксируется в положении нижней замыкательной пластины и шарнирно соединяется с верхней - вогнутой замыкательной пластиной. Всего производится протезы двух размеров: среднего и большого. Помимо этого,
верхняя замыкательная пластина может устанавливаться под разным наклоном- 6 и 11 градусов. Полиэтиленовые ядра выпускаются высотой 10, 12 и 14 мм.
Объем движений, обеспечиваемых протезом, превышает физиологический и зависит только от анатомических особенностей пациента. Фиксатор, при помощи которого замыкательная пластина крепится к телам позвонков, представляет собой центрально расположенный зубчатый киль. Замыкательные пластины покрыты порозным титановым напылением, позволяющим костной ткани прорастать в имплант для предотвращения его миграции.
Инструментарий и методика имплантации
Техника операции. После проведения дискэктомии, хирург использует специальный примерочный вариант импланта для определения конфигурации и правильности его расположения. При помощи долото и молотка в телах позвонков подготавливается ложе для зубчатых килей.
Далее, после введения замыкательных пластин, производится дистракция тел позвонков и при помощи специального толкателя вставляется полиэтиленовый вкладыш.
Основные этапы операции. В установке протеза выделяют 8 этапов.
- Доступ. Протез «ProDisc» и установочные инструменты устроены так, что позволяют использовать как микрохирургический, так и эндоскопический передний срединный доступ. Рентгеновские шаблоны позволяют проводить предоперационное планирование.
- Дискэктомия. Производится обычная дискэктомия. Задние отделы фиброзного кольца и задняя продольная связка сохраняются. С замыкательных пластин удаляются материал диск и хрящевая ткань.
- Установка примерочного импланта (шаблона). Для определения размера, высоты и положения импланта используются шаблоны. Расположение шаблона точно по средней линии определяет окончательное положение импланта. Проводится рентгенологический контроль.
- Формирование ложа для киля. Подготовка ложа для установки килей осуществляется долотом. После установки киля проводится рентгенологический контроль.
- Закрепление компонентов пластин. Для защиты мягких тканей, связок и нервных структур эта манипуляция производится без дистракции. Устанавливаются два компонента замыкательных пластин.
- Дистракция. Дистрактор закрепляется на специальном установочном инструменте.
- Установка полиэтиленового вкладыша. Установка и закрепление полиэтиленового вкладыша в компонент нижней замыкательной пластины осуществляется при помощи специального толкателя.
- Удаление инструмента. Весь установочный инструмент удаляется, после чего выполняется контрольная рентгенография.
За последние 35 лет было предложено большое количество подвижных имплантатов, однако большинство из них не дошло до клинического применения.
Подвижный имплантат должен воссоздавать биомеханические функции естественного диска. Он должен уменьшать механические нагрузки на смежные диски, предупреждать развитие в них дегенеративных процессов. После установки имплантата восстанавливается высота дискового промежутка и увеличиваются межпозвонковые отверстия, что предупреждает компрессию корешков. Установка имплантата должна восстановить нормальный объем движений, высоту дискового промежутка и лордоз.
Кроме того, материалы, из которых изготавливают имплантаты, должны удовлетворять ряду требований:
- Отсутствие токсичности и коррозии
- Прочность
- Технологичность
- Износостойкость
- Близкие к кости физико-механические свойства.
Несоответствие материала хотя бы по одному из параметров снижает функциональную ценность имплантата и сроки его функционирования. Оптимальное сочетание характеристик материала обеспечивает биосовместимость (в т.ч. биомеханическую) имплантата.
Требования к подвижному имплантату очень высокие. При трении его поверхностей не должна образовываться пыль, он не должен ломаться или стираться. Кроме того, он должен быть биологически инертен для организма, не приводить к развитию воспалительного процесса. Углы наклонов имплантата должны восстанавливать объем движений в трех плоскостях - сгибание-разгибание, латеральное сгибание, аксиальную ротацию.
Биомеханически и с учетом типа трущихся поверхностей различают подвижные имплантаты: металл-металл, металл-керамика, металл-пластик.
В настоящее время известны 4 различных типа подвижных имплантатов, разрешеных к клиническому применению.
«FlexiCore» - искусственный диск (SpineCore, Inc., Summit, NJ) полуфиксированной конструкции типа металл-металл с кобальтохромомолибденовыми пластинами. Подвижная часть выполнена в виде шара диаметром 13 мм. Она является центром ротации между двумя пластинами. На внешней поверхности пластин имеются шипы для фиксации к позвонкам.
Протез «Maverick» (Medtronic Sofamor Danek, Inc., Memphis, TN) - это полуфиксированная конструкция типа металл-металл. Конструкция протеза подобна описанной выше модели, но на его пластинах имеется выступающая поверхность с отверстиями для фиксации шурупов к телам позвонков.
Имплантаты типа металл-металл потенциально опасны из-за металлической пыли, образующейся в процессе трения. Применение металлических имплантатов всегда осложняется гальвано-электрическими явлениями, приводящими к металлозу окружающих тканей и коррозии деталей. Металлам свойственно вызывать резорбцию костной ткани.
Диск «ProDisc» (Spine Solutions, Inc., New York, NY) разработан Thierry Mamay в конце 80-х годов. «ProDisc» состоит из металлических пластин и ультравысокомолекулярного полиэтилена. Полиэтилен фиксирован к нижней пластине. Это диск полуфиксированной конструкции. В тела позвонков он фиксируется центральным гребнем, который имеется на пластинах.
В качестве прототипа выбран искусственный диск «Charite» (DePuy Spine, Raynham, MA), который состоит из двух кобальтохромомолибденовых пластин и свободно расположенного между ними ультравысокомолекулярного полимерного эллипсоида [1, 2]. Пластина фиксируются к телам шипами. С 1998 г. пластины покрываются слоем фосфата титана. Это покрытие обеспечивает инкорпорацию пластин в кость [3]. В настоящее время выпускаются диски 5 размеров.
Имплантаты типа металл-пластик могут изнашиваться со временем и обладают «холодной текучестью» и старением, типичной для пластика, что приводит к деформации и разрушению имплантата. Кроме того, продукты износа полимерных материалов нередко вызывают злокачественные перерождения окружающих тканей.
Целью изобретения является повышение биосовместимости, биомеханических свойств, износостойкости и улучшение остеоинтеграции имплантата в костных тканях с помощью имплантатов из изотропного пиролитического углерода.
Достижение указанной цели обеспечивается тем, что:
- имплантат межпозвонковый подвижный изготовлен из монолитного изотропного пиролитического углерода, без легирующих элементов или легированного бором или кремнием, с пределом прочности на сжатие не менее 450 МПа;
- на каждом торце имплантата имеется слой пористого углеродного материала, химически прочно связанный с изотропным пиролитическим углеродом;
- слой пористого углеродного материала представляет собой пену на основе углеродного нанокомпозита;
- он имеет на каждом торце шипы из титана;
- шипов из титана выполнено 4 или 6.
Перечисленные отличия предлагаемого имплантата сообщают ему ряд важных преимуществ по сравнению с прототипом.
Операция установки имплантата производится следующим образом. Имплантаты могут быть внедрены с переднего или заднего доступов. Задний доступ используется при необходимости удаления остеофитов или грыжи межпозвонкового диска. В этих случаях, имплантаты могут быть установлены с заднего доступа, при этом не надо делать дополнительный разрез в брюшной стенке (через живот).
Чаще всего имплантаты все-таки устанавливают через передний доступ к позвоночному столбу, разрез выполняется по переднебоковой стенке живота. Крупные кровеносные сосуды и органы аккуратно смещаются в сторону, удаляется нужный межпозвонковый диск, а на его место устанавливается имплантат. Между сосудами и дисковым промежутком прокладывают гемостатическую губку, устанавливают дренаж. Рану послойно зашивают.
После установки имплантата хирург проводит контроль с помощью передвижного рентгеновского аппарата.
При изготовлении имплантатов из изотропного пиролитического углерода будут повышены биосовместимость, биомеханические свойства, износостойкость и улучшена остеоинтеграция имплантата в костных тканях.
1.7 ЭНДОПРОТЕЗ МЕЖПОЗВОНКОВОГО ДИСКА «ЭНДОКАРБОН»
Область применения
Динамический эндопротез межпозвонкового диска «Эндокарбон» (далее эндопротез) является имплантатом нового поколения и применяется при артропластике шейного отдела позвоночника. Эндопротез предназначен для замещения поврежденных или патологически измененных естественных дисков при дегенеративно-дистрофических повреждениях, в операциях при протезировании патологий шейного отдела позвоночника. Эндопротез применяется для имплантации на уровнях от С3 до С7. Эндопротезы предназначены для применения квалифицированным медицинским персоналом.
Описание и конструкция эндопротеза
Эндопротез состоит из двух шарниров. Каждый шарнир конструктивно состоит из пластины с вставкой узла трения. Конструкция шарниров обеспечивает аксиальную ротацию и угловое смещение между позвонками во фронтальной и сагиттальной плоскости.
Рисунок 1
Внешняя геометрия поверхностей пластин эндопротеза повторяет анатомическую форму тел позвонков, что снижает травмирование в момент имплантации естественные поверхности позвонков и надежно стабилизирует эндопротез в межпозвоночном пространстве.

Рисунок 2
Рисунок 3
Внешняя поверхность имеет шипы фиксации и пористую поверхность. Шипы поверхности обеспечивают первичную фиксацию с позвонками, препятствующие передне-заднему смещению эндопротеза. Габаритные поверхности так же адаптированы под форму естественного межпозвонкового диска
Пористая поверхность позволяет ускорить процесс остеоинтеграции костной структуры
Рисунок 4
По требованию заказчика на пористое покрытие может быть нанесено кальций-фосфатное или биологически активное покрытие.
Материалы, используемые в эндопротезе
Пластины изготовлены из биологически инертного, титанового сплава ВТ-6 (ОСТ 1 90013), который обладает высокими механическими свойствами. Титановый сплав ВТ-6 уже давно и широко применяется в конструкциях различных эндопротезов суставов.
Узел подвижности эндопротеза изготовлен из монолитного изотропного пиролитического углерода (углеситалла) в соответствии с ТУ9493-001-2771122, обеспечивает высокую механическую прочность, износостойкость и биологическую совместимость эндопротеза. Функциональные возможности эндопротеза
Эндопротез восстанавливает высоту и функциональную подвижность оперированного сегмента межпозвоночного диска. Конструкция эндопротеза обеспечивает подвижность позвонков соответствующая естественной, физиологической подвижности позвоночника
Рисунок 5
Жесткость конструкции эндопротеза позволяет произвести декомпрессию нервных окончаний и канала спинного мозга, а также устранить «постдискэктомический синдром».
Противопоказания применения
- нарушения анатомических, физиологических и биомеханических свойств связочного аппарата позвоночного столба).
- инфекция и местное воспаление;
- измененная структура позвонков;
- беременность;
- несовместимый возраст или физическое состояние пациента.
Риски при эндопротезировании
- гнойные накопления;
- аллергические реакции, индивидуальная непереносимость (чувствительность) к металлам, индивидуальное отторжение материалов;
- самопроизвольное сращивание позвонков;
- нестабильность и дислокация из-за неправильно подобранного размера эндопротеза.
Рисунок 6
Исполнение
Динамические эндопротезы межпозвонковых дисков выпускаются в следующих исполнениях
Комплектация эндопротеза и форма поставки
|
Модель
|
Н,мм
|
S,мм
|
L,мм
|
|
C.13.17.5
|
5,25
|
13
|
17
|
|
C.13.17.6
|
6
|
13
|
17
|
|
C.13.17.7
|
6,75
|
13
|
17
|
|
C.13.17.8
|
7,5
|
13
|
17
|
|
C.13.20.6
|
6
|
15
|
20
|
|
C.13.20.7
|
6,75
|
15
|
20
|
|
C.13.20.8
|
7,5
|
15
|
20
|
|
C.13.20.9
|
8,25
|
15
|
20
|
Эндопротезы поставляются подшитыми к держателю, в индивидуальной стерильной упаковке. Поставляемый с каждым эндопротезом держатель изготавливается из поликарбоната медицинского назначения. Держатель состоит из кожуха и опоры, к которой при помощи нитей подшит эндопротез. Держатель предотвращает механическое воздействие на эндопротез при манипуляции в блистерной таре и подготовке к имплантации.
Рисунок 7
Двойная блистерная упаковка обеспечивает стерильность эндопротеза. Транспортная картонная коробка обеспечивает целостность комплекта изделия.
В комплект изделия входит:
- эндопротез в индивидуальной блистерной таре;
- карта идентификации пациента;
- наклейка с данными эндопротеза;
- инструкцию по использованию;
- памятка пациента.
По требованию заказчика комплект поставки может быть изменен. Необходимые принадлежности для проведения операции по имплантации Дополнительно по требованиям заказчика для операции по имплантации поставляется комплект принадлежностей:
- комплект пробников (8 шт.);
- принадлежность для имплантации (1 шт.).
манипуляции в блистерной таре и подготовке к имплантации.
Рисунок 8
Комплект пробников предназначен для определения необходимого размера эндопротеза. Принадлежность для имплантации необходима для удержания и манипуляций с эндопротезом при эндопротезировании, что обеспечивает точное позиционирование эндопротеза между позвонками. Принадлежности для имплантации поставляются стерильными и предназначены для многократного использования. Стерилизацию принадлежностей проводится согласно ГОСТ Р ИСО 11135.
Транспортирование и хранение Эндопротез, упакованный в транспортную тару, можно перевозить всеми видами транспортных средств (при температуре от -50°С до +50°С). Эндопротез следует хранить в транспортной таре в помещениях при температуре от -50°С до +40°С.
Гарантии изготовителя
Установленный срок стерильности эндопротеза указан на этикетках тары. Гарантийный срок хранения устанавливается 3 года с момента изготовления эндопротеза.
- РЕАБИЛИТАЦИЯ ПОСЛЕ ОПЕРАЦИЙ НА ГРЫЖУ МЕЖПОЗВОНОЧНОГО ДИСКА.
Общие знания об остеохондрозе и межпозвоночных дисках
Остеохондроз – хроническое деструктивно-дегенеративное заболевание, в основе которого лежит поражение межпозвоночных дисков.
Диски не способны к регенерации, то есть к самостоятельному восстановлению, и чрезвычайно плохо кровоснабжаются: у них нет собственных кровеносных сосудов. С возрастом, в связи с естественными процессами старения, происходит снижение содержания воды в межпозвоночных дисках с 95% до 65% и, следовательно, страдает упругость дисков и их амортизационная функция.
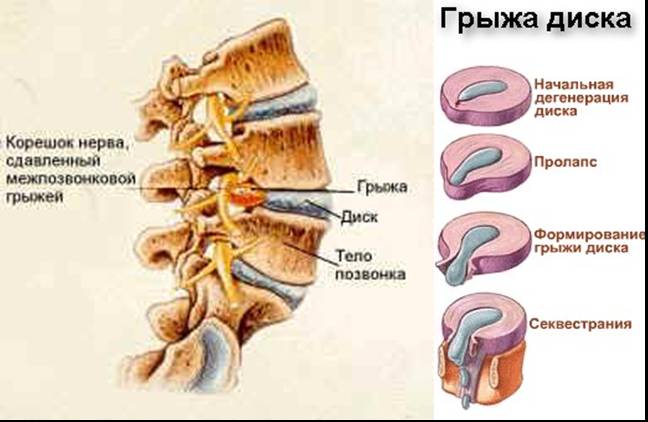
Рисунок 9
В межпозвоночном диске различают две основные зоны. Центральная – это пульпозное ядро, где происходит захват и отщепление воды. При захвате высота диска увеличивается и уменьшается давление позвонка на позвонок. Вторая зона – это краевая фиброзно-хрящевая пластинка, где диск иннервируется и где к нему прикрепляется задняя продольная связка.
Кратко представим курс реабилитации нашем центре на примере оперативного лечения грыжи в поясничном отделе позвоночника.
Ранний постоперационный период (стационарный этап)
В первые дни, чаще, это постельный режим. Задачи лечебной гимнастики: нормализация крово- и лимфообращения в зоне оперативного вмешательства, в конечностях, профилактика послеоперационных гипостатических осложнений, дыхательная гимнастика, нормализация тонуса центральной нервной системы, поддержание нормального функционирования всех физиологических систем организма.
Занятие проводится в по 10-15 минут, 3-5 раз в день, в относительно медленном темпе.
Постепенно двигательный режим расширяется, и пациент выполняет все более сложные упражнения в различных положениях. Через несколько дней разрешают вставать, пациент начинает самостоятельно перемещаться в пределах палаты, затем – этажа, и, наконец, по лестничным пролетам.
Постстационарный этап
Задачи – нормализация крово- и лимфообращения в оперированном сегменте, улучшение силовых качеств мышечного корсета туловища, восстановление физиологической подвижности позвоночника и страдающей конечности, разгрузка позвоночника, выработка навыков правильной ходьбы, адаптация к бытовым и трудовым нагрузкам, и др.
Занятия проводятся самостоятельно, по данным на стационарном этапе рекомендациям, по 15-25 минут каждое, несколько раз в день.
На базе реабилитационного центра в решении этих задач помогают и артрологические комплексы типа «Biodex» и «Primus», на которых возможно подобрать упражнения для любого сустава и с различной нагрузкой. Используются силовые и кардиотренажеры. Начинаются тренировки на балансировочных платформах для развития координации мышц-стабилизаторов позвоночника.
Благодаря разнообразию тренажеров и приспособлений, можно развивать и тренировать специфические двигательные навыки, необходимые в быту или для занятий спортом: от открывания дверной ручки или вращения руля до ударов теннисной ракеткой.
По завершении операции по установлению эндопротеза в тазобедренном суставе, требуется курс восстановления нормального функционирования сустава, а также прилегающих к нему мышц. В данном случае длительность и эффективность курса реабилитации зависит от множества факторов. Реабилитация после эндопротезирования тазобедренного сустава ведется по разным схемам. Поэтому необходимо применять индивидуальный подход к каждому конкретному пациенту.

Рисунок 10
Многое зависит от возраста пациента, от его общего состояния и физической развитости мускулатуры. Соответственно, чем старше пациент, а также, чем больше он физически ослаблен, тем дольше будет проходить процесс реабилитации.
Также огромное значение имеет и то, сколько времени прошло между травмой и операцией. В том случае, если прошёл довольно длительный срок, скорее всего, мышцы успели значительно атрофироваться, так как повреждённый сустав не мог полноценно функционировать.
Похожая ситуация может возникнуть при артрозе. Если операция была проведена своевременно, когда, несмотря на боль, человек еще мог самостоятельно передвигаться, и мышцам приходилось работать, но до критической точки дело ещё не дошло, тогда процесс восстановления пройдёт немного быстрее и успешнее.
Но бывает и так, что человек годами терпит боль, надеясь, что всё пройдёт самостоятельно. К врачу он обращается, когда боль становится совсем невыносимой, и человек уже попросту не может ходить.
В таких случаях мышцы успевают атрофироваться. Соответственно, процесс послеоперационной реабилитации будет проходить дольше и сложнее. Учитывая все подобные факторы, можно составить общую программу реабилитации, применимую для всех пациентов. Эта программа основывается на определённых принципах и целях, также применяется индивидуальный подход к каждому конкретному больному.
Процесс реабилитации можно разбить на несколько периодов или фаз.
Нулевая фаза
Эта фаза реабилитации начинается через несколько часов после операции. Во-первых, необходимо восстановить кровообращение. Это требуется для нормального функционирования конечности и предотвращения образования тромбов в кровеносных сосудах.
Как только пройдёт действие анестезии, обязательно необходимо делать следующие упражнения (надо помнить, что все упражнения должны выполняться обеими ногами, а не только больной):

Рисунок 11
- Движение стопой ноги вверх-вниз, так называемый «ножной насос». Упражнение необходимо повторять несколько раз каждые 10-15 минут, как только вернётся чувствительность ноги. Проделывать упражнение нужно в течение всего периода реабилитации.
- Вращение голеностопного сустава вправо, затем влево по 5 раз. Следует помнить, что вращение должно производиться только за счёт этого сустава. Колено в данном упражнении не участвует.
- Работа мышцы передней части бедра (четырёхглавая мышца). Нужно напрячь переднюю часть бедра, выпрямив. Носочки можно вытянуть вперёд. Поначалу полного выпрямления ноги не будет, возможно появление боли. Но необходимо стараться, и со временем упражнение начинает
получаться. Удерживать мышцы передней части бедра в напряжении требуется 5-10 секунд. Повторять упражнение по 10 подходов для обеих (!) ног.
- Согнуть колено, двигая пяткой по направлению к ягодицам. Пятку при этом следует прижимать к поверхности. Колено не должно поворачиваться при этом к другой ноге. Тазобедренный сустав не должен сгибаться свыше 90 градусов. Повторять упражнение 10 раз.
- Сжать ягодицы и удерживать в напряжении в течение 5-7 секунд. Повторять упражнение нужно не менее 10 раз.
- В положении лёжа отвести вытянутую ногу вбок на максимально возможную дистанцию, затем вернуть её в исходное положение. В послеоперационные дни это упражнение выполнить, скорее всего, не получиться, но с течением времени оно начинает получаться. Повторять упражнение 10 раз.
- Приподнять выпрямленную ногу вверх на несколько сантиметров. Как и в предыдущем случае, это упражнение сначала не получится выполнить. Повторить упражнение 10 раз.
Первая фаза
Следующая фаза реабилитации после эндопротезирования начинается на 2-й день после операции. В это время пациент сможет вставать и аккуратно передвигаться на костылях, опираясь при этом на больную ногу, но не в полную силу. Со временем эта нагрузка увеличится.
Цель 1-й фазы реабилитации – восстановить способность человека самостоятельно передвигаться, в том числе и по лестнице (первое время, конечно, при помощи костылей).
При передвижении важно соблюдать некоторые правила, а именно:
- Для предотвращения вывиха необходимо сгибать ногу в тазобедренном суставе не более чем на 90 градусов. Запрещено скрещивать ноги, садиться на корточки и закидывать ногу на ногу, когда такая возможность появится в силу стихания боли.
- Во избежание подобных действий во сне, необходимо подкладывать подушки между ног.
- Садиться можно только на такие стулья, где колени не будут возвышаться над уровнем пупка, то есть тазобедренный сустав не будет сгибаться свыше 90 градусов.
- В положении лёжа на спине ноги должны быть немного разведены в стороны, как и в положении сидя.
- Не нагибаться ниже пупка, при одевании обуви или иных действиях сидя, лёжа или стоя. Всегда помните про 90 градусов!

Рисунок 12
Упражнения 1-й фазы:
- В положении стоя поднять колено параллельно земле. Удерживать ногу в таком положении 5 секунд, затем опустить. Требуется несколько подходов для этого упражнения.
- В положении стоя выпрямить ногу и медленно отвести назад (спину в пояснице можно придерживать рукой). Удерживать конечность в таком положении 5 секунд, затем опустить. Повторить упражнение несколько раз.
- Стоя вытянутую ногу отвести в сторону. Удерживать конечность в течение 5 секунд, затем опустить. Повторить упражнение несколько раз.
�
Рисунок 13
Как лечить остеохондроз шейного отдела позвоночника? Помните, полное излечение возможно только на начальных стадиях.
Хруст или треск в коленном суставе не всегда говорит о наличии заболевания.
Вторая фаза
Эта фаза реабилитации после эндопротезирования тазобедренного сустава начинается примерно через неделю после операции, включает в себя упражнения, задача которых состоит в передвижении пациента по лестнице. Они проводятся только при наблюдении и помощи врача, поэтому здесь мы не будем касаться этих упражнений, так как необходимо руководство лечащего врача, которое основывается на состоянии пациента, а также некоторых других факторах.
Третья фаза
Третья фаза реабилитации начинается через 4-8 недель после операции, в зависимости от физического состояния и возраста больного.
В этой фазе необходимо освоить передвижение без костылей, но пока ещё с помощью трости.
Для успешной реализации третьей фазы помогут следующие упражнения:
- Эластичная лента крепится спереди вокруг лодыжки, а другим концом – к надёжной опоре. В положении стоя отвести ногу вперёд, затем вернуть ее в начальное положение. Повторить несколько раз для каждой ноги. Выполнять это упражнение необходимо по 10 раз в день, утром, днём и вечером.
- Упражнение, описанное выше, выполняется точно так же, только эластичная лента закреплена сзади лодыжки. В положении стоя отвести ногу назад, затем вернуть ее в начальное положение. Повторить несколько раз для каждой ноги. Выполнять это упражнение необходимо по 10 раз в день, утром, днём и вечером.
- Эластичная лента закреплена сбоку лодыжки. Отвести выпрямленную ногу вбок, вернуть конечность в начальное положение. Повторить упражнение несколько раз. Выполнять по 10 подходов в день.
- Занятия на велотренажёре прекрасно укрепляют мышцы ног и развивают подвижность суставов.Важно отрегулировать сидение так, чтобы ноги были максимально выпрямлены и едва достигали педалей в крайней нижней точке. Сначала следует заниматься по 10-15 минут 2 раза в день. Со временем нагрузку следует увеличить и заниматься по 30 минут 3-4 раза в неделю, либо чаще.
- Важно проводить упражнения на тренировку баланса. Для этого нужно стоять на одной ноге, опираясь рукой о стену, и приподниматься вверх на носочке. Выполнять по 10 повторов на каждую ногу.
- Ходьба на беговой дорожке в обратном направлении. Стопа перекатывается от пальцев к пятке. Когда стопа всей плоскостью устанавливается на беговой дорожке, колено полностью выпрямлено. Скорость дорожки должна составлять 1-2 км/час.
Итак, после прохождения всего курса реабилитации после эндопротезирования тазобедренного сустава, в результате выполняемых упражнений, человек должен полностью вернуть возможность нормально ходить без помощи трости. При этом тазобедренный сустав восстанавливает свои функции. Это происходит обычно через 7-8 недель после операции. Следует помнить, что для предотвращения травм в дальнейшем необходимо постоянно поддерживать своё тело в хорошей физической форме, и после прохождения курса реабилитации требуется выполнять все указанные выше упражнения.
Пассивное движение после тотального эндопротезирования коленного сустава не оказывает влияния на течение реабилитационного периода Исследователи из Мумбаи, Индия, показали, что выполнение пациентами пассивных упражнений после тотального эндопротезирования коленного сустава оказывает минимальное влияние на течение восстановительного периода. В исследовании приняло участие 84 пациента, все они перенесли операцию тотального эндопротезирования коленного сустава. Наблюдение за ними в послеоперационном периоде продолжалось три месяца. Пациентов разделили на три группы. Первая группа была контрольной: пациентам в послеоперационном периоде не назначались пассивные упражнения. Пациентам из второй группы стандартная схема физиотерапии дополнялась комплексом пассивных упражнений, которые выполнялись на вторые сутки послеоперационного периода два раза в день по 15 минут. В третьей группе пассивные упражнения выполнялись так же, как и во второй, но на 2, 3 и 4 сутки послеоперационного периода. До операции, а также на 3, 5, 14, 42 и 90 сутки послеоперационного периода пациенты проходили стандартизированные тесты для оценки боли, диапазона движения, отека колена и голени и параметров заживления операционных ран. При этом исследователями было обнаружено, что между тремя группами различия в каждом параметре были минимальны. «Мы пришли к выводу, что комплекс пассивных упражнений не дает никаких преимуществ в непосредственном функциональном восстановлении после тотального эндопротезирования коленного сустава и помимо этого еще и увеличивает длительность сохранения послеоперационного отека голени», - пишут авторы исследования.
Исследователи из Мумбаи, Индия, показали, что выполнение пациентами пассивных упражнений после тотального эндопротезирования коленного сустава оказывает минимальное влияние на течение восстановительного периода.
В исследовании приняло участие 84 пациента, все они перенесли операцию тотального эндопротезирования коленного сустава. Наблюдение за ними в послеоперационном периоде продолжалось три месяца. Пациентов разделили на три группы. Первая группа была контрольной: пациентам в послеоперационном периоде не назначались пассивные упражнения. Пациентам из второй группы стандартная схема физиотерапии дополнялась комплексом пассивных упражнений, которые выполнялись на вторые сутки послеоперационного периода два раза в день по 15 минут. В третьей группе пассивные упражнения выполнялись так же, как и во второй, но на 2, 3 и 4 сутки послеоперационного периода.
До операции, а также на 3, 5, 14, 42 и 90 сутки послеоперационного периода пациенты проходили стандартизированные тесты для оценки боли, диапазона движения, отека колена и голени и параметров заживления операционных ран. При этом исследователями было обнаружено, что между тремя группами различия в каждом параметре были минимальны.
«Мы пришли к выводу, что комплекс пассивных упражнений не дает никаких преимуществ в непосредственном функциональном восстановлении после тотального эндопротезирования коленного сустава и помимо этого еще и увеличивает длительность сохранения послеоперационного отека голени», - пишут авторы исследования.
Операцией на межпозвоночном диске не заканчивается лечение межпозвоночных грыж. Чтобы человек вернулся к нормальной жизни, необходим восстановительный период и интенсивная реабилитация. В ряде случаев, после операции развиваются осложнения, хотя в связи с развитием медицинской техники их количество минимально.

Рисунок 14
2.1 ВОЗМОЖНЫЕ ОСЛОЖНЕНИЯ ПОСЛЕ УДАЛЕНИЯ МЕЖПОЗВОНОЧНОЙ ГРЫЖИ
Осложнения можно разделить на интраоперационные и послеоперационные.
Интраоперационные развиваются в ходе операции и во многом зависят от навыков оперирующего хирурга, метода оперативного вмешательства, инструментов, которыми проводится манипуляция. Последствия от операции на позвоночной грыже встречаются разные.
Выделяют два основных осложнения:
- Повреждение нерва. В непосредственной близости от межпозвонковой грыжи, как правило, располагается корешок спинномозгового нерва, сдавливание которого и обуславливает клиническую картину грыжи. При дискэктомии возможно непреднамеренное повреждение этого корешка. В послеоперационный период данный факт будет проявляться нарушением чувствительности или мышечной слабостью в соответствующей ноге (парезы и параличи).
- Повреждение твердой мозговой оболочки. Замеченный разрыв тут же ушивается нейрохирургом, если же разрыв не замечен, то в послеоперационный период возможно развитие интенсивных головных болей вследствие постоянного вытекания ликвора из спинномозгового канала, что сопровождается снижением внутричерепного давления. Данные последствия могут сохраняться до нескольких недель до самостоятельного заживления твердой оболочки.
Послеоперационные осложнения:
- Ранние:
- гнойно-септические осложнения (местные – эпидурит, остеомиелит и общие – пневмония, сепсис);
- тромбоэмболические осложнения (тромбоэмболия легочной артерии, тромбоз вен нижних конечностей).
- Поздние:
- рецидив позвоночной грыжи – наиболее часто встречающееся осложнение. По разным данным составляет от 5 до 30% всех прооперированных грыж;
- рубцово-спаечный процесс в просвете позвоночного канала – сопровождается болевым синдромом в результате ущемления нервов рубцовой тканью.
Уменьшить вероятность развития поздних осложнений после операции на диске и добиться хорошего качества жизни поможет соблюдение рекомендаций врача в восстановительный период и качественная реабилитация.
2.2 РЕАБИЛИТАЦИОННЫЙ ПЕРИОД ПОСЛЕ ОПЕРАЦИИ НА ГРЫЖУ ПОЗВОНОЧНИКА

Рисунок 15
Непосредственно после операции человек чувствует значительное облегчение – уменьшается болевой синдром, восстанавливаются функции тазовых органов и нижних конечностей. Однако стоит помнить, что без восстановительного лечения никак не обойтись. Во время восстановительного периода после удаления грыжи проводятся мероприятия по закреплению достигнутого результата, адаптации позвоночника к новым условиям, формирование новой позвоночной биомеханики.
Условно восстановительный период можно разделить на три этапа:
- на первом человек выполняет рекомендации, направленные на профилактику и борьбу с болевым синдромом;
- на втором – адаптация человека к бытовой жизни;
- на третьем – проводится комплекс мероприятий, основное назначение которых – полное восстановление биомеханики позвоночника, профилактика рецидива межпозвонковой грыжи, укрепление опорно-двигательного аппарата и возвращение к полноценной жизни.
В зависимости от тяжести перенесенной операции и объема восстановительный период длится от 4 до 12 месяцев, в среднем занимая около полугода.
Рекомендации в ранний послеоперационный (восстановительный) период:
- В течение 1-1,5 месяцев после операции не сидеть – во избежание раннего рецидива грыжи и компрессии нервных корешков;
- Избегать резких и сильных движений с участием позвоночника – наклоны вперед и вбок, повороты со скручиванием позвоночника;
- Ездить в автомобиле или другом виде транспорта только в качестве пассажира на разложенных сиденьях, в положении полулежа;
- Избегать поднятия тяжелых предметов – максимальный вес 3-4 кг в каждой руке;
- Каждые 1,5-2 часа давать отдых позвоночнику – лежать в течение 15-25 минут;
- Носить полужесткий корсет. Для тренировки позвоночника время ношения стоит ограничить тремя часами в день.
Для ускорения процессов репарации (восстановления) в этот период можно рекомендовать физиотерапевтические методы воздействия: лазеротерапию, диадинамотерапию, синусоидальные модулированные токи, электрофорез в позвоночной области.
Для купирования болевого синдрома используют нестероидные противовоспалительные средства.
В общем, ранний реабилитационный период после удаления грыжи можно охарактеризовать охранительным режимом – за это время заживает послеоперационный рубец, стихает воспалительный процесс. Далее можно переходить к более интенсивной реабилитации.
Рисунок 16
2.3 ИНТЕНСИВНАЯ РЕАБИЛИТАЦИЯ В ПОСЛЕОПЕРАЦИОННЫЙ ПЕРИОД
После операции удаления грыжи открытым методом пациент выписывается из стационара через 3-4 недели, а при эндоскопической дискэктомии – через 1-2 недели. Со второго месяца можно приступить к интенсивной реабилитации, включающей профилактику межпозвонковой грыжи.
На этом этапе в программу реабилитации включается ЛФК, восстановительная гимнастика. Эти процедуры лучше проводить под руководством специалиста. Оптимальным вариантом является прохождение санаторно-курортного лечения. В санаториях работают опытные инструкторы ЛФК, имеются бассейны – плавание в восстановительный период имеет большое значение.
Если возможности попасть в санаторий или реабилитационный центр нет, можно воспользоваться видео-уроками – многие разработчики восстановительных программ публикуют видео-уроки в сети интернет.
Вот небольшой комплекс упражнений – восстановительная зарядка для самостоятельного выполнения:
- В положении на спине медленно сгибайте ноги, стараясь прижать колени к груди. Расслабьте ягодичные мышцы и попытайтесь удержать такую позу 45-60 секунд. Медленно выпрямите ноги.
- Лечь на спину, раскинуть руки. Ноги согнуть в коленях и, опираясь на них, приподнять таз. Удерживать сначала 10-15 секунд. Постепенно увеличить время до 60 секунд.
- Положение на спине. Руки заведены за голову, ноги согнуты в коленях. Поворачивайте ноги, стараясь коленями достать пола – влево и вправо. Верхняя часть туловища должна держаться горизонтально.
- Исходное положение – опираясь на руки и колени. Одновременно вытягиваем противоположные руку и ногу горизонтально и держим так 5-10 секунд – меняем ноги с руками. Время выполнения упражнения увеличить до 45-60 секунд.
- Лежа на животе, руки под подбородком. Медленно поднимайте вытянутую ногу вверх, не отрывая от пола таз, — опустите ногу. Повторите упражнение с другой ногой.
В дополнение к восстановительной гимнастике после операции по поводу межпозвонковой грыжи рекомендуется проходить сеансы иглотерапии.
Поздний период восстановления
Через 6-8 месяцев после операции на межпозвоночном диске под контролем врача можно приступить к восстановлению мышечного корсета. Активность упражнений на укрепление мышц спины значительно увеличивается.
В этот период в комплексное лечение добавляются процедуры мануальной терапии и массаж – не реже двух раз в год. Эти процедуры позволяют окончательно восстановить кровообращение в проблемном участке, вернуть пациента к активному образу жизни и проводить профилактику рецидива грыжи межпозвоночного диска после ее удаления.
Не рекомендуется поднимать вес более 5-9 кг, прыгать с высоты, длительно сидеть или стоять.
Выходя на улицу, не допускайте переохлаждения спины – на область поясницы необходимо надеть утепляющий пояс. Стоит отказаться от ношения укрепляющего корсета, чтобы избежать атрофии мышц спины.
3 ВАРИАНТ АППАРАТНОГО МОНИТОРИНГА КРИТИЧЕСКИХ ПАРАМЕТРОВ В ПЕРИОД РЕАБИЛИТАЦИИ.
ПРИМЕРНЫЙ ГРАФИК РЕАБИЛИТАЦИОННЫХ МЕРОПРИЯТИЙ ПОСЛЕ ОПЕРАЦИИ ЭНДОПРОТЕЗИРОВАНИЯ МЕЖПОЗВОНОЧНОГО ДИСКА
Таблица 1
|
Дни, недели,
месяцы
|
Двигат. режим
|
лечебная гимнастика (ЛФК)
|
массаж
|
физиотерапия
|
рефлексотерапия
|
КОНТРОЛЬ
|
|
До операции
|
|
|
|
|
|
предоперационное
обследование
|
|
операция
|
|
|
|
|
|
|
|
1 сутки
|
постельн.
|
постельная
гимнастика
|
М
|
|
|
|
|
2 сутки
|
постельн.
|
постельная
гимнастика
|
М
|
|
|
|
|
1 неделя
|
расшир.
|
постельная
гимнастика
|
М
|
ФТ
|
|
|
|
2 неделя
|
расшир.
|
расш.
|
М
|
ФТ
|
|
|
|
3 неделя
|
расшир.
|
расш.
|
М
|
ФТ
|
|
|
|
4 неделя
|
активный
|
спец. комплекс
|
М
|
ФТ
|
РТ
|
|
|
2 месяц
|
активный
|
спец. комплекс
|
М
|
ФТ
|
|
|
|
3 месяц
|
активный
|
спец. комплекс
|
М
|
|
|
|
|
4 месяц
|
активный
|
спец. комплекс
|
М
|
|
РТ
|
|
|
5 месяц
|
активный
|
спец. комплекс
|
М
|
|
|
|
|
6 месяц
|
активный
|
спец. комплекс
|
М
|
|
РТ
|
|
- рентгенография
- УЗИ исследование
- мониторинг во время ЛФК
- периодический мониторинг
ЗАКЛЮЧЕНИЕ
Накопленный опыт создания многоканальных систем мониторинга позволил реализовать на практике принципиально новый класс медицинского оборудования, предназначенного для системной диагностики дисфункций организма в режиме удалённой связи.
Положенный в основу разработки принцип интегративной медицины предполагает объединение нескольких методик и средств их реализации в одном комплексе. Применение такого комплекса на практике делает доступным в рамках одного сеанса обследования реализовать сразу несколько методик с синхронной визуализацией и обработкой полученных результатов. Клинические исследования показали, что контроль терапии, основанный на мультидиагностических принципах, применительно к каждому индивидуальному случаю позволяет достичь гораздо лучших результатов по сравнению с обычным подходом, исходящим только из выявленной патологии.
Клиническая эффективность комплексной диагностики определяется повышением качества и достоверности подготовки заключения и, как следствие, высокой эффективностью лечения. Количество интегрируемых средств и методов обследования определяется содержанием клинических задач и может варьироваться в широких пределах.
Функциональные возможности «ВебМультиМедик» удачно сочетаются с удобством его эксплуатации, как начинающими, так и опытными специалистами для разнообразных задач клинической практики.
Таким образом, можно сделать вывод, что созданная система для дистанционной мультидиагностики «ВебМультиМедик» открывает новые возможности в развитии медицинского обслуживания пациентов с различными видами заболеваний, однако ее широкое применение требует от медиков отказа от узкой специализации и расширения своих профессиональных компетенций с целью оптимального и полноценного использования возможностей мультидиагностики, каналов биологической обратной связи и современных информационных технологий.
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
- Адаскин А.В., Исакова О.И., Сергейчик В.В., Филатов И.А., Загребин Д.А. Мультимодальные средства функциональной диагностики летного и диспетчерского состава гражданской авиации // Вестник Московского авиационного института, 2011. Т. 18. № 3.
- Акжигитов Р.Ф., Истомина Т.В., Сафронов А.И., Киреев А.В. Мультиди-агностическая система для постоперационных больных с эндопротезами // Матер. региональной конференции (г. Пенза, 7 июля 2011 г.): Исследования и инновационные разработки в сфере медицины и фармакологии. – Пенза: Изд-во ПГУ, 2011. – С. 3-6.
- Белоглазова Т.И. Медицинская реабилитация больных после тотального эндопротезирования тазобедренного сустава / Т.И. Белоглазова, В.Г. Масленникова, О.В. Кузьменко // Медицина в Кузбассе. – 2003. – № 2 (спецвыпуск) – C. 108–110.
- Гаже П-М. Постурология. Регуляция и нарушения равновесия тела человека. / П-М. Гаже, Б. Вебер Пер. с французского под ред. В.И. Усачёва – СПб.: Издательский дом СПбМАПО, 2008. – 316 с.
- Гроховский С.С., Кубряк О.В., Филатов И.А. Архитектура сетевых медицинских систем для оценки функции равновесия (стабилометрия) и комплексной оценки состояния человека // Информационно-измерительные и управляющие системы. – №12, 2011.
- Гусев Е.И. Реабилитация в неврологии / Е.И. Гусев, А.Н. Коновалов А.Б. Гехт // Кремлевская медицина. 2001. – № 5, с. 29-32.
- Гусева А.Л., Бауш Я.А., Лучихин Л.А. Опыт применения стабилометрического комплекса ST-150 «Stabip» в физической реабилитации пациентов с вестибулярными расстройствами // Материалы IX Всероссийского конгресса оториноларингологов «Наука и практика в оториноларингологии», Москва. 8–9 ноября 2010.
- Девликанов Э.О., Болонев А.Г., Балязин В.А., Слива С.С. Стабилография в оценке эффективности лекарственных средств у больных с хронической сосудистой мозговой недостаточностью // Научно-практическая конференция «Неврология – реабилитация, биомеханика». Сборник научно-практический работ. – Москва, 23-25 апреля 2003. – С. 26-27.
- Епифанов В.А. Физическая реабилитация при цереброваскулярной патологии / В.А. Епифанов // ЛФК и массаж. 2002. – № 2. – С. 43-46.
- Жаворонкова Л.А., Максакова О.А., Киш А.А., Щекутьев Г.А. Использование стабилографии при комплексной оценке динамики реабилитационного процесса больных с последствиями тяжелой черепно-мозговой травмы // VII Международная конференция «Современные технологии восстановительной медицины». – Сочи, Центральный клинический Санаторий им. Ф.Э. Дзержинского, 11-16 мая 2004.
- Истомин В.В., Истомина Т.В., Киреев А.В., Сафронов А.И. Программно-методическое обеспечение системы дистанционной мультидиагностики и реабилитации больных после эндопротезирования тазобедренного сустава // Научно-технический вестник Поволжья, 2011. – № 1. – С. 113-115.
- Истомина Т.В., Киреев А.В., Истомин В.В., Сафронов А.И., Карамышева Т.В. Патент на полезную модель № 122009. Стабилометрический тренажер. Заявка № 2011137881. Зарегистрировано в Государственном реестре полезных моделей Российской Федерации 20 ноября 2012 г.
- Кадыков А.С. Реабилитация после инсульта / А.С. Кадыков. М.: МИК-ЛОШ, 2003. – 176 с.
- Киселев Д.А., Гроховский С.С., Кубряк О.В. Консервативное лечение нарушений опорной функции нижних конечностей в ортопедии и неврологии с использованием специализированного стабилометрического комплекса ST-150. М.: Маска. 2011.
- Кубряк О.В., Гроховский С.С. Постуральный тест с биологической обратной связью в оценке влияния привычного сеанса курения на показатели баланса у здоровых добровольцев // Наркология. 2011. № 9.
- Курбанов С.Х. Индивидуальная реабилитация больных после эндопротезирования тазобедренного сустава: Автореф. дис…докт.мед.наук. – СПб., 2009. – 38 с.,
- Майорникова С.А. Методические приемы восстановления функции ходьбы у больных с постинсультными гемипарезами: Автореф. дис. … канд. пед. наук. 2006.
- Неверов В.А., Курбанов С.Х. Восстановительное лечение дегенеративно-дистрофических заболеваний крупных суставов. Вестник хирургии – 2004. – № 2. С. 97 – 99.
- Святогор И.А. Метод биоуправления потенциалами головного мозга и его клиническое применение / И.А Святогор // Биологическая обратная связь. – 2000. – № 1.- С. 5-7.
- Скворцов Д.В. Диагностика двигательной патологии инструментальными методами: анализ походки, стабилометрия / Д.В. Скворцов – М.: Т.М. Андреева, 2007. – 640 с.
- Скворцов Д.В. Стабилометрическое исследование. М.: Маска. 2010.
- Скворцова В.И. Биомеханические аспекты реабилитации больных с инсультом / В.И. Скворцова, Е.А. Ковражкина, В.В. Гудкова // Журнал неврологии и психиатрии им. С.С. Корсакова. 2005. – Т. 105, № 7. – С. 2632.
- Слива, С.С. Отечественная компьютерная стабилография: состояние, проблемы и перспективы / С.С. Слива, И.В. Кондратьев, А.С. Слива // Материалы МИС–2008. – Таганрог, 2008.
- Сохадзе Э.М. Биологическая обратная связь: анализ тенденций развития экспериментальных исследований и клинического применения / Э.М. Сохадзе, В.И. Хиченко, М.Б. Штарк // Биоуправление-3: теория и практика. Новосибирск, 1988. – С. 7-16.
ПРИЛОЖЕНИЯ
ПРИЛОЖЕНИЕ 1
ПРИЛОЖЕНИЕ 2
Реабилитация больных после эндопротезирования межпозвоночного диска