Физические методы исследования в химии
ФИЗИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ В химиИ
Лекция № 1. ВВЕДЕНИЕ
1.1.Предмет «Физические методы исследования в химии.
Развитие всех разделов химии – неорганической, аналитической, физической, органической, биологической, химической технологии и т.д. – на современном этапе развития химической науки невозможно без использования физических методов исследования, поскольку чисто химические методы анализа и исследования себя практически исчерпали. Поэтому всякий уважающий себя современный химик обязан уметь применять любые физические методы исследования, которые могут оказать ему помощь в решении стоящих перед ним химических проблем. При этом исследователь должен знать основные принципы метода, его возможности и ограничения.
Без физических методов исследования невозможно решение очень сложной и актуальной задачи охраны природы, ибо позволяют весьма эффективно и быстро контролировать состояние (проводить мониторинг) окружающей среды, как невозможно автоматически контролировать технологический производственный процесс с целью предотвращения выбросов вредных веществ в окружающую среду.
Без физических методов невозможно представить себе автоматизацию научных исследований и повышение их эффективности, как невозможна и автоматизация химических производств. Более того, физические методы позволяют включить в автоматическую систему управления научными исследованиями (как и производством) ЭВМ и ускорить обработку получаемых результатов.
Среди физических методов исследования наибольшее распространение получили следующие методы спектроскопии: ядерный магнитный резонанс (ЯМР), электронный парамагнитный резонанс (ЭПР), электронной и колебательной спектроскопии. К электронной спектроскопии относится УФ (ультрафиолетовая) и видимая области, к колебательной спектроскопии относятся ИКС и СКР (инфракрасная и спектроскопия комбинационного рассеивания). Из методов, не использующих электромагнитное излучение, широко применяется метод масс-спектрометрии. Кроме названных, в химии применяют и другие методы: Месбауэровская спектроскопия (спектроскопия -резонанса), рентгеновская спектроскопия, хироптические методы – дисперсия оптического вращения (ДОВ) и круговой дихроизм (КД) , электронография и нейтронография, ядерный квадрупольный резонанс (ЯКР).
В предлагаемом вам курсе основное внимание будет уделено следующим методам: ЯМР, электронной и колебательной спектроскопии, масс-спектрометрии. Прежде чем перейти к рассмотрению каждого конкретного метода, остановимся на некоторых общих вопросах.
1.2. Природа света.
Световое излучение представляет собой поток фотонов – наименьших порций световой энергии, имеющих одновременно и корпускулярную, и волновую природу. Корпускулярная природа проявляется в том, что электромагнитное излучение испускается и поглощается квантами величиной h. Но световой поток одновременно является и электромагнитной волной, свойства которой проявляются в явлениях интерференции и дифракции.
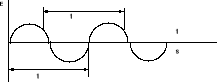
Распространение света можно представить себе как изменение электрического и магнитного полей в пространстве и во времени. Эти изменения носят синусоидальный характер и их можно представить графически:
По оси у откладывается напряженность (интенсивность) электрического (Е) или магнитного (Н) полей, по оси х либо время t изменения напряженности поля в данной точке пространства, либо расстояние при отображении изменения напряженности поля в пространстве в данный момент времени. Колебания электрического и магнитного полей совершаются во взаимно перпендикулярных плоскостях.
Электромагнитная волна в вакууме движется со скоростью С=31010 см/с. Длина волны - это расстояние между двумя соседними эквивалентными точками на графике изменения напряженности поля в пространстве. Эквивалентные точки – те, которые находятся в одной фазе, т.е. когда напряженность поля и знак и величина производной в таких точках одинаковы.
Время t, необходимое для прохождения волной расстояния, равного длине волны, равно t = /С. Величина, обратная t, известна подназванием частота волнового движения и равна числу колебаний в 1 с : 1/ t = = С/ ( с1) Отсюда получаем универсальное соотношение:
С = .
Следовательно, частоту, как и длину волны, можно использовать для характеристики электромагнитных колебаний, ибо зная одну из них, можно вычислить другую.
Для характеристики световой волны в ИКС используют также величину, обратную длине волны: 1/ . Если длину волны выразить в см, то величина 1/ означает число длин волн, вмещающихся на отрезке длиной в 1 см, и называется волновым числом с размерностью см1. Обозначают его через , тогда: = 1/ = (1/С). Волновое число пропорционально частоте, а коэффициент пропорциональности – 1/С. Символ не используется, а обозначают и волновое число и частоту одним символом . Это однако не вносит никакой путаницы, ибо либо из контекста, либо из размерности легко определить, о чем ведется речь. Частота имеет размерность с1 и измеряется в Герцах (Гц), тогда как волновое число в см1.
1.3. Единицы измерения длин волн и частоты.
Длины волн измеряются в следующих единицах:
– Ангстрем, 1 = 108 см (десять минус восьмая степень доли см);
нм – нанометр (одна миллиардная доля метра), 1нм = 109 м = 107 см = 10;
мкм – микрометр (одна миллионная доля метра), 1мкм = 106 м = 104 см;
см, м.
Частоты измеряются в Гц (1Гц =1колебание/с), 1МГц = 106 Гц.
1.4. Типы излучения
Весь диапазон длин волн, используемых в спектральных методах, разбит на поддиапазоны, типы излучения, как это представлено в таблице:
|
Излучение
|
Диапазон
, см
|
,
см
|
h,
Дж/моль
|
Процессы, происходящие при взаи-
модействии вещества с излучением
(вид спектроскопии)
|
|
-Излуч.
Рентген.
излучение
УФ и ви-
димое из- лучение
ИК-излу-
чение
Микро-
волны
Радио-
волны
|
1011108
108106
106104
104102
102100
100
|
1010
107
2105
103
1
500
|
1011
1,2108
6106
1,2104
12
0,024
|
Перестройка ядер (-резонанс)
Изменение состояния внутренних электронов атомов (рентгеновськая спектроскопия)
Изменение состояния валентных электронов атомов и молекул (электронная спектроскопия)
Изменение колебательных состоя-ний атомов в молекулах (колеба-тельная спектроскопия: ИКС, СКР)
Изменение вращательных состояний молекул (микроволновая спектро-скопия), изменение спиновых состо-яний электронов (ЭПР)
Изменение спиновых состояний
ядер (ЯМР, ЯКР)
|
Энергия связи: СС – 3,5105 , СС – 8,1105 Дж/моль
Вся область электромагнитного спектра не может быть исследована при помощи одного типа приборов, так как экспериментальные методы сильно изменяются при изменении типа излучения. Однако, основные блоки приборов остаются одними и теми же по назначению (но разными по устройству и конструкции, а принцип их действия может фундаментально изменяться) независимо от вида излучения. Для наблюдения спектров поглощения при любых длинах волн требуются следующие основные блоки:
- Источник излучения;
- Кювета с образцом;
- Монохроматор – диспергирующее устройство, позволяющее выделить из потока полихроматических волн монохроматичемкое излучение (характеризуется одной длиной волны, а кванты этого излучения имеют одинаковую энергию);
- Приемник излучения для измерения интенсивности излучения, прошедшего через образец;
- Регистрирующее устройство (гальванометр, дисплей или самописец).
1.5. Типы задач, решаемых спектральными методами.
При решении химических проблем спектральные методы позволяют решать две задачи – прямую и обратную.
Прямая задача – установление изменения излучения, поля или потока частиц вследствие взаимодействия с веществом с известным набором свойств, в том числе и строения его молекулы.
Обратная задача – установление совокупности свойств вещества, в том числе и строения его молекул, исходя из изменений излучения, поля или потока частиц вследствие их взаимодействия с исследуемым веществом.
Каждый спектральный метод решает только ему присущие задачи, имея при этом определенные ограничения. Каждый химик должен знать эти возможности и ограничения, чтобы поставить исследовательскую задачу корректно, когда метод может ее решить. Некорректно поставленная задача, когда метод решить ее в принципе не может, повлечет за собой бесполезную трату человеческих ресурсов, времени и материальных средств. В этом случае химик будет некомпетентным и не соответствующим своему положению и должности.
1.6. Историческая справка.
Авторство Рентгена об открытии рентгеновских лучей не было оспорено, хотя и оспаривалось физиком, выходцем из Западной Украины Иваном Полюем, который учился у выдающегося физика Макса Планка, работал в Вене. Именно Иван Полюй открыл излучение, изобрел свои рентгеновские лампы, которые, судя по научным публикациям, были лучше, чем у Рентгена (да и раньше появились). Рентген якобы открыл Х-лучи в 50-летнем возрасте, давно будучи профессором и директором физического института, вращался среди выдающих физиков, и, естественно, знал о работах Полюя, сумел заявить об изобретении как о своем собственном.
Попытки Полюя отстоять свое авторство (обращался во многие научные общества Европы) ни к чему не привели, он обращался даже к Эйнштейну, на что последний ответил, что за Рентгеном стоит вся Европа, а «за тобой, Иван, только далекая Рутения».
EMBED ISISServer 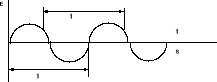
Физические методы исследования в химии