Ацилирование и алкилирование аминов
КУРСОВАЯ РАБОТА
по дисциплине: «Дополнительные главы органической химии»
на тему: «Ацилирование и алкилирование аминов»
Содержание
1. Введение ………………………………………………………………… 3
2. Ацилирование и алкилирование аминов ………………………………. 5
2.1. Амины: номенклатура, классификация, применение …………… 5
2.2. Химические свойства аминов ……………………………………... 9
2.2.1. Основные и кислотные свойства ……………………………. 9
2.2.2. Реакции ацилирования ……………………………………… 12
2.2.3. Реакции алкилирования …………………………………….. 17
2.2.4. Ацилирование и алкилирование по Фриделю-Крафтсу ….. 21
2.2.5. Взаимодействие аминов с азотистой кислотой …………… 25
2.3. Методы получения аминов ………………………………………. 28
2.3.1. Алкилирование аммиака и аминов ………………………… 28
2.3.2. Восстановление азотсодержащих органических соединений …………………………………………………... 29
2.3.3. Перегруппировка Гофмана …………………………………. 30
2.4. Биологически активные амины и их производные …………….. 30
2.5. Акридон: получение, свойства и применение ………………….. 36
2.6. 9-аминоакридин: получение, свойства и применение …………. 38
3. Заключение …………………………………………………………….. 39
4. Список литературы …………………………………………………….. 40
1. Введение
Амины — производные аммиака, в молекуле которого один, два или три атома водорода заметены углеводородными радикалами. По числу замешенных атомов водорода они делятся на первичные, вторичные и третичные амины.
Существуют и четвертичные аммониевые соли, например хлорид тетраметиламония, соответствующее ему основание — гидроксид тетраметиламмония, который представляет собой сильное основание, аналогичное щелочных металлов, так как связь с гидроксильной группой здесь ионная [10].
В зависимости от природы углеводородных радикалов амины подразделяются на алифатические, алициклические, ароматические и смешанные (имеющие алифатический и ароматический радикалы). Эти соединения отличаются друг от друга строением углеводородных радикалов.
Названия простых по строению аминов образуют от названий соответствующих углеводородных радикалов, связанных с атомом азота, добавляя в конце корень-амин. Кроме того, ароматические амины имеют тривиальные названия.
Химические свойства аминов определяются в основном присутствием атома азота с неподеленной парой электронов, наличие которой обуславливает их основные и нуклеофильные свойства.
Нуклеофильность и основность аминов изменяются, как правило, симбатно: они уменьшаются с уменьшением электроннной плотности на атоме азота или при его пространственном экранировании и увеличиваются с увеличением электронной плотности на атоме азота или с увеличением его доступности.
Амины, чаще в виде полифункциональных производных, находят применение, являясь обычно полупродуктами в органических синтезах. Получаются с применением аминов такие лекарственные препараты, как новокаин, спазмолитин, парацетамол, сульфаниламидные препараты [1].
Широко амины и их производные применяется в производстве инсектицидов, фунгицидов, ускорителей вулканизации, поверхностно-активных веществ, красителей, ракетных топлив, растворителей и т.д.
Все выше сказанное подтверждает актуальность темы представленной работы.
Цель работы: изучить реакции ацилирования и алкилирования аминов.
Для достижения поставленной цели были определены следующие задачи:
1. Рассмотреть общую характеристику аминов.
2. Рассмотреть химические свойства аминов.
3. Проанализировать методы получения аминов.
4. Дать характеристику биогенным аминам.
5. Представить получение, свойства и применение 9-аминоакридина.
2. Ацилирование и алкилирование аминов
2.1. Амины: номенклатура, классификация, применение
Аминами называются органические производные аммиака, в котором один, два или все три атома водорода замещены на углеводородные радикалы ( предельные, непредельные, ароматические).
Название аминов производят от названия углеводородного радикала с добавлением окончания -амин или от названия соответствующего углеводорода с приставкой амино-.
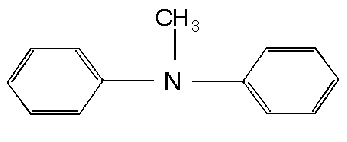
Примеры приведена на Рис. 1:
CH3 – NH2 CH3 – NH – C2H5
метиламин метилэтиламин метилдифениламин
фениламин (анилин)
Рис. 1. Примеры полуструктурных формул аминов и их названия
В зависимости от числа атомов водорода, замещенных в аммиаке на углеводородные радикалы, различают первичные, вторичные и третичные амины (Рис. 2):
R
R- NH2 R – NH – R’ R – N – R”
первичный амин вторичный амин третичный амин
Рис. 2. Классификация аминов. R, R’, R’’ – углеводородные радикалы
Алкиламины содержат только алифатические углеводородные радикалы, например (Рис. 3):
Рис. 3. Примеры алкиламинов
Ариламины содержат ароматические радикалы с атомом азота в ароматическом кольце, например (ри№с. 4):
Рис. 4. Примеры ариламинов
Алкилариламины содержат алифатические и ароматические радикалы, например (Рис. 5):
Рис. 5. Примеры алкилариламинов
Гетероциклические амины содержат азот в цикле, например (Рис. 6):
Рис. 6. Примеры гетероциклических аминов
Амины, чаще в виде полифункциональных производных, находят применение, являясь обычно полупродуктами в органических синтезах. Получаются с применением аминов такие лекарственные препараты, как новокаин, спазмолитин, парацетамол, сульфаниламидные препараты [5].
Широкое применение нашли соединения с упрощенной адреналиновой структурой, такие, как эфедрин, амфетамин, первитин и т.д. (Рис. 7)
Рис. 7. Формулы эфедрина (а), амфетамина (b), первитина (с)
Эти соединения, обладая структурой близкой к структуре адреналина, оказывают стимулирующее, возбуждающее действие, но более сильное и продолжительное.
Амины широко используются в качестве термо- и светостабилизаторов (Рис. 8):
Рис. 8. Формулы представителей аминов термо- и светостабилизаторов
Амины могут выступать в роли модификаторов резин и как вулканизирующие агенты (Рис. 9):
Рис. 9. Формулы представителей аминов модификаторов резин и вулканизирующие агенты
Мономеры для синтеза полиамидов (Рис. 10):
Рис. 10. Формулы представителей аминов
мономеров для синтеза полиамидов
Амины могут быть использованы и как красители (Рис. 11):
Рис. 11. Формулы представителей аминов красителей
Фотореактивы (Рис. 12):
Рис. 12. Формулы представителей аминов фотореактивов
Метиламин применяется в производстве инсектицидов, фунгицидов, ускорителей вулканизации, поверхностно-активных веществ, красителей, ракетных топлив, растворителей.
Триэтиламин применяется в производстве ускорителей вулканизации, ингибиторов коррозии, растворитель.
Анилин: производство N,N-диметиланилина, дифениламина, лекарственных средств, антиоксидантов, ускорителей вулканизации и фотоматериалов.
Некоторые амины применяются как селективные растворители для извлечения урана из сернокислых растворов. Амины, обладающие запахом рыбы, используются как приманка в борьбе с полевыми грызунами.
Третичные амины и соли четвертичных аммониевых оснований получили широкое распространение в качестве катализаторов межфазного переноса в органическом синтезе [2,3].
2.2. Химические свойства аминов
Химические свойства аминов определяются в основном присутствием атома азота с неподеленной парой электронов, наличие которой обуславливает их основные и нуклеофильные свойства.
2.2.1. Основные и кислотные свойства
Алифатические амины являются сильными основаниями (= 10-11) и превосходят по основности аммиак. Их водные растворы имеют щелочную реакцию:
RNH2 + H2O RNH3+ + OH – (1)
Ароматические амины – слабые основания (= 3-5), что связано с разрушением при протонированиии стабильной сопряженной системы, в которой участвует неподеленная пара электронов азота (см. лек. №4).
При взаимодействии с кислотами амины образуют растворимые в воде аммониевые соли:
RNH2 + HX RNH3+ X - (2)
Первичные и вторичные амины являются слабыми N-H кислотами (рКа=33-35) и образуют соли при взаимодействии с активными металлами:
RNH2 + Na RNH- Na+ + 1/2 H2 (3)
Характер групп, находящихся у атома азота, оказывает боль�шое влияние на основность амина. Обычно алифатические амины, являются сильными основаниями, обладают щелочной реакцией на лакмус и во влажном состоянии поглощают двуокись углерода. Низшие алифатические амины являются, более сильными основаниями, чем аммиак, и титруются кислотами в присутствии метилоранжа или бромфенолблау в качестве индикатора. При наличии ароматического остатка основность аминов выражена значительно слабее; например, анилин и его гомологи, хотя и образуют соли с разбавленными минеральными кислотами, однако не дают щелочной реакции на лакмус и не поглощают двуокись углерода из воздуха. Титрование таких аминов кислотой в присутствии обычных индикаторов не дает удовлетворительных результатов. Напротив, солянокислые соли ароматических аминов легко титруются водным раствором щелочи в присутствии фенолфталеина, т.е. ведут себя в этих условиях, как свободные кислоты. При увеличении числа ароматических радикалов у атома азота наблюдается еще большее уменьшение основности амина. Соли дифениламина гидролизуются в воде в значительной степени с частичным выделением свободного основания. Трифениламин является нейтральным соединением и не образует солей, за исключением комплексного соединения с хлорной кислотой.
Хотя введение нитрогруппы в ядро анилина заметно понижает его основность, нитранилины все же еще обладают основным характером и дают соли с минеральными кислотами, которые, однако, очень легко, гидролизуются при действии воды. Введение более одной нитрогруппы в ядро ведет к дальнейшему понижению основности; действительно, иолинитрамины проявляют лишь незначительную склонность к образованию солей. То же относится и к галоидозамещенным аминам [2].
Обычно, для получения соли к амину прибавляют небольшой избыток кислоты, например разбавленной серной, концентрированной или разбавленной соляной или бромистоводородной кислоты. Если при этом соль не выпадает, раствор упаривают на водяной бане или в вакуум-эксикаторе до начала кристаллизации. Если галоидоводородные соли плохо кристаллизуются из водного раствора, их получают другим путем, а именно пропусканием сухого галоидоводорода в раствор амина в бензоле, хлороформе или эфире. Этот метод особенно удобен для получения галоидоводородных солей алкиланилинов и диалкиланилинов, а также аминов, соли которых легко гидролизуются водой. При пропускании сухого хлористого водорода в раствор диалкиланилина в сухом эфире до насыщения соответствующие солянокислые соли легко выделяются в кристаллическом состоянии. При этом следует тщательно предохранять реакционную смесь от доступа влаги. Солянокислые соли низших алкиланилинов лучше всего получать в бензольном растворе. Впрочем, в случае алкиланилинов, содержащих сравнительно большие алкильные радикалы, этот способ не дает таких удовлетворительных результатов.
Большинство аминов образует хорошо кристаллизующиеся пикраты, которые могут служить для идентификации аминов или для выделения их из смесей. Обычно, пикраты получаются смешением обоих компонентов в подходящем растворителе, выбор которого определяется сравнительной растворимостью в нем пикриновой кислоты, пикрата и амина. Менее удобно пользоваться для этой цели реакцией обмена. Пикролоновая кислота также применяется для идентификации аминов, особенно в тех случаях, когда пикриновая кислота не дает удовлетворитель�ных результатов. Соли пикролоновой кислоты обычно труднее растворимы, чем пикраты, и обладают более высокой температурой плавления. Этот способ применяется главньм образом для идентификации простейших алифатических производных гидроксиламина, производных морфолина и некоторых алкалоидов. Кроме того, для идентификации аминов также применяется имидазолдикарбоновая кислота.
Ароматические амины образуют продукты присоединения с ди- и тринитросоединениями. Эти продукты также иногда служат для идентификации аминов. Некоторые амины при действии 70% водной хлорной кислоты дают хорошо кристаллизующиеся соли, которые могут служить для их выделения и идентификации [3,4].
2.2.2. Реакции ацилирования
Ацилирование – введение ацильной группы (ацила) RC в молекулу органического соединения путем замещения атома водорода. В широком смысле ацилирование это замещение любого атома или группы атомов на ацила. В зависимости от атома к которому присоединяют ацил различают C-, N-, O-, S – ацилирование.
Реакции ацилирования обладают очень многими полезными свойствами. Они позволяют вести в молекулу функциональную группу C=O путем реакций присоединения либо замещения, не подвергая исходную молекулу окислению (восстановлению). Таким образом, можно получать соединения различных классов: а) амиды; б) сложные эфиры; в) ангидриды карбоновых кислот; г) кетоны и другие полезные соединения. Неудивительно, что реакции ацилирования находят широкое применение в промышленности и в химических исследованиях. В своей курсовой работе я рассмотрю три наиболее важных типа реакций ацилирования C-ацилирование, O-ацилирование и N-ацилирование.
Ацилирование аминов ацилгалогенидами

Реакции аминодегалогенирования наиболее часто используются для синтеза амидов. Действие аммиака или аминов на ацилгалогениды представляет собой общий метод синтеза амидов (Рис. 13):
Рис. 13. Общий метод синтеза амидов
Реакция сильно экзотермична и требует тщательного контроля, обычно охлаждением или разбавлением. При использовании аммиака получают незамещенные амиды, из первичных аминов получают N-замещенные амиды, а из вторичных аминов – N, N-дизамещенные амиды. Аналогично можно ацилировать ариламины. В некоторых случаях для связывания выделяющейся галогеноводородной кислоты добавляют водный раствор щелочи. Такая реакция носит название метода Шоттена-Баумана.
Гидразин и гидроксиламин также реагируют с ацилгалогенидами, давая соответственно гидразиды RCONHNH2 и гидроксамовые кислоты RCONHOH; эта реакция часто используется для синтеза данных соединений. Если вместо ацилгалогенида взять фосген, то как ароматические, так и алифатические первичные амины дают хлороформамиды ClCONHR, которые теряя HCl, превращаются в изоцианаты RNCO. Это один из наиболее распространенных методов синтеза изоцианатов.
Тиофосген при аналогичной обработке дает изотиоцианаты. Фосген в этой реакции можно заменить более безопасным трихлорометилхлороформиатом. При действии первичных аминов на хлороформиаты ROCOCl получаются карбаматы ROCONHR’. Примером этой реакции служит защита аминогруппы в аминокислотах и пептидах действием карбобензоксихлорида (Рис. 14):
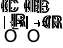
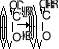
Рис. 14. Защита аминогруппы в аминокислотах и пептидах
действием карбобензоксихлорида
Аминогруппы вообще часто защищают превращением в более устойчивые – амидные. Взаимодействие ацилгалогенидов с нитридом лития дает N, N-диациламиды (триациламины).
Ацилирование аминов ангидридами
По механизму и диапазону применимости реакция амино-деацилоксизамещения может быть проведена с участием аммиака, первичных или вторичных аминов (Рис. 15)
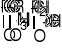
Рис. 15. Реакция аминодеацилоксизамещения
Однако при использовании аммиака и первичных аминов получаются также и имиды, в которых с атомом азота связаны две ацильные группы. Это происходит особенно легко в случае циклических ангидридов, из которых образуются циклические амиды (Рис. 16):
Рис. 16. Реакция 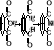
получения имидов
Второй стадией этой реакции, которая намного медленнее первой, является атака атома азота амидной группы на карбоновую кислоту.
Ацилирование аминов карбоновыми кислотами
При обработке карбоновых кислот аммиаком или аминами получаются соли. Соли, полученные из аммиака, а также первичных и вторичных аминов в результате пиролиза дают амиды, но этот метод менее удобен, чем реакции аминов с ангидридами, ацилгалогенидами и сложными эфирами, и редко используется в препаративных целях [5].
Хотя и взаимодействие кислот с аминами не приводит непосредственно к амидам, можно добиться чтобы эта реакция шла с хорошим выходом при комнатной или немного повышенной температуре (Рис. 17):

Рис. 17. Реакция получения амидов
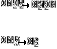
Кислоты можно превратить в амиды также нагреванием с амидами других карбоновых кислот (обмен), сульфоновых или фосфиновых кислот или действием трис(алкиламино) боранов [B(NHR’) 3] или трис(диалкиламино) боранов [B(NR’2) 3] (Рис. 18):
Рис. 18. Превращение кислот в амиды
Ацилирование аминов сложными эфирами

Превращение сложных эфиров в амиды – полезный метод синтеза незамещенных, N-замещенных и N, N-дизамещенных амидов из соответствующих аминов (Рис. 19):
Рис. 19. Превращение сложных эфиров в амиды
Реакцию можно проводить с алкильными или ароматическими группами R и R’. Особенно хорошей уходящей группой является n-нитрофенильная. Эта реакция весьма ценна, так как многие сложные эфиры легкодоступны или сравнительно легко получаются даже в тех случаях, когда этого нельзя сказать о соответствующем ангидриде кислоты или ацилгалогениде. Как и по реакции с ацилгалогенидами, этим методом из сложных эфиров можно синтезировать гидразиды и гидроксамовые кислоты действием гидразина и гидроксиламина соответственно. И гидразин, и гидроксиламин взаимодействуют быстрее, чем аммиак или первичные амины. Вместо сложных эфиров часто используют фенилгидразиды, получаемые из фенилгидразина.
Остаётся добавить, что реакция образования гидроксамовых кислот. которые в присутствии трёхвалентного железа дают окрашенные комплексы, часто используется как тест на сложные эфиры.
Ацилирование аминов амидами
Это реакция обмена, и ее обычно проводят с солью амина. Уходящей группой служит, как правило, NH2, а не NHR или NR2; в качестве реагентов наиболее широко применяются первичные амины (в виде солей).
Для образования комплекса с уходящим аммиаком можно добавлять BF3. Эту реакцию часто применяют для получения замещенных производных мочевины из самой мочевины (Рис. 20):

Рис. 20. Ацилирование аминов амидами
Диметилформамид можно превратить в другие формамиды продолжительным нагреванием с первичным или вторичным амином (Рис. 21) [10]:

Рис. 21. Превращение диметилформамида в другие формамиды
2.2.3. Реакции алкилирования
N-алкилирование нередко классифицируют как аммонолиз (или аминолиз) органических соединений).
Алкилирование по атомам других элементов (Si-, Pb-, AI-алкилирование) представляет собой важнейший путь получения элемент- и металлорганических соединений, когда алкильная группа непосредственно связывается с гетероатомом (Рис. 22):
2RCI + Si R2SiCI2
4C2H5CI + 4PbNa Pb(C2H5)4 + 4NaCI + 3Pb
3C3H6 + AI + 1,5H2 Al(C3H7)3
Рис. 22. Реакции алкилирования
Другая классификация реакций алкилирования основана на различиях в строении алкильной группы, вводимой в органическое или неорганическое соединение. Она может быть насыщенной алифатической (этильной и изопропильной) или циклической. В последнем случае реакцию иногда называют циклоалкилированием (Рис. 23):
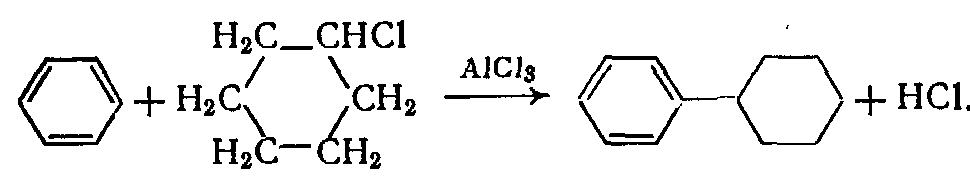
Рис. 23. Реакция циклоалкилированием
При введении фенильной или вообще арильной группы образуется непосредственная связь с углеродным атомом ароматического ядра (арилирование) (Рис. 24):
C6H5CI + NH3 C6H5NH2 + HCI
Рис. 24. Арилирование
В алкильную группу может входить ароматическое ядро или двойная связь, и, если последняя достаточно удалена от реакционного центра, реакция мало отличается от обычных процессов алкилирования (Рис. 25):
CH2=CH-CH2CI + RNH2 RNHCH2-CH=CH2 + HCI
Рис. 25. Реакция алкилирования
Однако введение винильной группы (винилирование) занимает особое место и осуществляется главным образом при помощи ацетилена (Рис. 26):
ROH + CHCH ROCH=CH2
CH3-COOH + CHCH CH3-COO-CH=CH2
Рис. 26. Реакция винилирования
Наконец, алкильные группы могут содержать различные заместители, например атомы хлора, гидрокси-, карбокси-, сульфокислотные группы (Рис. 27):
C6H5ONa + CICH2-COONa C6H5O-CH2-COONa + NaCI
ROH + HOCH2-CH2SO2ONa ROCH2–CH2SO2ONa + H2O
Рис. 27. Структура алкильных групп
Важнейшей из реакций введения замещенных алкильных групп является процесс -оксиалкилирования (в частном случае оксиэтилирование), охватывающий широкий круг реакций оксидов олефинов (Рис. 28):

Рис. 28. Оксиэтилирование
Алкилирующие агенты и катализаторы
Все алкилирующие агенты по типу связи, разрывающейся в них при алкилировании, целесообразно разделить на следующие группы:
1. Ненасыщенные соединения (олефин и ацетилен), у которых происходит разрыв -электронной связи между атомами углерода;
2. Хлорпроизводные с достаточно подвижным атомом хлора, способным замещаться под влиянием различных агентов;
3. Спирты, простые и сложные эфиры, в частности оксиды олефинов, у которых при алкилировании разрывается углерод-кислородная связь.
Олефины (этилен, пропилен, бутены и высшие) имеют первостепенное значение в качестве алкилирующих агентов. Ввиду дешевизны ими стараются пользоваться во всех случаях, где это возможно. Главное применение они нашли для С-алкилирования парафинов и ароматических соединений. Они неприменимы для N-алкилирования и не всегда эффективны при S- и O-алкилировании и синтезе металлорганических соединений [7].
Алкилирование олефинами в большинстве случаев протекает по ионному механизму через промежуточное образование карбокатионов и катализируется протонными и апротонными кислотами. Реакционная способность олефинов при реакциях такого типа определяется их склонностью к образованию карбокатионов:
(4)
Это означает, что удлинение и разветвление цепи углеродных атомов в олефине значительно повышает его способность к алкилированию:
CH2=CH2 < CH3-CH=CH2 < CH3-CH2-CH=CH2 < (CH3)2C=CH2 (5)
В ряде случаев алкилирование олефинами протекает под влиянием инициаторов радикально-цепных реакций, освещения или высокой температуры. Здесь промежуточными активными частицами являются свободные радикалы. Реакционная способность разных олефинов при таких реакциях значительно сближается.
Хлорпроизводные являются алкилирующими агентами наиболее широкого диапазона действия. Они пригодны для С-, О-, S- и N-алкилирования и для синтеза большинства элементо- и металлорганических соединений. Применение хлорпроизводных рационально для тех процессов, в которых их невозможно заменить олефинами или когда хлорпроизводные дешевле и доступнее олефинов.
Алкилирующее действие хлорпроизводных проявляется в трех различных типах взаимодействий: в электрофильных реакциях, при нуклеофильном замещении и в свободно-радикальных процессах. Механизм электрофильного замещения характерен для алкилирования по атому углерода, но, в отличие от олефинов, реакции катализируются только апротонными кислотами (хлориды алюминия, железа). В предельном случае процесс идет с промежуточным образованием карбокатиона:
(6)
в связи, с чем реакционная способность алкилхлоридов зависит от поляризации связи C-CI или от стабильности карбокатионов и повышается при удлинении и разветвлении алкильной группы:
(7)
При другом типе реакций, характерном для алкилирования по атомам кислорода, серы и азота, процесс состоит в нуклеофильном замещении атома хлора. Механизм аналогичен гидролизу хлорпроизводных, причем реакция протекает в отсутствие катализаторов:
(8)
Реакционная способность хлорпроизводных изменяется в данных процессах таким же образом, как при гидролизе, а именно:
ArCH2CI > CH2=CH-CH2CI > AIkCI > ArCI (9)
перв-AIkCI > втор-AIkCI > трет-AIkCI (10)
Целый ряд процессов алкилирования хлорпроизводными протекает по свободно-радикальному механизму. Это особенно характерно для синтезов элементо- и металлорганических соединений, когда свободные радикалы образуются за счет взаимодействия с металлами [6]:
4PbNa + 4C2H5CI 4Pb + 4NaCI + 4C2H 4NaCI + Pb(C2H5)4 + 3Pb (11)
2.2.4. Ацилирование и алкилирование по Фриделю-Крафтсу
Ацилирование по Фриделю-Крафтсу
Введение ацильной группы в ароматическое кольцо с помощью ацилирующего агента и кислоты Льюиса называют ацилированием по Фриделю-Крафтсу. Ацилирующими агентами обычно являются галогенангидриды и ангидриды кислот в присутствии галогенидов алюминия, трифторида бора или пентафторида сурьмы в качестве кислот Льюиса. Ацилгалогениды и ангидриды кислот образуют с кислотой Льюиса донорно-акцепторные комплексы состава 1:1 и 1:2. Спектральными методами было установлено, что хлорид алюминия, трифторид бора и пентафторид сурьмы координируются по карбонильному атому кислорода, так как он более основен чем соседний атом хлора. Электрофильным агентом в реакции ацилирования ароматических соединений является либо этот донорно-акцепторный комплекс, либо катион ацилия, образующийся при его диссоциации (Рис. 29).
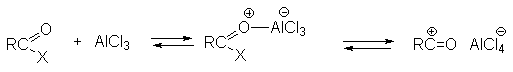
Рис. 29. Реакция ацилирования по Фриделю-Крафтсу
Можно полагать, что медленной стадией реакции является атака одного из трех электрофилов на арен, приводящая к -комплексу. Эффективность этих ацилирующих частиц зависит от природы субстрата, ацилгалогенида и растворителя, а также от количества взятого катализатора.
При ацилировании аренов ацилгалогенидами, катализируемом хлоридом или бромидом алюминия в полярных апротонных растворителях (нитробензоле, нитрометане и др.), ацилирующим агентом является катион ацилия, тогда как в малополярной среде (хлористом метилене, дихлорэтане или тетрахлорэтане) в реакции принимает участие донорно-акцепторный комплекс. Природа ацилгалогенида также оказывает влияние на образование и стабильность солей ацилия. Механизм реакции ацилирования аренов по Фриделю-Крафтсу под действием донорно-акцепторного комплекса (Рис. 30):
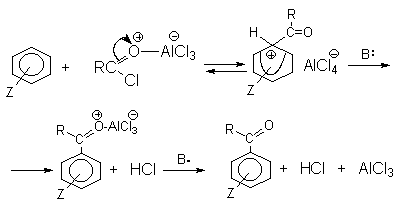
Рис. 30. Механизм реакции ацилирования аренов по Фриделю-Крафтсу
Ароматический кетон представляет собой более сильное основание Льюиса, чем ацилгалогенид и образует стабильный комплекс с AlCl3 или другой кислотой Льюиса. Поэтому для ацилирования ароматических соединений ацилгалогенидами требуется несколько больше эквимолярного количества катализатора, а при ацилировании ангидридами кислот два моля катализатора (т.к. они содержат два карбонильных атома кислорода). Кетон выделяют, разлагая его комплекс с AlCl3 водой или соляной кислотой.
Ацилирование по Фриделю-Крафтсу полностью лишено тех недостатков, которые присущи реакции алкилирования. При ацилировании вводится только одна ацильная группа, поскольку ароматические кетоны не вступают в дальнейшую реакцию (так же, как и другие арены, содержащие сильные электроноакцепторные группы: NO2, CN, COOR). Еще одним преимуществом этой реакции по сравнению с алкилированием является отсутствие перегруппировок в ацилирующем агенте. Кроме того, для ацилирования не характерны реакции диспропорционирования продуктов реакции [4,7].
Алкилирование по Фриделю-Крафтсу
Реакция Ш.Фриделя-Дж.Крафтса (1877 г.) представляет собой удобный метод прямого введения алкильной группы в ароматическое кольцо. Алкилирование ароматических соединений осуществляется под действием алкилгалогенидов, только в присутствии в качестве катализатора подходящей кислоты Льюиса: AlBr3, AlCl3, GaBr3, GaCl3, BF3, SbF5, SbCl5, FeCl3, SnCl4, ZnCl2 и др. (Рис. 31):
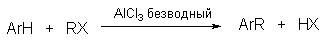
Рис. 31. Алкилирование ароматических соединений
Наиболее активными катализаторами являются безводные сублимированные бромиды алюминия и галлия, пятифтористая сурьма, хлориды алюминия и галлия, менее активны галогениды железа (III), SbCl5, к малоактивным катализаторам относятся SnCl4 и ZnCl2. В целом активность кислот Льюиса, как катализаторов алкилирования бензола, уменьшается в ряду AlBr3>GaBr3>AlCl3>GaCl3>FeCl3>SbCl5>TiCl4>BF3>BCl3>SnCl4>SbCl3. Самым распространенным катализатором этой реакции является предварительно сублимированный хлористый алюминий.
Например, механизм реакции бензилирования хлористым бензилом в нитробензоле в присутствии безводного AlCl3 в качестве катализатора следующей схемой (Рис. 32):
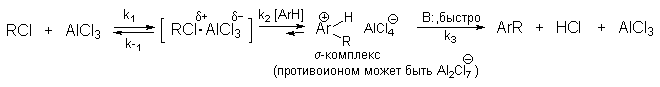
Рис. 32. Механизм реакции бензилирования, где В: =AlCl4-; H2O или др. основание. Скорость реакции лимитируется второй стадией
Точное строение интермедиата неизвестно. В принципе, можно представить целый ряд структур от молекулярного комплекса до диссоциированных карбокатионов (Рис. 33):
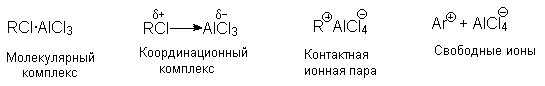
Рис. 33. Строение интермедиата
Участие свободных карбокатионов как алкилирующих агентов маловероятно.
Если бы алкилирующими агентами были свободные карбокатионы, то медленной стадией была бы стадия их образования (k1), а реакция с аренами была бы быстрой и третьего порядка не должно было наблюдаться. Крайне маловероятно, что алкилирующим агентом является молекулярный комплекс. При низких температурах иногда удается выделить комплексы алкилгалогенидов с кислотами Льюиса. Для них характерен медленный обмен галогенов по схеме (Рис. 34):

Рис. 34. Получение комплексов алкилгалогенидов с кислотами Льюиса
Скорость обмена возрастает в ряду перв.R< втор.R<трет.R, что можно объяснить и ион-парным строением, и структурой координационного аддукта.
Многие исследователи, работающие в данной области, полагают, что строение комплексов RX. MXn постепенно изменяется от структуры координационного аддукта в случае R=СН3 до структуры ионной пары в случае R=t-Bu, однако экспериментально это пока не подтверждено.
Способность атома галогена в RX к комплексообразованию с AlCl3 или другой жесткой кислотой Льюиса резко уменьшается от фтора к иоду, вследствие этого активность алкилгалогенидов в качестве алкилирующих агентов в реакции Фриделя-Крафтса также уменьшается в ряду RF>RCl>RBr>RI. По этой причине алкилиодиды не применяют в качестве алкилирующего агента.
Различие в активности алкилфторидов и алкилбромидов настолько велико, что позволяет селективно замещать фтор в присутствии брома в одной и той же молекуле (Рис. 35) [3]:
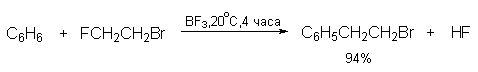
Рис. 35. Различие в активности алкилфторидов и алкилбромидов
2.2.5. Взаимодействие аминов с азотистой кислотой
Первичные, вторичные и третичные амины по-разному взаимодействуют с азотистой кислотой, что используется для установления типа амина. Неустойчивую азотистую кислоту генерируют действием сильной кислоты на нитриты.
Третичные алифатические амины при обычной температуре с азотистой кислотой не взаимодействуют.
Вторичные амины образуют с азотистой кислотой устойчивые нитрозамины – жидкие или твердые продукты желтого цвета:
R2NH + NaNO2 + HCl R2N-N=O + NaCl + H2O (12)
Нитрозамины являются сильными канцерогенами. Показана возможность синтеза нитрозаминов в желудке человека из содержащихся в пище и лекарственных препаратах вторичных аминов и нитритов Канцерогенное действие нитрозаминов основано на их способности алкилировать нуклеофильные центры ДНК, что приводит к онкогенным мутациям.
Первичные алифатические амины реагируют с азотистой кислотой с выделением газообразного азота. Реакция идет через образование неустойчивого первичного нитрозамина, который изомеризуется в диазогидроксид, превращающийся далее в соль диазония:
(13)
Дальнейший ход реакции зависит от природы углеводородного радикала.
Если R – алифатический радикал, то соль диазония очень неустойчива и немедленно разлагается с образованием молекулы азота и карбокатиона, который затем взаимодействует с находящимися в реакционной среде нуклеофилами (например, с растворителем) или отщепляет протон и дает продукт элиминирования. Например, превращения катиона н-пропилдиазония могут быть представлены следующей схемой (Рис. 36):
Рис. 36. Превращение катиона н-пропилдиазония
Реакция не имеет препаративного значения. Процесс используется в аналитических целях для количественного определения первичных алифатических аминов, в том числе природных -аминокислот, по объему выделяющегося азота.
Соли арилдиазония более устойчивы и могут быть выделены из реакционной смеси. Они являются высокореакционноспособными соединениями и широко используются в органическом синтезе.
Процесс получения ароматических диазосоединений называется диазотированием и выражается следующим суммарным уравнением.
ArNH2 + NaNO2 + 2HCl ArN2+Cl- + NaCl + 2H2O (14)
Реакции солей арилдиазония можно разделить на два типа: реакции с выделением азота и реакции без выделения азота.
Реакции, протекающие с выделением азота. Этот тип реакций представляет собой замещение в ароматическом кольце, уходящей группой в котором является молекула азота N2 (Рис. 37):
Рис. 37. Реакции солей арилдиазония
Реакции используются для введения различных заместителей в ароматическое кольцо.
Реакции, протекающие без выделения азота. Наиболее важной реакцией этого типа является азосочетание. Катион диазония обладает слабыми электрофильными свойствами и вступает в реакции электрофильного замещения с аренами, содержащими сильные электронодонорные заместители. При этом образуются азосоединения (Рис. 38):
Рис. 38. Реакции азосочетания
Азосоединения содержат длинную систему сопряженных связей и поэтому окрашены. Они используются как красители. Образование окрашенных соединений при взаимодействии солей арилдиазония с ароматическими аминокислотами (тирозин, гистидин) используется для их качественного и количественного определения.
Аминогруппа является сильным активирующим заместителем и ориентантом II рода.
Анилин легко бромируется бромной водой с образованием триброманилина (Рис. 39):
Рис. 39. Реакция бромирования анилина
В большинстве реакций электрофильного реакционноспособная аминогруппа предварительно защищается путем ацилирования. После проведения реакции ацильную защиту снимают кислотным или щелочным гидролизом (Рис. 40) [1]:
Рис. 40. Реакция ацилирования
2.3. Методы получения аминов
2.3.1. Алкилирование аммиака и аминов
Аммиак взаимодействуют с алкилгалогенидами RX с образованием на первой стадии соли алкиламмония, которая с избытком аммиака дает алкиламин. Алкиламин, будучи более сильным нуклеофилом, чем аммиак, далее вступает в реакцию алкилгалогенидом с образованием продукта диалкилирования. Таким образом образуется смесь моно-, ди-, триалкиламинов и четвертичной аммониевой соли (Рис. 41):
Рис. 41. Реакции с алкилгалогенидом
Спирты алкилируют аммиак и амины в присутствии катализаторов дегидратации (Al2O3, SiO2) при 300-5000C. В этом случае также образуется смесь продуктов алкилирования (Рис. 42) [10]:
Рис. 42. Алкилирование аммиака и аминов спиртами
2.3.2. Восстановление азотсодержащих органических соединений
Нитросоединения могут быть восстановлены до первичных аминов. Реакция используется в основном для получения первичных ароматических аминов из доступных нитроаренов:
ArNO2ArNH2 (15)
В качестве восстановителей используют водород в присутствии катализаторов (Ni, Pt, Pd), металл (Fe, Zn, Sn) и кислоту, соли металлов в низших степенях окисления (SnCl2, TiCl3).
Нитрилы при восстановлении также дают первичные амины (Рис. 43):
RCN RCH2NH2
[H]: H2/Ni; LiAlH4
Рис. 43. Восстановление нитрилов
Амиды карбоновых кислот восстанавливаются до аминов комплексными гидридами металлов. Из соответствующих амидов могут быть получены первичные, вторичные и третичные амины (Рис. 44):
Рис. 44. Восстановление амидов карбоновых кислот
Восстановительное аминирование альдегидов и кетонов (Рис. 45) [3]:
Рис. 45. Восстановительное аминирование альдегидов и кетонов
2.3.3. Перегруппировка Гофмана
RCONH2 + Br2 + 2NaOH RNH2 + 2NaBr + CO2 + H2O (16)
Используется для получения первичных аминов [2].
2.4. Биологически активные амины и их производные
Биологическую активность проявляют гетерофункциональные соединения, содержащие аминогруппу – аминокарбоновые кислоты, аминоспирты, аминофенолы, аминосульфокислоты.
К ним можно отнести гормоны надпочечников (норадреналин, адреналин), щитовидной железы (тироксин, трийодтиронин), а также медиаторы ЦНС (ацетилхолин, ГАМК и др.), медиатор воспаления (гистамин) и другие соединения.
Некоторые аминокислоты и их производные могут подвергаться декарбоксилированию - отщеплению карбоксильной группы. В тканях млекопитающих декарбоксилированию может подвергаться целый ряд аминокислот или их производных: Три, Тир, Вал, Гис, Глу, Цис, Apr, Орнитин, SAM, ДОФА, 5-окситриптофан и др. Продуктами реакции являются СО2 и амины, которые оказывают выраженное биологическое действие на организм (биогенные амины) (Рис. 46):
Рис. 46. Реакция получения биогенных аминов
Реакции декарбоксилирования необратимы и катализируются ферментами декарбоксилазами. Простетическая группа декарбоксилаз в клетках животных - пиридоксальфосфат. Некоторые декарбоксилазы микроорганизмов могут содержать вместо ПФ остаток пирувата - гистидиндекарбоксилаза Micrococcus и Lactobacilus, SAM-декарбоксилаза Е. coli и др. Механизм реакции напоминает реакцию трансаминирования с участием пиридоксальфосфата и также осуществляется путём формирования Шиффова основания и аминокислоты на первой стадии.
Амины, образовавшиеся при декарбоксилировании аминокислот, часто являются биологически активными веществами. Они выполняют функцию нейромедиаторов (серотонин, дофамин, ГАМК и др.), гормонов (норадреналин, адреналин), регуляторных факторов местного действия (гистамин, карнозин, спермин и др.).
Этаноламин (коламин) HOCH2CH2NH2 является структурным компонентом сложных липидов. В организме образуется при декарбоксилировании аминокислоты серина [9].
Холин HOCH2CH2N+(CH3)2 – гидроокись 2-оксиэтилтриметиламмония. Относят к витаминам группы В, хотя животные и микроорганизмы способны его синтезировать. Холин входит в состав фосфолипидов (например, лецитина, сфингомиелина), служит источником метильных групп в синтезе метионина. Из холина в организме животных синтезируется ацетилхолин — один из важнейших химических передатчиков нервных импульсов. Холин является т.н. липотропным веществом — предотвращает тяжёлые заболевания печени, возникающие при её жировом перерождении.
Холин - в медицине для лечения заболеваний печени применяют хлорид холина. Его вводят также в состав комбикормов сельскохозяйственным животных. Для аналитических целей используют способность холина давать плохо растворимые соли с фосфорновольфрамовой, платинохлористоводородной и некоторыми др. гетерополикислотами.
Ацетилхолин CH3COOCH2CH2N+(CH3)2 - посредник при передаче нервных импульсов (нейромедиатор). Накопление ацетилхолина в организме приводит к непрерывной передаче нервных импульсов и сокращению мускульной ткани. На этом основано действие нервнопаралитических ядов (зарин,табун), которые ингибируют действие фермента ацетилхолинэстеразы, катализирующего расщепление ацетилхолина.
Катехоламины – дофамин, норадреналин, адреналин – биогенные амины, продукты метаболизма аминокислоты фенилаланина (Рис. 47):
Рис. 47. Формулы катехоламинов
Дофамин обладает рядом физиологических свойств, характерных для адренергических веществ.
Дофамин вызывает повышение сопротивления периферических сосудов (менее сильное, чем под влиянием норадреналина). Он повышает систолическое артериальное давление в результате стимуляции -адренорецепторов. Также дофамин увеличивает силу сердечных сокращений в результате стимуляции -адренорецепторов. Увеличивается сердечный выброс. Частота сердечных сокращений увеличивается, но не так сильно, как под влиянием адреналина.
Потребность миокарда в кислороде под влиянием дофамина повышается, однако в результате увеличения коронарного кровотока обеспечивается повышенная доставка кислорода.
В результате специфического связывания с дофаминовыми рецепторами почек дофамин уменьшает сопротивление почечных сосудов, увеличивает в них кровоток и почечную фильтрацию. Наряду с этим повышается натрийурез. Происходит также расширение мезентериальных сосудов. Этим действием на почечные и мезентериальные сосуды дофамин отличается от других катехоламинов (норадреналина, адреналина и др.). Однако в больших концентрациях дофамин может вызывать сужение почечных сосудов.
Дофамин ингибирует также синтез альдостерона в коре надпочечников, понижает секрецию ренина почками, повышает секрецию простагландинов тканью почек.
Основной физиологический эффект мелатонина заключается в торможении секреции гонадотропинов. Кроме того, снижается, но в меньшей степени, секреция других тропных гормонов передней доли гипофиза — кортикотропина, тиротропина, соматотропина.
Секреция мелатонина подчинена суточному ритму, определяющему, в свою очередь, ритмичность гонадотропных эффектов и половой функции. Синтез и секреция мелатонина зависят от освещённости — избыток света тормозит его образование, а снижение освещённости повышает синтез и секрецию гормона [3,5].
Серотонин — это вещество, являющееся химическим передатчиком импульсов между нервными клетками человеческого мозга и контролирующее аппетит, сон, настроение и эмоции человека.
Серотонин «руководит» очень многими функциями в организме. Например, очень интересны исследования его влияния на проявление боли. Доктором Виллисом доказано, что при снижении серотонина повышается чувствительность болевой системы организма, то есть даже самое слабое раздражение отзывается сильной болью.
Катехоламины — физиологически активные вещества, выполняющие роль химических посредников в межклеточных взаимодействиях.
Адреналин оказывает стимулирующее воздействие на ЦНС. Он повышает уровень бодрствования, психическую энергию и активность, вызывает психическую мобилизацию, реакцию ориентировки и ощущение тревоги, беспокойства или напряжения, гегенируется при пограничных ситуациях.
Структурно близки к катехоламинам некоторые природные и синтетические биологически активные вещества, также содержащие аминогруппу в b-положении к ароматическому кольцу (Рис. 48):
Рис. 48. Формулы фенамина и эфедрина
Фенамин является стимулятором центральной нервной системы, снимает чувство усталости. Эфедрин – алкалоид, обладающий сосудорасширяющим действием.
Производные п-аминофенола – парацетамол и фенацетин – лекарственные препараты, обладающие обезболивающим и жаропонижающим действием (Рис. 49):
Рис. 49. Формулы парацетамола и фенацетина
В настоящее время фенацетин рассматривается как вещество, возможно являющееся канцерогеном для человека.
п-Аминобензойная кислота и ее производные (Рис. 50):
Рис. 50. п-Аминобензойная кислота и ее производные
п-Аминобензойная кислота – витаминоподобное вещество, фактор роста микроорганизмов; участвует в синтезе фолиевой кислоты (витамина ВС). Сложные эфиры п-аминобензойной кислоты вызывают местную анестезию.
Анестезин и новокаин применяются в виде растворимых в воде гидрохлоридов.
Сульфаниловая кислота (п-аминобензолсульфокислота) и сульфаниламиды. Амид сульфаниловой кислоты (стрептоцид) и его N-замещенные производные – эффективные антибактериальные средства. Синтезировано более 5000 производных сульфаниламида. Наибольшую активность проявляют сульфониламиды, содержащие гетероциклические основания (Рис. 51):
Рис. 51. Формулы производных сульфаниловой кислоты
Антибактериальное действие сульфамидных препаратов основано на том, что они имеют структурное сходство с п-аминобензойной кислотой и являются ее атиметаболитами. Присутствующие в бактериальной среде сульфаниламиды включаются в процесс биосинтеза фолиевой кислоты, конкурируя с п-аминобензойной кислотой, и на определенной стадии блокируют его, что ведет к гибели бактерий. Сульфаниламиды не влияют на организм человека, в котором фолиевая кислота не синтезируется [8].
2.5. Акридон: получение, свойства и применение
Незамещенный акридон – очень устойчивое в обычных растворителях желтое вещество; оно плохо растворимо и плавится при высокой температуре – 354 °C. Кристаллизуется в виде игл (Рис. 52):
Рис. 52. Формула акридона
Акридоны удобнее всего рассматривать как циклические винилоги амидов кислот. Они представляют собой ассоциированные, высоко плавящиеся и довольно слабо растворимые соединения, которые лучше всего перекристаллизовывать из пиридина или высококипящих растворителей. Химически они очень устойчивы, и при восстановлении их в акридины приходится преодолевать высокий энергетический барьер, следствием чего является последующая стадия восстановления с образованием акриданов. Процесс восстановления до акридана, однако, не имеет существенного значения, так как акриданы легко окисляются в акридины и более глубоко эта реакция уже не протекает. Существуют и другие пути превращения акридонов в акридины, не включающие непосредственного восстановления. Акридоны окрашены в кремовый или желтый цвет, многие сильно флуоресцируют. Хемилюминесценции и раздражающего действия у соединений акридона не наблюдается. Почти все акридоны (даже аминопроизводные) - чрезвычайно слабые основания. Акридон отличается от изомерных ему оксиакридинов отсутствием явно выраженных кислых и основных свойств. Спектр акридона тоже значительно отличается от спектров оксиакридинов. Молекулярный вес акридона был определен криоскопически в феноле; оказалось, что в этих условиях акридон мономерен; однако показано, что вещества такого типа могут состоять из коротких цепей молекул, соединенных водородной связью.
Акридон получается при окислении акридина дихроматом натрия в уксусной кислоте и при циклизации дифениламин-2-карбоновой кислоты (Рис. 53):
Рис. 53. Получение акридона
Натрием в этаноле он восстанавливается в акридан, который может быть окислен в акридин (Рис. 54):
Рис. 54. Получение акридана
Производные акридона находят применение в медицине, например циклоферон, обладающий антивирусными и иммуномоделирующими свойствами и способный подавлять развитие ряда микробов [9,10].
2.6. 9-аминоакридин: получение, свойства и применение
9-аминоакридин представляет собой светло-желтый порошок (Рис. 55):
Рис. 55. Формула 9-аминоакридина
Методы получения аминоакридинов более многочисленны, чем методы синтеза самого акридина. 9-аминоакридин можно получить несколькими способами. Один из них – это получение его из 9-хлоракридина нагреванием с карбонатом аммония в присутствии фенола (Рис. 56):
Рис. 56. Получение 9-аминоакридин
9-аминоакридин может быть также получен из акридина по реакции с амидом натрия (реакция Чичибабина) (Рис. 57):
Рис. 57. Получение 9-аминоакридин по реакции Чичибабина
Кроме того, 9-аминоакридин может быть получен гидролизом 9-цианакридина (из акридина или 9-хлоракридина) до соответствующего амида кислоты, и последующим превращением амида в желаемый амин, а также разложением азида кислоты. При восстановлении хлоропроизводного водородом на Ni-Ренея образуется 9,10-дигидроакридин, окисление которого хромовой кислотой приводит к незамещенному акридину.
Синтез новых веществ в ряду аминоакридинов представляет собой большой практический интерес [7].
3. Заключение