Обмен железа и нарушение обмена железа. Гемоседероз
РЕФЕРАТ
ПО ДИСЦИПЛИНЕ «Биохимия»
«Обмен железа и нарушение обмена железа. Гемоседероз.»
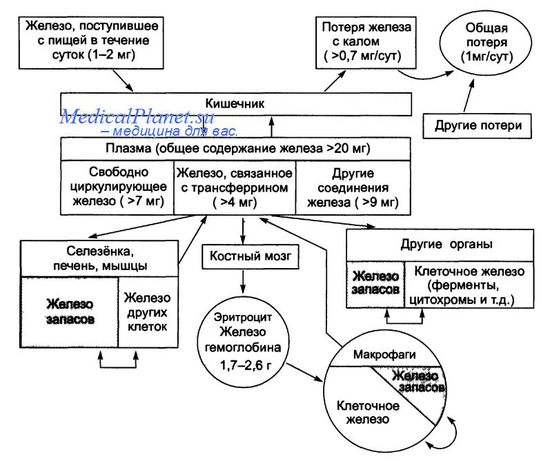
Железо является важнейшим микроэлементом, принимает участие в дыхании, кроветворении, иммунобиологических и окислительно-восстановительных реакциях, входит в состав более 100 ферментов. Железо является незаменимой составной частью гемоглобина и миогемоглобина. В организме взрослого человека содержится около 4 г железа, из них более половины (около 2,5 г) составляет железо гемоглобина. Часть железа депонируется в организме человека, преимущественно в печени, селезенке и костном мозге.
Суточная потребность человека в железе составляет 10-30 мг, с учетом того, что всасывание железа из продуктов питания составляет около 10%. Эта доза обеспечивается суточным пищевым рационом (15-40 мг) за счет животной и растительной пищи. Основными источниками железа служат: крупа, печень, мясо. Всасывание поступившего с пищей железа происходит в кишечнике, но обычно не превышает 5-20% от общего содержания в пище. Значительно лучше железо всасывается из мясных продуктов (телятина - 17-21%, печень - 10-20%), из рыбных продуктов - 9-11%. Меньше всего железо всасывается из растительных продуктов (1-7%). Добавка мяса в блюда, содержащие растительные продукты, значительно улучшает всасывание железа из них.
Железо сыворотки:
•женщины 50 – 160 мкг/дл
•мужчины 40 - 150 мкг/дл
Продукты содержащие железо. Железо содержится в таких продуктах как: мясо животных, птиц, субпродукты. Особенно большое содержание железа в бобовых, печени и почках животных. Железо из щавеля, шпината, айвы, черники всасывается очень плохо, хотя и содержится в достаточно больших количествах. Происходит это из-за большого содержания в этих продуктах щавелевых кислот и дубильных веществ. Красное мясо, мясопродукты, печень, бобы, хлеб из недробленого зерна, овощи с зелеными листьями - это лучшие продукты содержащие железо.
Существует две формы пищевого железа:
•гемо-железо, извлекаемое из гемоглобина, встречается в продуктах животного происхождения;
•негемо-железо содержится в растительных продуктах.
Также, в качестве дополнительного источника, можно принимать витамины содержащие железо.
Гемо-железо поглащается организмом лучше, чем негемо-железо. Организм регулирует запасы железа в зависимости от его потребностей путем увеличения его усвоения при прежнем количестве. Кальций способствует усвоению железа, за исключением тех случаев, когда дозы кальция чрезвычайно велики. Фосфаты, входящие в состав яиц, сыра и молока; оксалаты, фитаты и танины, содержащиеся в черном чае, отрубях, кофе препятствуют усвоению железа. Витамин Е и цинк в высоких концентрациях снижают усвоение железа. Витамины С, В12, кислота желудочного сока, пепсин, медь способствуют усвоению железа, особенно если они поступают из животных источников. Снижение кислотности желудочного сока в результате продолжительного приема антацидов или препаратов для уменьшения кислотности (таких как зантак, тагамет, пепцид, аскид) сопровождается уменьшением усвоения железа. Кофе, чай, молоко, темная овощная зелень, а также дефицит витамина А могут снижать способность организма усваивать железо. Избыток железа уменьшает способность организма усваивать медь и цинк.
Недостаточность железа в организме может быть вызвана экзогенными (за счет недостаточно поступления с пищей) и эндогенными (за счет нарушения всасываемости в кишечнике: заболевания слизистой оболочки кишечника или понос) факторами. Нарушение обмена и недостаточность железа в организме приводит к развитию железодефицитной анемии. При повышении содержания железа в организме происходит его отложение в виде зерен (сидероз) в органах.
Нарушение всасывания и обмена железа
Всасываемость железа определяется взаимоотношением трех главных факторов:
•количеством железа в просвете тонкой кишки
•формой катиона железа
•функциональным состоянием слизистой оболочки кишечника
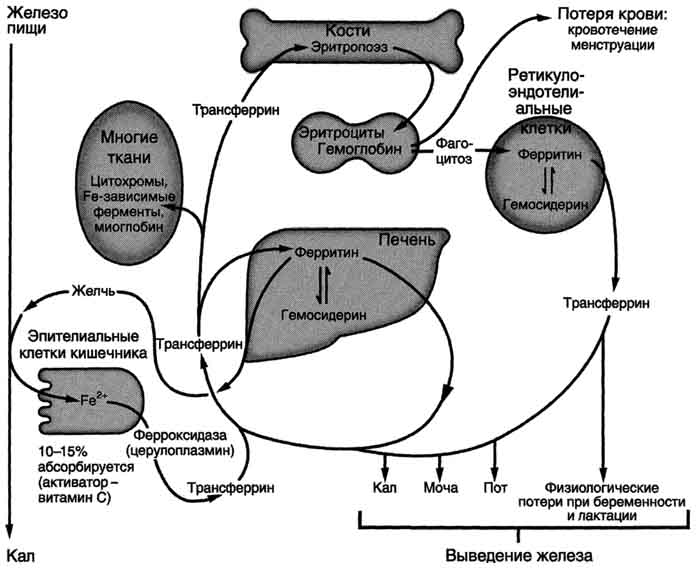
Современный человек, находящийся на смешанной диете, потребляет за сутки 10 - 20 мг железа, главным образом в форме миоглобина и гемоглобина. Всасывается около 10% диетического железа и примерно такое же количество его ежесуточно теряется организмом.
В желудке железо освобождается от связи с белком. Под влиянием содержащейся в диете аскорбиновой кислоты трехвалентное железо переходит в двухвалентную форму. В кислом содержимом желудка двухвалентное железо вступает в связь с мукополисахаридом (фактор Касла), образуя большой железный комплекс. В просвете двенадцатиперстной кишки из этого стабильного макрокомплекса образуются малые комплексы, которые состоят из железа, аскорбиновой кислоты, лимонной кислоты, гексоз и некоторых аминокислот, в частности цистеина. Эти малые комплексы всасываются главным образом в верхней части тонкой кишки. Когда железо поступает в отделы тонкой кишки, где рН выше, чем в желудке, оно полимеризуется в большой коллоидный комплекс. Осажденное железо выделяется из организма в виде гидроокиси.
Всасывание железа осуществляется и наиболее эффективно протекает главным образом в двенадцатиперстной и в начальной части тощей кишки. Этот процесс проходит следующие этапы:
|
Таблица. Вещества, влияющие на всасывание железа
|
|
Активаторы
|
Ингибиторы
|
|
Аскорбиновая кислота
Янтарная кислота
Пировиноградная кислота
Фруктоза
Сорбит
Алкоголь
Мясо
Рыба (белок)
Молочная кислота
|
Оксалаты
Фитаты
Фосфаты
Танины
Антациды
Тетрациклины
Витамины группы B
Фолиевая кислота
Соли кальция
Альмагель
Соли магния
Медь
Ингибиторы образования соляной кислоты
Соевый протеин
Молоко
Пищевые волокна
Полифенолы (чай, кофе, бобы, орехи, крупы, свежие овощи, фрукты и др.)
Карбонаты
|
•захват клетками слизистой оболочки (ворсинками) тонкого кишечника двухвалентного железа и окисление его в трехвалентное в мембране микроворсинок
•перенос железа к собственной оболочке, где оно захватывается трансферрином и быстро переходит в плазму
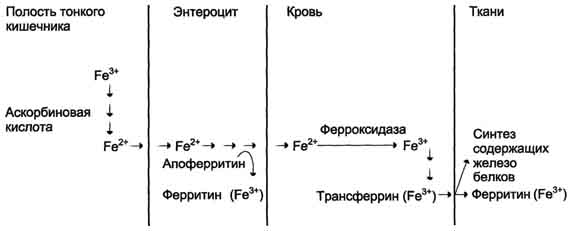
Механизмы регуляции всасывания железа окончательно не выяснены, но твердо установлено, что всасывание ускоряется при его дефиците и замедляется при увеличении его запасов в организме.
Факторы, влияющие на поглощение железа:
•факторы органов пищеварения - аиболее важные из них: желудочный сок; термолабильные белки сока поджелудочной железы, препятствующие поглощению органического железа; восстановительные агенты пищи, увеличивающие поглощение железа (аскорбиновая, янтарная и пировиноградная кислота, фруктоза, сорбит, алкоголь) или тормозящие его (бикарбонаты, фосфаты, соли фитовой кислоты, оксалаты, кальций)
•эндогенные факторы - количество железа в запасе влияет на скорость его поглощения; высокая эритропоэтическая активность увеличивает поглощение железа в 1,5–5 раз и наоборот; уменьшение количества гемоглобина в крови увеличивает поглощение железа
Атрофия слизистой оболочки желудка понижает способность расщеплять диетический белок и способствует возникновению дефицита железа в организме.
После расщепления гемоглобина и миоглобина в желудке освобождается гем. В двенадцатиперстной кишке он подвергается действию панкреатических ферментов, которые препятствуют его полимеризации. При внешнесекреторной недостаточности поджелудочной железы всасывание гема слизистой оболочкой двенадцатиперстной кишки резко нарушается из-за его быстрой полимеризации в слишком большие комплексы. Запасы железа в организме при болезнях поджелудочной железы пополняются за счет небольших количеств гема, который всасывается в неизмененном виде.
Большая часть всосавшегося железа быстро поступает в кровяную плазму, где связывается с трансферрином. Небольшая часть его связывается с апоферритином и сохраняется в эпителиальной клетке слизистой оболочки кишечника. Это железо теряется вместе со слущивающимися клетками кишечного эпителия. После поступления внутрь клетки гем расщепляется, а освободившееся из него железо усваивается.
Причины дефицита железа:
•недостаточное поступление (неадекватное питание, вегетарианская диета, недоедание)
•снижение всасывания железа в кишечнике
•нарушение регуляции обмена витамина С
•избыточное поступление в организм фосфатов, оксалатов, кальция, цинка, витамина Е
•поступление в организм железосвязывающих веществ (комплексонов)
•отравление свинцом, антацидами
•усиленное расходование железа (в периоды интенсивного роста и беременности)
•потери железа связанные с травмами, кровопотерями при операциях, обильными менструациями, язвенными болезнями, донорством, занятиями спортом
•гормональные нарушения (дисфункция щитовидной железы)
•гастриты с пониженной кислотообразующей функцией, дисбактериоз;
•различные системные и опухолевые заболевания
•глистная инвазия
Основные проявления дефицита железа:
•развитие железодефицитных анемий
•головные боли и головокружения, слабость, утомляемость, непереносимость холода, снижение памяти и концентрации внимания
•замедление умственного и физического развития у детей, неадекватное поведение;
•учащенное сердцебиение при незначительной физической нагрузке
•растрескивание слизистых оболочек в углах рта, покраснение и сглаженность поверхности языка, атрофия вкусовых сосочков
•ломкость, утончение, деформация ногтей
•извращение вкуса (тяга к поеданию непищевых веществ), особенно у детей младшего возраста, затрудненное глотание, запоры
•угнетение клеточного и гуморального иммунитета
•повышение общей заболеваемости (простудные и инфекционные болезни у детей, гнойничковые поражения кожи, энтеропатии)
•увеличение риска развития опухолевых заболеваний.
Железодефицитная анемия является самым распространенным типом анемии. В прошлом она имела чаще всего алиментарное происхождение. В настоящее время диетический фактор перестал играть решающую роль, и железодефицитная анемия развивается чаще всего под влиянием комплекса причин, главными из которых являются:
•повышенные потребности организма в железе (1)
•кровопотери (2)
•нарушение всасывания железа (3).
(1) Потребность организма в железе резко возрастает во время беременности и в периоды усиленного роста. Девушки во время полового созревания болеют анемией чаще юношей из-за неблагоприятного сочетания повышенных потребностей в железе, вызванных быстрым ростом, с началом кровопотерь, которые иногда (например, при мелкокистозном перерождении яичников и при так называемых дизовариальных кровотечениях) могут быть значительными.
(2) Кровопотери считаются наиболее частой причиной железодефицитных анемий. В большинстве случаев они обусловлены дефектами слизистой оболочки желудочно-кишечного тракта. Особенно часто наблюдаются анемии, вызванные повторными носовыми или геморроидальными кровотечениями. Иногда причиной железодефицитной анемии оказываются тромбоцитопеническая пурпура, гемофилия, телеангиэктазии, диафрагмальная грыжа, эрозия, язва и опухоль желудочно-кишечного тракта, у женщин-маточные кровотечения.Железодефицитная анемия может быть связана с гемолизом, который является одним из частых осложнений у больных с протезированными клапанами.
(3) Недостаточность всасывания железа нередко наблюдается у больных, перенесших резекцию желудка, при энтероколитах, целиакии, спру, дуоденитах.
Железодефицитная анемия. Больные железодефицитной анемией обращаются к врачу почти всегда с жалобами на слабость, одышку даже при незначительной физической нагрузке, головокружение, потемнение в глазах, которые обычно сочетаются с пульсирующей болью в голове. Значительно реже встречается сидеропеническая дисфагия в сочетании с глосситом (синдром Пламмера - Винсона). Перечисленные жалобы с особым постоянством отмечаются после больших кровопотерь и у больных с диареей и пострезекционными синдромами. Клинические исследования выявляют бледность кожи и слизистых оболочек, трещины в углах рта, атрофию сосочков языка, иногда глоссит, ложкообразные ногти повышенной ломкости. Селезенка иногда оказывается слегка увеличенной, безболезненный край ее выступает на 1 - 2 см из-под реберной дуги. Выраженность нарушений сердечнососудистой системы зависит от тяжести анемии. В более легких случаях отмечаются сосудистые шумы (например, шум волчка), систолический шум над верхушкой сердца. Когда содержание гемоглобина в крови падает ниже 50 г/л, сердце расширяется. Ахлоргидрия встречается примерно у половины больных; после коррекции анемии она не исчезает. Дефицит железа в организме может существовать без каких-либо изменений в морфологии эритроцита. По мере прогрессирования дефицита вначале появляется гипохромия, а позднее микроцитоз. В случаях выраженной железодефицитной анемии средний объем эритроцита оказывается менее 80 мкм3, содержание гемоглобина в нем падает ниже 30 пг, а концентрация гемоглобина - ниже 30 %. Появляются пойкилоцитоз, анизоцитоз. В случаях тяжелой анемии в периферической крови появляются нормобласты. Количество тромбоцитов в крови при железодефицитной анемии в одних случаях резко увеличивается, в других - уменьшается. Иногда незначительно повышается количество билирубина в крови. Содержание железа в крови ниже нормального (500-1000 мкг/л) и обычно ниже 400 мкг/л. Низкие цифры насыщения трансферрина не имеют диагностического значения, так как наблюдаются не только при железодефицитной анемии, но и при многих инфекциях. Стернальная пункция обнаруживает нормобластический тип кроветворения. Количество эритробластов может достигать 30%; характерно резкое уменьшение или почти полное исчезновение в них зерен гемосидерина. Содержание сидероцитов в периферической крови также уменьшено. Железодефицитная анемия может встречаться одновременно с другими анемиями, например с пернициозной. Примерно 90% всех микроцитарных и гипохромных анемий вызываются дефицитом железа в организме. Диагноз этого вида анемии всегда должен быть подтвержден определением концентрации железа в крови. Для определения объема лечебных мероприятий необходимо выяснить причину анемии. Иногда эта задача оказывается чрезвычайно трудной и для ее разрешения приходится прибегать к многим методам исследования. Роль кровопотерь из желудочно-кишечного тракта проверяют по радиоактивности кала после внутривенного введения эритроцитов, меченных хромом. После этого определяют всасывательную способность тонкой кишки и проверяют возможную связь анемии с гемолизом эритроцитов. Проведение указанного комплекса мероприятий заметно уменьшает число так называемых идиопатических железодефицитных анемий. Гипохромная микроцитарная анемия, развивающаяся при недостатке железа в организме, лишь отдаленно напоминает талассемию, которая тоже протекает с гипохромией и уменьшением объема эритроцитов. Дифференциальный диагноз между этими болезнями, как правило, нетруден.
Лабораторная диагностика железодефицитного состояния
Перечень необходимых лабораторных и инструментальных исследований определяется на основании анамнеза и клинических данных. «Баланс» железа в организме оценивают по совокупности показателей:
•развернутый анализ крови
•определение концентрации сывороточного железа
•содержание ферритина в сыворотке крови
Определение железа сыворотки крови дает представление об уровне транспортируемого железа в плазме крови, связанного с трансферрином. Большие вариации содержания железа в сыворотке крови, возможность его увеличения при некротических процессах в тканях (острый гепатолизис), его снижение при воспалительных процессах ограничивают диагностическое значение измерения железа сыворотки. Измеряя только содержание железа в сыворотке крови, мы не получим информации о причинах нарушенного обмена железа. Для этого необходимо определять содержание в кровиферритина (норма 58-150 мкг/л).
Ферритин – растворимый в воде комплекс гидроокиси железа с белком апоферритином. Он находится в клетках печени, селезенки, костного мозга и ретикулоцитах. Ферритин является основным белком человека, депонирующим железо. Хотя в крови ферритин присутствует в небольших количествах, его концентрация в плазме отражает запасы железа в организме. Низкие значения ферритина – это первый показатель уменьшенных запасов железа в организме. Определение ферритина в сыворотке используется для диагностики и мониторинга дефицита или избытка железа, дифференциальной диагностики анемий, слежения за развитием опухолей.
Повышенное содержание железа в организме
При некоторых наследственных и хронических заболеваниях, при избыточном поступлении извне, железо может накапливаться в организме. Люди с избыточным содержанием железа страдают от физической слабости, теряют вес, чаще болеют. При этом избавиться от избытка железа часто намного труднее, чем устранить его дефицит.
Токсическая доза железа для человека составляет 200 мг. Летальная доза для человека составляет 7-35 г.
При тяжелом отравлении железом повреждается слизистая оболочка кишечника, развивается печеночная недостаточность, появляются тошнота и рвота. Для детей младшего возраста отравление железом является одним из самых распространенных видов случайного отравления. Летальным исходом для ребенка может стать прием сульфата железа в дозе 3 г и выше.
Причины избытка железа:
•избыточное поступление извне (напр., при повышенном содержании в питьевой воде)
•заболевания печени, селезенки, поджелудочной железы (в том числе, в результате хронического алкоголизма)
•нарушение регуляции обмена железа
Основные проявления избытка железа:
•отложение железа в тканях и органах, сидероз
•головные боли, головокружения, повышенная утомляемость, слабость
•пигментация кожи
•изжога, тошнота, рвота, боли в желудке, запор или диарея, изъязвление слизистой оболочки кишечника
•печеночная недостаточность, фиброз
•повышенная насыщенность железом трансферрина
•снижение уровня сывороточного железа (в 1,5-3 раза)
•повышение риска развития атеросклероза, болезней печени и сердца, артритов, диабета и т.д.
•угнетение клеточного и гуморального иммунитета
•увеличение риска развития инфекционных и опухолевых заболеваний
•потеря аппетита, уменьшение массы тела
Гемосидероз - избыточное отложение гемосидерина в тканях организма. Возможные причины гемосидероза — усиленный распад эритроцитов, нарушение утилизации этого пигмента в процессе эритроцитопоэза, усиленное всасывание его в кишечнике, нарушение обмена железосодержащих пигментов,ацерулоплазминемия.
Виды гемосидероза:
- Местный гемосидероз. Возникает при внесосудистом (экстраваскулярном) гемолизе в очагах кровоизлияний. Накопление гемосидерина не повреждает ткань или орган, но если гемосидероз сочетается со склерозом, функция нарушается.
- Общий гемосидероз. Развивается при избытке железа из-за внутрисосудистого (интраваскулярного) гемолиза или при повышении всасывания железа из пищи. В этих случаях гемосидерин откладывается преимущественно в гепатоцитах, макрофагах печени, селезёнки, костного мозга и других органах. В большинстве случаев пигмент не повреждает паренхиматозные клетки и не вызывает нарушений функций органа. Если повышеное содержание железа сопровождается повреждением тканей с атрофией паренхимы, склерозом, снижением функции органа, такое состояние называется гемохроматоз.
-
|
|
Гемосидероз – заболевание группы пигментных дистрофий, характеризующееся избыточным накоплением железосодержащего пигмента гемосидерина в тканях организма. Различают местные формы заболевания (кожный и легочный гемосидероз) и общие (с отложением гемосидерина в клетках печени, селезенки, почек, костного мозга, слюнных и потовых желез). Диагностика гемосидероза основывается на определении содержания железа в плазме крови, общей железосвязывающей способности крови, а также содержания пигмента в биоптатах тканей и органов. В зависимости от клинической картины лечение гемосидероза включает медикаментозную терапию (глюкокортикоиды, цитостатики, ангиопротекторы, витамин С), в некоторых случаях плазмаферез, местную PUVA-терапию.
|
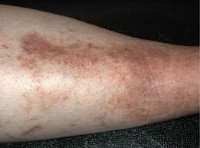
Гемосидероз - нарушение обмена гемоглобиногенного пигмента гемосидерина с его локальным или системным отложением в тканях. Гемосидерин представляет собой железосодержащий внутриклеточный пигмент, образующийся в процессе ферментативного расщепления гемоглобина. Синтез гемосидерина происходит в клетках-сидеробластах. Наряду с другими производными гемоглобина (ферритином, билирубином) гемосидерин участвует в транспорте и депонировании железа и кислорода, метаболизме химических соединений. В норме в небольших количествах гемосидерин обнаруживается в клетках печени, селезенки, костного мозга, лимфатической ткани. При различных патологических состояниях может происходить избыточное образование гемосидерина с развитием гемосидероза. Изучение эпидемиологии гемосидероза затруднено ввиду большого разнообразия форм данного нарушения.
В зависимости от распространенности патологического процесса различают локальный (местный) и генерализованный (общий) гемосидероз. Локальный гемосидероз служит результатом экстраваскулярного гемолиза, т. е. внесосудистого разрушения эритроцитов. Местный гемосидероз может развиваться как в очагах ограниченных кровоизлияний (гематомах), так и в пределах целого органа (легкого, кожи). Генерализованный гемосидероз является следствием интраваскулярного гемолиза - внутрисосудистого разрушения эритроцитов при различных общих заболеваниях. В этом случае гемосидерин депонируется в клетках печени, селезенки и костного мозга, придавая органам бурую («ржавую») окраску.
К самостоятельным формам гемосидероза относят:
- гемосидероз кожи (болезнь Шамберга, кольцевидная телеангиэктатическая пурпура Майокки, старческий гемосидероз, лихеноидный пигментный и пурпурозный ангиодермит, охряный дерматит и др.)
- идиопатический легочный гемосидероз (бурая индурация легких)
В том случае, когда отложение гемосидерина сопровождается структурными изменениями тканей и нарушением функции органа, говорят о гемохроматозе. Вследствие многообразия причин и форм гемосидероза его изучением занимаются иммунология, дерматология, пульмонология , гематология и другие дисциплины.
Причины гемосидероза
Общий гемосидероз является вторичным состоянием, этиологически связанным с болезнями системы крови, интоксикациями, инфекциями, аутоиммунными процессами. Возможными причинами избыточного отложения гемосидерина могут служить гемолитические анемии, лейкоз, цирроз печени, инфекционные заболевания (сепсис, бруцеллез, малярия, возвратный тиф), резус-конфликт, частые гемотрансфузии, отравления гемолитиче¬скими ядами (сульфаниламидами, сви¬нцом, хинином и др.).
Этиология гемосидероза легких не вполне ясна. Высказаны предположения относительно наследственной предрасположенности, иммунопатологического характера заболевания, врожденных нарушений структуры стенки легочных капилляров и др. Известно, что развитию гемосидероза легких в большей степени подвержены пациенты с декомпенсированной сердечной патологией (кардиосклерозом, пороками сердца и пр.).
Кожный гемосидероз может быть первичным (без предшествующего поражения кожи) или вторичным (возникает на фоне кожных заболеваний). К развитию первичного гемосидероза кожи предрасполагают эндокринные заболевания (сахарный диабет),
сосудистая патология (хроническая венозная недостаточность, гипертоническая болезнь). К вторичному накоплению гемосидерина в слоях дермы могут приводить дерматиты, экзема, нейродермит, травмы кожи, фокальная инфекция (пиодермии). Провоцировать дебют заболевания могут переохлаждение, переутомление, прием лекарственных средств (парацетамола, НПВС, ампициллина, диуретиков и др.).
Гемосидероз легких
Идиопатический легочный гемосидероз – заболевание, характеризующееся повторными кровоизлияниями в альвеолы с последующим отложением гемосидерина в легочной паренхиме. Заболевание поражает преимущественно детей и людей молодого возраста. Течение гемосидероза легких характеризуется легочными кровотечениями различной интенсивности, дыхательной недостаточностью игипохромной анемией.
В острой фазе заболевания у больных возникает влажный кашель с выделением кровянистой мокроты. Следствием длительного или обильного кровохарканья служит развитие тяжелой железодефицитной анемии, бледность кожных покровов, иктеричность склер, жалобы на головокружение, слабость. Прогрессирующее течение гемосидероза легких сопровождается развитием диффузногопневмосклероза, отражением которого является одышка и цианоз. Периоды обострения сопровождаются болями в грудной клетке и животе, артралгиями, лихорадкой. Объективные данные характеризуются притуплением перкуторного звука, наличием влажных хрипов,тахикардии, артериальной гипотонии, сплено- и гепатомегалии.
В периоды ремиссии жалобы не выражены или отсутствуют, однако после каждой последующей атаки длительность светлых промежутков, как правило, сокращается. У больных с хроническим течением гемосидероза часто формируется легочное сердце; нередко возникают тяжелые инфаркт-пневмонии, рецидивирующие пневмотораксы, которые могут послужить причиной летального исхода. Идиопатический гемосидероз легких может сочетаться с геморрагическим васкулитом, ревматоидным артритом, системной красной волчанкой, гломерулонефритом, синдромом Гудпасчера.
Гемосидероз кожи
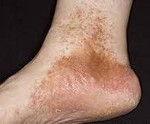
При кожном варианте гемосидероза отложение железосодержащего пигмента происходит в дерме. Клинически заболевание характеризуется появлением на коже геморрагической сыпи или пигментных пятен диаметром 0,1-3 см. Свежие высыпания имеют кирпично-красную окраску; старые приобретают бурый, темно-коричневый или желтоватый цвет. Чаще всего пигментированные очаги локализуются на коже лодыжек, голеней, кистей, предплечий; иногда высыпания сопровождаются легким зудом. В местах поражения кожи могут возникать петехии, узелки, лихеноидные папулы, телеангиэктазии, бляшки «ржавого» цвета.
Гемосидероз кожи носит хроническое течение (от нескольких месяцев до нескольких лет), чаще встречается у мужчин в возрасте 30-60 лет. Общее состояние пациентов при кожном гемосидерозе остается удовлетворительным; внутренние органы не поражаются. Заболевание следует отличать от атипичных форм красного плоского лишая, псевдосаркомы и саркомы Капоши.
Диагностика гемосидероза
В зависимости от формы гемосидероза его диагностика может осуществляться дерматологом, пульмонологом, инфекционистом, гематологом и другими специалистами. В дополнение к физикальному обследованию проводится общий анализ крови, определение сывороточного железа, общей железосвязывающей способности крови. Для выявления гемосидероза наибольшее значение имеют данные биопсии тканей (кожи, печени, легкого, костного мозга), при гистологическом исследовании которых обнаруживается отложение гемосидерина. В качестве диагностического теста применяется десфераловая проба - определение количества железа в моче после внутримышечного введения 500 мг десферала. При содержании более 1 мг железа в моче проба считается положительной.
При гемосидерозе легких дополнительно проводится рентгенография грудной клетки, КТ, перфузионная сцинтиграфия легких, микроскопическое исследование мокроты, спирометрия. Проведение бронхоскопии с взятием промывных вод позволяет обнаружить сидерофаги и эритроциты в лаважной жидкости.
Лечение гемосидероза
Препаратами первого ряда, применяемыми для терапии легочного гемосидероза, служат глюкокортикостероиды, однако они оказываются эффективны лишь в половине случаев. Предложена методика комбинированного лечения иммунодепрессантами (азатиоприн, циклофосфан) в сочетании с плазмаферезом. Кроме этого, используется симптоматическая терапия: препараты железа, кровоостанавливающие средства, гемотрансфузии, бронхолитики, ингаляции кислорода. В некоторых случаях ремиссия заболевания наступает после проведения спленэктомии.
Лечение гемосидероза кожи включает местное использование кортикостероидных мазей, криотерапию, прием аскорбиновой кислоты, рутина, препаратов кальция, ангиопротекторов. При тяжелых кожных проявлениях гемосидероза прибегают к ПУВА-терапии, назначению дефероксамина (десферала).
Прогноз и профилактика гемосидероза
Идиопатический легочный гемосидероз - трудно диагностируемое заболевание с серьезным прогнозом. Прогрессирующее течение патологии приводит к инвалидизации пациента, развитию жизнеугрожающих осложнений – массивного легочного кровотечения, дыхательной недостаточности, легочной гипертензии. Течение гемосидероза кожи благоприятное. Заболевание в большей степени представляет косметический дефект и склонно к постепенному разрешению.
Предупреждению нарушения обмена гемосидерина может способствовать своевременная терапия кожных и общих инфекционных, сосудистых, гематологических и других заболеваний, предупреждение гемотрансфузионных осложнений, исключение лекарственных и химических интоксикаций.
Обмен железа и нарушение обмена железа. Гемоседероз