Влияния диоксида кремния на анионную полимеризацию -КЛ в присутствии натриевой соли -КЛ, промышленного активатора, а также изучить свойства полученного ПКА
СПИСОК ПРИНЯТЫХ СОКРАЩЕНИЙ
ПА – полиамид
ПКА – поликапроамид
-КЛ – -капролактам
ДК – диоксид кремния
ПНК– пирогенный нанокремнезём
ЛК – лактам
ТГА термогравиметрический анализ
TMA – термомеханический анализ
Тпл – температура плавления
СОДЕРЖАНИЕ
Стр.
Введение 7
1 Аналитический обзор 9
1.1 Исторические аспекты получения полиамидов 9
1.2 Полимеризация -капролактама 12
1.3 Катализаторы анионной полимеризации
-капролактама 15
1.4 Активаторы анионной полимеризации лактамов 19
1.5 Диоксида кремния 23
1.6 Применение диоксида кремния в полимерных композициях
2 Экспериментальная часть 31
2.1 Характеристика исходных веществ 31
2.2 Методика полимеризации -капролактама 33
2.3 Методы исследования синтезированных веществ 33
3 Обсуждение результатов 38
Выводы 44
Список используемых источников 45
ВВЕДЕНИЕ
В связи с высокими темпами развития человечества начался бурный рост потребления товаров полимерной промышленности, что сделало важной проблему создания новых полимеров с заданной структурой и свойствами. Решение данной проблемы принесло много дивидендов в экономике и технологии производства за счет улучшения качества полимеров, увеличения срока службы и расширения сфер их практического использования. Благодаря этому, создание новых полимеров с определёнными свойствами и модификация уже известных многотоннажных полимеров на стадии синтеза или переработки, играют важную роль в современной полимерной химии [1].
Поликапроамид (ПКА) обладает высокими прочностными и эксплуатационными свойствами со сравнительно небольшим удельным весом и доступной ценой. Но существует и ряд недостатков: низкие значения эластичности, термической стабильности и большое водопоглощение [2].
Улучшить свойства ПКА можно при помощи введения на стадии синтеза различных модификаторов, которые способны изменять химическую или надмолекулярную структуру полимера.
Одним из основных способов получения ПКА является анионная полимеризация в массе, которая очень чувствительна к примесям. Кроме того, данный метод синтеза ПКА используют для получения из мономера уже готовых изделий, исключая стадию переработки, на которой возможно введение добавок, поэтому выбор дополнительных структурирующих соединений очень сильно осложняется. Анионная активированная полимеризации -капролактама (-КЛ) в присутствии полимеров другой природы позволяет модифицировать свойства ПКА. Такое преобразование является особенно успешным, если макромолекулы ПКА и полимерного модификатора оказываются химически связанными между собой. Одним из способов решения данной задачи является использование твердофазных материалов, в частности, диоксида кремния, который характеризуется широким спектром физико-химических свойств, благодаря чему находят применение во многих технологических процессах. Введение данного веществ в систему может позволить активировать процесс анионной полимеризации -КЛ и получить соединения с требуемыми характеристиками (плотности, прочности, термостойкости). Диоксид кремния (ДК) широко используется в качестве наполнителя для полимеров. Его обычно вводят в среду для полимеризации в начале процесса [3].
Целью данной работы являлось изучение влияния диоксида кремния на анионную полимеризацию -КЛ в присутствии натриевой соли -КЛ, промышленного активатора, а также изучить свойства полученного ПКА.
Конкретными задачами исследования являлись:
1. Провести литературный обзор об особенностях анионной полимеризации лактамов, роли активаторов и катализаторов, перспективах получения и модификации полимерных композиционных материалов на основе ПКА.
2. Установить зависимость влияния ДК и его концентрации на полимеризацию -КЛ.
3. Оценить влияние ДК на свойства получаемого ПКА.
1 АНАЛИТИЧЕСКИЙ ОБЗОР
- Исторические аспекты получения полиамидов и их свойства
ПА класс термостойких полимеров, ароматическая природа молекул которых определяет их высокую прочность вплоть до температуры разложения, химическую стойкость, тугоплавкость. К ПА относится как синтетические, так и природные полимеры, содержащие амидную группу -CO-NH-.
Промышленный процесс получения ПА освоен довольно давно. Это или поликонденсация амидов (многоосновные кислоты с альдегидами), или поликонденсация высших аминокислот или диаминов с дикарбоновыми кислотами, или конденсация капролактама и солей диаминов дикарбоновых кислот.
Первые ПА получили еще в 1862-м году (синтетический ПА), а массово стали использовать примерно в пятидесятые годы двадцатого столетия. Масштабное изготовление ПА теперь освоено достаточно хорошо [4].
Основные промышленные способы получения ПА полимеризация с раскрытием цикла (главным образом ЛК) и поликонденсация -аминокарбоновых кислот или их эфиров, а также дикарбоновых кислот (их эфиров или галогенангидридов) с диаминами. Для синтеза ПА широко используют -капролактам (-КЛ), -додекалактам, адипиновую, себациновую, фталевые кислоты (терефталевую и изофталевую), гексаметилендиамин, фенилендиамины (пара- и метаизомеры).
Наибольшее распространение получили алифатические ПА (в частности, полигексаметиленадипинамид, ПКА, а также полигексаметилен-себацинамид, полидодеканамид и др.); из ароматических ПА в промышленности производят поли-м-фениленизофталамид (из м-фенилендиамина и изофталевой кислоты) и поли-п-бензамид (из n-аминобензойной кислоты).
Большинство ПА твёрдые рогоподобные кристаллические вещества белого цвета (степень кристалличности до 4060%), некоторые ПА вязкие жидкости (смолы). Температура плавления алифатических ПА 150260°С, ароматических около 400°С и выше. ПА лёгкие термопластичные полимеры, характеризуются высокими механической прочностью (например, при растяжении 60120 МН/м2, или 6001200 кгс/см2, при изгибе 70100 МН/м2, или 7001000 кгс/см2), твёрдостью, эластичностью (относительное удлинение алифатических ПА 100400%), износостойкостью, теплостойкостью (например, по Вика, 160200°С для алифатических ПА, 270320°С для ароматических), химической стойкостью (при комнатной температуре устойчивы в воде, растворах кислот, щелочей, аминов и др.), растворяются только в сильнополярных растворителях (например, в концентрированной серной и муравьиной кислотах, крезоле, фторированных спиртах).
ПА легко перерабатываются прессованием, литьём под давлением, экструзией, хорошо обрабатываются на станках; при формовании из расплавов или растворов образуют волокна.
Благодаря сочетанию таких свойств ПА широко используют в промышленности, главным образом для производства синтетических волокон, плёнок, а также в качестве конструкционного материала для изготовления различных деталей машин (шестерён, втулок, подшипников и др.).
Мировое производство ПА конструкционного назначения в 1973 составило приблизительно 300 тыс. т. [5].
Помимо обычного производят так же модифицированный ПА, свойства которого улучшаются и изменяются в соответствии с необходимостью путем добавления тех или иных химических составов (в частности укрепляющих добавок или эластомеров). Состав ПА может быть различным. Все зависит от того, для чего будет использоваться конечная продукция (в соответствии с этим присваиваются и марки ПА). Различаются ароматические (как правило, бесцветные высокоплавкие аморфные или кристаллические) и алифатические ПА.
Алифатические ПА являются гибкоцепными кристаллизующимися (Скр=4070%) термопластами, молекулярная масса которых равна 840 тысячям, их плотность 10101140 кг/м3, Тпл 2102600С, расплав обладает низкой вязкостью в узком температурном интервале. ПА гидрофильные полимеры, их водопоглощение достигает нескольких процентов (иногда до 8) и существенно влияет на прочность и ударную вязкость. Наибольшее значение имеют ПА общих формул: [-HNRNHOCR'CO-]n и [-HNR"CO-]n, где R,R'=Alk, Ar, R"=Alk. Макромолекулы связаны между собой водородными связями, что обусловливает относительно высокие Тпл ПА.
Растворяется в сильно полярных растворителях (концентрированной H2SO4, HCOOH, крезолах), диметилацетамиде. Большинство ароматических ПА растворяется в ограниченном числе растворителей, что заметно сужает области их применения и усложняет технологию переработки. Введение в ПА цепь сульфогрупп сказывается на растворимости полимеров. При определенном содержании сульфогрупп ароматические ПА приобретают способность растворяться в воде. Следует отметить, что все представленные ПА вне зависимости от строения и количества сульфогрупп растворимы в 96%-ной серной кислоте [6].
ПКА (поли--капроамид, полиамид–6) [NH(CH2)5CO-]n линейный полимер -КЛ, алифатический ПА. Белое рогоподобное вещество, без запаха, молекулярная масса 10000 – 35 000, плотность 1,13–1,14г/см3 (20°С): степень кристалличности ~60%, tпл 225 °С.
ПКА впервые был получен в 1899 г. Габриэлем и Маасом при поликонденсации -аминокапроновой кислоты. При этом было сделано очень важное наблюдение, что нагревание -аминокапроновой кислоты приводит к образованию наряду с полимером также и низкомолекулярного циклического продукта -КЛ [7].
ПКА – один из наиболее известных ПА; характеризуется высокой износостойкостью и механической прочностью, например, прочность при изгибе ~90 МН/м2 или ~900 кгс/см2, ударная вязкость 150–170 кдж/м2, или кгс. см/см2. Химически стоек, устойчив к действию большинства растворителей, растворяется только в концентрированной серной и муравьиной кислотах, фторированных спиртах; физиологически безвреден, в организме человека рассасывается медленно. При комнатной температуре и нормальной влажности воздуха ПКА поглощает 2–3% влаги (максимально до 12%).
В промышленности ПКА получают полимеризацией мономера; перерабатывают методами, обычными для ПА. При полимеризации в формах получают крупногабаритные изделия из ПКА, не требующие механической обработки. ПКА используется в основном для производства волокон, а также для изготовления различных деталей машин.
ПКА выпускают под названием капрон, капролон (СССР), перлон (ФРГ), дедерон (ГДР), силон (ЧССР), амилан (Япония), найлон-6, пласкон, капролан (США) [8].
- Полимеризация -капролактама
Среди промышленных способов получения ПА, полимеризация лактамов (ЛК) является одним из основных и самых распространённых методов. Это связано с тем, что ЛК, содержащие 6 или более атомов углерода, могут полимеризоваться любым способом, в то время как ЛК с числом атомов углерода пять и меньше полимеризуются только по ионному механизму (анионная или катионная полимеризации). Так, один из важнейших и широко распространенных представителей класса ПА ПКА, получают в промышленных масштабах гидролитической полимеризацией -КЛ. Это обусловлено тем, что применяемый активатор (вода) является дешевым, хорошо растворяется в КЛМ, не изменяется с повышением температуры и т.д. [10]:
При гидролитической полимеризации, число образующихся активных центров, на которых происходит рост цепи, пропорционально начальной концентрации воды или катализатора. При присоединении мономера к активным центрам образуется полимер с очень узким молекулярно-массовым распределением. Для достижения такого распределения необходимо обрывать реакцию до получения полимера с высокой молекулярной массой.
Однако с целью уменьшения продолжительности процесса в последнее время полимеризацию -КЛ проводят по катионному или анионному механизмам.
При катионной полимеризации капролактама, осуществляемой в безводной среде, реакция протекает ступенчато. В результате при полном отсутствии воды получается промежуточный продукт гидрохлорид N-аминокапроилкапролактама:
который реагирует с КЛ, раскрывая цикл и обусловливая полимеризацию по схеме [9]:
Для катионной полимеризации характерно, что довольно высокая в начале процесса скорость реакции затем быстро падает. Процесс резко ускоряется при использовании сокатализаторов. Метод катионной полимеризации -КЛ в промышленных условиях в настоящее время не используется, в основном из-за того, что мало изучен.
Анионная полимеризация -КЛ является реакцией, катализируемой основаниями. Применение соответствующих инициаторов способствует установлению равновесного состояния системы за несколько минут, что является большим преимуществом для промышленного использования этого процесса.
После первого описания анионной полимеризации ЛК были проведены широкие исследования механизма этой реакции. Общепринятая в настоящее время схема анионной полимеризации была предложена Маттесом и др. и независимо Шебендой и Краличеком. Было показано, что при нагревании -КЛ в присутствии основания, например, капролактамата натрия, ускорение полимеризации наблюдается только после прохождения определенного индукционного периода. Было предположено, что первоначально происходит образование аминных и имидных групп, но так как аминогруппы в большей степени подавляют полимеризацию, чем инициируют, то активными инициирующими группами были признаны имидные. Считается, что полимеризация представляет собой нуклеофильную атаку карбоксила имидной группы анионом -КЛ.
Медленное обычное инициирование, может быть полностью исключено при использовании инициаторов с имидными группами, например ацетиллактама. Процесс активированного инициирования осуществляется очень быстро, так что в присутствии катализатора и имидного инициатора полимеризация в блоке может осуществляться в диапазоне температур 100200°С, т. е. при температурах ниже Тпл полимера, которая составляет примерно 225°С.
Процесс полимеризации -КЛ экзотермический, а в случае активированной полимеризации, характеризующейся большой скоростью превращения, он часто протекает в адиабатических условиях. Высокая вязкость и низкая теплопроводность реакционной массы приводят к значительному подъему температуры образца. Скорость повышения температуры можно использовать в качестве критерия оценки скорости реакции.
Теплота полимеризации лактама зависит от размера кольца. Было замечено, что при протекании полимеризации при температуре ниже Тпл полимера равновесное содержание мономера оказывается гораздо меньшим, нежели подсчитанное теоретически. Этот эффект объясняется сосуществованием кристаллической и аморфной фаз, причем первая не содержит мономера и не участвует в установлении равновесия полимер мономер. При низкотемпературной полимеризации также должно приниматься во внимание изменение энтропии вследствие кристаллизации образующегося полимера; при этом экзотермические эффекты реакции различны для разных лактамов [11].
По многим свойствам ПКА, получаемый этим методом, превосходит ПКА, синтезируемый гидролитической полимеризацией: прочность при сжатии и статическом изгибе, а также твердость в 1,51,6 раза выше, водопоглащение в 2,5 раза ниже, теплостойкость на 300С выше и т.д. Содержание мономера в таком ПКА не превышает 1,52,5%, поэтому нет необходимости в его удалении [12].
1.3 Катализаторы анионной полимеризации капролактама
Среди наиболее часто применяемых катализаторов можно отметить лактаматы различных щелочных и щелочно-земельных металлов, а также алюминия, магния и т.д., которые получают взаимодействием -КЛ, например, с диалкоксиалюминийгидридом натрия, реактивами Гриньяра и др. металлоорганическими соединениями [13].
Реакция роста цепи происходит в две стадии: нуклеофильное присоединение аниона лактама к эндоциклическому карбонильному атому углерода концевого имидного звена (стадия I) и протонирование N-аниона мономером (стадия II). При каждом акте присоединения регенерируется оба активных центра (анион ЛК и концевая имидная группа) [14].
Активность катализаторов определяется степенью диссоциации используемых солей и уменьшается в следующем ряду: MgBr KЛ > l/2(Mg KЛ2 + MgBr2) > Na КЛ > Na(Al -KЛ2(OC2H4OCH3)2) > Mg КЛ2 > Mg KЛ(OC3H7) > Al KЛ3. Высокая эффективность магнийбромкапролактама (MgBrКЛ) связана не только с его высокой степенью диссоциации (Кд=5,51x10-3 гэкв/л), но и, по-видимому, с увеличением электрофильности карбонильных атомов углерода концевой имидной группы растущей цепи за счет координации с MgBr2, образующимся в результате реакции диспропорционирования MgBrКЛ [15].
Однако следует отметить, что одним из недостатков широко используемого в промышленности MgBrКЛ является применение в процессе его синтеза диэтилового эфира.
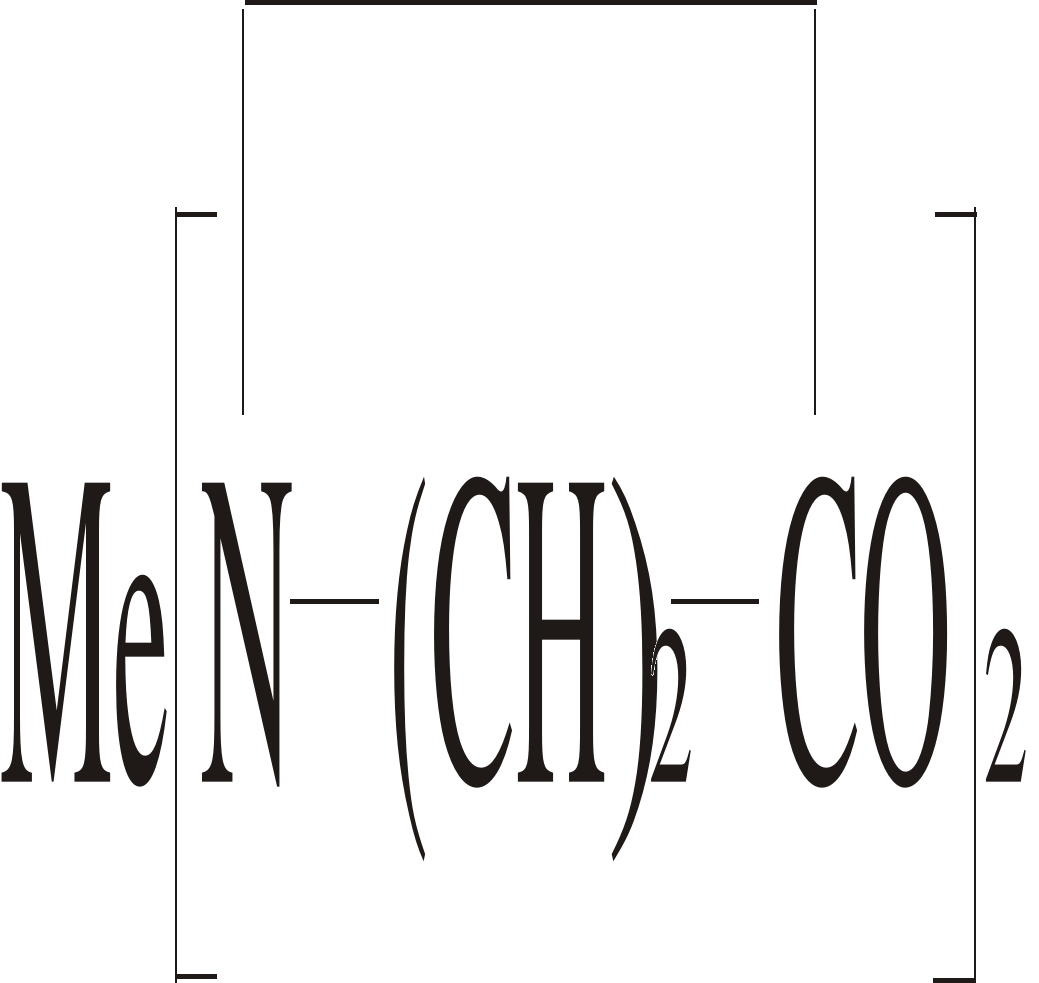
Котельников В. А. и сотрудники синтезировали капролактаматы щелочно-земельных металлов и магния общей формулы
из алкоксидных, гидридных и металлорганических соединений и -КЛ. Сопоставление кинетической активности полученных лактаматов показало, что наиболее чистые, а, следовательно, и более эффективные катализаторы получаются из металлорганических и гидридных (например, NaН) соединений этих металлов. Реакционная способность алкоголятов щелочно-земельных металлов и магния в реакциях металлирования -КЛ росла в ряду Mg<Ca<Sr<Ba [16].
В работах [17, 18] показано, что активными центрами полимеризации могут являться не только свободные анионы лактама, но и ионные пары. Вклад последних в суммарную скорость полимеризации определяется природой катиона. Так, например, в случае использования в качестве катализатора дикапролактамата магния рост цепи осуществляется исключительно на контактных ионных парах, а при использовании капролактамата калия вклад ионных пар в суммарную скорость процесса < 30 % [15].
Каталитическая активность щелочных солей лактамов (более активных по сравнению с солями щелочно-земельных металлов) возрастает в зависимости от катиона в следующей последовательности: Li<Na<K, что следует из увеличения наклона кривых “начальная скорость полимеризации (v0) – функция концентрации этих катализаторов” (рисунок 1.1) [19].
Большой интерес представляет влияние природы катиона катализатора на константы скорости роста цепи на ионных парах (kр±) и на свободных анионах (kр-). Так показано, что kр- не зависит от катиона, в то время как kр± изменяется в ряду К+>Na+>Li+ (таблица 1.1) [20].
Наблюдаемая тенденция уменьшения реакционной способности ионной пары с уменьшением радиуса катиона, как правило, указывает на контактный характер ионных пар.
Таблица 1.1 – Кинетические параметры анионной полимеризации -КЛ, катализируемой капролактаматами щелочных металлов [20]
|
Противоион
|
Т,°С
|
Кд*·104,моль/л
|
kр-
|
kр±
|
|
|
|
|
л/(моль с)
|
|
К+
|
135
|
1,02
|
18,3
|
2,0
|
|
|
150
|
1,85
|
66,5
|
3,4
|
|
|
160
|
3,10
|
103,0
|
4,7
|
|
Na+
|
135
|
0,62
|
18,6
|
1,6
|
|
|
150
|
1,05
|
68,0
|
2,8
|
|
|
160
|
1,45
|
104,7
|
3,8
|
|
Li+
|
135
|
0,15
|
19,1
|
1,3
|
|
|
150
|
0,24
|
67,0
|
2,4
|
|
|
160
|
0,31
|
100,5
|
3,4
|
* в присутствии 0,0191 моль/л N-ацетил-КЛМ
Следует отметить, что свободные анионы лактама более активны, чем контактные ионные пары; в то же время отношение kр-/kр± 30 - 40 свидетельствует (с учетом Кд) о заметном вкладе ионных пар в суммарную скорость рассматриваемого процесса полимеризации -КЛ. Увеличение температуры синтеза способствует повышению вклада свободных анионов лактама (по сравнению с ионными парами) в суммарную скорость полимеризации.
Совместное применение капролактаматов щелочных металлов и алюминия позволяет существенно увеличить молекулярную массу образующегося ПА. Так, Gnanou Y. и сотрудники разработали новый класс катализаторов на основе щелочных металлов и диалкилалюминийгидридов для анионной полимеризации -КЛ. Подобные катализаторы (ди- или тетра--капролактамалюминаты Na и др.) для получения ПА были использованы в работах [21].
При высоких температурах переработки катализатор, присутствующий в ПА, вызывает интенсивные деструктивные процессы, среди которых отмечают обменные реакции типа переамидирования и переацетилирования. В работе [22] с помощью термогравиметрических и вискозиметрических исследований было показано, что термическая стабильность ПА возрастает при использовании различных катализаторов в следующей последовательности: (NaКЛ < 1/2(MgКЛ2+MgBr2) < MgBrKЛ < MgКЛ2 < Na[AlКЛ2(ОС2Н4ОСН3)2]).
1.4 Активаторы анионной полимеризации капролактама
В настоящее время в качестве активаторов анионной полимеризации ЛК предложено использовать широкий круг как органических, так и неорганических соединений. Предпринято несколько попыток классификации активирующих соединений. Рассматривалось влияние структуры и электронного строения указанных соединений на их активирующую способность. По способу действия в условиях анионной полимеризации ЛК было предложено подразделить активаторы на «прямые», обладающие собственной активирующей способностью, и «косвенные», которые взаимодействуют с ЛК или его солью с образованием активатора.
В основу классификации активирующих соединений, предложенной Стегличеком и др. положено их химическое строение:
1) эфиры органических и неорганических кислот и лактоны;
2) ангидриды и галогенангидриды карбоновых кислот;
3) амиды, нитрилы и цианамиды карбоновых кислот;
4) карбодиимиды, изоцианаты, изотиоцианаты, мочевины, уретаны и
гуаниды;
5) производные сульфо- и фосфорных кислот;
6) окислы и хлориды металлов (катализаторы Фриделя – Крафтса);
7) другие соединения, такие как фторпроизводные, органические перекиси, сероуглерод, ароматические нитросоединения, алифатические полигалогениды и др.
При таком разделении активаторов косвенного действия в один класс попадают соединения, которые при взаимодействии с лактамом или его щелочной солью образуют активирующие центры и побочные продукты (спирты, кислоты, амины и др.) различной химической природы. Так, например, объединенные в один класс амиды и нитрилы при взаимодействии с анионом лактама образуют различные по химическому строению активирующие соединения; изоцианаты при взаимодействии с лактамом не образуют никаких побочных продуктов, а уретаны, относящиеся, к тому же классу, дают спирты. Нами предпринята попытка классификации активаторов с учетом химической природы образующихся активирующих групп и побочных продуктов взаимодействия. Таблица 1.2 охватывает известные из патентной литературы активаторы анионной полимеризации лактамов. Все соединения разбиты на семь классов. Каждый класс разделен на подгруппы вследствие некоторых различий в природе образующихся активных соединений внутри каждого класса. Так как невозможно однозначно указать механизм образования активных центров, в ряде случаев приведено несколько вариантов предполагаемого механизма. Соединения, относящиеся к первому классу, являются активаторами прямого действия, не образующими никаких побочных продуктов, отравляющих каталитическую систему, и поэтому выделены отдельно.
Таблица 1.2 – Классификации активаторов с учетом химической природы образующихся активирующих групп и побочных продуктов взаимодействия
|
№ п.п.
|
Класс соединений
|
Предполагаемый механизм активирования
|
|
1
|
2
|
3
|
|
1
|
а) Имиды , карбамоиллактамы, ациллактамы
|
|
|
|
б) Изоцианаты, изотиоцианаты
|
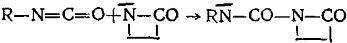
|
|
2
|
а) Ангидриды и галогенангидриды карбоновых кислот
|
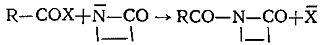
|
|
|
б) Галогенированные линейные и циклические алканоны
|
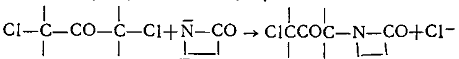
|
|
|
б) Органические перекиси
|

|
|
3
|
а) Эфиры органических и неорганических кислот
|
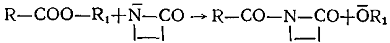
|
|
|
б) Лактоны , тиолактоны
|
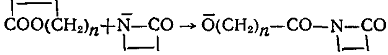
|
|
|
в) Уретаны
|
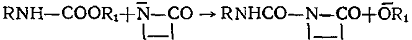
|
|
4
|
а) Амиды
|
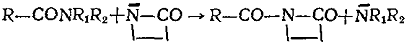
|
|
|
б) Мочевины , тиомочевины
|
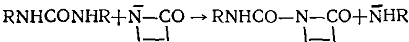
|
|
|
в) Карбонилимидазолы
|
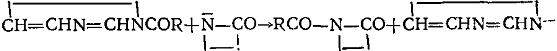
|
Окончание таблицы 1.2
|
1
|
2
|
3
|
|
|
г) Кетоамиды
|
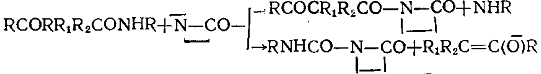
|
|
|
д) Дикетоны
|
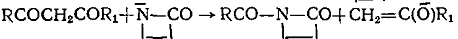
|
|
5
|
а) Нитрилы, CN-лактамы
|
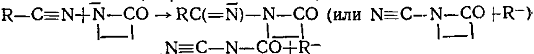
|
|
|
б) CN-галогениды
|
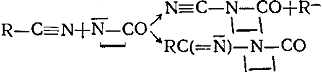
|
|
|
в) Дилактиловые эфиры
|
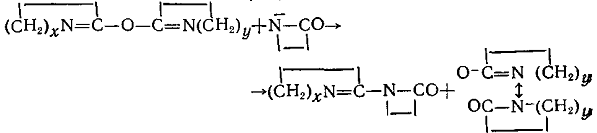
|
|
|
г) Цианамиды
|
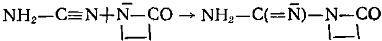
|
|
|
д) Карбодимиды, гуанидины, имины, иминокарбонаты
|
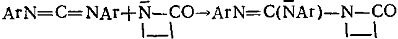
|
|
|
е) Азиды
|
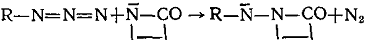
|
|
|
ж) Триазины, пиридазины, пиримидины, бензтиазолы
|
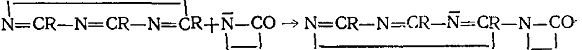
|
|
6
|
Фосфонитрильные соединения, (PNX2)3
|
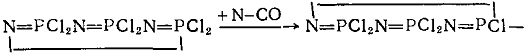
|
|
|
Алкилгалогенидфосфины, алкилгалогенидфосфиты, фосфины, фосфаты, галогениды
|
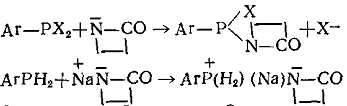
|
|
|
Р2О5
|
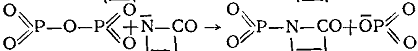
|
|
7
|
Окислы элементов VI группы СО, СО2, CS2
|
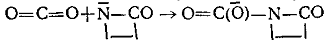
|
Соединения второго, третьего и четвертого классов образуют активные центры одинаковой ациллактамной структуры. Несмотря на это, эти соединения все же не объединены в один класс, так как образующиеся побочные продукты отличаются по своей химической природе. У соединений пятого класса образующаяся активная частица содержит группировку, в которой азот лактамного цикла связан с ненасыщенной системой:
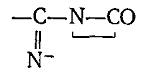
Побочные продукты для соединений пятого класса не характерны. В шестой класс объединены фосфорсодержащие соединения, образующие при взаимодействии с ЛК или его анионом активные центры:
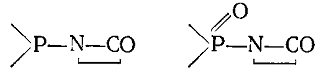
и дающие в качестве побочных продуктов кислоты. К седьмому классу отнесены окислы элементов VI группы, СО, СО2, CS2.
Таким образом, предложенная классификация активаторов учитывает не только природу образующегося активного центра, но и характер побочных продуктов, которые оказывают существенное влияние на скорость анионной полимеризации ЛК. Так, возникающие при образовании активирующих соединений спирты, амины, кислоты и другие продукты приводят к многочисленным побочным процессам, вызывающим отравление каталитической системы, среди которых следует отметить уменьшение щелочности системы, конденсацию образующихся альдегидов, аминолиз продуктов реакции и др. [23].
1.5 Диоксид кремния
Oксид кремния (IV) (ДК, кремнезём, SiO2) — бесцветные кристаллы, обладают высокой твёрдостью и прочностью.
ДК существует в нескольких полиморфных модификациях (таблица 1.3). Разнообразие модификаций кремнезёма объяснимо сродством кремния к кислороду и образованием прочных одинарных связей между этими атомами [24].
Наиболее распространенной формой ДК является -кварц (обычно самую высокую температурную форму обозначают буквой ; следующие формы, возникающие по мере охлаждения – , и т.д.). -кварц
Таблица 1.3 – Структура и свойства различных форм кремнезема
|
Модифи-кация
|
Число формульных единиц в ячейке
|
Плотность г/см3
|
Ng
|
С0р, Дж/ (моль*К)
|
Hобр
кДж/моль
|
S0298,кДж, (моль*К)
|
|
|
|
|
|
|
|
|
|
-Кварц
|
3
|
2,65
|
1,55
|
44,60
|
-910,7
|
41,5
|
|
-Кварц
|
3
|
2,53
|
1,54
|
-
|
-
|
|
|
-Тридимит
|
64
|
2,30
|
1,47
|
-
|
-905,2
|
|
|
-Кристобалит
|
4
|
2,33
|
1,48
|
44,56
|
-908,0
|
42,6
|
|
Китит
|
8
|
2,50
|
1,52
|
-
|
|
|
|
Коэсит
|
12
|
3,01
|
1,60
|
45,39
|
-905,9
|
40,4
|
|
Стишовит
|
16
|
4,35
|
1,82
|
42,97
|
-861,5
|
27,8
|
|
Волокнистый кремнезем
|
2
|
1,97
|
-
|
-
|
|
|
|
Стеклоообразный SiO2
|
4
|
2,21
|
-
|
43,99
|
-901,4
|
47,86
|
* N - Показатели преломления. ** У - и -кварца по две пространственные группы, так как для обеих форм возможны левый и правый оптические изомеры. *** -120°С.
-Кварц устойчив до 8700С; -кварц переходит в -форму после 5730С. При 5730С переход в -формы в -форму сопровождается поглощением теплоты (250 кал/моль) и увеличением объема. Кристаллы -формы имеют гексогональную структуру, а -модификация кварца представляет собой бесцветные кристаллы призматической формы с тригональной системой. -Кварц после 8700С становится неустойчивой модификацией вплоть до 16000С, т.е. до расплавления.
Наиболее важная для практики модификация ДК – -тридимит (Тпл 16700С) – устойчива в интервале 870-14700С, после чего медленно переходит в -кристаболит, обладающий максимальной Тпл (17130С). Кристобалит устойчив лишь выше 14700С в модификации -кристобалита. Метастабильная модификация – -кристобалит может существовать при обычных условиях и встречается в природе, но при нагреве выше 2400С быстро переходит в -модификацию. Это превращение происходит также со значительным увеличением объема [25].
ДК – это твердое тугоплавкое вещество полимерного строения (SiO2)n с атомной кристаллической решёткой. Молекул SiO2 при обычных условиях подобно молекулам СО2 не существует, SiO2 – формульная единица (или простейшая формула) оксида.
Строение кристаллической решётки ДК в плоскостном изображении можно представить так:
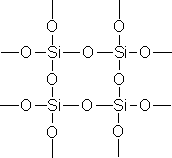
Несходство строения ДК с родственным ему углекислым газом (CO2) (который имеет молекулярную структуру: O=C=O) вызвано тем, что атомы Si в отличие от атомов углерода, не могут образовывать устойчивых -связей, как между собой, так и с другими атомами. Поэтому все связи атомов кремния в соединениях одинарные (-связи).
Плотность ДК равняется 2,648 г/см. Вещество плавится в пределах температур от 1600 до 1725°С, кипит при температуре 2590°С [26].
ДК не растворяется в большинстве органических растворителей. Аморфный ДК медленно растворяется в водных растворах щелочей, Na2CO3 (давая силикаты) и NH4F (образуя фторосиликаты), скорость растворения увеличивается при повышении давления и температуры. При нагревании смесей порошкообразного ДК с различными оксидами образуются силикаты Кислоты, за исключением плавиковой, не действуют на ДК. Плавиковая кислота же легко вступает с ним в реакцию, образуя фторид кремния и воду [27].
Аэросил представляет собой высокодисперсный чистый ДК, это – химически инертное вещество, пожаро- и взрывобезопасное, не оказывает общетоксического действия. Некоторые физико-химические показатели аэросила приведены в таблице 1.4 [28]:
Таблица 1.4 – Физико-химические показатели аэросила [28]
|
Наименование показателя
|
Норма
|
|
1
|
2
|
|
Внешний вид неуплотненного
|
Рыхлый голубовато-белый порошок
|
|
Массовая доля диоксида кремния в пересчете на прокаленное вещество, %, не менее
|
99,9
|
|
Массовая доля оксида железа, %, не более
|
0,003
|
|
Массовая доля оксида алюминия, %, не болеее
|
0,05
|
|
Массовая доля диоксида титана, %, не более
|
0,03
|
Окончание таблицы 1.4
|
1
|
2
|
|
рН суспензии
|
3,8-4,5
|
|
Массовая доля влаги, %, не более
|
1,5
|
|
Потери в массе при прокаливании, %, не более
|
1
|
|
Насыпная плотность неуплотненного, г/дм3
|
40-60
|
|
Насыпная плотность уплотненного, г/дм3
|
120-140
|
|
Удельная поверхность по методу БЕТ, м2/г
|
150-200
|
|
Массовая доля крупных частиц (грита),%, не более
|
0,04
|
Важное свойство наноструктур ДК и их отличие от силикагелей (по химическому составу аналогичных с ПНК) – они не образуют устойчивых пористых структур, т.е. не «слипаются навсегда». Пористость у них есть, но она обусловлена образованием временных структур – агрегатов, слипающихся в агломераты. Перемешивание разрушает эти структуры, вместо которых сразу образуются новые.
Это обуславливает трудности в его использовании. Например, было бы неплохо равномерно распределить наночастицы такими замечательными свойствами в красках или пластмассах. Но не выходит – они агрегируются даже после мощной ультразвуковой обработки. В итоге наполнение получается неравномерным.
Несмотря на агрегацию, частиц ПНК так много, что уже при 2-3 мас. % в смолах, маслах и даже воде (при 5-7%) они приводят к загустеванию композиции. Эффект примерно такой же, словно в жидкость ввели огромное количество микропророшка (мела, опилок, глины и др). При дальнейшем наполнении, ПНК приводят к образованию «пластилинов», включающих густые агломераты, иногда едва смоченные жидкой фазой.
Отвержденные пластмассы с ПНК приобретают другие свойства – например, прочность и химическая стойкость их может повышаться на 20-40%. При этом изменяется их пластичность и характер разрушения – например, эпоксидный полимер при сжатии перестает бочковаться (как сжимаемый пластилин) и начинает трескаться подобно хрупкому стеклу.
Эта особенность (плюс дороговизна) ПНК привели к тому, что в больших количествах (для наполнения) его используют редко, зато в качестве загустителей, замутнителей и модификаторов свойств, а также в качестве медсорбентов его используют уже десятилетиями [28].
1.6 Применение диоксида кремния в полимерных композициях
Для модификации полимеров применяют как чистый ДК, так и силикаты продукты взаимодействия ДК с основными оксидами, щелочами, а также с карбонатами щелочных и щелочноземельных металлов сочетанием с другими неорганическими оксидами, которые могут находиться в различных минералах литосферы [29].
Аэросил применяется для загущения, придания тиксотропных свойств жидкостям и активного наполнения каучуков и герметиков. Широко применяется также для придания сыпучести порошкообразным продуктам. Служит наполнителем, существенно улучшающим физико-механические, диэлектрические свойства материалов (твёрдость, упругость, прочность на разрыв, прочность к стиранию, термическую стойкость и др.). Выполняет функцию стабилизатора, выступает в качестве антиседиментационной добавки многокомпонентных систем.
Также применяется в полимерных композициях для изготовления оправки. Композиция содержит, мас.ч.: кварцевый песок 100–1000, поливиниловый спирт 3–80, нанодисперсный наполнитель аэросил 4–6. Введение аэросила в состав композиции в виде нанодисперсного наполнителя способствует повышению коэффициента теплопроводности оправки за счет изменения плотности и более однородной структуры отвержденной полимерной композиции. Достигается повышение эксплуатационных характеристик изделия, получаемого методом намотки.
Изобретение относится к высоконаполненным полимерным композициям на основе поливинилового спирта и может быть использовано для изготовления разрушаемых оправок, применяемых при намотке изделий из композиционных материалов [30].
ДК применяют в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и др. Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках.
Аэросил является важным сырьем для изготовления высокочистых силикатов, применяемых для покрытия телевизионных и осветительных трубок. При этом аэросил, как правило, в виде водной суспензии приводят в реакцию с подходящим соединением металлов. Особое значение имеют силикаты калия, цинка, бария и кадмия. Описанным способом возможно изготовление смешанных силикатов и смешанных окислов. В областях применения, требующих очень чистое жидкое стекло с высоким модулем можно добавлять аэросил в щелочной силикатный раствор, за счет чего повышается доля силиката [31].
Другие области применения:
Аэросил приобретает все большее значение в катализаторных системах, которые для развития их полного действия требуют носитель или компонент из двуокиси кремния. Важными свойствами аэросила для этого применения являются высокая чистота, а также беспористая и большая удельная поверхность. Особое внимание при разработке катализаторов находят смешанные оксиды, которые также изготовляются методом высокотемпературного гидролиза.
ДК применяют в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и др. Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках.
ДК главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87 % массы литосферы.
Аморфный непористый ДК применяется в пищевой промышленности в качестве вспомогательного вещества E551, препятствующего слёживанию и комкованию, парафармацевтике (зубные пасты), в фармацевтической промышленности в качестве вспомогательного вещества (внесён в большинство Фармакопей), а также пищевой добавки или лекарственного препарата в качестве энтеросорбента.
Искусственно полученные плёнки ДК используются в качестве изолятора при производстве микросхем и других электронных компонентов.
Также используется для производства волоконно-оптических кабелей. Используется чистый плавленый диоксид кремния с добавкой в него некоторых специальных ингредиентов.
Кремнезёмная нить также используется в нагревательных элементах электронных сигарет, так как хорошо впитывает жидкость и не разрушается под нагревом спирали.
Крупные прозрачные кристаллы кварца используются в качестве полудрагоценных камней; бесцветные кристаллы называют горным хрусталём, фиолетовые аметистами, жёлтые цитрином.
В микроэлектронике ДК является одним из основных материалов. Его применяют в качестве изолирующего слоя, а также в качестве защитного покрытия. Получают в виде тонких плёнок термическим окислением кремния, химическим осаждением из газовой фазы, магнетронным распылением [31].
Из проведенного аналитического обзора видно, что ДК в основном применяю в качестве наполнителя и стабилизатора. Добавление ДК в структуру полимера приводит к улучшению физико-механических свойств.
2 ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
2.1 Характеристика исходных веществ
2.1.1 Характеристика лактама
В качестве основного мономера был выбран e-КЛ, свойства которого приведены в таблице 2.1.
Таблица 2.1 – Некоторые свойства использованного лактама
|
Свойства
|
e-КЛ
|
|
Внешний вид
|
Твердое кристаллическое белое вещество
|
|
Молекулярная масса, г/моль
|
113
|
|
Структурная формула
|
|
|
Температура кипения, °С
|
262
|
|
Температура плавления,°С
|
69
|
2.1.2 Характеристика катализатора
В качестве катализатора в работе использовался Bruggolen C 10, представляющий собой продукт взаимодействия металлического натрия с e-КЛ со следующими свойствами: молекулярная масса 190 г/моль, температура плавления 72С.
2.1.3 Характеристика активаторов
В качестве активатора использовался промышленный активатор Bruggolen С 20 Р.
2.1.4 Характеристика диоксида кремния
Аэросил – высокодисперсный, высокоактивный, аморфный, пирогенный ДК (SiO2), получаемый пламенным гидролизом четыреххлористого кремния (SiCl4) высокой чистоты. Аэросил представляет собой очень чистый аморфный непористый диоксид кремния с размером частиц от 5 до 40 нм. Это чрезвычайно легкий белый порошок, который в тонком слое кажется полупрозрачным, голубоватым. Массовая доля ДК не менее 99,9%; массовая доля влаги не более 1,5%; насыпная плотность 40-60 г/дм3; массовая доля крупных частиц не более 0,04%.
2.1.5 Характеристика растворителей
Свойства использованных в работе растворителей приведены в таблице 2.2. Все растворители перед применением очищались при помощи перегонки [32].
Таблица 2.2 – Общие характеристики растворителей
|
Название
|
Молекулярная масса, г/моль
|
Плотность, кг/м3
|
Температура плавления, оС
|
Температура кипения, оС
|
|
Ацетон
|
59
|
790
|
-95
|
57
|
|
Гексан
|
86
|
659
|
-95
|
69
|
|
Муравьиная кислота
|
46
|
1220
|
9
|
101
|
2.2 Методика полимеризации -капролактама
Реакция проводилась в трехгорлой колбе, снабженной обратным холодильником и мешалкой в токе аргона. Расчетное количество -КЛ и катализатора (1 мас.%) расплавлялись при температуре 100оС, после чего температуру поднимали до 180оС, добавляли расчетное количество активатора и ДК при постоянном перемешивании. Реакцию вели в течение 150 мин. Полученный продукт экстрагировали в ацетоне, сушили, взвешивали, определяли выход и анализировали.
2.3 Методы исследования синтезированных веществ
2.3.1 Определение выхода полимера
Выход полимера определяли методом гравиметрического анализа, который основан на определении массы вещества. Он является простым и быстрым.
В колбу с ацетоном (15 мл) вводили 3 грамма образца. Выдерживали в течении четырех часов при температуре 450С, после чего полученный раствор фильтровали и сушили до полного высыхания. Высушенный образец взвешивали и рассчитывали выход полимера по формуле 2.1:
=mвысуш/mнач100%, (2.1)
где mнач – начальная масса, г; mвысуш – масса после высушивания, г.
2.3.2 Определение кинетики полимеризации
Для построения кинетических кривых через определенные промежутки времени из реакционной среды отбирали пробы, из которых удаляли непрореагировавшие мономеры. Удаление непрореагировавших мономеров осуществляли методом экстракции в растворителе (ацетоне) в аппарате Сокслета в течение 8 часов. В том случае, если сополимеры растворялись в растворителе, их высаживали из соответствующего раствора гексаном.
2.3.3 Дифференциальный термический анализ, совмещенный с термогравиметрией
Термические характеристики исходных и модифицированных полимеров оценивались с помощью дифференциально-термического (ДТА) и термогравиметрического (ТГА) анализов, совместное использование которых позволяет достаточно подробно охарактеризовать поведение полимера в условиях изменяющегося температурного поля. Термогравиметрия – метод термического анализа, при котором регистрируется изменение массы образца в зависимости от температуры.
Типичные кривые ДТА и ТГА кристаллических полимеров представлены на рисунок 2.1.
Рисунок 2.1 Типичные кривые ДТА и ТГ кристаллических полимеров
Термо- и дериватограммы образцов снимались на приборе STA 6000 (Perkin Elmer, США) с учетом релаксационного характера при скорости нагревания 3оС/мин до 500оС. Перед снятием дериватограмм все образцы подвергались отжигу в термошкафу при соответствующей температуре.
В качестве критериев термодеструкции были выбраны температура начала деструкции и температуры 5 и 50-ти %-ой потери массы [36].
2.3.4 Термомеханический анализ
Термомеханический анализ (ТМА) предназначен для определения температурной зависимости изменения линейных размеров образца (расширения, усадки, инденторного изменения поверхности) при контролируемой нагрузке и температуре. В традиционном ТМА нагрузка на образец поддерживается постоянной, а температура линейно меняется, что делает этот метод полным аналогом классической дилатометрии. Современный термомеханический анализ позволяет прикладывать различные нагрузки к образцу (постоянную, с постоянной скоростью изменения, синусоидальную и т.п.) одновременно используя простые или сложные зависимости температуры от времени. Метод термомеханического анализа очень полезен для характеристики различных материалов: он позволяет достаточно точно определить такие физические свойства материала, как точку плавления, температуру стеклования, плотность поперечных сшивок в полимерах, степень кристалличности полимеров, коэффициент термического расширения и многое другое. Температурным переходам отвечает какое-либо изменение структуры образца. Результаты анализа регистрируются в виде зависимости показателя механических свойств образца от температуры. График этой зависимости называют термомеханической кривой. Наибольшее распространение получили методы, в которых регистрируют динамический модуль сдвига образцов или деформацию сжатия [34].
Рисунок 2.2 Типичная термомеханическая кривая кристаллического полимера (при постоянной нагрузке)
Образцы диаметром 3,5 мм и толщиной 3 мм вырубали из отпрессованных пластин и подвергали нагреванию со скоростью 3С/мин. Термограммы снимались на приборе ТMA 402 Fфирмы Netzsch (Германия) при постоянной нагрузке 1Н. По термомеханическим кривым рассчитывали температуру текучести.
2.3.6 Определение твердости по Шору полимеров
Твердость по Шору один из методов измерения твердости материалов. Метод позволяет измерять глубину начального вдавливания, глубину вдавливания после заданных периодов времени или и то и другое вместе. Метод является эмпирическим испытанием. Не существует простой зависимости между твердостью, определяемой с помощью данного метода, и каким-либо фундаментальным свойством испытуемого материала.
Измеряется глубина вдавливания в материал определенного индентора под действием силы в заданных условиях.
Твердость при вдавливании обратно пропорциональна глубине вдавливания и зависит от модуля упругости и вязкоэластичных свойств материала.
Испытуемый образец помещают на твердую ровную горизонтальную поверхность. Дюрометр устанавливают в вертикальном положении так, чтобы кончик индентора находился на расстоянии не менее 12 мм от любого края образца. Как можно быстрее без толчка к образцу прижимают опорную поверхность дюрометра, держа ее параллельно поверхности испытуемого образца. К опорной поверхности с помощью специального приспособления или груза прилагают давление, достаточное для обеспечения надежного контакта с образцом. Снимают показания индикаторного устройства спустя (15 + 1) с.
2.3.7 Определение физико-механических характеристик
Испытания проводили на разрывной машине Inspect mini. Определение прочностных свойств при растяжении проводим в соответствии с ГОСТ 270-81. Образцы для испытаний, представляющие собой двухсторонние лопатки, готовили на вырубном прессе. Контактным толщиномером измерили толщину образцов в 3-х точках рабочего участка. В расчет принимается минимальное значение. Специальным штампом на образцы нанесли метки в виде белых штрихов.
Сущность метода заключается в растяжении образца и измерении значений с измерительной шкалы, с дальнейшими расчетами, которые давали значения условной прочности при растяжении, при котором происходит разрыв образца, и остаточное удлинение после разрыва [35].
2.3.8 Определение водопоглощения полимеров
Водопоглощение определяли выдерживанием полученных образцов в дистиллированной воде до прекращения изменения массы образца. Водопоглощение рассчитывалось по формуле 2.2:
В, (2.2)
где В – водопоглощение,%; – масса полимера после набухания, г;
m0 – масса полимера до набухания, г.
3 ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
В работе было изучено влияние различных концентраций ДК на анионную полимеризацию -КЛ в присутствии натриевой соли -КЛ, промышленного активатора Bruggolen С 20 Р. Для исследования свойств полученного ПКА были выбраны следующие концентрации ДК: 1 – 0 мол.%; 2 – 10-2 мол.%; 3 – 10-4 мол.%; 4 – 10-6 мол.% .
Анализ зависимости выхода ПКА от времени полимеризации показал, что ДК в начальный момент времени (в течение первых 10 мин) тормозит реакцию (рисунок 3.1). Затем скорость реакции становится сопоставимой с полимеризацией -КЛ без содержания ДК.
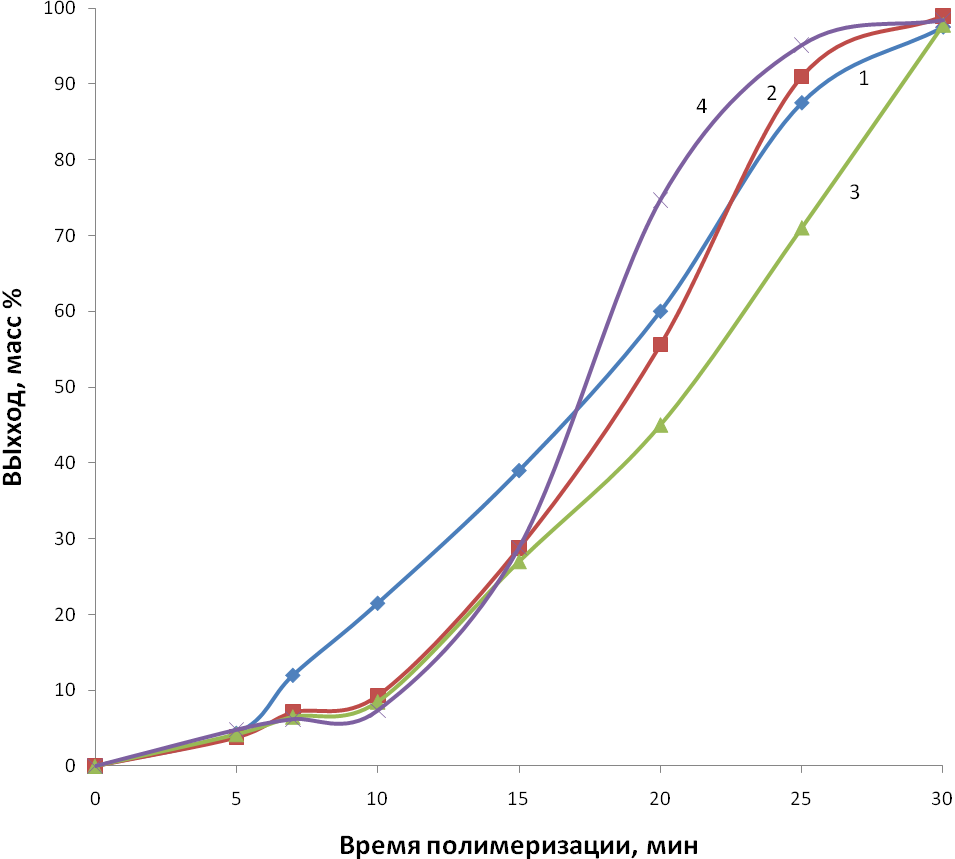
Рисунок 3.1 – Зависимость выхода полимера -КЛ от времени полимеризации при различном содержании диоксида кремния: 1 – 0 мол.%; 2 – 10-2 мол.%; 3 – 10-4 мол.%; 4 – 10-6 мол.%.
Конечный выход всех полимеров был больше 97% (таблица 3.1).
Таблица 3.1 Выход, температура начала плавления (Тн.пл), равновесная температура плавления (Т°пл), температура потерь массы (Тm)
|
Образец
|
Концентрация ДК, масс.%
|
Тн.пл, °С
|
Тпл,
°С
|
Тm=5%, °С
|
Тm=50%, °С
|
Выход, %
|
|
ПКА
|
-
|
209
|
222
|
253
|
316
|
99,1
|
|
ПКА+SiO2
|
10-2
|
207
|
218
|
283
|
369
|
99,2
|
|
ПКА+SiO2
|
10-4
|
210
|
221
|
274
|
365
|
99,1
|
|
ПКА+SiO2
|
10-6
|
204
|
218
|
207
|
343
|
97,5
|
По данным ДТА-кривых отчетливо видна равновесная температура и температура начала плавления (рисунок 3.2-3.5). Введение ДК в концентрации 10-4 – 10-2 масс.% приводит к уменьшению диффузности плавления на 3 градуса, что свидетельствует об влияние неорганического наполнителя на надмолекулярную структуру ПКА. Скорее всего ДК выступает зародышеобразователем, в результате кристаллиты ПКА получаются более однородными по размеру.
ДК в структуре ПКА также увеличивает термостабильность полученного полимера (таблица 3.1, рисунок 3.6.). Чем выше концентрация ДК, тем больше термостабилизирующий эффект.
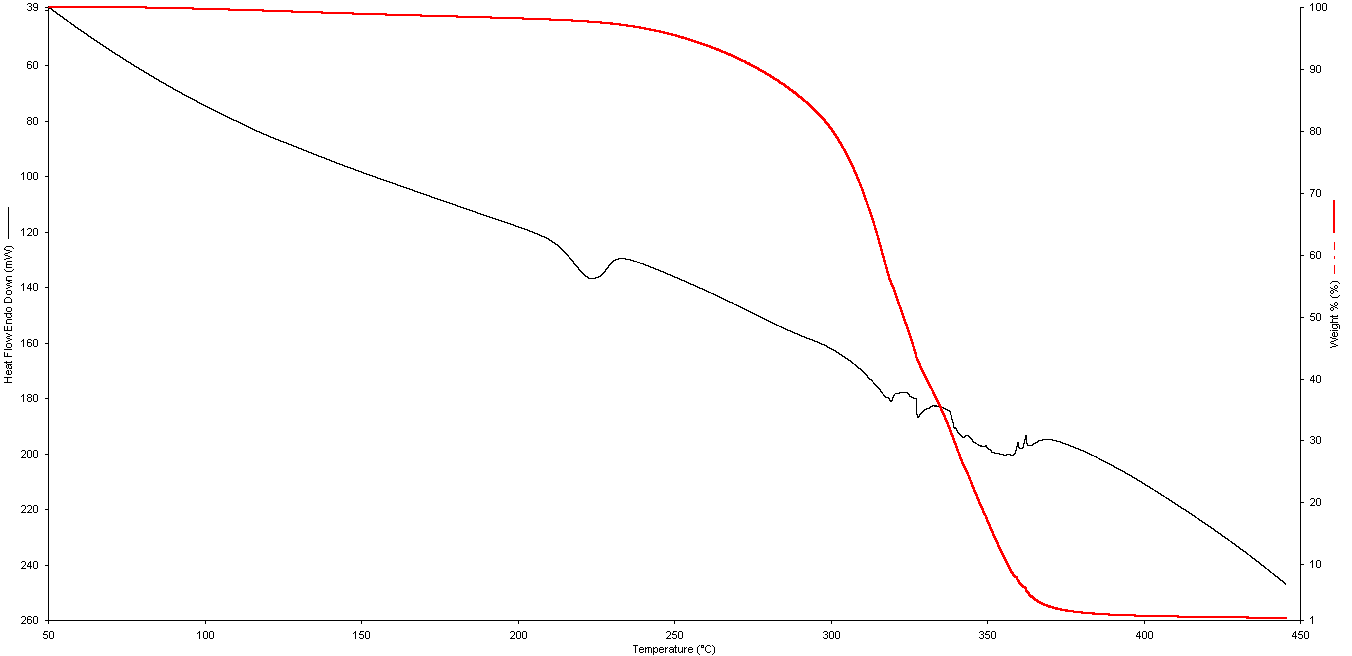
Рисунок 3.2 – ДТА и ТГА-кривые исходного ПКА
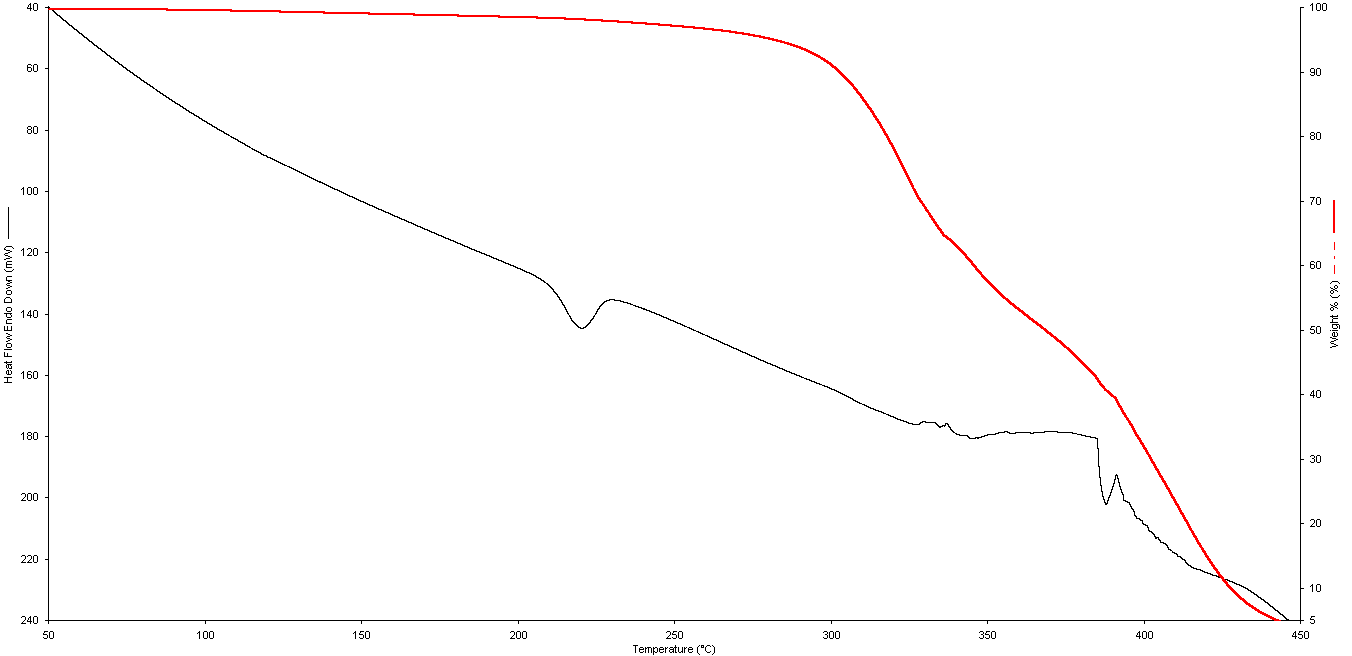
Рисунок 3.3 – ДТА и ТГА-кривые поликапроамида при содержании диоксида кремния 10-2 мол.%
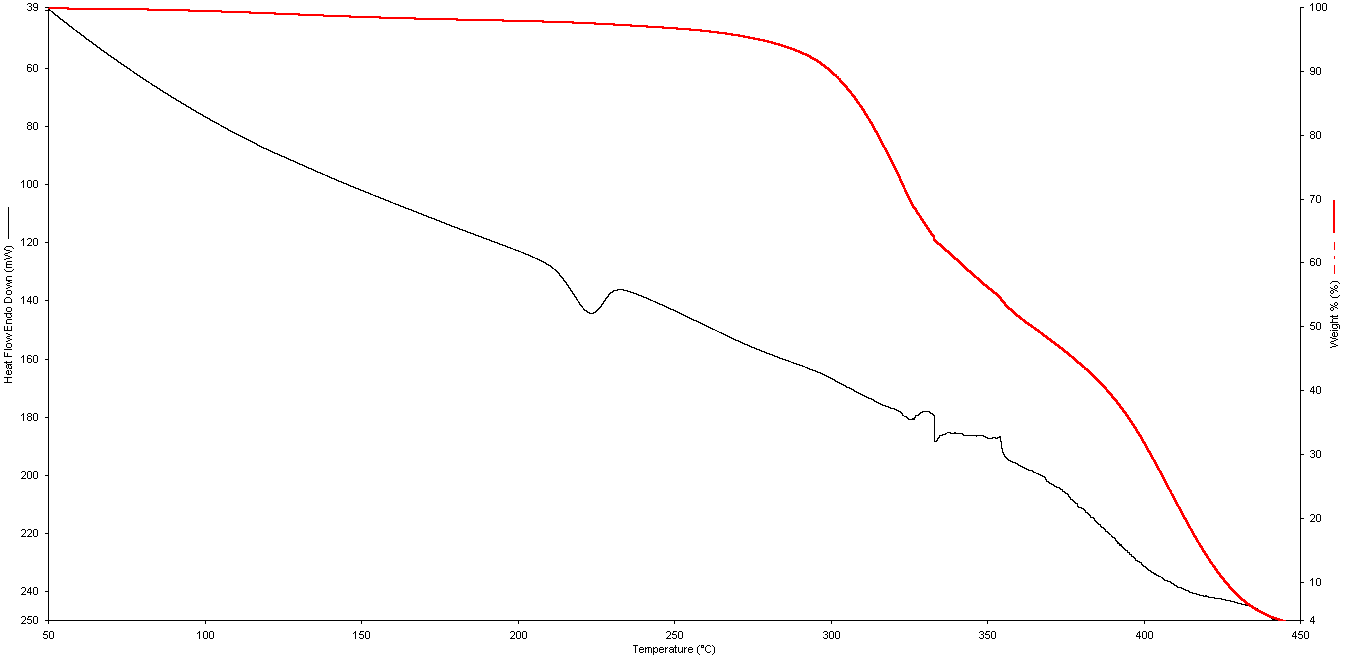
Рисунок 3.4 – ДТА и ТГА-кривые поликапроамида при содержании
диоксида кремния 10-4мол.%
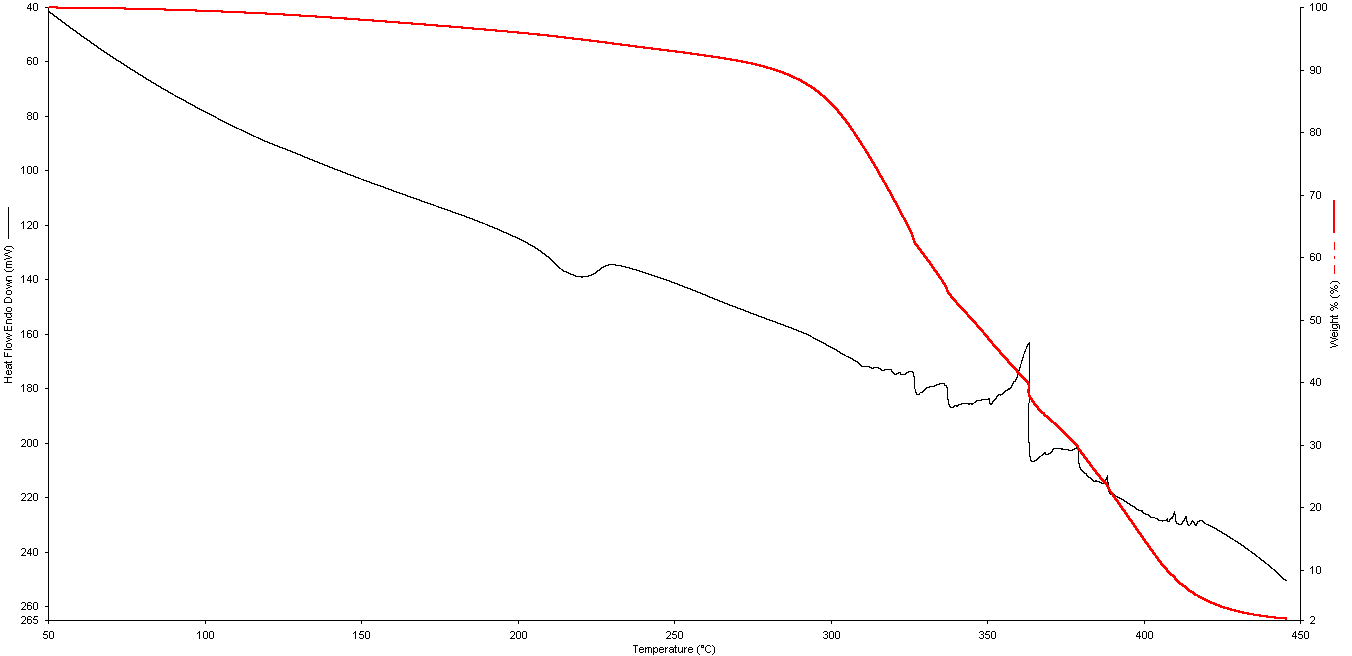
Рисунок 3.5 – ДТА и ТГА-кривые поликапроамида при содержании
диоксида кремния 10-6 мол.%
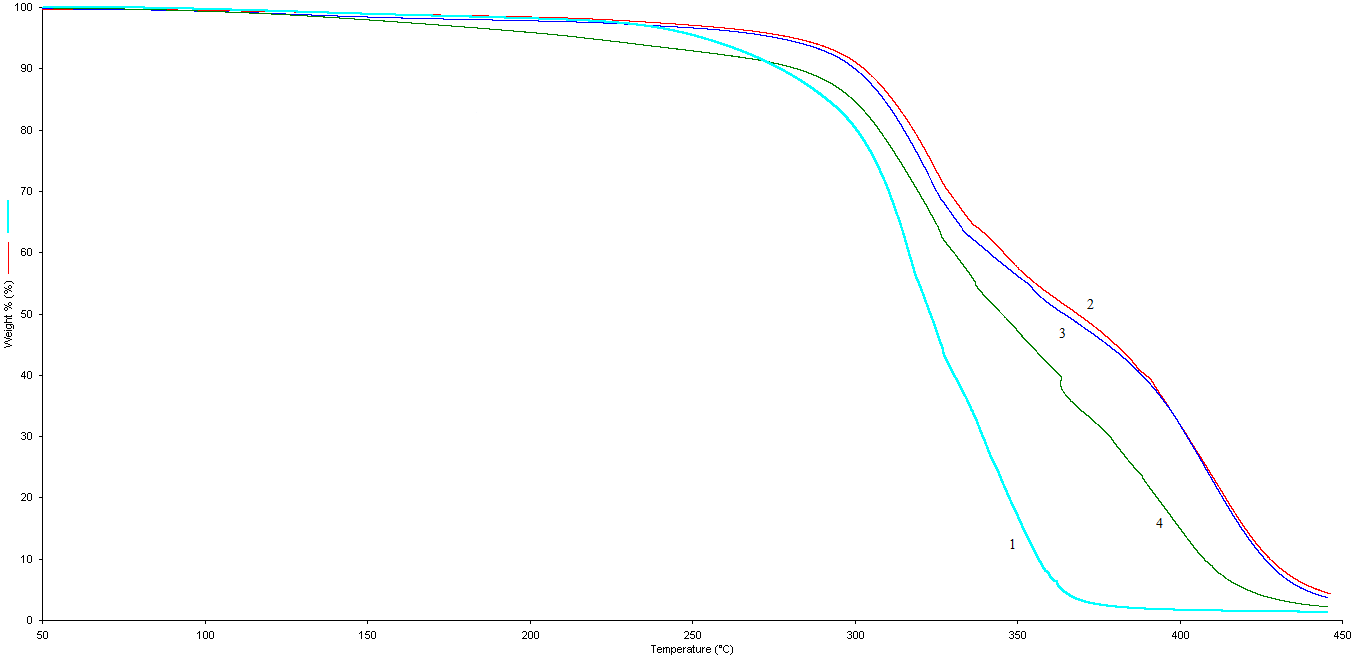
Рисунок 3.6 – ТГА-кривые поликапроамида при различном содержании диоксида кремния: 1 – 0 мол.%; 2 – 10-2 мол.%; 3 – 10-4 мол.%; 4 – 10-6 мол.%.
Изучив физико-механические свойства полученных образцов, видно что добавление ДК в полимеризацию -КЛ приводит к увеличению относительного удлинения. Также присутствие ДК повышает прочность полученного ПКА.
Таблица 3.2 – Физико-механические свойства поликапроамида, содержащего диоксид кремния
|
Образец
|
Концентрация ДК, масс.%
|
, %
|
р, МРа
|
|
ПКА (исх.)
|
-
|
180
|
30
|
|
ПКА+SiO2
|
10-2
|
173
|
56
|
|
ПКА+SiO2
|
10-4
|
198
|
54
|
|
ПКА+SiO2
|
10-6
|
228
|
51
|
Введение ДК в полимеризацию -КЛ не оказывает существенного влияния на показатели водопоглощения полученного ПКА (таблица 3.3) и на твердость образцов (таблица 3.4).
Таблица 3.3 – Водополгощение полимеров -КЛ с добавлением диоксида кремния
|
Образец
|
Концентрация ДК, масс.%
|
Водопоглощение, %
|
|
ПКА
|
-
|
5,8
|
|
ПКА+SiO2
|
10-2
|
5,9
|
|
ПКА+SiO2
|
10-4
|
6,0
|
|
ПКА+SiO2
|
10-6
|
5,9
|
Таблица 3.4 – Твердость по Шору полимера -КЛ с добавлением диоксида кремния.
|
Образец
|
Концентрация ДК, масс.%
|
Твердость по Шору D,%
|
|
ПКА
|
-
|
73
|
|
ПКА+ SiO2
|
10-2
|
73
|
|
ПКА+ SiO2
|
10-4
|
74
|
|
ПКА+ SiO2
|
10-6
|
75
|
ВЫВОДЫ
1. Литературный обзор показал, что диоксид кремния применяется для загущения, придания тиксотропных свойств жидкостям и активного наполнения каучуков и герметиков. Служит наполнителем, существенно улучшающим физико-механические, диэлектрические свойства материалов (твёрдость, упругость, прочность на разрыв, прочность к стиранию, термическую стойкость и др.). Выполняет функцию стабилизатора, выступает в качестве антиседиментационной добавки многокомпонентных систем.
2. Проведение полимеризации -капролактама в присутствии диоксида кремния показало, что данное соединение замедляет скорость полимеризации ПКА в начальный период времени, затем скорость реакции становится сопоставимой с полимеризацией -капролактама без содержания диоксида кремния.
3. Изучение влияния диоксида кремния на полимеризацию -капролактама показало, что введение диоксида кремния позволяет увеличить термостойкость, повысить физико-механические свойства полимера. При этом диоксид кремния не оказывает существенного влияния на показатели водопоглощения и твердость полученного поликапроамида.
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1. Энциклопедия полимеров: в 3 т. Т.2. В. А. Кабанов (глав. ред. ) - М.: Советская энциклопедия, 1977. – 1454 с.
2. Нельсон У.Е. Технология пластмасс на основе полиамидов: пер. с англ./под ред. А.Я. Малкина. – М.: Химия, 1979.-256 с.
3. Ю. Д. Семчиков. Высокомолекулярные соединения: Учеб. для вузов. – М.: «Академия», 2005. – с. 256 – 263.
4. В.В. Киреев. Высокомолекулярные соединения. М.Высшая школа, 1992.
5. Полиамиды [Электронный ресурс] Режим доступа: http://www.xumuk.ru/bse/2117.html
6. Полиамид – сайт РустХим [Электронный ресурс] Режим доступа: http://poliamid.ru/
7. Вольф Л.А. Производство поликапроамида / Л.А.Вольф, Б.Ш. Хайтин.– М.: Химия, 1977. - 207 c.
8. Поликапроамид [Электронный ресурс] Режим доступа: http://www.xumuk.ru/bse/2133.html
9. Роговин З.А. Основы химии и технологии химических волокон / З.А.Роговин. – В 2-х томах. – М.: Химия, 1974. – Т. 2. –344 с.
10. В.Р.Говарикер, Н.В.Висванатхан, Дж.Шридхар. Полимеры. М. Наука, 1990.
11. Химические основы аниооной полимеризации [Электронный ресурс] Режим доступа: http://msd.com.ua/texnologiya-plastmass-na-osnove-poliamidov/ximicheskie-osnovy-anionnoj-polimerizacii/
12. Энциклопедия полимеров В.А. Каргин, М.С. Акутин.
13. Активные центры и некоторые особенности анионной полимеризации -капролактама, инициируемой лактаматами магния / В. А. Котельников, В. В.Курашев, Л. Б. Данилевская, И. О. Конова, В. В. Гавриленко, Л. А. Чекулаева, И. А. Гарбузова, И. Е. Персии // ВМС. – 1992. – Сер. А. – Т. 34. – № 1. – С. 69–76.
14. Odian, G. Principles of polymerization / G. Odian. Hoboken. New Jersey, 2004.
15. / В. А. Котельников, Л. Б. Данилевская, В. В. Курашев, М. Н. Ильина, В. С. Папков, В. В. Гавриленко, Л. А. Чекулаева / Влияние природы катализатора анионной полимеризации лактамов на термостабильность образующихся полиамидов / В. А. Котельников, Л. Б. Данилевская, В. В. Курашев, М. Н. Ильина, В. С. Папков, В. В. Гавриленко, Л. А. Чекулаева // ВМС. – 1993. – Сер. А. – Т. 35. – № 8. – С. 1257–1261.
16. Синтез капролактаматов металлов II группы / Л. А. Чекулаева, В. В. Гавриленко, Т. Ю. Васильева, Л. Б. Данилевская, В. А. Котельников // Изв. АН. – 1995. – Сер. Хим. – № 11. – С. 2272–2275.
17. / Т. М. Фрунзе, С. П. Давтян, В. А. Котельников, Т. В. Волкова, В. В. Курашев, И. В. Станкевич К вопросу об активных центрах в анионной активированной полимеризации -капролактама / Т. М. Фрунзе, С. П. Давтян, В. А. Котельников, Т. В. Волкова, В. В. Курашев, И. В. Станкевич // Acta Polymerica. – 1981. – Т. 32. – № 1. – С. 31–34.
18. Природа противоиона в анионной полимеризации -капролактама / В. В. Коршак, В. А. Котельников, Ю. А. Авакян, В. В. Курашев, Т. М. Фрунзе, С. П. Давтян // Докл. АН СССР. – 1982. – Т. 266. – № 4. – С. 896–899.
19 Кинетика анионной полимеризации -капролактама, инициируемой лактаматами щелочных металлов / В. А. Котельников, Л. Б. Данилевская, Ю. А. Авакян, И. Е. Персиц, Н. Н. Сурин // ВМС. – 1994. – Сер. А. – Т. 36. – № 12. – С. 1965–1971
20. Шварц, М. Анионная полимеризация. Карбанионы, живущие полимеры и процессы с переносом электрона / М. Шварц. – М: Мир, 1971. – 669 с.
21. Синтез и некоторые свойства поликапроамида, образующегося в присутствие трехмерных активаторов / В. В. Курашев, Р. Б. Шлейфман, С. В. Цуцуран, В. А. Котельникова, А. А. Аскадский // Докл. АН СССР. – 1989. – Т. 307. – № 1. – С. 121–124.
22. Puffr, R. Anionic polymerization of -caprolactam. Catalysis by potassium-graphite intercalate / R. Puffr, N. Vladimirov // Macromol. Chem. – 1993. – Vol. 194. – № 6. – P. 1765–1771.
23. «Активаторы анионной полимеризации лактамов» Т. М. Фрунзе , В. В. Курашев, В. А. Котельников,Т. В. Волкова
24. « Химия кремнезема» Айлер Р. перевод с английского, т. 1-2, М., 1982
25. «Химия кремния. Учебное пособие» И.С. Белостоцкая
26.«Моделирование поведения огнестойких эластомерных материалов с микродисперсным карбидом кремния при воздействии высокотемпературных тепловых потоков» Лифанов В.С., Каблов В.Ф., Новопольцева О.М., Кочетков В.Г.
27.«Общая химия» Н. Л. Глинка
28. Аэросил [Электронный ресурс] Режим доступа: http://www.science-techno.ru/nt/article/aerosil/page/1
29. Оксид кремния (4) – образовательный портал по химии [Электронный ресурс] Режим доступа: http://himege.ru/oksid-kremniya
30. Пат 2346784 Российская Федерация «Полимерная композиция для изготовления оправки»/ Шайдурова Г. И., Лузенин А. Ю., Жукова Ю. С./ Патентообладатель: Открытое акционерное общество Научно-производственное объединение «Искра» (RU)
31.«Химическая энциклопедия» И.Л.Кнунянц. Том 2.
32. Артеменко А.И Справочное руководство по химии /А.И.Артеменко, И.В Тикунова. �– М.: Высшая школа, 2003.– 323 с.
33. Физико-механические методы анализа. Под ред. У. Мзэоиа. М., Издат. 1962, т. 1, ч. А, 592 с; М., «Мир», 1969, т. 2, ч. Б, 420 с.
34. Перепечко И.И.Методы исследования полимеров. М.,«Химия», 1973. 296с.
35. Шнуров В.Н. Крашение пластмасс /В.Н. Шнуров. – Л.: Химия, 1980. – 319с.
Влияния диоксида кремния на анионную полимеризацию -КЛ в присутствии натриевой соли -КЛ, промышленного активатора, а также изучить свойства полученного ПКА