Молекулярно-кинетическая теория (МКТ) идеального газа
Введение
В первой части издания представлены шесть лекций, посвященных раскрытию физического смысла основных законов и понятий механики.
Вторая часть продолжает курс лекций по физике и содержит девять лекций по молекулярной физике и термодинамике.
Предметом изучения молекулярной физики является движение больших совокупностей молекул. При изучении используются статистиче�ский и термодинамический методы.
Молекулярная физика исходит из представлений о молекулярном строении вещества. Поскольку число частиц в макросистеме велико, зако�номерности в ней имеют статистический, т.е. вероятностный, характер. На основе определенных моделей молекулярная физика позволяет объяс�нить наблюдаемые свойства макросистем (систем, состоящих из очень большого числа частиц) как суммарный эффект действий отдельных мо�лекул. При этом используется статистический метод, в котором нас инте�ресуют не действия отдельных молекул, а средние значения определенных величин.
В термодинамике используют понятия и физические величины, от�носящиеся к системе в целом, например, объем, давление и температура. Термодинамика основана на общих принципах, или началах, которые представляют собой обобщение опытных фактов.
Термодинамический и статистический методы изучения макросис�тем дополняют друг друга. Термодинамический метод позволяет изучать явления без знания их внутренних механизмов. Статистический метод по�зволяет понять суть явлений, установить связь поведения системы в целом с поведением и свойствами отдельных частиц.
Цель автора, как и в первой части представленного издания, - сде�лать для начинающего студента фактически доступными основные поня�тия и закономерности молекулярной физики, порой весьма непростые. Студенту нужно не «зазубривать» материал, а постараться понять, раз�мышлять, проверить себя по вопросам для самоконтроля после каждой лекции, а также прорешать соответствующие задачи, например из пособия [9]. Максимальное внимание должно быть уделено физическому смыслу изучаемого материала.
ВНИМАНИЕ! ПРЕДЛАГАЕМОЕ ИЗДАНИЕ ОБЛЕГЧАЕТ РАБОТУ СТУДЕНТА, НО НЕ ЗАМЕНЯЕТ САМИ ЛЕКЦИИ В АУДИТОРИИ!
МОЛЕКУЛЯНАЯ ФИЗИКА
Лекция №7
Молекулярно-кинетическая теория (МКТ)
идеального газа
План
- Понятие идеального газа. Молекулярно-кинетическое толкование температуры. Макроскопические параметры системы.
- Число степеней свободы. Закон равнораспределение энергии. Внутренняя энергия идеального газа.
- Давление газа с точки зрения молекулярно-кинетической теории идеального газа (основное уравнение молекулярно-кинетической теории).
- Уравнение состояния идеального газа (уравнение Клапейрона-Менделеева).
1. Понятие идеального газа.
Идеальным называется газ, взаимодействие, между молекулами которого пренебрежимо мало и состояние которого описывается уравнением Клапейрона-Менделеева.
Модель идеального газа.
1. Собственный объём молекул газа пренебрежимо мал по сравнению с объёмом сосуда.
2. Между молекулами газа отсутствует силы взаимодействия.
3. Столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
Взаимодействие между молекулами всякого газа становится пренебрежимо слабым при малых плотностях газа, при большом разрежении. Такие газы как воздух, азот, кислород, даже при обычных условиях, т.е. при комнатной температуре и атмосферном давлении мало отличаются от идеального газа. Особенно близки к идеальному газу гелий и водород.
Не следует думать, что взаимодействие между молекулами идеального газа вовсе отсутствует. Напротив, его молекулы сталкиваются друг с другом и эти столкновения существенны для установления определённых тепловых свойств газа. Но столкновения проходят настолько редко, что большую часть времени молекулы движутся как свободные частицы.
Именно столкновения между молекулами позволяют ввести такой параметр как температура. Температура тела характеризует энергию, с которой движутся его молекулы. Для идеального газа в равновесных условиях абсолютная температура пропорциональна средней энергии поступательного движения молекул.
Определение. Макроскопической называется система, образованная огромным числом частиц (молекул, атомов). Параметры, характеризующие поведение системы (например, газа), как целого, называется макропараметрами. Например, давление Р, объём V и температура Т газа – макропараметры.
Параметры, характеризующие поведение отдельных молекул (скорость, масса и т.п.) называется микропараметрами.
2. Число степеней свободы.
Определение. Числом степеней свободы механической системы называется количество независимых величин, с помощью которых может быть задано положение системы в пространстве.
а) Так, положение в пространстве материальной точки полностью определяется заданием трёх её координат (например, декартовых x, y, z или сферических , т.е. число степеней свободы i=3).
б) Система из 2-х жёстко связанных материальных точек (отрезок, их соединяющий, фиксирован ). Координаты этих 2-х точек связаны соотношением , при этом достаточно задать 5 координат, а шестую можно найти из приведённого соотношения, т.е. i=5. Если точки не связаны между собой жёстко, то число степеней свободы i=6. Изменение даёт ещё одну степень свободы, которая называется колебательной.
Положение системы, состоящей из 2-х жёстко связанных материальных точек (или, например, стержня) можно задать следующим образом: задать 3 координаты центра инерции системы С и 2 угла и , которыми определяется направление в пространстве оси системы (Рис. 7.1).
|
|
Первые три степени свободы называется поступательными, а две другие – вращательными. Вращательные степени свободы соответствуют вращению вокруг 2-х взаимно перпендикулярных осей (всего i =5).
в) Положение абсолютно твёрдого тела можно определить, задав 3 координаты центра инерции (поступательные степени свободы) и 3 угла (вращательные степени свободы). Т.е.i=6
|
|
Рис. 7.1
|
|
Закон равнораспределения энергии
В классической статической физике выводится закон Больцмана о равномерном распределении энергии по степеням свободы молекул: на каждую степень свободы молекулы приходится в среднем одинаковая кинетическая энергия, равная кТ. Необходимо отметить, что поступательное и вращательное движения связаны только с кинетической энергией, в то время как колебательное движение связано с наличием и кинетической и потенциальной энергий, причём среднее значение потенциальной и кинетической энергии оказывается одинаковым. Поэтому на каждую колебательную степень свободы приходится в среднем две половинки кТ. Средняя энергия молекулы должна равняться:
где (постоянная Больцмана); здесь i – сумма числа поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекул:
Для молекул с жёсткой связью между атомами i совпадает с числом степеней свободы молекулы.
Внутренняя энергия идеального газа
Определение. Внутренней энергией какого-либо тела называется энергия этого тела за вычетом кинетической энергии тела как целого и потенциальной энергии тела во внешнем поле сил. Она является функцией внутреннего состояния системы. Для идеального газа внутренняя энергия состоит из суммы энергий поступательного, вращательного и колебательного движений молекул. (Заметим, что в общем случае во внутреннюю энергию входят энергия взаимодействия атомов, энергия электронных оболочек, внутриядерная энергия и др.). Внутреннюю энергию одного моля идеального газа найдём, умножив число Авогадро на среднюю энергию одной молекулы:
Учитывая, что , получим:
т.е. внутренняя энергия идеального газа является функцией температуры и пропорциональна ей, а также зависит от числа степеней свободы молекул. То, что внутренняя энергия является функцией состояния системы, означает, что всякий раз, когда система оказывается в данном состоянии, ее внутренняя энергия принимает присущее этому состоянию значение, независимо от предыстории системы. Следовательно, изменение внутренней энергии при переходе системы из одного состояния в другое будет всегда равно разности значений внутренней энергии в этих состояниях, независимо от пути, по которому совершался переход.
Свяжем внутреннюю энергию с теплоёмкостью. По определению теплоёмкость в процессе при постоянном объёме , для идеального газа
Соответственно
3. Основное уравнение молекулярно-кинетической теории.
Постановка задачи. Требуется получить связь между макропараметрами – давлением P, температурой T, с микропараметрами – массой молекулы m, её скоростью и концентрацией молекул n.
Пусть имеется некоторый сосуд с газом. Будем считать, что молекулы могут двигаться вдоль осей x, y, z. Выберем на стенке сосуда участок поверхности (Рис. 7.2). Если в сосуде N молекул, то вследствие равновероятности этих направлений вдоль каждой оси будет двигаться
|
|
молекул. Половина из них движется вдоль данного направления, т.е.
(ось имеет два направления).
Предположим, что все молекулы движутся с одинаковой скоростью, равной . Тогда за время до элемента стенки долетят молекулы, заключённые в объёме параллелепипеда с основанием и высотой . Число этих молекул равно
|
|
Рис. 7.2
|
|
произведению плотности молекул (где объём сосуда) на объём , т.е. число молекул, летящих к площади
(1)
По закону сохранения импульса каждая молекула при ударе о стенку передаёт ей импульс (удар считается упругим), равный изменению импульса молекулы (Рис. 7.3, а, б).
. (2)
По 2-му закону Ньютона:
, (3)
где сила, действующая со стороны молекулы на стенку; длительность взаимодействия молекулы со стенкой.
Для всех молекул, находящихся в параллелепипеде:
|
|
, где
средняя сила, с которой молекулы действуют на стенку . Учитывая соотношение (3):
,
подставляя (1) и (2) в последнее соотношение, получим:
|
|
рис. 7.3
|
|
.
Поделив правую и левую части на , учитывая, что
по определению давления и производя необходимые сокращения, получим или .
Если в выводе учесть, что скорости отдельных молекул могут быть различными, то величину следует заменить средней величиной квадрата скорости .
А так как средняя энергия поступательного движения молекулы
,
то
|
|
Основное уравнение молекулярно-кинетической теории.
|
Физический смысл уравнения: давление, оказываемое газом на стенки сосуда прямо пропорциональна числу молекул в единице объёма и средней кинетической энергии поступательного движения одной молекулы.
4. Уравнение состояния идеального газа Клапейрона-Менделеева
(Клапейрон (1799 – 1864) – французский физик и инженер; Менделеев Дмитрий Иванович (1834 – 1907) – великий русский учёный). Опыт даёт, что при небольших плотностях газы подчиняются уравнению (Клапейрона):
.
В соответствии с законом Авогадро моли всех газов занимают при одинаковых условиях одинаковый объём.
Отсюда const будет одинакова для всех газов, если количество равно 1 молю. Обозначив const=R, получим (Менделеев):
Уравнение состояния идеального газа для одного моля, где газовая постоянная , а - объем 1 моля газа.
Если у нас имеется молей, то объём будет , , подставим в уравнение состояния для 1-го моля:
или .
Количество вещества можно представить в виде отношения массы газа m к молярной массе газа М и окончательно уравнение состояния идеального газа (уравнение Клапейрона-Менделеева) для массы газа m:
(4)
Следствие из уравнения Клапейрона-Менделеева. Газовую постоянную выразим как . Произведение , тогда . Разделим обе части последнего уравнения на V и, учитывая, что
концентрация молекул, получим
(5)
Оба уравнения (4) и (5) представляют различные формы записи уравнения состояния идеального газа. Это уравнение позволяет достаточно просто оценить параметры газа, если его можно считать идеальным.
Вопросы для самоконтроля.
- Какой газ называется идеальным? Опишите модель идеального газа.
- Что называется числом степеней свободы механической системы i?
- Чему равно число i для одноатомной и многоатомной молекул? Обоснуйте свой ответ.
- Что утверждает закон равнораспределения?
- Как зависит внутренняя энергия идеального газа от его абсолютной температуры?
- Как объясняют давление газа в МКТ?
- Запишите основное уравнение молекулярно-кинетической теории. Что называют микро- и макропараметрами системы?
- Проделайте вывод основного уравнения МКТ.
- Что позволяет рассчитать уравнение состояния идеального газа Клапейрона-Менделеева?
Лекция №8
Элементы классической статистики
(статистической физики)
План
- Статистический метод исследования системы. Понятие функции распределения. Статистическое усреднение.
- Фазовое пространство, фазовая точка, фазовая ячейка. Распределение Максвелла (распределение молекул по абсолютным значениям скорости). Средние скорости молекул.
- Барометрическая формула. Распределение Больцмана.
- Распределение Больцмана для дискретных уровней энергии.
- Статистика Максвелла-Больцмана.
1. Статистический метод исследования системы. Понятие функции распределения.
Цель молекулярно-кинетической теории – истолковать свойства тел, которые непосредственно наблюдаются на опыте (давление, температура и т.п.) как суммарный результат действия молекул. При этом используется статистический метод, при котором учитывается не движение отдельных молекул, а средние величины, характеризующие движение огромной совокупности частиц. В статистической физике рассматривается конкретная молекулярная модель и к ней применяются математические методы статистики, основанной на теории вероятности.
Понятие о функции распределения.
Пусть имеется некоторая система из большого числа микрочастиц. Предположим, что какая-то характерная для системы величина Х, может иметь дискретные значения . Осуществим над системой очень большое число N измерений величины Х. Допустим, что измерений дали результат , измерений результат , результат .
Отношение называется относительной частотой появления результата .
Вероятность появления результата называется величина:
Так как на практике N всегда конечно, то для вычисления вероятности стараются, чтобы N и были достаточно большими. Тогда можно считать, что
(Заметим, что вероятность случайного события есть количественная мера ожидаемой возможности его появления).
Рассмотрим случай, когда случайная величина Х имеет непрерывный характер (например, скорости молекул). Для этого разобьём всю область измерения Х на отдельные интервалы и будем считать число попаданий случайной величины в тот или иной интервал. Возьмём малую величину и найдём число измерений при которых , измерений при ….., измерений при которых результат измерений находится в интервале от х до х+а (). Вероятность того, что результат измерений окажется в интервале от 0 до а обозначим , от а до 2а соответственно от х до х+а
Начертим ось х и отложим вверх полоски высотой (рис. 8.1)
|
|
Полученная столбчатая диаграмма называется гистограммой.
Площадь всей гистограммы равна 1.
(т.к. ).
В пределе при ступенчатая линия, ограничивающая гистограмму, превратится в гладкую кривую (рис. 8.2).
|
|
Рис. 8.1
|
|
|
|
Или, учитывая (1)
|
|
(2)
|
|
|
Функция f(x) имеет смысл плотности вероятности распределения частиц по х. Вероятность того, что результат измерения окажется в пределах от х до x+dx:
(Площадь)
Вероятность того, что величина х попадёт в интервал (a,b):
|
|
Рис. 8.2
|
|
|
|
Вероятность того, что величина х может принять хотя бы какое-нибудь значение (вероятность достоверного события), равна единице:
Это условие называется условием нормировки. Интегрирование производится по всему интервалу возможных значений величины х. Из этого условия следует, что вся площадь под кривой f(x) равна единице.
Смысл условия нормировки легко понять на примере бросания монеты. Сумма вероятностей выпадения «орла» или «решки» (при достаточно большом числе опытов) . Аналогично для игрального кубика сумма вероятностей того, что выпадет 1, или 2, или 3…. .
Статистическое усреднение
Зная функцию распределения f(x), можно найти среднее значение результатов измерения величины х. Из N измерений в случаях (из **):
Получается результат, равный х. Сумма таких результатов . Сумма всех возможных результатов:
(в левой части фактически стоит сумма х). Разделив обе части на N, получим среднее значение величины х:
|
|
Формула статистического усреднения
|
Т.е. для определения среднего х необходимо знать функцию распределения f(x). Интегрирование проводится по интересующему нас интервалу значений х.
2. Фазовое пространство, фазовая точка, фазовая ячейка
Введём воображаемое шестимерное пространство, каждая точка которого характеризуется шестью координатами x, y, z, , , , где x, y, z – координаты, , , – соответствующие им проекции импульсов каждой молекулы. Такое пространство называется фазовым пространством молекул, а его точки – фазовыми точками.
Таким образом, мгновенное состояние отдельной молекулы полностью характеризуется положением её фазовой точки в фазовом пространстве.
Разобьём теперь всё фазовое пространство молекул на достаточно малые области с одинаковыми фазовыми объёмами. Такие области называются фазовыми ячейками (например, фазовая ячёйка может иметь форму бесконечно малого шестимерного прямоугольного параллелепипеда и иметь объём ).
Примем произвольную точку пространства О за начало координат. Отложим от неё в какой-то момент времени t векторы скоростей всех молекул газа: (рис. 8.3).
|
|
Концы этих векторов называются скоростными точками. Совокупность всех скоростных точек образуют 3-х мерное пространство, называемое пространством скоростей. Пространство скоростей является частным случаем фазового пространства. В пространстве скоростей можно ввести прямоугольные оси, по которым можно откладывать проекции , , вектора на эти оси.
|
|
Рис. 8.3
|
|
Распределение Максвелла (английский физик 1831-1879).
Скорости каждой молекулы в пространстве скоростей соответствует точка. Распределение этих точек в пространстве характеризует распределение молекул по скоростям. Вследствие равноправности всех
направлений движения, расположение точек относительно начала координат будет сферически симметричным. (Рис. 8.4). Плотность точек в пространстве будет зависеть только от модуля скорости . Для скоростей, лежащих в пределах от до +d соответствующий объём в пространстве (объём сферического слоя). Число точек, находящихся в этом слое (каждая точка соответствует скорости отдельной молекулы) , где плотность точек в пространстве (подобно тому, как из выражения (2) следует). Смысл далее.
Смысл функции распределения Максвелла. – это число молекул, величина скоростей которых лежит в интервале от до +d. Разделим выражение для на N, тогда получим вероятность того, что скорость молекулы окажется в пределах от до +d.
, где имеет смысл объёмной плотности вероятности распределения скоростных точек в пространстве скоростей.
Обозначим функцию распределения молекул газа по скоростям. Вид функции F() был установлен теоретически Максвеллом. Опуская вывод (желающие могут ознакомиться с ним, например в [1] ) приведём окончательный результат:
Где m – масса молекулы, k – постоянная Больцмана, T – абсолютная температура газа, – скорость молекулы. F() показывает, какая относительная доля молекул имеет скорость в интервале от до +d (). Функция F() образована произведением функций вида и (Рис. 8.5). Функция F() нормирована на 1.
Средние скорости молекул
Найдём наиболее вероятную скорость, соответствующую максимуму функции распределения. Эта скорость определяется из условия
, т.е.
Проведя дифференцирование произведения функций, получим
Средняя скорость молекул (имеется в виду средняя арифметическая скорость) по определению из формулы статического усреднения
Средняя скорость входит в коэффициенты диффузии, вязкости, теплопроводности и, соответственно используется в расчётах этих процессов.
Среднеквадратичная скорость ;
, откуда
Эта скорость входит в основное уравнение молекулярно-кинетической теории. Качественно положение характерных (средних) скоростей показано на рис. 8.6
|
|
Проанализируем, как будет меняться ход кривой при изменении температуры газа. При увеличении температуры (или уменьшении массы молекулы) максимум кривой смещается вправо (из ) и становится ниже (площадь под кривой остаётся неизменной) (Рис. 8.7)
|
|
Рис. 8.6
|
|
|
|
|
Рис. 8.7
|
3. Барометрическая формула.
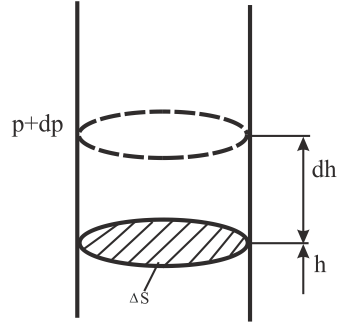
Атмосферное давление на высоте h обусловлено весом вышележащих слоёв газа. Давление на высоте h+dh будет P+dP (dh>0, dP<0, т.к. вес и давление с высотой убывают).
Разность давлений P и P+dP обусловлена весом газа, заключённого в объёме цилиндра, с площадью основания, равной и высотой dh (Рис. 8.8).
|
|
,
где – плотность газа на высоте , отсюда
(*)
При нормальных условиях воздух можно считать идеальным газом. Тогда
можно найти из уравнения состояния идеального газа , здесь
|
|
Рис. 8.8
|
|
М – средняя масса моля воздуха. Плотность , подставим в (*), получим
. Поделим обе части на Р: . Возьмём интеграл от левой и правой частей:
.
Предел давление на уровне h=0. Для случая, когда температура постоянная (изотермическая атмосфера), интегрируя, получим:
, отсюда получаем барометрическую формулу.
|
|
|
|
Графическая иллюстрация этой формулы на рис. 8.9 Давление убывает с высотой тем быстрее, чем тяжелее газ и чем ниже температура.
|
|
Рис. 8.9
|
|
Распределение Больцмана
В барометрической формуле в отношении M/R разделим и числитель и знаменатель на число Авогадро .
, где
масса одной молекулы,
постоянная Больцмана.
Вместо Р и подставим соответственно. (см. лекцию №7), где плотность молекул на высоте h, плотность молекул на высоте .
Из барометрической формулы в результате подстановок и сокращений получим распределение концентрации молекул по высоте в поле силы тяжести Земли.
Из этой формулы следует, что с понижением температуры число частиц на высотах, отличных от нуля, убывает (рис. 8.10), обращаясь в 0 при Т=0 (при абсолютном нуле все молекулы расположились бы на поверхности Земли). При высоких температурах n слабо убывает с высотой, так
|
|
что молекулы оказываются распределёнными по высоте почти равномерно. Распределение молекул по высоте является результатом конкуренции между притяжением молекул к Земле и тепловым движением, стремящимся разбросать молекулы по всем высотам. На разной высоте молекула обладает различным запасом потенциальной энергии
|
|
Рис. 8.10
|
|
.Следовательно, распределение молекул по высоте является и распределением их по значениям потенциальной энергии.
где плотность молекул в том месте пространства, где потенциальная энергия молекулы имеет значение ; плотность молекул в том месте, где потенциальная энергия равна 0.
Больцман доказал, что распределение (*) справедливо не только в случае потенциального поля сил земного тяготения, но и в любом потенциальном поле сил для совокупности любых одинаковых частиц, находящихся в состоянии хаотического теплового движения.
Таким образом, закон Больцмана (*) даёт распределение частиц, находящихся в состоянии хаотического теплового движения, по значениям потенциальной энергии. (рис. 8.11)
- Распределение Больцмана при дискретных уровнях энергии.
Полученное Больцманом распределение относится к случаям, когда молекулы находятся во внешнем поле и их потенциальная энергия может применяться непрерывно. Больцман обобщил полученный им закон на случай распределения, зависящего от внутренней энергии молекулы.
Известно, что величина внутренней энергии молекулы (или атома) Е может принимать лишь дискретный ряд дозволенных значений . В этом случае распределение Больцмана имеет вид:
,
где число частиц в состоянии с энергией ;
коэффициент пропорциональности, который удовлетворяет условию
,
где N – полное число частиц в рассматриваемой системе.
Тогда и в результате для случая дискретных значений энергии распределение Больцмана
|
|
Качественная иллюстрация этого распределения представлена на рис. 8.12. Это распределение характерно для состояния термодинамического равновесия.
Заметим, что в активных средах лазеров населённость уровней с большим значением энергии может быть выше, чем с меньшим. Это так называемая инверсная населённость уровней.
|
|
Рис. 8.12
|
|
Но состояние системы в этом случае термодинамически неравновесное.
- Статистика Максвелла-Больцмана
Распределение Максвелла и Больцмана можно объединить в один закон Максвелла-Больцмана, согласно которому число молекул, компоненты скорости которых лежат в пределах от до , а координаты в пределах от x, y, z до x+dx, y+dy, z+dz, равно
где , плотность молекул в том месте пространства, где ; ; ; полная механическая энергия частицы.
Распределение Максвелла-Больцмана устанавливает распределение молекул газа по координатам и скоростям при наличии произвольного потенциального силового поля.
Примечание: распределение Максвелла и Больцмана являются составными частями единого распределения, называемого распределением Гиббса (этот вопрос подробно рассматривается в спецкурсах по статической физике, и мы ограничимся только упоминанием этого факта).
Вопросы для самоконтроля.
- Дайте определение вероятности.
- Каков смысл функции распределения?
- Каков смысл условия нормировки?
- Запишите формулу для определения среднего значения результатов измерения величины x с помощью функции распределения.
- Что представляет собой распределение Максвелла?
- Что такое функция распределения Максвелла? Каков ее физический смысл?
- Постройте график функции распределения Максвелла и укажите характерные особенности этой функции.
- Укажите на графике наиболее вероятную скорость . Получите выражение для . Как изменяется график при повышении температуры?
- Получите барометрическую формулу. Что она определяет?
- Получите зависимость концентрации молекул газа в поле силы тяжести от высоты.
- Запишите закон распределения Больцмана а) для молекул идеального газа в поле силы тяжести; б) для частиц массой m, находящихся в роторе центрифуги, вращающейся с угловой скоростью .
- Объясните физический смысл распределения Максвелла-Больцмана.
Лекция №9
Реальные газы
План
- Силы межмолекулярного взаимодействия в газах. Уравнение Ван-дер-Ваальса. Изотермы реальных газов.
- Метастабильные состояния. Критическое состояние.
- Внутренняя энергия реального газа.
- Эффект Джоуля – Томсона. Сжижение газов и получение низких температур.
1. Силы межмолекулярного взаимодействия в газах
Многие реальные газы подчиняются законам идеальных газов при нормальных условиях. Воздух можно считать идеальным до давлений ~ 10 атм. При повышении давления отклонения от идеальности (отклонение от состояния, описываемого уравнением Менделеева - Клайперона) возрастают и при p=1000 атм достигают более 100%.
|
|
Дело в том, что между молекулами действуют значительные по величине силы, называемые молекулярными силами. При удалении молекул друг от друга молекулярное взаимодействие проявляется в виде сил притяжения, при сближении – в виде сил отталкивания. Молекулярные силы имеют электромагнитное и квантовое происхождение. На рис. 9.1 а) представлена качественная зависимость сил межмолекулярного взаимодействия от расстояния r между молекулами, где Fотт и Fпр – соответственно силы отталкивания
|
|
Рис. 9.1
|
|
и притяжения, а F – их результирующая. Силы отталкивания считаются положительными, а силы взаимного притяжения – отрицательными. Соответствующая качественная кривая зависимости энергии взаимодействия молекул от расстояния r между центрами молекул приведена на
рис. 9.1б). На малых расстояниях молекулы отталкиваются, на больших притягиваются. Быстро возрастающие на малых расстояниях силы отталкивания означают грубо говоря, что молекулы как бы занимают некоторый определённый объём, дальше которого газ не может быть сжат.
Уравнение Ван-дер-Ваальса
(голландский физик, 1837 - 1923)
Ван-дер-Ваальс ввёл поправки в уравнение состояния идеального газа, учитывающие силы взаимодействия между молекулами и их собственный объём. Из уравнения Клапейрона – Менделеева для 1 моля следует, что при . Учтём в уравнении ограниченную сжимаемость газа. Заменим на , где b – некоторая константа, учитывающая размеры молекул. Теперь при , т.е. смысл поправки b – это объём, к которому стремится моль газа при наиболее «плотной упаковке» молекул, а уравнение состояния с этой поправкой .
Учтём взаимодействие молекул. Сила взаимодействия между двумя элементарными объёмами пропорциональна плотности молекул, заключённых в одном и другом объёмах . Плотность – величина, обратная объёму, занимаемому молекулами. . Отсюда поправка на взаимодействие молекул , где a – некоторая константа, характеризующая силы молекулярного притяжения. В результате уравнение состояния одного моля реального газа приняло вид:
Это и есть уравнение Ван-дер-Ваальса. Здесь a и b – постоянные Ван-дер-Ваальса, для разных газов они имеют свои значения.
Заметим, что поправка имеет размерность давления, и её часто называют внутренним давлением. На стенку сосуда такой газ оказывает давление Р, однако, если бы силы притяжения между молекулами мгновенно исчезли, то давление на стенку стало бы , т.е. при переходе от идеального газа к реальному давление на стенку уменьшается – из-за сил притяжения между молекулами. Поправка b связана с собственным объёмом молекул и её размерность .
Изотермы реального газа
Для исследования поведения реального газа рассмотрим изотермы Ван-дер-Ваальса – кривые зависимости от при заданных температурах Т, определяемые уравнением Ван-дер-Ваальса для 1 моля газа (рис. 9.2). Эти кривые рассматриваются для четырёх различных температур. При высоких температурах изотерма реального газа отличается от изотермы идеального газа только некоторым искажением её формы, оставаясь монотонно спадающей кривой. При некоторой температуре на изотерме имеется точка перегиба К. Эта изотерма называется критической, соответствующая ей температура – критической температурой, а точка К – критической точкой. Состояние с критическими параметрами называется критическим состоянием.
|

|
|
Рис. 9.2
|
При температурах изотермы имеют волнообразный участок. У реальных изотерм такого завитка нет, вместо него у них имеется прямолинейный горизонтальный участок (на рис. 9.2 обозначены пунктиром). Если через крайние точки горизонтальных участков семейства изотерм провести линию, то получится колоколообразная кривая, ограничивающая область двухфазных состояний вещества. Эта кривая и критическая изотерма делят диаграмму P, V под изотермой на три области: под колоколообразной кривой располагается область двухфазных состояний (жидкость и насыщенный пар Ж+П), слева от неё находится область жидкого состояния (Ж), а справа – область пара (П). Пар отличается от остальных газообразных состояний тем, что при изотермическом сжатии претерпевает процесс сжижения. Газ же при температуре выше критической не может быть превращён в жидкость ни при каком давлении.
2. Метастабильные состояния (греч. meta – после, за, в данном случае за стабильным состоянием, неустойчивые состояния).
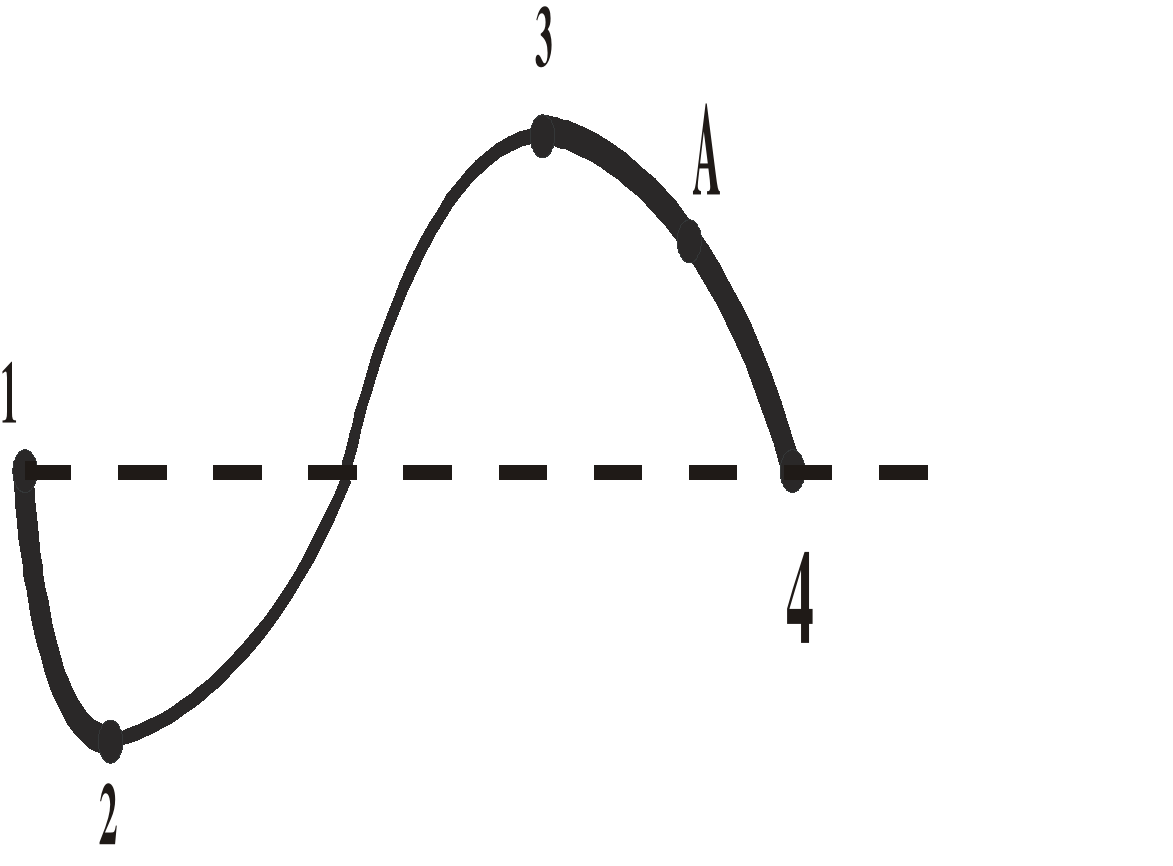
Рассмотрим часть изотермы рис. 9.3. Состояния на участке 2-3 не реализуются, т.к. на нём , т.е. увеличение объёма газа сопровождалось бы не уменьшением, а ростом давления – совершенно противоестественное свойство. На участках 1-2 и 3-4 , это нормально, но оказывается, что эти состояния не вполне устойчивы. Достаточно в состоянии А попадание в пар пылинки, чтобы вещество распалось на две фазы и перешло в состояние В. (Напомним, что фазой называется однородная, одинаковая по свойствам часть системы. Например, в закрытом сосуде вода и смесь воздуха и паров воды. Пар, находящийся в равновесии со своей жидкостью называется насыщенным.
|
|
Давление, при котором наблюдается равновесие, называется давлением насыщенного пара ). Состояния, подобные состоянию А (неустойчивые) называются метастабильными. Состояние 1-2, где давление меньше при данной температуре называется перегретой жидкостью, а 3-4
|
|
Рис. 9.3
|
|
() – пересыщенным паром. Рассмотрим состояние пересыщенного пара. Для образования капелек жидкости необходимо сближение молекул на расстояние порядка расстоянию между молекулами в жидкости. Для этого необходимо наличие центров конденсации (пылинки, заряженные частицы, капельки жидкости). В камере Вильсона (английский учёный, лауреат Нобелевской премии 1927г.) воздух, насыщенный парами воды резко расширяется и, соответственно, охлаждается. Пары оказываются в состоянии перенасыщения. Если заряженная частица попадёт в камеру, то пар конденсируется на ней в мелкие капельки, образуя видимый след («трек») при её движении.
Рассмотрим перегретую жидкость. Если жидкость тщательно очистить от твёрдых включений, то путём нагревания или понижения давления до её можно перевести в состояние перегрева. Прохождение заряженной частицы приводит к образованию вдоль следа частицы зародышевых центров кипения. Пузырьки фотографируют.
Критическое состояние
Рассмотрим подробнее состояние в т. К (рис. 9.2.). В этой точке различие в плотностях жидкости и насыщенного пара полностью исчезает. Одновременно исчезает всякое различие между жидкостью и паром. Границы раздела между жидкостью и паром также нет. Первая и вторая производные давления по объёму равны нулю.
; .
3. Внутренняя энергия реального газа. Кроме кинетической энергии включает потенциальную энергию взаимодействия молекул газа. Работа, совершаемая при расширении газа против сил взаимного притяжения молекул друг к другу, равна приращению энергии взаимодействия . Ван-дер-Ваальса поправка к давлению . Тогда работа , отсюда потенциальная энергия
При реальный газ стремится к идеальному и тогда :
.
Ранее для кинетической энергии хаотического теплового движения молекул было получено: .
Внутренняя энергия реального газа, учитывающая и кинетическую и потенциальную энергии:
То есть внутренняя энергия моля Ван-дер-Ваальского газа есть функция состояния газа.
4. Эффект Джоуля-Томсона
Эффект Джоуля – Томсона заключается в изменении температуры газа в результате адиабатического дросселирования – медленного протекания газа под действием постоянного перепада давления через дроссельное препятствие (например, пористую перегородку Др - дроссель на рис. 9.4). Термин «адиабатическое» означает без теплообмена с окружающей средой. Адиабатичность может быть осуществлена, например, с помощью теплоизолирующей оболочки вокруг канала. При
|
|
перемещении поршня (П) образуется постоянный перепад давлений (). Различают а) положительный эффект для Т, когда температура реального газа понижается и б) отрицательный эффект, когда (для идеального газа T=const). Практический интерес представляет положительный эффект. Положительный эффект наблюдается в области давлений, где преобладают силы притяжения
|
|
Рис. 9.4
|
|
между молекулами. При расширении молекулы газа совершают работу против сил притяжения и температура уменьшается. При этом кинетическая энергия теплового движения газа расходуется на работу против сил молекулярного притяжения.
Изменение температуры может быть значительным. Например, воздух, расширяясь при комнатной температуре от давления 200 атм до давления 1 атм охлаждается примерно на 40.
Процесс используется в технике для сжижения газов. На эффекте Джоуля – Томсона основана работа так называемой машины Линде.
Сжижение газов и получение низких температур
Газ может быть превращён в жидкое состояние, если его температура ниже критической и ниже температуры кипения при данном давлении.
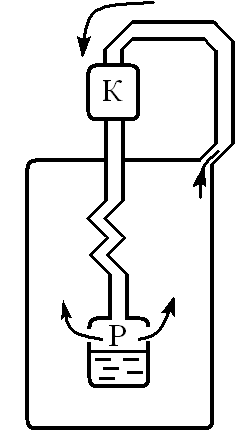
Машина Линде (немецкий учёный) (Рис. 9.5)
Атмосферный воздух сжимается компрессором (К) до давления 220 атм. Сжатый воздух проходит по трубопроводу и охлаждается проточной водой до 1015. Далее воздух поступает во внутренний канал
|
|
змеевика откуда в резервуар (Р), где давление 20 атм. При этом воздух охлаждается на 50 .(Расширение происходит в области положительного эффекта Джоуля – Томсона). Охлаждённый воздух по наружному каналу змеевика отводится к компрессору, охлаждая следующие порции воздуха, идущие по внутреннему каналу и т.д. При температуре 180 и давлением 20 атм. начинается конденсация воздуха. Жидкий воздух стекает в резервуар.
|
|
|
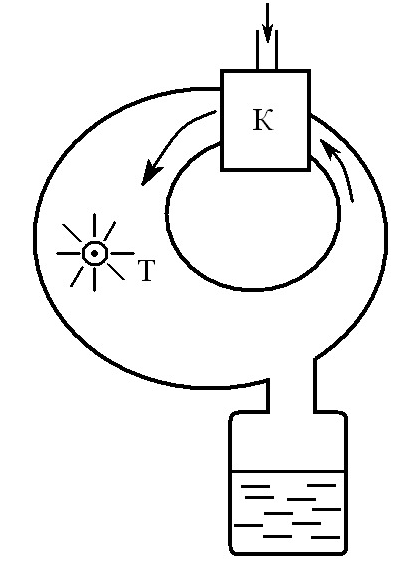
Турбодетандер Капицы (русский учёный, лауреат Нобелевской премии, 1894 – 1984). Газ, сжатый компрессором (К) до давления 6-7 атм, поступает в турбину (Т), расширяется до давления 1,3 атм., совершает работу, охлаждается, далее охлаждает газ, поступающий в компрессор, циркулирует и т.д., и, наконец, конденсируется. Таким методом можно получить жидкие азот, кислород, водород, гелий. (Отметим, что температура кипения жидкого кислорода 90К, азота 78К, водорода 20К, гелия 4,2К).
Применяются жидкие газы в металлургии, медицине, авиации.
|
|
Рис. 9.5
|
|
|
|
|
|
Рис. 9.6
|
|
Вопросы для самоконтроля.
- При каких термодинамических условиях газ не подчиняется уравнению состояния идеального газа? Что такое реальный газ?
- Запишите уравнение Ван-дер-Ваальса. Какой смысл имеют константы Ван-дер-Ваальса, входящие в это уравнение?
- Какое состояние называется метастабильным? Критическим? Критической температурой?
- Что такое пересыщенный пар? Перегретая жидкость? Как используются эти состояния?
- Запишите выражение для внутренней энергии Ван-дер-Ваальсовского газа.
- Объясните положительный эффект Джоуля-Томсона.
- Какими методами можно получить жидкие газы? Где они применяются?
PAGE 28
Молекулярно-кинетическая теория (МКТ) идеального газа