Диффузия. Каково влияние диффузии на свойства
СОДЕРЖАНИЕ
12
Задание 1
Что такое диффузия в металлах и сплавах? Каково влияние диффузии на свойства? Приведите примеры.
ОТВЕТ:
Диффузия – движение частиц среды, приводящее к необратимому переносу вещества или к установлению равновесного распределения концентраций частиц данного сорта в среде. В качестве диффундирую�щих частиц рассматривают молекулы, атомы, электроны проводимости, дырки, нейтроны и другие частицы. Диффузия в твердых веществах приводит к переносу атомов на расстояния, превышающие межатом�ные расстояния для данного вещества.
Частным случаем диффузии в чистом веществе или растворе постоянно�го состава, при котором диффундируют собственные частицы вещества, а его химический состав не меняется, является самодиффузия. При самодиф�фузии диффузионные перемещения частиц твердого вещества могут приво�дить к изменению его формы и другим явлениям. Так, длительное воздей�ствие сил поверхностного натяжения, тяжести, упругих, электрических и др. может привести к сращиванию двух пришлифованных поверхностей образцов одного и того же вещества, спеканию порошков, растягиванию образцов под действием подвешенного к ним груза (диффузионная ползучесть мате�риалов) и т.д.
В отсутствие макроскопического движения среды диффузия молекул (атомов) определяется их тепловым движением. При наличии в среде стационарных перепадов температуры, электрических полей и т.п. диф�фузия приводит к установлению равновесного распределения концентра�ций, характеризуемого соответствующими градиентами (термодиффузия, электродиффузия и т.п.). В однородной системе (газ, жидкость) при мо�лекулярной диффузии в отсутствие внешних воздействий диффузион�ный поток (поток массы) пропорционален градиенту его концентрации. Коэффициент пропорциональности называется коэффициентом диффу�зии. Последний зависит от строения и структуры взаимодействующих веществ и особенно сильно – от температуры.
В твердых кристаллических веществах различают следующие виды диффузии: по механизму протекания, по геометрическому месту переноса атомов, по месту поглощения атомов и по природе процесса.
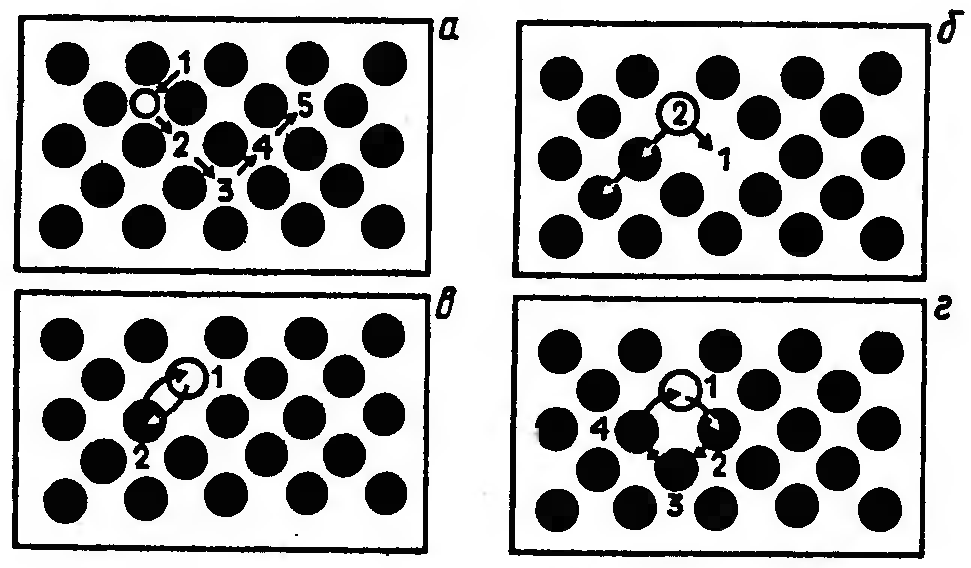
Рис. . Схемы механизмов протекания диффузии:
а – межузельный; б – вакансионный; в – обменный; г – циклический
Механизм протекания диффузии может быть межузелъным, вакансионным, обменным и циклическим (рис. 1). Реализация того или иного механизма протекания диффузии определяется кристаллическим строе�нием вещества и типом дефектов его кристаллической решетки. Так, доказано, что основным механизмом диффузии примесных атомов в твердых растворах замещения является вакансионный, а в твердых ра�створах внедрения – межузельный.
По геометрическому месту переноса атомов выделяют объемную, по�верхностную (из внешней среды) и граничную (по границам зерен) диф�фузии. Для совершения элементарного акта диффузии атом должен преодолеть энергетический барьер. Наиболее легко диффузия протекает по поверхности и границам зерен, где сосредоточены дефекты кристаллического строения (вакансии, дислокации и др.). Объемная диффузия в твердых веществах обусловлена перескоками атомов из одного поло�жения в другое, относительно свободное.
Поверхностная диффузия связана с переносом вещества или на по�верхность материала из внешней среды, или с поверхности материала во внешнюю среду, или на поверхность материала из его объема, или же вглубь материала с его поверхности (сорбционные процессы).
Сорбция – поглощение твердым телом или жидкостью какого-либо ве�щества из окружающей среды. Поглощающее тело называется сорбентом, поглощаемое – сорбтивом (сорбатом).
По месту поглощения атомов различают поверхность и объем. При этом сорбционные процессы, протекающие на поверхности, называются адсорбцией, а в объеме – абсорбцией. Сорбционные процессы избира�тельны и обратимы. Обратный процесс выделения поглощенного ком�понента называется десорбцией.
Адсорбция – поглощение вещества из газовой или жидкой среды поверх�ностным слоем твердого тела (адсорбента) или жидкости.
Абсорбция – поглощение какого-либо вещества из окружающей среды всей массой поглощающего тела (абсорбента). Абсорбция жидким абсор�бентом какого-либо компонента из газовой смеси называется растворением, из жидкой смеси – экстракцией.
Природу диффузии по характеру сорбционных процессов рассмат�ривают как физическую, если вещество при сорбционных процессах со�храняет все свои свойства, или химическую (хемосорбция), если вещество в этих процессах вступает в реакции. При физической природе сорбци�онные процессы обусловлены вандерваальсовыми силами притяжения частиц окружающей среды к частицам вещества.
Диффузионные процессы лежат в основе кристаллизации и рекристаллизации, фазовых превращений и насыщения поверхности сплавов другими элементами. С процессом диффузии связаны структурные изменения в материалах, которые могут ухудшать их физические и механические свойства.
Фазовые и структурные превращения при нагреве и охлаждении, получение того или иного структурного состояния металла и соответственно его свойства, связаны с протеканием диффузионных процессов. Даже образование при закалке мартенсита, считающееся бездиффузионным превращением, зависит от однородности твердого раствора перед закалкой, определяемого диффузией растворенных элементов.
Диффузия в значи�тельной степени определяет кинетику физико-химических процессов, обусловливающих разрушение материалов, ползучесть, старение, кор�розию и др. Так, например, адсорбция газов или жидкостей из внешней среды приво�дит к ухудшению диэлектрических свойств изоляционных материалов, понижает прочность металлов и изменяет другие свойства.
Очень большое значение процессы диффузии имеют при различных видах сварки. При сварке давлением в твердой фазе диффузия является основным процессом, определяющим рекристаллизацию и улучшение свойств сварного соединения после установления связи между свариваемыми активированными поверхностями. При сварке плавлением процессы диффузии влияют на степень химической и механической неоднородности металла шва и сварного соединения. Особенно большое значение процессы гетеродиффузии имеют для формирования сварных соединений разнородных сталей и разнородных металлов, так как обычные закономерности диффузионного процесса осложняются специфическими условиями диффузии – реакционной диффузией и диффузией, вызванной влиянием состава на изменение термодинамической активности растворенного и диффундирующего вещества.
Задание 2
1. Начертить диаграмму состояний железо-цементит, провести на ней ординату, соответствующую сплаву (1,5%С), обозначить на ней все критические точки.
2. Рядом с диаграммой справа начертить кривую охлаждения данного сплава, показав связь критических точек на диаграмме и кривой охлаждения.
3. Описать сущность превращений, происходящих в сплаве при медленном охлаждении от температуры в жидком состоянии до комнатной. Обязательно пояснить причины, вызывающие превращения.
4. На ординате сплава отметить точку, соответствующую температуре 650С, и провести через нее коноду. Пользуясь правилом отрезков, определить фазы, составляющие сплав при заданной температуре; их количество, %, и состав (содержание компонентов, %).
ОТВЕТ:
Диаграмма состояния Fe–Fe3C (рис. 2) характеризует фазовый состав и структуру в системе с концентрацией от чистого железа до цементита, содержащего 6,67 % С. По оси абсцисс диаграмма имеет две шкалы, показывающих содержание углерода в сплаве и количество цементита. Координаты характерных точек приведены в табл. 1.
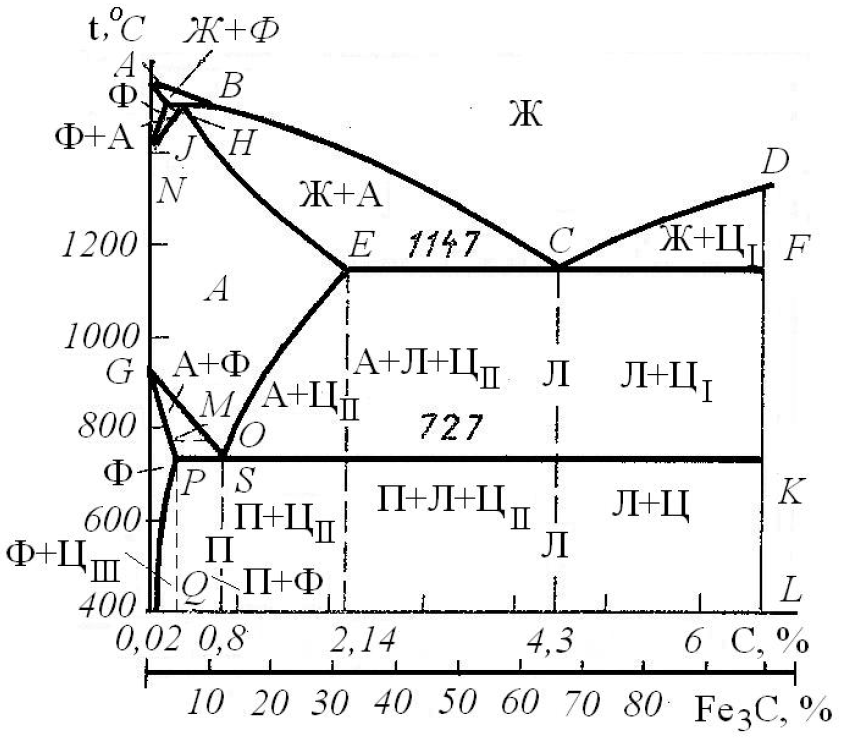
Рис. . Диаграмма состояния Fe–Fe3C
Таблица . Характерные точки диаграммы состояния железо–цементит
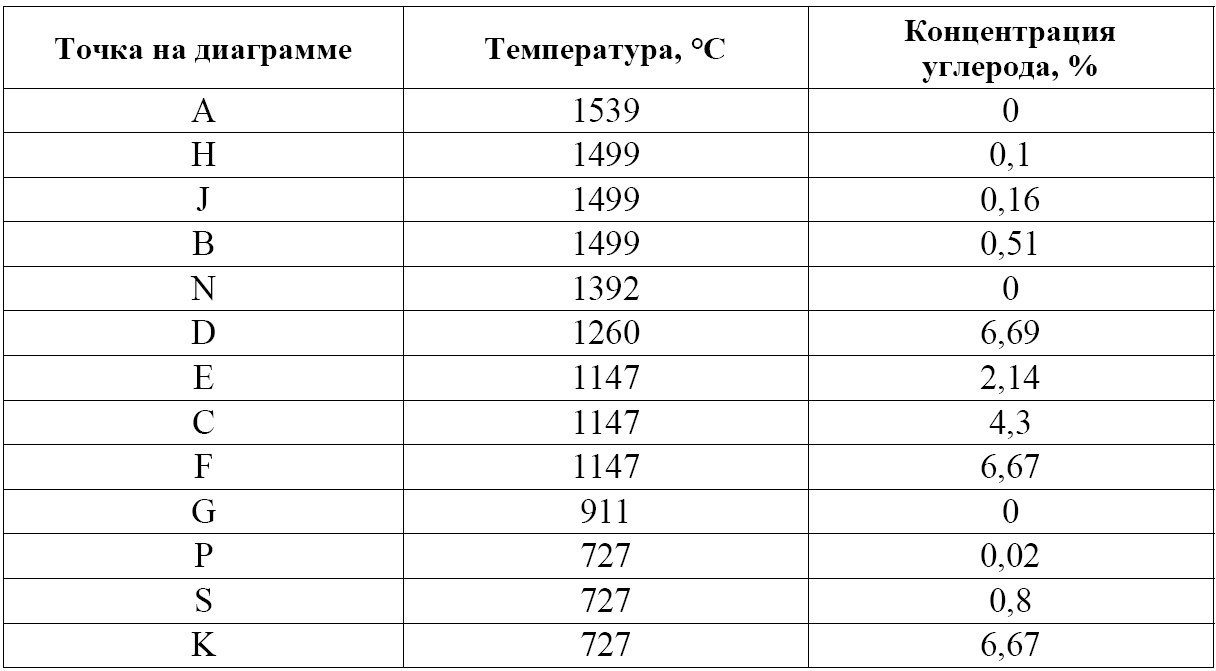
Точки А и D характеризуют температуру плавления железа и цементита соответственно. Точки N и G – температуры полиморфных превращений железа. Точки Н и Р характеризуют максимальную растворимость углерода в ОЦК решетке железа в высокотемпературной и низкотемпературной областях. Точка Е определяет максимальную растворимость углерода в железе с ГЦК решеткой. Фазовые превращения в системе Fe–Fe3C происходят как при затвердевании из жидкого агрегатного состояния, так и в твердом агрегатном состоянии. Первичная кристаллизация идет в областях между линиями ликвидус (ABCD) и солидус (AHJECF). Вторичная кристаллизация в твердом агрегатном состоянии является следствием полиморфного превращения железа и изменения растворимости углерода в железе с изменением температуры.
На линии ликвидус начинается кристаллизация из расплава соответственно на участке АВ – феррита (Ф) , на участке ВС – аустенита (А) и на участке СD – цементита первичного (ЦI). На линиях АН и JЕ завершается кристаллизация Ф и аустенита из жидкой фазы. Для диаграммы Fe–Fe3C характерны три изотермических превращения:
– перитектическое на линии HJВ при температуре 1499 °С
ФН + ЖB 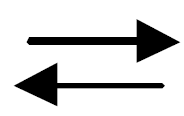 АJ;
АJ;
– эвтектическое на линии ECF при температуре 1147 °С
ЖC 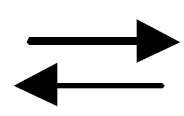 АE + ЦF;
АE + ЦF;
– эвтектоидное на линии PSK при температуре 727 °С
АS 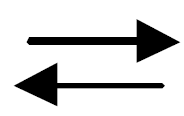 ФP + ЦK.
ФP + ЦK.
Эвтектическая смесь аустенита и цементита называется ледебуритом (Л), а эвтектоидная смесь феррита и цементита вторичного – перлитом (П). Ледебурит и перлит рассматривают как самостоятельные структурные составляющие. Перлит чаще всего имеет пластинчатое строение и обладает высокими механическими свойствами: в = 800…900 МПа, 0,2 = 450 МПа, 16%, твердость НВ 180…220.
Ледебурит имеет сотовое или пластинчатое строение. Сотовая структура образуется при медленном охлаждении и представляет собой пластины цементита, переплетенные кристаллами аустенита. Большое количество цементита, присутствующего в ледебурите, обеспечивает его большую твердость, порядка 600 НВ, и хрупкость, что затрудняет механическую обработку сплавов с ледебуритной структурой.
Стали в зависимости от содержания углерода подразделяются на эвтектоидные, содержащие ~ 0,8 % С, доэвтектоидные (от 0,02 до 0,8 % С) и заэвтектоидные (более 0,8 и до 2,14 % С).
Вычертим кривую охлаждения заэвтектоидного сплава 1,5%С, рис. 3:
Такой сплав называется заэвтектоидной сталью (>0,8%С), ниже 727°С будет иметь следующую перлитно-цементитную структуру.
Рис. 3 иллюстрирует охлаждение заэвтектоидной стали.
Основные фазы диаграммы:
- жидкость – жидкий раствор углерода в железе;
- аустенит – твердый раствор углерода в -железе;
- феррит – твердый раствор углерода в -железе;
- цементит – химическое соединение железа и углерода Fе3С;
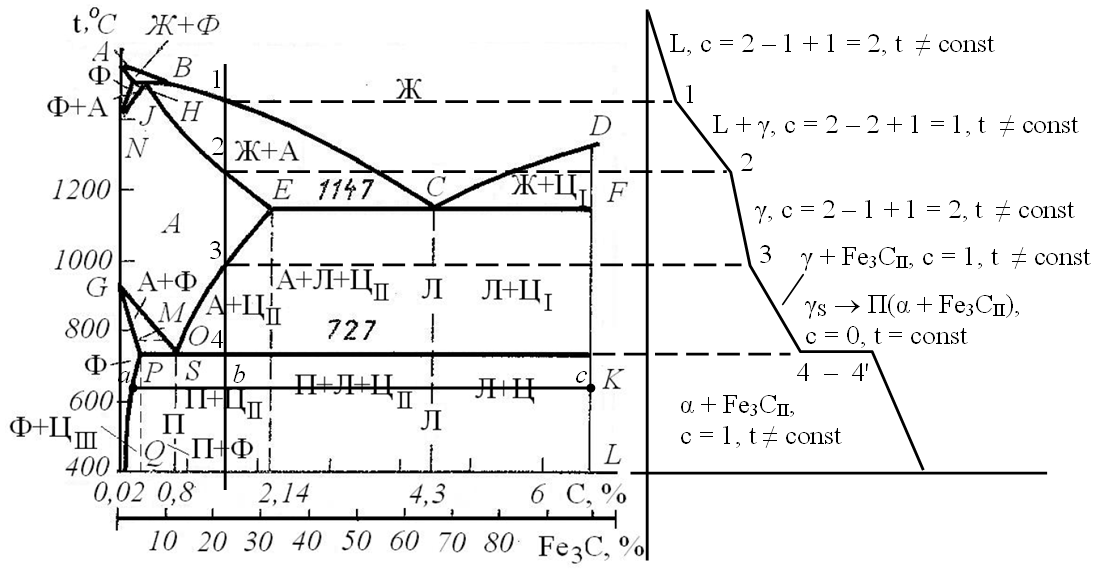
Рис. . Диаграмма железо-цементит (слева),
кривая охлаждения для сплава, содержащего 1,5% углерода (справа)
Выше точки 1 сплав находится в жидкой фазе (жидкий расплав углерода и Fe, фаза L), число степеней свободы – С = 2 – 1 + 1 = 2 (температура может изменяться).
При достижении точки 1 в жидкости начинается первичная кристаллизация аустенита. Ниже точки 1 и выше точки 2 сплав имеет двухфазное состояние: жидкость и кристаллы аустенита (Ж Ж + А, С = 2 – 2 + 1 = 1, температура может меняться). Состав кристаллов меняется по линии солидус JE, а жидкой фазы по линии ликвидус BC.
Ниже линии солидус точки 2 сплав находится в твердом однофазном состоянии твердого раствора (аустенит). При дальнейшем охлаждении (2 3) аустенит просто остывает, не меняя состава.
В т.3 из аустенита начинает кристаллизоваться вторичный цементит. По мере понижения температуры состав аустенита изменяется по линии ES. В т.4 (7270С) имеем цементит (6,67%С) и аустенит, содержаний 0,8% углерода, распадающийся на перлит (С = 2 – 3 + 1 = 0, температура не меняется до полного превращения, горизонт 4–4').
Ниже 7270С структура перлит + вторичный цементит.
Нанесем на диаграмму коноду abc, соответствующую температуре 650С и определим при этой температуре количественное со�отношение фаз и процентное содержание углерода в этих фазах.
Процентное содержание углерода в феррите определяем при помощи точки а коноды abc: 0,015%С. Процентное содержание углерода в цементите определяем при помощи точки с коноды abc: 6,67%С.
Тогда количество феррита:
Q = bc/ac 100% = (6,67 – 1,5) / (6,67 – 0,015) 100% 78%
Количество цементита:
QFe3C = 100 – 78% = 22%
Соотношение фаз: QFe3C : Q = 1 : 3,54.
СПИСОК ЛИТЕРАТУРЫ:
- Лахтин, Ю. М. Материаловедение / Ю. М. Лахтин, В. П. Леонтьева. – Москва : Машиностроение, 1990. – 528 с.
- Металловедение и технология металлов : учеб. для вузов / Ю. П. Солнцев [и др.]. – Москва : Металлургия, 1988.– 512 с.
- Материаловедение : учеб. для вузов / Б. Н. Арзамасов [и др.] под ред. Б. Н. Арзамасова. – 2-е изд. – Москва : Машиностроение, 1986. – 383 с.
- Материаловедение / Б. Н. Арзамасов [и др.]. – 7 изд. – Москва: Изд-во МГТУ им. Н. Э. Баумана, 2005. – 648 с.
- Материаловедение : учебник / В. А. Струк [и др.]. – Минск : ИВЦ Минфина, 2008. – 519 с.
- Сидорин И.И. Косолапов Г.Ф. Материаловедение: Учебник для высших технических учебных заведений. 2006 – 215 с.
- Солнцев Ю.П., Пряхин Е.И. Материаловедение. 2006 – 263 с.
Диффузия. Каково влияние диффузии на свойства