Исследование кинетики окисления олеокса и растительных масел в присутствии различных соединений и определение их эффективности
PAGE \* MERGEFORMAT 3
Введение.
Кожа типа замши, обладающая уникальными характеристиками, широко используется для изготовления верхней одежды, обивки автомобильных салонов, при изготовлении фильтрующих материалов и т.д.
Натуральная замша вырабатывается по технологии, предусматривающей удаление лицевого слоя, и последующее жирование в присутствии ворваней с обязательной продувкой воздухом, способствующей окислению непредельных компонентов жира. В процессе окисления образуются альдегиды и эпоксиды, обладающие дубящим действием, а жирующие компоненты обволакивают структурные элементы дермы, обеспечивая необходимые потребительские свойства. Традиционный технологический процесс жирового дубления достаточно трудоемкий, энергозатратный и не отвечает современным экологическим требованиям. Представляется интересной и практически значимой разработка готового препарата с помощью которого можно проводить замшевание в типовых технологических условиях кожевенного предприятия.
Целью работы является исследование кинетики окисления олеокса и растительных масел в присутствии различных соединений и определение их эффективности.
В рамках работы решались такие задачи ,как :
1.исследование наиболее эффективных методов модификации природных жиров и растительных масел;
2.изучение физико-химических свойств модифицированных масел;
3. оптимизация технологических режимов дубления с использованием модифицированных масел;
4.исследование потребительских свойств замши
Замша обувная- кожа жирового дубления, выделанная из шкур лосей, овец и диких коз. Особенностью замши является отсутствие лицевого слоя, который спиливают в процессе про�изводства. Замша отличается повышенной тягучестью, низкой плотностью. Она вырабатывается в натуральном или окрашен�ном виде и подразделяется по видам сырья, размерам, тол�щине. Замша хорошего качества имеет густой низкий блестя�щий ворс с однородной окраской, устойчивой к сухому и влажному трению. Лучшей является замша из оленьих шкур (оленья замша).
Кожи для верха обуви из бахтармяного спилка- -кожа, выделанная из полученного при двоении сетчатого слоя дермы. По назначению (в зависимости от толщины, плотности и ха�рактера отделки) различают спилок для верха тяжелой обуви, Для обуви повседневной носки, велюр и сандальный. Первые три вида спилка вырабатывают из шкур крупного рогатого скота и конских, сандальный спилок -из свиных шкур.
1.ЖИРОВОЕ ДУБЛЕНИЕ
Жировое дубление (замшевание) осуществляется путем пропитки голья ненасыщенными жирами типа ворваней с последующим окислением их под действием кислорода воз�духа. В результате дубления получается очень пористая, мяг�кая и тягучая кожа, называемая замшей.
Одним из главных факторов, обусловливающих эффект жирового дубления и свойства замши, является ненасыщенность
жира. Лучшая по свойствам замша получается при использовании ворваней( жиры морских животных и рыб), йодное число которых превышает 140, а кислотное число меньше 15. Следует иметь в виду, что исходные ненасыщенные жиры (ворвани), взятые для замшевания. дубящего действия не оказывают. Дубящие вещества образуются в результате окисления входящих в них ненасыщенных жирных
кислот. К ним относятся соединения, содержащие альдегидные
группы, а также этиленоксидные циклы (эпоксидные группы)

(см. п2)
Экспериментально доказано, что при окислении ворвани в условиях жирового дубления образуются даже свободные ду�бящие альдегиды, такие, как акролеин, глиоксаль. формальде�гид и некоторые другие. В результате дубящего действия аль�дегидов и эпоксидных соединений замша приобретает некото�рые свойства, характерные для кож альдегидного дубления. К этим свойствам относятся повышенная устойчивость к дей�ствию щелочей и обратимость сваривания- образец замши не теряет прочности при нагревании в воде при температуре выше температуры сваривания, длина его при этом плавно умень�шается, а при охлаждении в значительной степени восстанавливается.
Как известно, основными центрами фиксации альдегидов коллагеном являются аминогруппы остатков лизина. Установлено, что в результате жирового дубления число свободных аминогрупп в коллагене резко снижается, изоэлектрическая точка его смещается в область меньших значении рН, а кислотная емкость уменьшается. Дезаминирование голья перед дублением приводит к тому, что температура сваривания его при замшевании не повышается, а снижается на 14-180С. Это объясняется частичной окислительной деструкцией коллагена, протекающей сопряжено с окислением жиров [1]. В условиях нормального жирового дубления преобладающим является процесс сшивания структуры белка продуктами окисления жи�ром, содержащими альдегидные и эпоксидные группы, вследствие чего температура сваривания голья повышается на 6-80С, достигая значения 70—720С. Опыт показывает, что эпоксидные соединения могут взаимодействовать с различными функциональными группами коллагена, образуя прочные химические связи. Схематично это можно представить следующим образом:
Б1 —2 + С2 —C — . . . — C —C2+ —Б2
O O
Б1 ——С2 —С — ... — С — С2 — — Б2
Однако неправильно было бы сводить процесс замшевания только к альдегидному и эпоксидному дублению. В отличие от кож, выдубленных альдегидами и эпоксидами, замша характе�ризуется большой мягкостью, высоким формированием объема и леофильностью, т. е. преимущественно смачивается не водой, а неполярными жидкостями. Эти свойства замши обусловли�ваются химическим взаимодействием окисленных жирных кис�лот с коллагеном, а также отложением на структурных элементах дермы и в пространстве между ними несвязанного жира.
Связывание непредельных жиров и продуктов их окислении с коллагеном при жировом дублении происходит в широком диапазоне значений рН голья- от 2 до 9,5. Однако лучшая по свойствам замша получается при дублении голья, рН которого 7~7,5. Чтобы жир хорошо проникал в дерму и равномерно распределялся в ней, влажность голья перед дублением должна быть в пределах 55-65%. При правильном проведении замшевания содержание влаги в голье убывает, идет ее замещение жиром. Обычно в конце дубления влажность замши устанавли�вается на уровне 8-10%. Продолжительность дубления зави�сит от скорости окисления введенного в дерму жира. Повыше�ние температуры воздуха и применение инициаторов окисления ускоряют процесс.
На практике для окисления жира в барабан через специ�альное устройство подается воздух, нагретый до температуры 60 °С. Температура полуфабриката при этом не должна пре�вышать 40 °С и только в конце дубления может доходить до 45 °С. Несоблюдение температурного режима может привести к порче полуфабриката.
Длительность жирового дубления по принятой в настоящее время методике не превышает 4 суток (по старым методикам до 11 суток); расход жира— 20-25% от массы голья при 60%-ной влажности (по старым методикам расход жира до 60%). Как показывает опыт, продолжительность дубления может быть еще более сокращена, а расход жира уменьшен, если окисление его проводить не кислородом воздуха, а с помощью соответствующих окислителей, например перманганата калия. Подготовительные процессы в производстве замши отличаются более продолжительным, чем при выработке из данного сырья кож других видов, золением. В некоторых случаях (например, при обработке шкур оленей) голье золится до 5 суток. Золеное голье обрабатывают на двоильно-ленточной машине с целью удаления тонкого лицевого слоя. В результате при последующем дублении облегчается проникание жира в дерму. Перед дублением голье частично обезвоживают сульфатом натрия и отжимают на прессе до влажности примерно 60%.
После замшевания полуфабрикат промывают 2-3 раза раствором карбоната натрия и водой для удаления избыточного количества несвязанного жира, особенно с поверхности полуфабриката. Иногда для этой цели применяют органические растворители.
В последнее время жировое дубление все чаще комбинируют с дублением формальдегидом [2, 3]. Предварительное формалирование сообщает дерме повышенную проницаемость, вследствие чего ворвань быстрее поглощается гольем и равно�мернее распределяется в нем. Очень важно обеспечить равномерное распределение и оптимальное связывание формальдегида в толще голья. В противном случае получается кожа со свойствами не характерными для замши.
Если формальдегидная обработка и последующее жировое дубление проведены правильно , то получаемая кожа по свойствам не уступает обычной хорошей замше. Описанный способ дубления известен в специальной литературе под названием «новое замшевое дубление». Вместо формальдегида при таком дублении может быть использован глутаровый альдегид.
В меховом производстве жировое дубление применяют очень редко для повышения мягкости и тягучести кожевой ткани некоторых видов сырья с низким жестким волосяным покровом( опоек, жеребок, шкуры морского зверя). Это связано с тем, что при дублении волосяной покров сильно зажиривается и окрашивается в желто-коричневый цвет.
1.1.Дубящие жиры
Дубящие, или замшующие, жиры находят широкое применение в производстве замши.
Дубящими свойствами обладают только жиры ряда морских животных и рыб. Решающим фактором, определяющим дубящую способность таких жиров, является ненасыщенность. Жиры морских животных и рыб (ворвани) отличаются содержанием множества ненасыщенных (непредельных) жирных кислот с разным числом атомов углерода. Наиболее часто встречаются жирные кислоты с числом атомов углерода от 18 до 22. Типичными непредельными кислотами, входящими в состав ворваней, являются олеиновая, линолевая, линоленовая к клупанадоновая.
Лучшая по свойствам замша получается при использова�нии тюленьего и трескового печеночных жиров, содержащих наибольшее количество этих жирных кислот.
Результаты исследований, а также практика работа коже�венных заводов свидетельствуют о том, что оптимальной дубя�щей способностью обладают те ворвани, йодное число кото�рых не ниже 140. С этой точки зрения жир дельфинов и кито�вый жир для дубления непригодны, что подтверждается практикой.
Согласно современным представлениям [1] автоокисление жиров молекулярным кислородом развивается так, что моле�кула последнего присоединяется к свободным углеводородным радикалам, образующимся в результате отщепления водорода от углеводородного радикала жирных кислот, в том числе и от непредельных.
Общая схема автоокисления такова:
СН2— +O2 —CH— + O—OH; — CH— + O2 — —CH —
O—O
При окислении, например, олеиновой кислоты наибольшему воздействию кислорода подвергается не двойная связь, а метиленовая группа жирных кислот, находящаяся рядом с двойной связью [4].В этом случае реакция проходит по схеме
—CH2—CH=CH — CH2— + O2 —CH2—CH=CH—CH— + OOH
—CH2—CH=CH—CH— + O2 —CH2—CH= CH—CH—
O—O
Таким образом, при окислении жирных кислот сначала образуются своеобразные вещества пероксидного характера, в которых один из атомов кислорода пероксидной группы имеет свободную степень окисления. Эти свободные радикалы отличаются высокой активностью.
При столкновении с углеводородными радикалами жирных кислот других молекул глицеридов свободные пероксидные радикалы стабилизируются, отрывая от них атомы водорода. В результате образуются достаточно стабильные вещества, называемые гипероксидами, и новые свободные радикалы
—СH = CH—CH— + —CH2— CH2— —CH = CH—CH—+ CH2CH
O—O O—OH
Гидропероксидные соединения могут образовывать цикли�ческие пероксиды по схеме
- СН = СН — СН — СН2- — СН — СН — СН — СН2 -
О-----О О------О
Образовавшийся циклический пероксид водорода очень не�стоек вследствие наличия в нем атома углерода, имеющего свободную степень окисления и расположенного рядом с пероксидной группой. Поэтому такое соединение легко распадается с образованием альдегидов:
-СН-СН-СН-СН2- -СН-СНО + СН2-СНО
O--O
Установлено также, что гидропероксиды являются силь�ными окислителями. При взаимодействии их с двойными свя�зями радикалов ненасыщенных жирных кислот образуются эпоксидные соединения:
— СН= СН —CH— + —CH = CH — — СН =СН —CH— + —CH CH—
O—OH OH O
Эти реакции играют большую роль в процессах жирового дубления( см.п1)
Автоокисление непредельных жиров может быть значи�тельно ускорено, если к ним добавить соединения металлов переменной степени окисления. К таким соединениям отно�сятся растворимые в жирах жирнокислые или нафтеновокислые соли кобальта и марганца. Еще не так давно считали, что эти соединения являются катализаторами окисления. В настоя�щее время установлено, что растворимые в жирах соли метал�лов переменной степени окисления прежде всего являются инициаторами свободных радикалов, начинающих цепи окис�ления. В практике дубления широко используются такие соединения[5].
1.2.Окисление жиров.
Окисление жиров происходит за счет реакции присоединения кислорода воздуха к свободным активным радикалам R, появляющимся в жире в результате воздействия энергии.
Реакция носит цепной характер. Механизм процесса окисления происходит на углеводородной цепочке, т. е. радикале жирной кислоты:

Как правило, начальный период окисления характеризуется образованием ROOH - гидроперекисей. В процессе последующего окисления при температуре до 50 °C образуются также альдегиды R-OH и кетоны 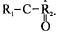 В этом случае кислород присоединяется к углеродному атому по соседству с двойной связью, а не по месту двойной связи.
В этом случае кислород присоединяется к углеродному атому по соседству с двойной связью, а не по месту двойной связи.
При температурах выше 50 °C происходит присоединение O2 по месту двойных связей и образуются 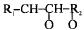 - циклические перекиси, а при температурах выше 170-300 °C
- циклические перекиси, а при температурах выше 170-300 °C 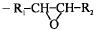 - эпоксидные соединения.
- эпоксидные соединения.
Ускорение окисления происходит в присутствии: кванта света, ионизирующего излучения, электрического разряда, повышенных температур, наличия свободных жирных кислот и перекисей, катализирующих процесс солей металла. О ходе окисления судят по перекисному числу, которое выражают количеством граммов йода, вытесняемого из йодида калия (KI) перекисями, содержащимися в 100 граммах жира.
При значениях перекисных чисел (п. ч., % I) больше 0,1 жир непригоден в пищу. В реальных технологических условиях в течение первых 3-9 ч после убоя животных в жире происходят малые изменения, и перекисное число практически не меняется. Этот период называют индукционным (тинд. - продолжительность хранения), ч (рис.1.8)
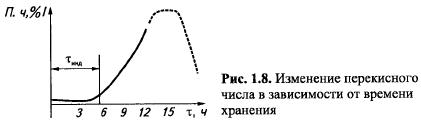
Индукционный период связан с наличием в жире естественных антиокислителей, которые какое-то время связывают кислород воздуха. После окончания индукционного периода происходит резкое увеличение значений перекисного числа, накопление карбонильных и эпоксидных соединений.
2.Растительные масла
Растительные масла— продукты, извлекаемые из растительного сырья и состоящие из триглицеридов жирных кислот и сопутствующих им веществ (фосфолипиды, свободные жирные кислоты, воски, стеролы, вещества придающие окраску и др.).
Триглицериды составляют главную массу (до 95—98 %) липидов масличных плодов и семян. Они являются сложными эфирами глицерина и жирных кислот. Карбоновые кислоты — это органические вещества, содержание одну или несколько карбоксильных групп, соединенных с углеводородным радикалом.
Жирные кислоты, входящие в состав растительных масел, за очень редким исключением, одноосновные с чётным числом атомов углерода — 6, 8, 10, 12, 14, 16, 18. Все триглицериды имеют одинаковую глицериновую часть, поэтому различие свойств обусловлено жирными кислотами. Жирные кислоты могут отличаться по следующим параметрам:
длина цепи (количество атомов углерода);
количество и положение двойных связей;
положение в молекуле триглицерида.
Изменение этих характеристик отвечают за химические и физические различия жиров и масел
Модификация растительных масел.
Большинство природных растительных масел и жиров имеют ограниченное применение в своем естественном виде из-за специфического состава, свойств. Чтобы расширить применение таких масел, их подвергают различным модификациям, наиболее известными из которых являются переэтерификация, гидрогенизация, фракционирование.
Гидрогенизация — процесс частичного или полного насыщения водородом непредельных связей ненасыщенных жирных кислот триглицеридов, входящих в состав растительных масел. Проводится для превращения жидких масел в твёрдые (подбор условий процесса позволяет получать саломасы различной степени твёрдости), что позволяет расширить сферу их применения (гидрогенизированные жиры используются в кондитерской и хлебобулочной промышленности).
Переэтерификация — процесс перераспределения ацильных групп в триглицеридах масла без изменения жирнокислотного состава триглицеридов. Добавление переэтерифицированных жиров в жировую основу спреда способствует улучшению структурно-механических характеристик (в охлаждённом виде легче намазывается, чем сливочное масло).
Фракционирование — разделение растительных масел термомеханическим способом на фракции с различной температурой плавлении
3. Экспериментальная часть.
Так как натуральная замша вырабатывается по технологии, предусматривающей удаление лицевого слоя, и последующее жирование в присутствии ворваней с обязательной продувкой воздухом, способствующей окислению непредельных компонентов жира. В процессе окисления образуются альдегиды и эпоксиды, обладающие дубящим действием, а жирующие компоненты обволакивают структурные элементы дермы, обеспечивая необходимые потребительские свойства. Традиционный технологический процесс жирового дубления достаточно трудоемкий, энергозатратный и не отвечает современным экологическим требованиям.
Поэтому интересной и практически значимой представляется разработка готового препарата с помощью которого можно проводить замшевание в типовых технологических условиях кожевенного предприятия. Сначала в качестве объекта был взят олеокс, на его примере установлено необходимое количество пероксида водорода, надуксусной кислоты и олеокса. На основе этого проводились эксперименты с растительными маслами, так как олеокс довольно дорог для использования.
Цели:
Основной задачей является целевая модификация природных жиров и масел, содержащих непредельные жирные кислоты, и их использование в производстве замши.
-Исследование наиболее эффективных методов модификации природных жиров и растительных масел.
-Изучение физико-химических свойств модифицированных масел.
-Оптимизация технологических режимов дубления с использованием модифицированных масел;
-Исследование потребительских свойств замши
3.1. Исследование наиболее эффективных методов модификации природных жиров и растительных масел.
Объекты изучения:
-продукт на основе оксиэтилированной олеиновой кислоты – Олеокс.
-растительные масла, в частности рапсовое и кукурузное
Методика проведения
Олеокс окисляли в гетерогенной системе (водная эмульсия) при 45 0С. В качестве окислителей использовали надуксусную, надмуравьиную и фосфомолибденовую кислоты. Предварительно смешивали Олеокс с кислотой и затем в эту смесь вводили пероксид натрия в соотношении кислота : пероксид (1:1). За кинетикой окисления следили по накоплению пероксидных соединений, которые определялись иодометрическим методом, значению йодного числа и показателю преломления. Конечные продукты окисления оценивали по содержанию эпоксидных групп.
1.Аппаратура,реактивы и растворы
Стаканчики для взвешивания внешним диаметром 10мм, высотой 15мм,с притертой пробкой.
Колбы с притертой пробкой 250, 500см3
Бюретки 1-2-25 и 1-2-50
Спирт этиловый ректификованный технический по ГОСТ 18300. высший сорт
Калий йодистый по ГОСТ 4232. х.ч. или ч.д.а., 20 %-ный раствор.
Йод квалификации не ниже ч.д.а. Натрий серноватистокислый (тиосульфат натрия) по ГОСТ 27068. раствор 0.1 моль \дм3
Крахмал растворимый по ГОСТ 10163, 0,5 %-ный водный раствор
Вола дистиллированная pH 5.4 - 6.0.
Калий двухромовокислый (бихромат калия).
2. Подготовка к испытанию.
25,4 г кристаллического йода растворяют в 1000 см3 этилового спирта.
Порядок эксперимента
Готовим смесь олеокса, берем 5 мл и кислоты, 2.5 мл, затем вводим перекись водорода 2.5мл. Нагреваем на электрической плитке при t=45-50C. Поддерживаем температуру, и через каждые 20 мин измеряем показатели.
Определение йодного числа.
Необходимое количество испытуемого продукта,1,5 мл, отбирают при помощи пипетки.
Наливают в коническую колбу вместимостью 500 см3 с притертой пробкой 15 см3 этилового спирта и опускают туда стаканчик с продуктом, слегка приоткрывая крышку стаканчика.
Из бюретки добавляют 25 см3 спиртового раствора йода, плотно закрывают колбу пробкой, предварительно смоченной раствором йодистого калия, осторожно встряхивают колбу. Прибавляют 150 см3 дистиллированной воды, быстро закрывают колбу пробкой. Содержимое колбы встряхивают в течение 5 мин и оставляют в темноте еще на 5 мин. Обмывают пробку и стенки колбы небольшим количеством дистиллированной воды, добавляют 20-25 см3 раствора йодистого калия и титруют раствором тиосульфата натрия. Жидкость в колбе примет светло-желтый цвет, затем прибавляют от 1 до 2 см3 раствора крахмала и продолжают титровать до исчезновения синевато-фиолетового окрашивания.
Для вычисления йодного числа проводят контрольный опыт.
Йодное число ( X ) испытуемого продукта, г йода на 100 г нефтепродукта, вычисляют по формуле
Х = (V-V1)Р 0,01269 100%/т
где V - объем раствора тиосульфата натрия 0,1 моль/дм3, израсходованный на титрование в контрольном опыте, см3;
V1 - объем раствора тиосульфата натрия 0,1 моль/дм3, израсходованный на титрование испытуемого продукта, см3;
Р - фактор раствора тиосульфата натрия 0,1 моль/дм3;
0,01269 - количество йода, эквивалентное 1 см3 раствора тиосульфата натрия точно 0,1 моль/дм3;
т- масса испытуемого продукта, г.
Определение перекисного числа.
Перекисное число выражают в граммах йода, вытесняемого из йодистого калия перекисными соединениями, содержащимися в 100 г.жира. 1,5 мл олеокса растворяют в колбе в смеси 7.5 мл ледяной уксусной кислоты и 5 мл хлороформа, добавляют 1 мл свежеприготовленного насыщенного раствора йодистого калия. Колбу закрывают пробкой, встряхивают в течение 5 мин, добавляют 60 мл воды и 1 мл 1 %-ного раствора крахмала. Вытесненный перекисями йод оттитровывают 0,01 н. раствором тиосульфата натрия с теми же реактивами, но без добавления олеокса:
ПЧ = (А - Б) • 100 • 0,00127 К/р
где А --расход 0,01 н. раствора тиосульфата натрия на титрование опытной пробы, мл; Б - расход 0,01 н. раствора тиосульфата натрия на титрование контрольной пробы, мл; р -масса навески, г; К -поправка к титру раствора тиосульфата натрия;0,00127- количество йода, связывающее 1 мл 0,01 н. раствора тиосульфата натрия, г.
Обработка результатов.
Йодное число.
|
|
Надуксусная кислота
|
Надмуравьиная кислота
|
Фосфомолибденовая кислота
|
|
Время, мин
|
Результаты титрования. мл
|
Результаты титрования. мл
|
Результаты титрования. мл
|
|
20
|
29,46
|
23,5
|
29,01
|
|
40
|
29,86
|
29,82
|
29,14
|
|
60
|
30,34
|
29,9
|
29,39
|
|
80
|
30,64
|
30,34
|
29,59
|
Таблица 1.Результаты титрования для определения йодного числа.
Таблица 2. Значение йодного числа, рассчитанного по формуле, указанной выше.
|
|
Надуксусная кислота
|
Надмуравьиная кислота
|
Фосфомолибденовая кислота
|
|
Время, мин
|
Значение йодного числа
|
Значение йодного числа
|
Значение йодного числа
|
|
0
|
39
|
39
|
39
|
|
20
|
38,4
|
37,8
|
42,2
|
|
40
|
35
|
35,4
|
41,1
|
|
60
|
31
|
34,6
|
39
|
|
80
|
28,4
|
31
|
37,3
|
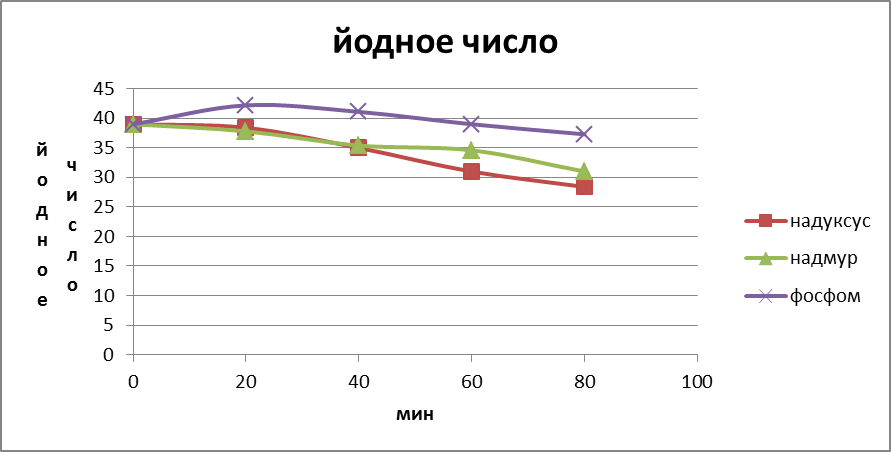
Рис1. График изменения йодного числа кислот с течением времени.ю
Из графика видно, что йодное число в начале резко возрастает, а затем наблюдается определенная стабилизация спустя 60 минут от начала окисления.
Перекисное число.
Таблица 3.Результаты титрования для определения перекисного числа
|
|
Надуксусная кислота
|
Надмуравьиная кислота
|
Фосфомолибденовая кислота
|
|
Время, мин
|
Результаты титрования. Мл
|
Результаты титрования. Мл
|
Результаты титрования. Мл
|
|
20
|
6,27
|
6,29
|
8,64
|
|
40
|
4,79
|
4,48
|
8,27
|
|
60
|
3,79
|
3,49
|
6,98
|
|
80
|
3,48
|
2,69
|
5,85
|
Таблица 4.Значение перекисного числа, рассчитанного по формуле, представленной выше.
|
|
Надуксусная кислота
|
Надмуравьиная кислота
|
Фосфомолибденовая кислота
|
|
Время, мин
|
Значение перекисного числа
|
Значение перекисного числа
|
Значение перекисного
числа
|
|
0
|
0.4
|
0.4
|
0.4
|
|
20
|
0.448
|
0.45
|
0.65
|
|
40
|
0.322
|
0.296
|
0.618
|
|
60
|
0.237
|
0.212
|
0.508
|
|
80
|
0.211
|
0.144
|
0.412
|
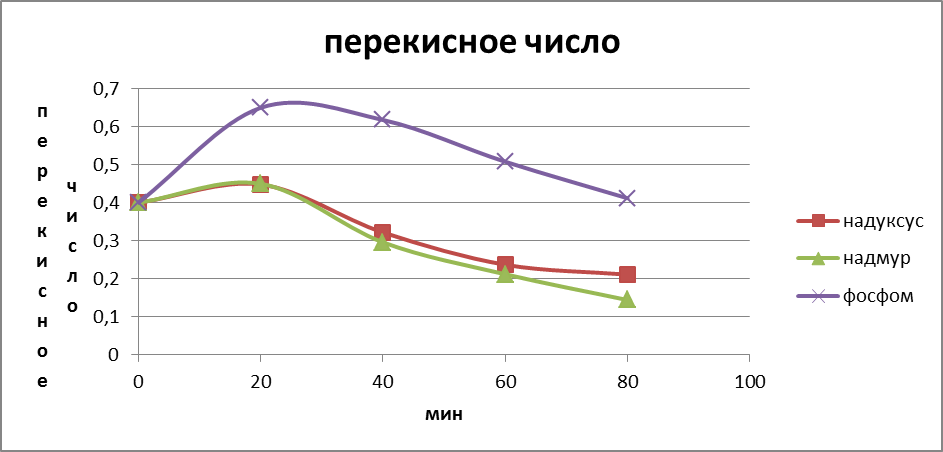
Рис.2.График изменения перекисного числа с течением времени
Как следует из представленных данных, наиболее эффективно действует на двойные связи в олеоксе надуксусная кислота. Содержание перекисных соединений также увеличивается, а затем стабилизируется.
Характер изменения этих показателей во времени свидетельствует о сложности механизма перекисного окисления. В окисленном олеоксе обнаружены эпоксидные группы, являющиеся наряду с альдегидами, основными компонентами, обуславливающими дубящее действие окисленных жиров.
Таблица 5.Значения показателя преломления.
|
|
Надмуравьиная кислота
|
Фосфомолибденовая кислота
|
|
Время, мин
|
Показатель преломления
|
Показатель преломления
|
|
0
|
1.456
|
1.424
|
|
20
|
1.468
|
1.432
|
|
40
|
1.47
|
1.438
|
|
60
|
1.479
|
1.442
|
|
80
|
1.482
|
1.452
|
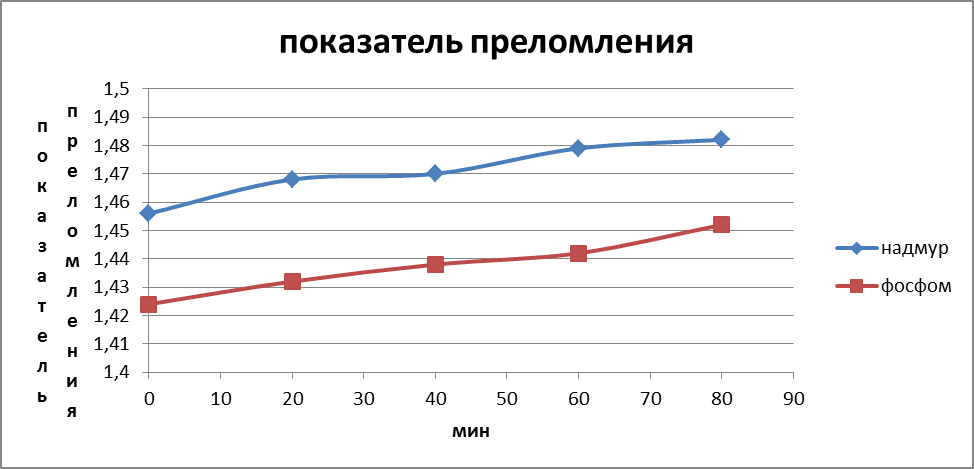
Рис.3. График изменения показателя преломления во времени.
Увеличение значения показателя преломления олеокса в процессе окисления является следствием изменения химического состава и образования новых соединений.
Окисленный олеокс имеет следующие показатели.
Таблица 6. Показатели окисленного олеокса.
|
рН
|
4.3
|
|
Показатель преломления
|
1.452
|
|
Эпоксидное число
|
3.67
|
|
Йодное число
|
15.23
|
|
Альдегидное
число
|
7.2
|
|
Внешний вид
|
Олеокс становится более прозрачным и менее вязким,по сравнению с неокисленной формой.
|
3.1.2.Исследование растительных масел.
Готовится смесь масла (рапсового или кукурузного) 5 мл с надуксусной кислотой. 2,5 мл перекиси водорода и 2,5 мл уксусной кислоты.
Йодное число.
Это масса иода (в г), присоединяющегося к 100 г органического вещества ,оно характеризует содержание двойных связей в ненасыщенном соединении.
Чем выше иодное число, тем больше ненасыщенных кислот содержится в жире, то есть тем больше иода вещество может присоединить.
Таблица 7.Результаты титрования масел
|
|
Кукурузное масло
|
Рапсовое масло
|
|
Время, мин
|
Результаты титрования, мл
|
Результаты титрования, мл
|
|
0
|
17,74
|
19,33
|
|
20
|
18,16
|
14,8
|
|
40
|
16,98
|
14,78
|
|
60
|
17,06
|
14,54
|
|
80
|
17,29
|
14,27
|
Йодное число, рассчитанное по формуле, указанной выше.
Табл.8.Значение йодного числа
|
|
Кукурузное масло
|
Рапсовое масло
|
|
Время, мин
|
Значение йодного числа
|
Значение йодного числа
|
|
0
|
93,06
|
103,2
|
|
20
|
100,5
|
121,82
|
|
40
|
108
|
122
|
|
60
|
107,5
|
123,5
|
|
80
|
106
|
125,21
|
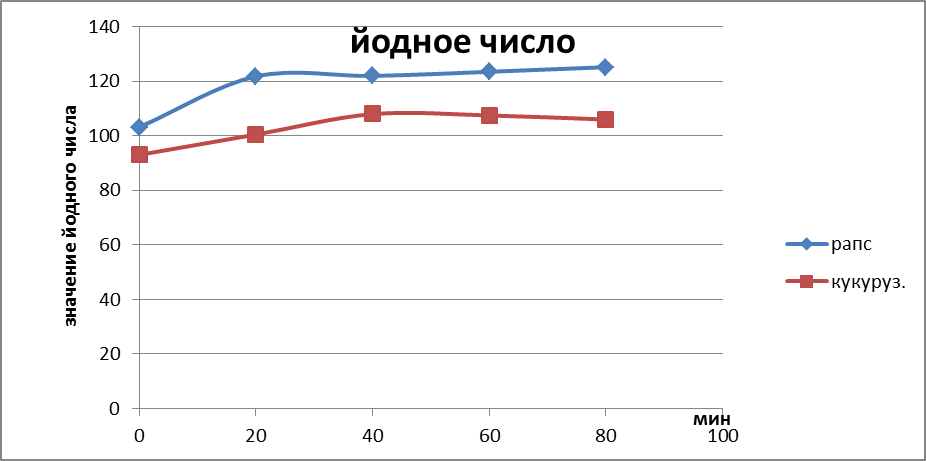
Рис.4. График изменения йодного числа
Йодное число сначала резко возрастает , а затем плавно стабилизируется,что указывает на образование двойных связей в соединениях.
Перекисное число.
Для оценки количества перекисных соединений в жире используют метод определения перекисного числа (ПЧ). Предварительно следует как можно тщательнее отделить жир от других компонентов, например, белка, поскольку эти вещества могут влиять на результаты титриметрического анализа. Определение количества перекисей обычно производят в чистых жирах и маслах. Этот показатель указывает на степень окисления, поскольку перекиси являются первыми соединениями, образующимися при окислении жиров.
Методика определения перекисного числа более эффективна для оценки качества насыщенных жиров, чем ненасыщенных. Перекисные соединения, которые образуются в таких ненасыщенных жирах, как свиной и куриный, содержащих достаточно большое количество ненасыщенных жирных кислот, нестабильны и быстро вступают в последующие реакции, образуя вторичные продукты окисления.
В связи с этим получение точных данных по содержанию продуктов окисления является довольно сложной задачей. Хотя перекиси сами по себе не ощущаются органолептически, они являются промежуточными продуктами, которые вступают в новые реакции с образованием кетонов и альдегидов — вторичных продуктов окисления, придающих характерный запах окисленным жирам. В результате перекисное число ненасыщенных жиров может быть небольшим даже при значительной степени окисления.
Таблица 9.Результаты титрования масел.
|
|
Кукурузное масло
|
Рапсовое масло
|
|
Время, мин
|
Результаты титрования, мл
|
Результаты титрования, мл
|
|
0
|
1,354
|
1,394
|
|
20
|
2,024
|
2,575
|
|
40
|
5,724
|
6,984
|
|
60
|
5,252
|
6,354
|
|
80
|
3,362
|
5,016
|
Таблица 10.Значение перекисного числа.
|
|
Кукурузное масло.
|
Рапсовое масло
|
|
Время, мин
|
Значение перекисного числа
|
Значение перекисного числа
|
|
0
|
0,045
|
0,05
|
|
20
|
0,13
|
0,2
|
|
40
|
0,6
|
0,76
|
|
60
|
0,54
|
0,68
|
|
80
|
0,3
|
0,51
|
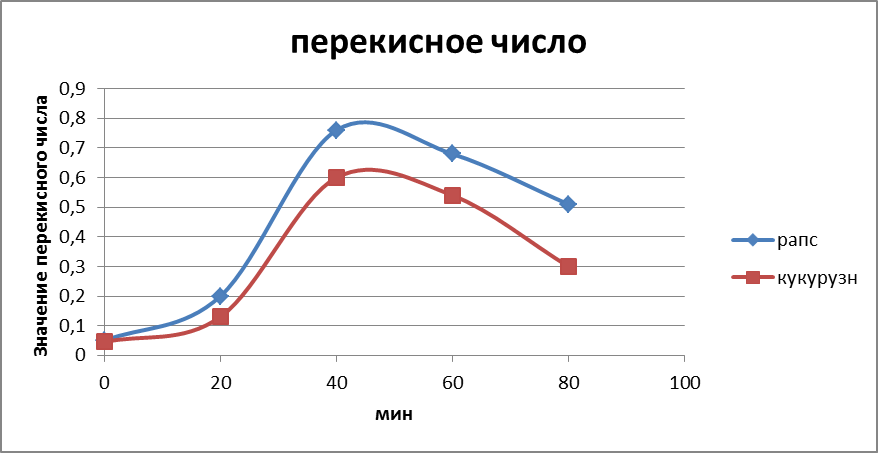
Рис.5. График изменения перекисного числа.
Перекисное число, характеризующее количество перекисных соединений, выражается в миллимолях активного кислорода на килограмм жира (ммоль О/кг).
Образование перекисей на начальных стадиях окисления происходит с небольшой скоростью, зависящей от температуры хранения и присутствия антиоксидантов, однако после достижения «критической массы» начинается экспоненциальное увеличение количества этих соединений.
Также определялось альдегидное число и эпоксидное.
Для рапсового масла: альдегидное число 2,45 ,эпоксидное 5,81
Для кукурузного: альдегидное 2,15 ,эпоксидное 5,06
На основе данных чисел было выбрано рапсовое масло, как наиболее пригодное для дальнейших процессов.
3.2.Изучение физико-химических свойств модифицированных масел.
Эксперименты с растительными маслами с добавлением олеокса.
Так как в процессе предыдущего эксперимента выяснилось, что растительные масла (кукурузное и рапсовое) не смешиваются в однородную систему со взятыми реагентами, то необходимо добавить олеокс в систему.
1.Бралось 20 мл рапсового масла, затем добавлялось 20 мл надуксусной кислоты и 5мл олеокса. При 45 С
2. 20 мл рапсового масла + 10 мл уксусной кислоты +20 мл перекиси + 5мл олеокса при 45С
3. 20 мл рапсового масла, затем добавлялось 20 мл надуксусной кислоты и 5мл олеокса. При 70С
4. 20 мл распового масла + 20 мл перекиси+5 мл олеокса при 45С
5. 10 мл распового масла+ 5 мл уксусной кислоты + 15 мл перекиси +5 мл олеокса при 45С
Йодное число
Таблица 11.результаты титрования смесей.
|
|
20мл масла+20мл к-ты+5мл олеокса
|
20мл масла+10мл укс.кты+20мл перекиси+5мл олеокса
|
Температура 70С
|
20мл масла+20мл перекиси +5мл олеокса
|
10 мл масла+5мл кты+15мл перекиси+5 мл олекоса
|
|
Время, мин
|
|
|
|
|
|
|
0
|
20,3
|
21,01
|
20,13
|
19,66
|
20,75
|
|
20
|
22,6
|
22,12
|
22,18
|
19,96
|
21,97
|
|
40
|
24,5
|
23,14
|
24,15
|
21,2
|
23,11
|
|
60
|
24,67
|
24,39
|
24,59
|
21,68
|
24,07
|
|
80
|
24,86
|
24,46
|
24,81
|
24,01
|
24,46
|
Таблица 12.Значения йодного числа.
|
|
20мл масла+20мл к-ты+5мл олеокса
|
20мл масла+10мл укс.кты+20мл перекиси+5мл олеокса
|
Температура 70С
|
20мл масла+20мл перекиси +5мл олеокса
|
10 мл масла+5мл кты+15мл перекиси+5 мл олекоса
|
|
Время,мин
|
|
|
|
|
|
|
0
|
86,92
|
82,4
|
88
|
91
|
84,1
|
|
20
|
72,33
|
75,4
|
75
|
89,1
|
76,3
|
|
40
|
60,28
|
68,9
|
62,5
|
81,2
|
69,1
|
|
60
|
59,2
|
61
|
59,7
|
78,2
|
63
|
|
80
|
58
|
60,5
|
58,3
|
63,4
|
61,3
|
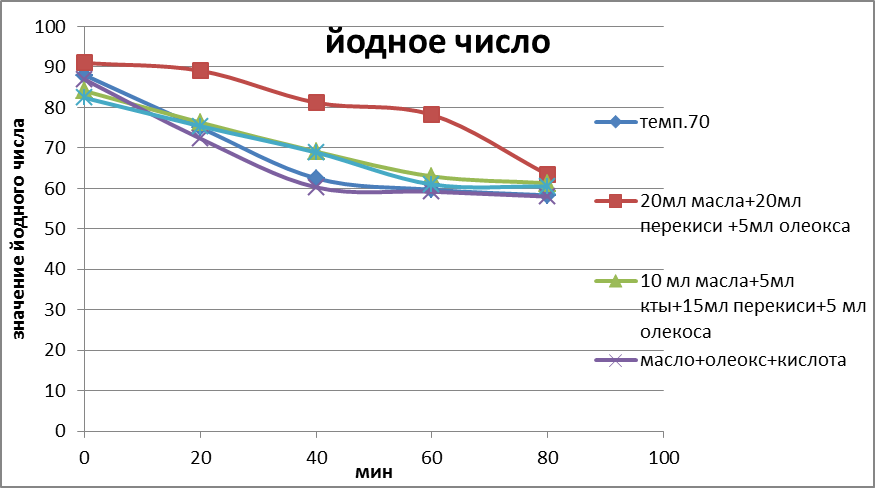
Рис 6. График изменения йодного числа.
Как видно из графика, наибольшее количество двойных связей образуется при варианте без добавления кислоты.
Перекисное число.
Таблица 13.Результаты титрования смесей.
|
|
20мл масла+20мл к-ты+5мл олеокса
|
20мл масла+10мл укс.кты+20мл перекиси+5мл олеокса
|
Температура 70С
|
20мл масла+20мл перекиси +5мл олеокса
|
10 мл масла+5мл кты+15мл перекиси+5 мл олекоса
|
|
Время,мин
|
|
|
|
|
|
|
0
|
4,008
|
3,504
|
4,15
|
4,008
|
3,63
|
|
20
|
5,504
|
3,583
|
5,74
|
5,55
|
3,677
|
|
40
|
5,283
|
5,346
|
5,425
|
5,394
|
5,49
|
|
60
|
5,22
|
5,252
|
5,252
|
5,28
|
5,315
|
|
80
|
2,937
|
5,063
|
5
|
5,22
|
5,126
|
Таблица 14.Значения перекисного числа.
|
|
20мл масла+20мл к-ты+5мл олеокса
|
20мл масла+10мл укс.кты+20мл перекиси+5мл олеокса
|
Температура 70С
|
20мл масла+20мл перекиси +5мл олеокса
|
10 мл масла+5мл кты+15мл перекиси+5 мл олекоса
|
|
Время,мин
|
|
|
|
|
|
|
0
|
0,191
|
0,159
|
0,2
|
0,191
|
0,167
|
|
20
|
0,286
|
0,164
|
0,301
|
0,289
|
0,17
|
|
40
|
0,272
|
0,276
|
0,281
|
0,279
|
0,285
|
|
60
|
0,268
|
0,27
|
0,27
|
0,272
|
0,274
|
|
80
|
0,25
|
0,258
|
0,254
|
0,268
|
0,262
|
|
|
|
|
|
|
|
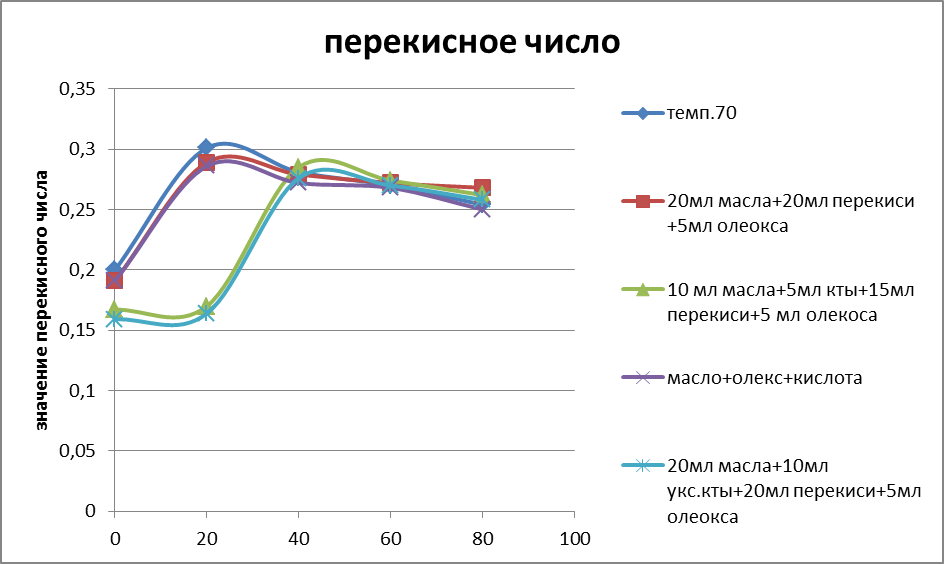
Рис.7.График изменения перекисного числа
Таблица 15. Значения альдегидного и эпоксидного чисел.
|
|
20мл масла+20мл к-ты+5мл олеокса
|
20мл масла+10мл укс.кты+20мл перекиси+5мл олеокса
|
Температура 70С
|
20мл масла+20мл перекиси +5мл олеокса
|
10 мл масла+5мл кты+15мл перекиси+5 мл олекоса
|
|
А.Ч
|
3,29
|
3
|
3,1
|
2,5
|
3,2
|
|
Э.Ч
|
4,11
|
6,4
|
3,99
|
7,2
|
6,6
|
По проведенным опытам, оптимальным вариантом выбран синтез №4 , 20 мл распового масла + 20 мл перекиси+5 мл олеокса при 45С.
3.3.Оптимизация технологических режимов дубления с использованием модифицированных масел.
По данным, представленным выше, выбран наиболее успешный метод синтеза.
20мл рапсового масла+ 20 мл перекиси водорода +5мл олеокса.
Альдегидное число- 2,5
Эпоксидное число-7,2
Йодное число-81
На основе выбранного модифицированного масла проводилось производство замши по следующим методикам.
Для каждой партии бралось по три образца из голья золеного.
1 методика
Объекты. Окисленное масло в присутствии олеокса
Голье после золения, съема лицевой поверхности и обжорного золения:
Тсв –32 С
1. Промывка: ж.к. 2,5 30°С 10 мин
2. Обеззоливание: ж.к. 1,2 35°С Сульфат аммония 2,5 % 45 мин
Контроль обеззоливиния на ФФ Протосубтилин 1,5% 20 мин
3. Отжим
Контроль Тсв -37С
4. Дубление 1 вариант;
ж.к. 0,6 35°С Хлорид натрия 3 % 30 мин
Ортан 4% 2 часа
Контроль Тсв – 45С
Окисленное масло 5% 4 часа
Контроль Т св 2 часа -50С
Контроль Т Св 4 часа -52С
оставить на ночь в растворе
на второй день обработать в отработанном растворе подогретом до 60°С в течение 6 часов
Контроль Т св 2 часа – 56С
Контроль Т св 4 часа -60С
Контроль Т св 6 часа -65С
5. Обезжиривание: ж.к. 4 40°С
Карбонат натрия 3 %
неонол 0,2% 30 мин
Карбонат натрия 3 %
неонол 0,2% 30 мин
Карбонат натрия 3 %
неонол 0,2% 30 мин
Сушка взавес 24 часа подшлифовка
2 Методика
Объекты. Модифицированное масло
Голье после золения, съема лицевой поверхности и обжорного золения:
Тсв –32 С
1. Промывка: ж.к. 2,5 30°С 10 мин
2. Обеззоливание: ж.к. 1,2 35°С Сульфат аммония 2,5 % 45 мин
Контроль обеззоливиния на ФФ
Протосубтилин 1,5% 20 мин
3. Отжим
Контроль Тсв -37С
4. Пикелевание: ж.к.1 20°С NaCl 10%
НСООH 2% 2 часа
Контроль рН - 3, Т св-40С
Обработка глутаровым альдегидом 1,5% (1:3) 2 часа,
Т св -48С
Фиксация формиат натрия 1% (1:20)
карбонат натрия 1% (1:20) 40 мин Контроль рН - 8, Т св-52С
Пролежка на ночь
Промывка на проточной воде 10 мин
Дубление: ж.к. 1,5 45 °С карбонат натрия 0,5%
окисленное масло 15% 6 часов
Контроль Т св 2 часа-57С
Контроль Т св 4 часа-62С
Контроль Т св 6 часа-67С
оставить на ночь
с утра 1 час, Т св-70С
Завесить на 3 суток
Мойка: ж.к. 2 карбонат натрия 3%
Неонол 0,2%
в три приема со сливом жидкости
Сушка взавес 24 часа Подшлифовка
3 Методика
Объекты. Модифицированное масло
Голье после золения, съема лицевой поверхности и обжорного золения:
Тсв –32 С
1. Промывка: ж.к. 2,5 30°С 10 мин
2. Обеззоливание: ж.к. 1,2 35°С
Сульфат аммония 2,5 % 45 мин
Контроль обеззоливиния на ФФ
Протосубтилин 1,5% 20 мин
3. Отжим
Контроль Тсв -37С
4. Пикелевание: ж.к.1 20°С NaCl 10%
НСООH 2% 2 часа
Контроль рН - 3, Т св-40С
Обработка ортаном 4% 2 часа,
Т св -42С
Фиксация формиат натрия 1% (1:20)
карбонат натрия 1% (1:20) 40 мин Контроль рН - 8, Т св-44С
Пролежка на ночь
Промывка на проточной воде 10 мин
Дубление: ж.к. 1,5 45 °С карбонат натрия 0,5%
окисленное масло 15% 6 часов
Контроль Т св 2 часа-48С
Контроль Т св 4 часа-52С
Контроль Т св 6 часа-55С
оставить на ночь
с утра 1 час, Т св-60С
Завесить на 3 суток
Мойка: ж.к. 2 карбонат натрия 3%
Неонол 0,2%
в три приема со сливом жидкости
Сушка взавес 24 часа Подшлифовка
По органолептическому анализу, наиболее успешным является методика №2, с пикелеванием и добавлением глутарового альдегида, так как полуфабрикат получился наиболее мягкий и приятный на вид.
3.4. Исследование потребительских свойств замши
Выделанную замшу подвергали физико-химическим испытаниям , в связи с показаниями ГОСТ3774-84.Брались три образца, по одному из каждого метода дубления. Проводились опыты по учебному практикуму [10]
Далее представлена таблица о полученных данных
Таблица 16. Физико-химические показатели выделанной замши.
|
|
Голье с пикелеванием
|
Непикелеванное голье
|
Голье, обработанное без глутарового альдегида
|
|
Толщина,мм
|
1,1
|
1
|
0,9
|
|
рН водной вытяжки
|
4,0
|
4,3
|
4,4
|
|
Содержание золы,%
|
1
|
1,2
|
1,3
|
|
Предел прочности на разрыв при напряжении 10 МПа (%)
|
0,7
|
0,9
|
0,3
|
|
Удлинение при разрыве, при напряжении 10 МПа (%)
|
19
|
30
|
14
|
|
Намокаемость,%
2 часа
|
80
|
95
|
67
|
|
Намокаемость,%
24 часа
|
110
|
127
|
100
|
|
Жесткость на ПЖУ,Н
|
0,2
|
0,18
|
0,3
|
Данные в таблице показывают, что достаточно многие показатели удовлетворяют показатели ГОСТа, но не во всех методиках. Нужно работать над такими свойствами, как предел прочности, удлинение при разрыве. Наиболее успешной являются также показатели второй методики, пикелеванное голье с глутаровым альдегидом.
Заключение.
На основе исследований влияния различных окислителей на кинетику модифицирования олеокса установлено, что наибольшая степень окисления у надуксусной кислоты.
Эксперименты окисления растительных масле в исходном состоянии не позволяют добиться высокой степени окисления.
Введение в реакционную смесь олеокса показывает максимальный эффект окисления за счет образования гетерогенной системы.
В результате работ разработаны режимы окисления олеокса, позволяющие получить конечный продукт с максимальными значениями эпоксидного числа.
Проведены сравнительные испытания трех методик жирового дубления с использованием оксиленных масле и показано, что наиболее эффективной является вторая, с пикелеванием и добавлением глутарового альдегида.
Проведен анализ замши, выработанной по этим методикам, и показано, что почти все они соответствуют показателям ГОСТ.
Список используемой литературы
- Михайлов А.Н. Коллаген кожного покрова и основы его переработки. М., Легкая индустрия, 1971
- Zange J., Pauckner W. Untersuchungen zur Neusmischgerbung.- Das Leder, 1979. N 9, S. 152-161
- Elsinger F.J. Rationalisierung in der Samischgerberei.- Leder- und Hautemarkt, 1984, N 24, S. 96-102
- Блажей А.,Шутый Л. Фенольные соединения растительного происхождения. М., Мир, 1977
- Химия и технология кожи и меха: Учебник для вузов- 4-е изд.,- И.П.Страхов, И.С.Шестакова и др.-М., Легпромбытиздат, 1985. -496с.
- Д. И. Метелица, Механизмы реакций прямого эпоксидирования олефинов в жидкой фазе.,- Н. А. Прилежаев, Вег., 42, 4811 (1909); 43, 959 (1910).,-Успехи химии, М., 1972
- Д. И. Метелица, Механизмы реакций прямого эпоксидирования олефинов в жидкой фазе- Н. А. Прилежаев, ЖРФХО, 42, 1397 (1910); 43, 609 (1911); 44, 613 (1912). -Успехи химии, М., 1972
- О.И.Славгородская, В.Г.Бондалетов, Е.П.Фитерер, В.Д.Огородников, Получение эпоксидированных смол по реакции Прилежаева, -Ползуновский вестник №1- 2013
- ГОСТ 3717-84
- Лабораторный практикум по химии и технологии кожи и меха : Учебн.пособие для вузов 3-е изд., перераб. и доп.- Головтеева А.А, Д.А. Куциди, Л.Б. Санкин – М., Легпромбытиздат, 1987 – 312с.
- 4.Grynyshy O, Bratychak M., Krinitskiy V. Petroleum resins for bitumens modifications. // Chemistry and Chemical Technology. – 2008. – Vol.2. – №1. – Р.47-53.
- 5. Братичак М.М., Гагiн М.Б., Гринишин О.Б., Гевусь О.I. Синтез нафтополiмерних смол з епоксидними групами в присутностi 1,2-епокси-3- трет-бутилпероксипропану // Док. Нац. АН Украiни. – 2002. – № 9. – С. 141-143.
- 6.В.В.Жебровский. Технология синтетических смол, применяемых для производства лаков и красок. – М.: Высшая школа.ю 1968. – 128с.
- 7.Чайковский Т.В. Эпоксидирование ненасыщенных углеводородов фракции С5 органическими пероксидами: автрореф. дис. … канд. тех. наук. – Львов, 2008. – 17с.
- 8.Руководство к практическим работам по химии полимеров: Учеб. пособие / Под ред. В. С. Иванова. — Л.: Изд-во Ленингр. ун-та, 1982.— 176
- Бондалетов О.В., Бондалетова Л.И, Огородников В.Д. Использование циклопентадиеновой фракции жидких продуктов пиролиза в синтезе модифицированных нефтеполимерных смол // Известия Томского политехнического университета. – 2010. – № 3. –С. 77-82.
- Bratychak M., Grynyshyn О., Shyshchak О. Obtaining of petroleum resins using pyrolysis by-products // Ecological Chemistry and Engeneering. – 2007 – Vol.14 – №2. – Р.325-328.
- Machmuller, G., Metzger J.O., Klaas, M.R., Schafer, H.J., Schneider, M.P., 2000. New syntheses with oils and fats as renewable raw materials for the chemical industry Angew. Chem. Int. Ed. 39, 2206–2224.
- Petrovic, ZS Zlatanic, A Lava, CC and Sinadinovic-Fiser, S 2002; Epoxidation of soybean oil in toluene with peroxy acetic and peroxy formic acids-kinetics and side reactions, European Journal of Lipid Science and Technology, Vol 104, no.5, p.p 293-299.
- Epoxidation of karanja(Pongamia Glabra) oil by hydrogen peroxide J. Am. Oil Chem. Soc. 83, 635–640.
- Edy Purwanto, ‘The synthesis of polyols from RBO through epoxidation and hydroxylation reaction’. Master of Engineering Science Thesis July 2010.
Исследование кинетики окисления олеокса и растительных масел в присутствии различных соединений и определение их эффективности