Тепломасообмін у двокомпонентних середовищах
Тепломасообмін у двокомпонентних середовищах. Загальні відомості. У виробничих процесах відбуваються різноманітні масообмінні процеси: сушіння, абсорбція, адсорбція, екстракція, дистиляція, випаровування, розчинювання, кондиціонування повітря.
Будь-яке середовище може складатися з елементарних часток одного виду або різних видів (різної хімічної природи). Компонентом середовища називають будь-яку хімічно індивідуальну речовину. Частина неоднорідної термодинамічної системи, що обмежена поверхнями поділу, називається фазою. Наприклад, при випаровуванні слід розрізняти рідку і пароподібну фази, що розділені поверхнею випаровуваної рідини. Фаза може характеризуватися рівномірним чи нерівномірним розподілом її компонентів в об’ємі.
Двофазні потоки називаються гомогенними, якщо фази розподілені рівномірно в об’ємі, якщо ж нерівномірно, то потік буде гетерогенним. Двофазні потоки називаються адіабатними, якщо між потоком і поверхнею каналу чи огородженням і між фазами немає теплообміну. За наявності теплообміну з поверхнею каналу (огородження тощо) потік називається діабатним. Якщо фази мають однакову температуру, то потік буде термодинамічно рівноважним.
В ізобарно-ізотермічних умовах вирівнювання компонента відбувається під впливом хімічного потенціалу. Хімічним потенціалом називають приріст внутрішньої енергії фази системи при збільшенні маси даного компонента на одиницю, якщо ентропія, об’єм і маси всіх інших компонентів фази залишаються постійними.
Масообміном називають довільний необоротний процес перенесення маси даного компонента у просторі з неоднорідним полем хімічного потенціалу цього компоненту (у найпростішому випадку – з неоднорідним полем парціального тиску або полем температур цього компонента).
Масообмін через поверхню поділу або проникну стінку між двома речовинами чи фазами називають масопередачею. Наприклад, проникнення повітря крізь огородження, інфільтрація крізь щілини тощо. Поверхню поділу фаз, що беруть участь у масообміні, називають поверхнею масообміну.
Для характеристики інтенсивності масообміну використовують поняття потоку маси і густини потоку маси. Під потоком маси даного компонента суміші , кг/с, розуміють його масу, що проходить за одиницю часу крізь довільну поверхню. Потік маси, віднесений до одиниці площі поверхні, називають густиною потоку маси , кг/(м2 с). Вектор густини потоку визначають як вектор, що проходить крізь площину, перпендикулярну до обраного напрямку.
Відношення об’ємної витрати компонента до перерізу каналу називають зведеною швидкістю , м/с. Швидкість суміші , м/с, дорівнює сумі зведених швидкостей компонентів. Відношення масової витрати суміші до площі перерізу каналу називають масовою швидкістю , кг/(м2 с), де і – відповідно густина і швидкість середовища.
Сукупність миттєвих значень концентрації компонентів у середовищі називають концентраційним полем: . Воно може бути однорідним або неоднорідним. У першому випадку концентрація компонента постійна в об’ємі фази, тобто = const. У другому випадку – = var. Крім того, поле може бути стаціонарним (незмінюваним у часі) або нестаціонарним (змінюваним у часі). Сукупність точок неоднорідного концентраційного поля, де компоненти мають однакову концентрацію, утворює ізоконцентраційну поверхню.
Перенесення маси подібне до перенесення теплоти. Теплота передається в напрямку зменшення температури; маса, звичайно, переноситься у напрямку меншої концентрації. Подібно до теплообміну масообмін може відбуватися як шляхом молекулярної дифузії, так і конвекцією. У більшості практичних випадків процеси теплообміну супроводжуються перенесенням маси тієї чи іншої інтенсивності і, таким чином, обидва процеси виявляються взаємопов’язаними.
Використання хімічного потенціалу як рушійної сили на практиці незручне, оскільки його, як правило, не можна виміряти безпосередньо. Тому в розрахунках рушійну силу звичайно виражають через відповідні градієнти (концентрації, тиску, температури).
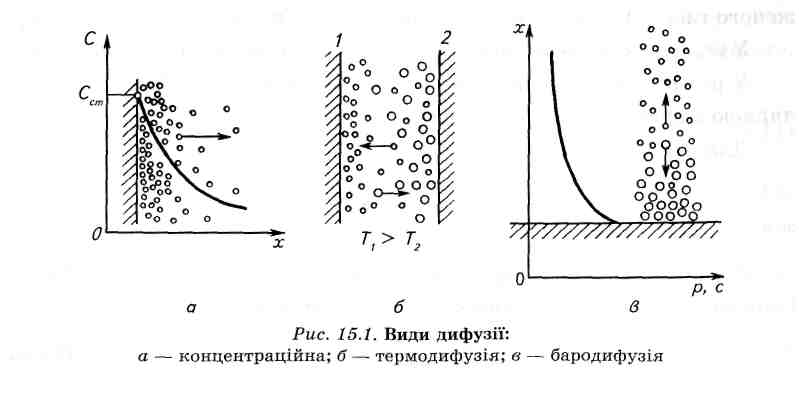
Дифузія у двокомпонентних середовищах. Перенесення речовини у суміші зумовлене тепловим рухом мікрочасток (наприклад, молекул), називається молекулярною дифузією. Молекулярну дифузію, спричинену неоднорідним розподілом концентрацій компонентів у суміші, називають концентраційною дифузією (рис. 15.1, а). При постійних температурі і тиску густина потоку маси дифундуючого компонента прямо пропорційна градієнту його концентрації (закон Фіка):
, (15.1)
де – вектор густини потоку маси, кг/(м2 с); – коефіцієнт дифузії, м2/с; С — концентрація розподілюваного компонента, кг/м3.
Градієнт концентрації – це вектор, спрямований по нормалі до ізоконцентраційної поверхні в бік збільшення концентрації. Чисельно він дорівнює частинній похідній від концентрації за цим напрямом:
, (15.2)
де – одиничний вектор, спрямований по нормалі в бік зростання концентрації.
Коефіцієнт дифузії дорівнює кількості маси, що пройшла за одиницю часу через одиницю поверхні, нормальну векторові дифузійного потоку, якщо градієнт концентрації дорівнює одиниці. Знак мінус у рівнянні враховує, що вектори і спрямовані у протилежні боки.
Рівняння (15.1) подібне до основного закону теплопровідності (закону Фур’є). Для нерухомого середовища ( = 0), якщо немає внутрішніх джерел маси ( = 0) і коефіцієнт дифузії постійний, диференціальне рівняння дифузії запишеться аналогічно відповідному рівнянню теплопровідності, тобто
(15.3)
або
. (15.4)
У цих рівняннях – декартові координати; – час.
Рівняння (15.3) можна записати також для одно- чи двовимірних процесів дифузії.
Інтегрування (15.3), за умов однозначності, що відповідають тому чи іншому реальному процесу, дає функцію . Як і для теплопровідності, умови однозначності складаються з фізичних, геометричних, граничних і початкових умов.
Якщо у середовищі є різниця температур, то легші молекули, що мають більшу рухомість, прагнуть перейти у теплі області, а важкі молекули – у холодні. Це так званий ефект Соре. У даному випадку має місце термодифузія (рис. 15.1, б). Поступово встановлюється стаціонарний стан, при якому врівноважуються вплив термодифузії та концентраційної дифузії. Якщо в нерухомому середовищі наявний градієнт тиску, то важкі молекули переходять в області високого тиску, а легкі – в області зниженого тиску. Цей вид дифузії називається бародифузією (рис. 15.1, в). У технічних процесах переважає, як правило, концентраційна дифузія.
У рухомому середовищі речовина переноситься не тільки молекулярною дифузією, а й конвекцією.
Для певного компонента суміші
, (15.5)
де – густина компонента.
Сумарна густина потоку компонента за рахунок молекулярного і конвективного перенесення визначиться рівнянням:
. (15.6)
Диференціальні рівняння тепломасообміну. Критерії подібності. Потрійна аналогія. Розглянемо систему диференційних рівнянь, які описують розподіл одного компонента в середовищі що рухається. Середовище приймаємо як таке, що нестислеве і без джерел маси в середині його. Крім того, вважаємо, що маса переноситься за рахунок концентраційної дифузії і конвекції. В наближенні теорії пограничного шару маємо:
рівняння нерозривності:
; (15.7)
рівняння руху:
; (15.8)
рівняння дифузії:
; (15.9)
рівняння енергії:
. (15.10)
Якщо гравітаційні сили відсутні (або малі), повздовжній градієнт тиску , теплофізичні властивості приймаються постійними, то система рівнянь матиме вигляд:
; (15.11)
; (15.12)
; (15.13)
. (15.14)
У цих рівняннях, крім зазначених уже позначень, прийняті позначення і – питомі теплоємності при постійному значені компонентів суміші; – середнє значення питомої теплоємності; – оператор Лапласа.
У практичних задачах велике значення має конвективний масообмін між рідиною та твердою поверхнею і навколишнім середовищем. За аналогією з тепловіддачею такий масообмін називають масовіддачею.
Для кількісного опису масовіддачі використовують закон масовіддачі:
, (15.15)
де – густина потоку маси від поверхні поділу фаз у ядро потоку (або навпаки), кг/(м2 с); – коефіцієнт масообміну, м/с; , – концентрації розподіленої речовини відповідно біля поверхні поділу фаз і в ядрі потоку (середовища), кг/м3.
Величина, обернена коефіцієнтові масообміну, має назву дифузійного опору пограничного шару: .
На основі теорії подібності з математичного опису маємо критерії подібності:
масообмінне число Нуссельта ;
критерій (число) Рейнольда ;
критерій (число) Прандтля для масообміну , де – визначальний (характерний) розмір, м; – кінематична в’язкість, м2/с.
Число дорівнює відношенню опору дифузії пограничного шару до опору масопередачі тобто .
Критерій характеризує фізичні властивості середовища, істотні для масовіддачі.
Критеріальне рівняння конвективного масообміну при вимушеному русі середовища звичайно записується у формі степеневої функції:
, (15.16)
де – дослідні константи.
Якщо розглядати сумісно рівняння масообміну, енергії та руху, то легко виявити спільність форми запису їх. Коефіцієнти рівнянь мають одну й ту саму розмірність – квадратний метр на секунду. Сукупність цих трьох рівнянь називається потрійною аналогією.
Контрольні запитання
1. Що називають компонентом багатофазного середовища?
2. Дайте означення хімічного потенціалу.
3. Що таке масообмін, масопередача, потік і густина потоку маси, концентраційне поле (однорідне, неоднорідне, стаціонарне, нестаціонарне), ізоконцентраційна поверхня?
4. Сформулюйте закон концентраційної дифузії і розкрийте фізичний зміст коефіцієнта дифузії.
5. У чому проявляється взаємозв’язок процесів дифузії і теплопровідності?
6. Охарактеризуйте процеси термо- і бародифузії.
7. Запишіть диференціальне рівняння тепломасообміну, а також закон масовіддачі.
8. Дайте означення коефіцієнта масообміну.
9. Як обчислюють коефіцієнт масообміну? Який фізичний зміст критеріїв ?
Тепломасообмін у двокомпонентних середовищах