ВОССТАНОВЛЕНИЕ ДЕТАЛЕЙ ЭЛЕКТРОЛИТИЧЕСКИМИ И ХИМИЧЕСКИМИ ПОКРЫТИЯМИ
ВОССТАНОВЛЕНИЕ ДЕТАЛЕЙ ЭЛЕКТРОЛИТИЧЕСКИМИ И
ХИМИЧЕСКИМИ ПОКРЫТИЯМИ
Основные принципы электролиза.
Электролитическое наращивание металлов основано на явлении электролиза – химического процесса, происходящего при прохождении постоянного тока через электролит 2, которым служит раствор солей металла, наращиваемого на изношенную деталь. Электроды 3 и 4 опущены в электролит и подключены к источнику питания 1. Под действием постоянного тока молекулы раствора расщепляются на положительно заряженные частицы (катионы), которые перемещаются к отрицательному электроду 3 (катоду), и отрицательно заряженные частицы (анионы), перемещающиеся к положительному электроду 2 (аноду).
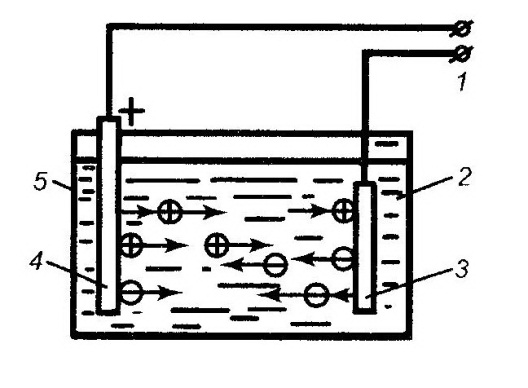
Рис. 4.58. Схема электролитического наращивания металла: 1 – источник питания; 2 – электролит; 3 – катод; 4 – анод: 5 – ванна.
Положительно заряженные ионы металла получают от катода недостающие электроны, разряжаются и осаждаются на нем в виде нейтральных атомов металла. На катоде происходит также выделение водорода. Анионы, взаимодействуя с анодом, теряют свой электрический заряд и превращаются в нейтральные атомы. В результате на нем выделяются кислород и кислотные остатки. Процесс электролиза происходит непрерывно, так как электролит постоянно пополняется новыми ионами за счет растворения анода.
Катодом является деталь, а анодом в большинстве случаев — пластины из металла, подлежащего осаждению. Для получения качественных покрытий площадь анода должна в 2—3 раза превышать площадь покрываемых поверхностей деталей. Металл анода растворяется, и его атомы образуют новые ионы металла, переходящие в раствор взамен выделенных на катоде. Вместо растворимых анодов (медь, железо, никель и др.) применяют и нерастворимые (свинец, уголь), например при хромировании. В этом случае раствор соли по мере протекания процесса непрерывно обедняется и поэтому должен периодически обогащаться.
Согласно законам Фарадея, масса металла, осажденного на катоде, прямо пропорциональна количеству электричества (току, умноженному на время), прошедшего через электролит, а количество вещества, осажденного при прохождении тока через электролит, прямо пропорционально его эквивалентной массе. Аналитически это выражается зависимостью
G = сIТ,
где G - теоретическое значение массы осажденного металла, кг; с - электрохимический эквивалент, кг/А ч; I - ток, А; Т - продолжительность электролиза, ч.
Из-за примесей в электролите и других факторов действительная масса осажденного металла меньше теоретической. Отношение фактической массы к теоретической называется выходом по току (КПД ванны). Выход по току при хромировании составляет 0,12—0,18, а при других электролитических процессах 0,60—0,90.
Таким образом, действительная масса осажденного металла
G = сIТ,
а средняя толщина h покрытия
h = cIT/F,
где F— площадь покрытия, м2; — плотность осажденного металла, кг/м3.
Учитывая, что катодная плотность тока Dк = I/F (А/м2), и h = cDкT/,
Следовательно, длительность процесса электролиза
T = h/cDк.
Хорошее качество покрытия обеспечивается только при определенном соотношении температуры электролита и катодной плотности тока, свойственных данному электролитическому процессу и составу электролита.
Из электролитических способов нанесения покрытий в промышленности применяются хромирование, осталивание (железнение), омеднение, никелирование, кадмирование, оцинкование, лужение, алитирование, свинцевание и др. Они служат для повышения износостойкости, восстановления изношенных поверхностей деталей (хромирование, железнение и др.), защиты деталей от коррозии (цинкование, оксидирование, фосфатирование и др.), защитно-декоративных целей (никелирование, хромирование, цинкование, оксидирование и др.), улучшения прирабатываемости трущихся поверхностей деталей (меднение, лужение, свинцевание и пр.), защиты от науглероживания при цементации (меднение). Часто покрытия имеют многоцелевое назначение.
Технологический процесс гальванического нанесения покрытий
Технологический процесс нанесения любого гальванического покрытия включает три этапа:
—подготовка поверхностей детали к нанесению покрытия;
—нанесение покрытия;
—обработка нанесенного покрытия.
Подготовка деталей к покрытию. Она заключается в проведении: механической обработки покрываемых поверхностей, обезжиривании обработанных поверхностей и их активации (химическая или анодная). Качество выполнения операций подготовительного этапа в значительной степени определяет прочность сцепления электролитического покрытия с поверхностью детали и его сплошность.
Механическая обработка в зависимости от назначения покрытия может осуществляться шлифованием, пескоструйной обработкой и полированием. Шлифование необходимо для придания восстанавливаемой поверхности правильной геометрической формы, а полирование — для получения необходимой шероховатости поверхности.
При подготовке к нанесению противокоррозионных покрытий детали обычно обрабатывают металлическим песком в металлопескоструйных установках. Мелкие детали иногда подвергают обработке в галтовочных барабанах.
Детали, подлежащие покрытию с декоративной целью, шлифуют и полируют на шлифовально-полировочных станках. Полирование обычно проводят мягкими бязевыми кругами с полировальной пастой, нанесенной на их поверхность.
Обезжиривание деталей проводят в два этапа — предварительно и окончательно. Предварительное обезжиривание обеспечивается промывкой деталей органическими растворителями: уайт-спиритом, четыреххлористым углеродом, чистым бензином и др. Проводят также механическую очистку венской известью, состоящей из смеси окиси кальция и окиси магния с добавлением 3%-ной кальцинированной соды и 1,5%-ного едкого натра. Эту смесь разводят водой до кашицеобразного состояния и наносят на поверхность детали кистью. Венская известь обладает хорошей адсорбцией и способствует полному удалению жиров и масел. Так обезжиривают детали простой формы, а также громоздкие детали, у которых гальванические покрытия наносятся на небольшие участки поверхности.
Окончательное обезжиривание проводят в щелочных растворах (химическим или электрохимическим способами). В первом случае деталь погружают в горячий щелочной раствор при температуре 60 °С на 5—6 мин. Недостатком обезжиривания поверхностей деталей в щелочных растворах является нагревание деталей и необходимость хорошей их промывки в горячей воде. При электрохимическом обезжиривании детали погружают на 1—2 мин в нагретый до 70—80 °С щелочной раствор, через который пропускают ток плотностью 5—10 А/дм2. При этом деталь является катодом, а анодом служат пластины из малоуглеродистой стали. Электрохимическое обезжиривание более производительно, так как кроме химического воздействия на жировую пленку происходит ее механическое разрушение образующимися на поверхности детали пузырьками водорода. Во избежание насыщения поверхности детали водородом в конце обезжиривания изменяют полярность тока на обратную и проводят обработку в течение 0,2—0,3 мин.
После обезжиривания детали промывают в горячей, а затем холодной воде.
Обезжиренные, промытые горячей водой детали быстро окисляются, что может привести к некачественному сцеплению покрытия с деталью. Поэтому непосредственно перед нанесением покрытия проводится активация — удаление тонких окисных пленок, образовавшихся в процессе подготовки деталей к гальваническому нанесению покрытий, с легким протравливанием поверхностного слоя металла. Эта операция обеспечивает наиболее прочное сцепление гальванического покрытия с поверхностью детали.
Активация возможна химическим или электрохимическим способами.
Химическую активацию деталей из малоуглеродистых и углеродистых сталей проводят в 3—5%-ном растворе серной кислоты. Для активации сталей с высоким содержанием хрома используют 5—10%-ный раствор соляной кислоты, чугунов — 3—5%-ный раствор плавиковой кислоты, а для активации меди и ее сплавов 5—10%-ный раствор серной кислоты.
Электрохимическая активация (анодная обработка или декапирование) состоит в протравливании поверхностей деталей на аноде в растворах серной, фосфорной или хромовых кислот. Например, при подготовке к хромированию активацию проводят в том же электролите, в котором выполняется хромирование. Активация длится 30—45 с при анодной плотности тока 20— 40 А/дм2. После этого, не вынимая деталь из электролита, ее подключают к катоду и производят хромирование. Поверхности деталей, не подлежащие восстановлению, изолируют с помощью синтетических материалов.
Содержание каждого из этапов может изменяться в зависимости от свойств и назначения гальванического покрытия. Например, при железнении активацию анодной обработкой проводят в специальной ванне с 30%-ным водным раствором серной кислоты в течение 2—3 мин при температуре 18—25 °С и анодной плотности тока для стальных деталей 60—70 А/дм2, а деталей из чугуна 10—15 А/дм2. После завершения активации детали промывают в холодной, а затем в горячей воде с температурой 50—60 °С, близкой к температуре электролита в ванне для железнения.
Обработка после нанесения покрытия включает в себя ряд операций: нейтрализацию остатков электролита, промывку деталей в воде, удаление изоляции, сушку деталей, при необходимости термическую обработку, механическую обработку для получения требуемого размера и шероховатости поверхности. Порядок выполнения заключительных операций сохраняется при гальваническом нанесении любых покрытий, однако каждый гальванический процесс имеет некоторые особенности.
Восстановление деталей хромированием
Характеристика метода. Гальваническое хромирование является одним из распространенных технологических процессов восстановления деталей. Покрытия из хрома обладают высокими износостойкостью и химической стойкостью, не корродируют и не чувствительны к нагреву до 400 °С. Твердость хромовых покрытий достигает 850—1200 единиц по Виккерсу, а прочность сцепления хрома со сталью, чугуном, медью на сдвиг — до 300 МПа.
Хромовое покрытие увеличивает срок службы деталей до 5 раз. Поэтому оно применяется для восстановления номинальных размеров изношенных деталей, обеспечения их износостойкости, защитно-декоративных и др. целей. Например, иногда детали подвергают хромированию перед закалкой. Такие детали после термической обработки не имеют окалины, поэтому отпадает необходимость их очистки.
Хромирование выполняют при напряжении 6—12 В и плотности тока не менее 2*103 А/м2. В зависимости от его назначения хромирование подразделяется на гладкое и пористое. Свойства хромовых покрытий зависят от состава и температуры электролита, катодной плотности тока. Изменяя соотношение плотности тока и температуры, можно получить различные по свойствам гладкие хромовые покрытия: блестящие, молочные и матовые.
Блестящие покрытия имеют высокую твердость (до 9000 МПа), повышенную износостойкость и хрупкость. На их поверхности образуется сетка пересекающихся трещин, видимых под микроскопом. Такое покрытие получается при температуре электролита свыше 65 °С. Молочные покрытия создаются при повышенной плотности тока и температуре электролита 45— 65 °С. Обладая высокой износостойкостью, они по сравнению с блестящими покрытиями имеют повышенную вязкость и в 1,5 раза меньшую твердость, благодаря чему сетка трещин на них не образуется. Из-за отсутствия трещин такие покрытия эффективны при повышенных требованиях к коррозионной стойкости деталей.
Матовые или серые покрытия образуются при низкой температуре электролита и повышенной плотности тока. Они характеризуются максимальной твердостью (до 12000 МПа) и хрупкостью, имеют пониженную износостойкость и поэтому в ремонтных целях практически не применяются. Образование матовых покрытий часто считается браком при хромировании. Поэтому в ремонтном производстве из гладких применяются блестящие и молочные покрытия. Для деталей неподвижных соединений (посадки подшипников качения на валах и др.) используются оба вида покрытия. Для трущихся деталей, работающих при небольших давлениях (до 0,5 МПа), рекомендуются блестящие покрытия, а для работающих при больших давлениях и знакопеременной нагрузке — молочные.
Пористое хромовое покрытие обладает повышенной износостойкостью благодаря лучшим условиям смазки и поэтому находит широкое применение в машиностроении и ремонтном производстве. Оно особенно эффективно при высоком удельном давлении и повышенной температуре в трущейся паре. Необходимая пористость слоя хрома может быть создана механическим, химическим и электрохимическим способами. При механическом способе перед хромированием на поверхности детали наносятся углубления в виде каналов или пор, которые сохраняются после осаждения хрома. При таком способе отпадает необходимость в анодной обработке покрытия хрома. Химическим способом пористость достигается путем травления блестящего хромового покрытия в соляной кислоте. Электрохимическим способом пористое покрытие получается за счет анодной обработки такого покрытия.
Анодная обработка для образования пор производится в электролите того же состава, что и хромирование, при плотности тока 40—50 А/дм2 и температуре электролита 50 °С. Деталь в этом случае является анодом. При обработке в течение 10 мин глубина пор составляет 0,05 мм. После анодной обработки детали промываются в проточной воде и проверяется качество покрытия.
Основными характеристиками пористого покрытия являются твердость, износостойкость, пористость, маслоемкость, которые весьма важны для деталей, работающих в условиях граничного трения (шейки валов, валики насосов и др.). Поскольку хром по хрому работает плохо, т.е. с большим износом обеих деталей, то хромируется только одна из сопряженных деталей трущейся пары. Более износостойкими являются покрытия, имеющие пористость 30—40 % площади поверхности.
К недостаткам хромирования и хромовых покрытий относятся:
—длительность процесса, что связано с малой скоростью осаждения металла (за 1 ч наносится слой хрома толщиной 0,01—0,03 мм);
—возможность наносить покрытия небольшой толщины, так как при толщине свыше 0,3—0,4 мм они менее износостойки, а при толщине свыше 0,5 мм склонны к отслаиванию;
—низкий (12—18 %) выход по току;
—значительное снижение усталостной прочности восстановленных деталей;
—относительно высокая стоимость восстановления;
—сравнительно низкая шероховатость покрытой поверхности;
—вредные условия труда.
При хромировании деталей, работающих в условиях знакопеременных нагрузок, следует учитывать, что их усталостная прочность понижается на 15—25 %. Это происходит вследствие значительных напряжений растяжения в поверхностном слое детали.
Этот недостаток проявляется в меньшей мере при ведении процесса хромирования на токе переменной полярности. Варьируя величиной продолжительности между переключениями полярности, можно уменьшить шероховатость поверхности покрытия и обеспечить в нем незначительные по величине остаточные напряжения растяжения, а следовательно, и несущественное понижение усталостной прочности, что важно для деталей, работающих в условиях знакопеременных нагрузок.
Подготовка деталей к хромированию проводится по описанной выше общей технологии нанесения гальванических покрытий. Поверхности, не подлежащие покрытию хромом, изолируют целлулоидным лаком, а отверстия в детали закрывают свинцовыми пробками. Лучшие результаты обеспечивает обезжиривание деталей электролитическим способом при следующем составе электролита: 100 г NaOH, 2—3 г Na2Si03 (жидкое стекло), 1 л воды. При этом анодом служит железная пластина, а катодом — очищаемые детали. Процесс обезжиривания длится 5—6 мин при плотности тока (5—7) 102 А/м2, напряжении 5—6 В и температуре раствора 65—70 °С. После этого детали промывают в горячей воде, выдерживают для удаления окислов в течение 3—5 мин в 10%-ном растворе серной кислоты и снова промывают в горячей воде.
Вместо травления в растворе серной кислоты применяют анодное декапирование в хромовой ванне. Для этого деталь подключают в качестве анода и выдерживают в течение 5—8 мин до выравнивания температур детали и электролита. Затем ее выдерживают 30—60 с при плотности тока (2—3)-103 А/м2. После декапирования деталь промывают в холодной проточной воде. При хромировании ответственных деталей рекомендуется после декапирования протереть их кашицей из извести, чтобы обеспечить лучшее приставание хрома к детали.
Материалы и оборудование для хромирования
Электролиты. Обычно применяются сернокислые электролиты, основными компонентами которых являются хромовый ангидрид и серная кислота в соотношении 100:1. В этом случае выход хрома по току максимальный. В зависимости от концентрации хромового ангидрида электролиты бывают низкой (12—15 %), средней (20—25 %) и высокой (30—35 %) концентрации. Первые применяются при повышенных требованиях к износостойкости, так как обеспечивают более высокий выход хрома по току и получение твердых, износостойких покрытий. Электролиты высокой концентрации применяются преимущественно для получения защитно-декоративных покрытий, так как обеспечивают лучшую устойчивость процесса электролиза и получение плотного блестящего слоя хрома с хорошей отражательной способностью. Электролиты средней концентрации по своим свойствам являются универсальными и применяются для нанесения всех видов покрытий с выходом по току 12—14 %.
Совершенствование процесса хромирования обеспечивается применением саморегулирующего электролита, в котором автоматически поддерживается оптимальное соотношение между его компонентами. Это достигается, например, за счет введения в электролит солей сернокислого стронция и кремнефтористого калия в количестве, превышающем их растворимость, так что избыток этих солей присутствует в электролите в виде осадка. Растворением или увеличением осадка достигается стабилизация состава электролита. Саморегулирующие электролиты обеспечивают более высокую катодную плотность тока и стабильность процесса хромирования с более высоким выходом по току, который может достигать 40 %, что позволяет в 1,3—1,5 раза повысить производительность хромирования. Однако эти электролиты более токсичны.
Все более широко в ремонтном производстве для хромирования применяются холодные электролиты, например, тетрахроматные с рабочей температурой 17—23 °С. Процесс хромирования ведется при катодной плотности тока 50—100 А/дм2 и выходом по току 30—33 %.
Этот электролит позволяет получать качественные покрытия с большой производительностью и меньшими внутренними напряжениями. Покрытия получаются более мягкие, без трещин и поэтому эффективны для защитно-декоративных целей. Важно и то, что тетрахроматные электролиты менее агрессивны к углеродистым сталям, поэтому для хромирования можно применять стальные ванны без защитной облицовки внутренней поверхности. При выборе холодных электролитов следует учитывать то, что поддержание низкой их температуры при высокой плотности тока требует применения холодильных агрегатов.
Ванны для хромирования. Ванну изготовляют из листового железа толщиной 4—5 мм обычно с двойными стенками, что позволяет нагревать электролит горячей водой, прокачиваемой между стенками ванны. Внутреннюю ванну облицовывают сплавом свинца, содержащим 5—6 % сурьмы, или кислотостойкими материалами.
Если материал облицовки имеет низкую теплопроводность, то электролит нагревают, прокачивая горячую воду по погруженному в него освинцованному змеевику, или с помощью электрических нагревателей. Емкость ванн определяются габаритами и формой деталей, которые должны находиться примерно на 100 мм выше дна и 50 мм ниже верхнего уровня электролита. Расстояние между анодами и катодами должно быть 100—155 мм.
Для хромирования крупных деталей применяют передвижные ванны (рис. 4.59, а) и накладные ванны из листового целлулоида толщиной 3— 4 мм, которые устанавливают непосредственно на деталь (рис. 4.59, б).
Для хромирования отдельных участков крупных деталей, например, шеек валов эффективным является струйное хромирование, при котором ванна для хромирования монтируется вокруг покрываемого участка детали, а электролит прокачивается в зазоре между ванной и деталью. Хромирование проводят в стандартном, саморегулирующемся, тетрахроматном и других электролитах при катодно-анодном расстоянии — 15 мм. В зависимости от типа электролита и режима электролитического процесса скорость осаждения хрома составляет 0,1—0,25 мм/ч. При этом получают блестящие покрытия.
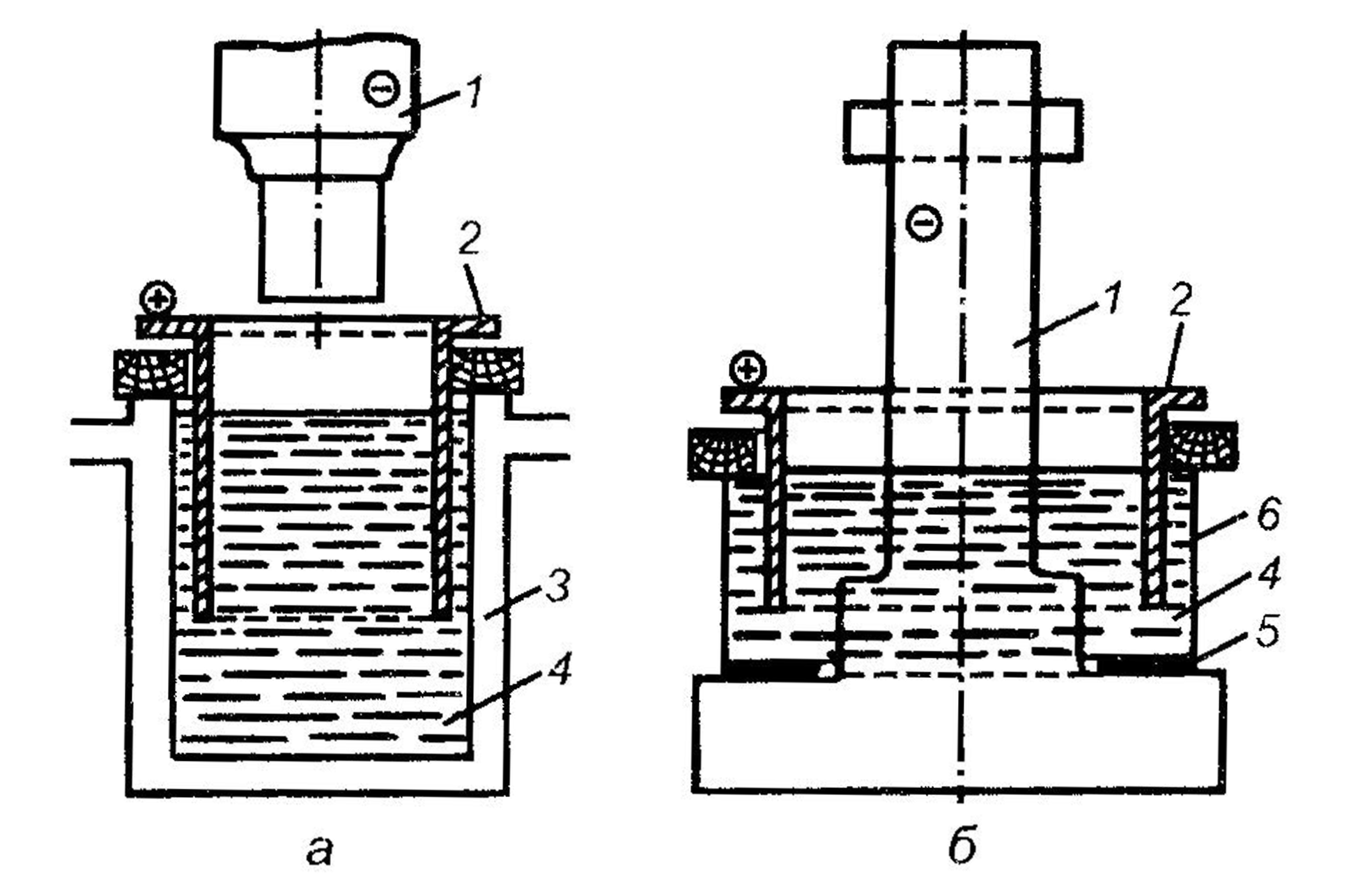
Рис. 4.59. Конструктивные схемы ванн для хромирования крупных деталей: а — передвижной; б — накладной; 1 — деталь (катод); 2 — анод; 3 — ванна с двойными стенками; 4 — электролит; 5 — уплотнение; 6 — ванна
Эффективным для крупногабаритных деталей является также хромирование в проточном электролите и безванное хромирование с использованием для электролита полости в самой детали.
Для хромирования в ваннах применяют нерастворимые свинцовые аноды с содержанием сурьмы 6 %, выполненные обычно в виде плоских пластин. Хромирование крупных круглых деталей при двух анодах не позволяет получить одинаковое по толщине покрытие. Лучшие результаты получаются при четырех анодах, удаленных на одинаковое расстояние от детали (катода). Для получения равномерного слоя хрома на фасонных поверхностях применяют фасонные аноды.
Источником тока при хромировании могут служить специальные низковольтные двухполюсные генераторы постоянного тока или выпрямители.
Выделяющиеся при хромировании на электродах газы (водород — на аноде, кислород — на катоде) выносят с собой также экологически вредные пары электролита. Поэтому оборудование для гальванических покрытий должно оснащаться надежной вентиляцией для отсасывания газов непосредственно с поверхности ванны.
При неудовлетворительном качестве покрытия удалить хром можно электролитическим путем, поместив деталь в качестве анода в ванну с электролитом из 10—15%-ного раствора едкого натра. Катодом служит железная пластина. Температура раствора 40—50 °С, плотность тока 500—1000 А/м2, продолжительность выдержки — 15—30 мин.
Восстановление деталей осталиванием
Характеристика метода. Осталиванием называется процесс электролитического осаждения железа из водных растворов хлористого или сернокислого железа. Электролитически осажденное железо по своему химическому составу близко к малоуглеродистой стали, а по своим свойствам (твердости, прочности, износостойкости) приближается к свойствам незакаленной среднеуглеродистой стали, поэтому процесс получил название осталивания.
При пропускании постоянного тока через электролит ионы железа разряжаются на катоде (детали), покрывая его слоем металла. Одновременно с этим происходит растворение анода с поступлением в раствор новых ионов вместо разрядившихся на катоде. Вместе с ионами железа на катоде разряжаются ионы водорода, которые, внедряясь в кристаллическую решетку покрытия, придают ему повышенную твердость и хрупкость. Для освобождения покрытия от водорода детали после железнения необходимо подвергать низкотемпературному сульфидированию с последующей обработкой пластическим деформированием. Это позволяет существенно повысить усталостную прочность и износостойкость деталей.
Особенностями процесса осталивания по сравнению с хромированием являются:
—применение растворимых анодов и более дешевых электролитов;
—высокие плотность тока (10—50 А/дм2) и скорость формирования покрытия (0,2—0,8 мм/ч в зависимости от плотности тока);
—большая толщина покрытия (более 3 мм при мягком и до 2 мм при твердом осталивании);
—высокий выход железа по току, достигающий 80—95 % вместо 12— 15% при хромировании, что позволяет вести процесс осталивания при меньшей мощности источника постоянного тока;
—меньшие длительность и стоимость, что обуславливает эффективность его применения при ремонте машин.
Процесс осталивания характеризуется высокой универсальностью в отношении микротвердости создаваемых покрытий, которая может находиться в диапазоне 1600—7800 МПа. Износостойкость мягких покрытий несколько меньше износостойкости углеродистой стали той же твердости, а твердых покрытий приближается к износостойкости закаленной стали. Получение того или иного покрытия зависит от состава электролита и режима осталивания. При необходимости мягкие покрытия подвергают последующему упрочнению (цементации, азотированию, сульфоцианированию).
Полученные осталиванием покрытия хорошо хромируются, что позволяет создавать более экономичные комбинированные покрытия, имеющие одинаковую с хромовыми износостойкость. Высокая экономичность осталивания подтверждается тем, что стоимость восстановленных им деталей составляет 0,3—0,5 стоимости новых при одинаковой износостойкости.
Наряду с осаждением чистого железа применяют электролитические легированные покрытия, обладающие повышенной износостойкостью и коррозионной стойкостью. Для получения таких покрытий в электролит вводят добавки, например, хлориды никеля и кобальта или другие компоненты в различных концентрациях. Изменяя состав электролита, температуру и плотность тока, можно регулировать механические свойства получаемого покрытия.
Область применения твердых покрытий при ремонте: восстановление изношенных рабочих поверхностей ответственных чугунных и стальных деталей (шеек валов, пальцев и др.); восстановление посадочных поверхностей валов и осей; гнезд под подшипники; исправление брака механической обработки.
При выборе деталей для восстановления осталиванием необходимо учитывать, что их усталостная прочность из-за образующихся в покрытии остаточных напряжений растяжения снижается на 10—20 %. Предварительная накатка или дробеструйная обработка деталей перед осталиванием позволяет создать в них напряжения сжатия, которые уменьшают влияние растягивающих напряжений в покрытии. Прочность сцепления покрытия с основным металлом достигает 120 МПа. Покрытие не отслаивается даже при нагрузках, вызывающих пластическую деформацию самих деталей. Для устранения хрупкости, повышения твердости и прочности покрытия детали после осталивания рекомендуется подвергать низкому отпуску при температуре 300—350 °С с выдержкой в течение 30 мин и постепенным охлаждением на воздухе.
Одним из методов повышения эффективности процесса осталивания является ведение его на асимметричном переменном токе промышленной частоты при пониженной (18—25 °С) температуре электролита. Регулируя силу тока в прямом и обратном направлениях (асимметрию тока) получают покрытия с различными механическими свойствами. При этом способе не требуется подогревать электролит, упрощается конструкция установки и снижается ее стоимость. Перспективным для повышения производительности является применение при осталивании трехфазного переменного тока.
Технологический недостаток процесса осталивания — необходимость систематической коррекции состава электролита и его фильтрования.
Материалы и оборудование для осталивания
Электролиты и аноды. Применяемые при осталивании электролиты различаются по химическому составу (хлористые, сернокислые и др.) и рабочей температуре (горячие и холодные). Электролит готовят растворением в воде солей хлористого железа и других компонентов, а также используют обезжиренную стружку из малоуглеродистой стали, которую травят до насыщения соляной кислоты.
Наиболее производительны и экономичны хлористые электролиты. Они состоит из раствора соляной кислоты, хлористого железа, хлористого марганца и поваренной соли. Широко применяется электролит следующего состава: 200—350 г/л хлорида железа; 100—150 г/л хлорида натрия; 1,5— 2,5 г/л соляной кислоты.
Процесс ведется при плотности тока 1000—1500 А/м2 и температуре электролита 75—90 °С
Для определения состава электролита задаются определенной концентрацией хлорида железа (от 200 до 350 г/л), рассчитывают максимально допустимую плотность тока и минимально допустимую кислотность электролита. Кислотность корректируют, периодически добавляя в электролит соляную кислоту
Горячие электролиты (рабочая температура 60—95 °С) обеспечивают более высокую производительность осталивания, однако требуются повышенный расход энергии на поддержание температуры и более тщательная вентиляция в связи с интенсивным испарением электролита.
Холодные электролиты (температура меньше 50 °С) лишены указанных недостатков. Они позволяют получать гладкие покрытия большей толщины с высокими механическими свойствами. Кроме того, они имеют более длительный срок службы.
При осталивании применяют растворимые аноды, изготовленные из стали с содержанием углерода до 0,2 %. Для предотвращения загрязнения электролита шламом, образующимся при растворении анодов, их рекомендуется помещать в футляры из пористых материалов (стеклоткани, специальной керамики и т.п.).
Ванны для осталивания. Осталивание проводят в стальных ваннах, внутренние поверхности которых изолируют от электролита кислотостойкими материалами (керамикой, полимерными материалами, резиной, эмалями и др.)- Ванна 3 (рис. 4.60) установлена на подставке 5 внутри металлического наружного кожуха 2 так, что между ними образовано пространство, заполняемое трансформаторным маслом. Масло служит для нагревания электролита во внутренней ванне. Для этого под ней установлен электронагреватель 7, связанный кабелем 8 с источником питания.
Вневанное осталивание. Для осталивания небольших по площади поверхностей у крупных деталей применяют вневанный способ, который позволяет отказаться от применения больших ванн, уменьшить объем используемого электролита, сократить или исключить некоторые подготовительные операции, связанные с изоляцией не покрываемых поверхностей, значительно снизить затраты энергии и материалов.
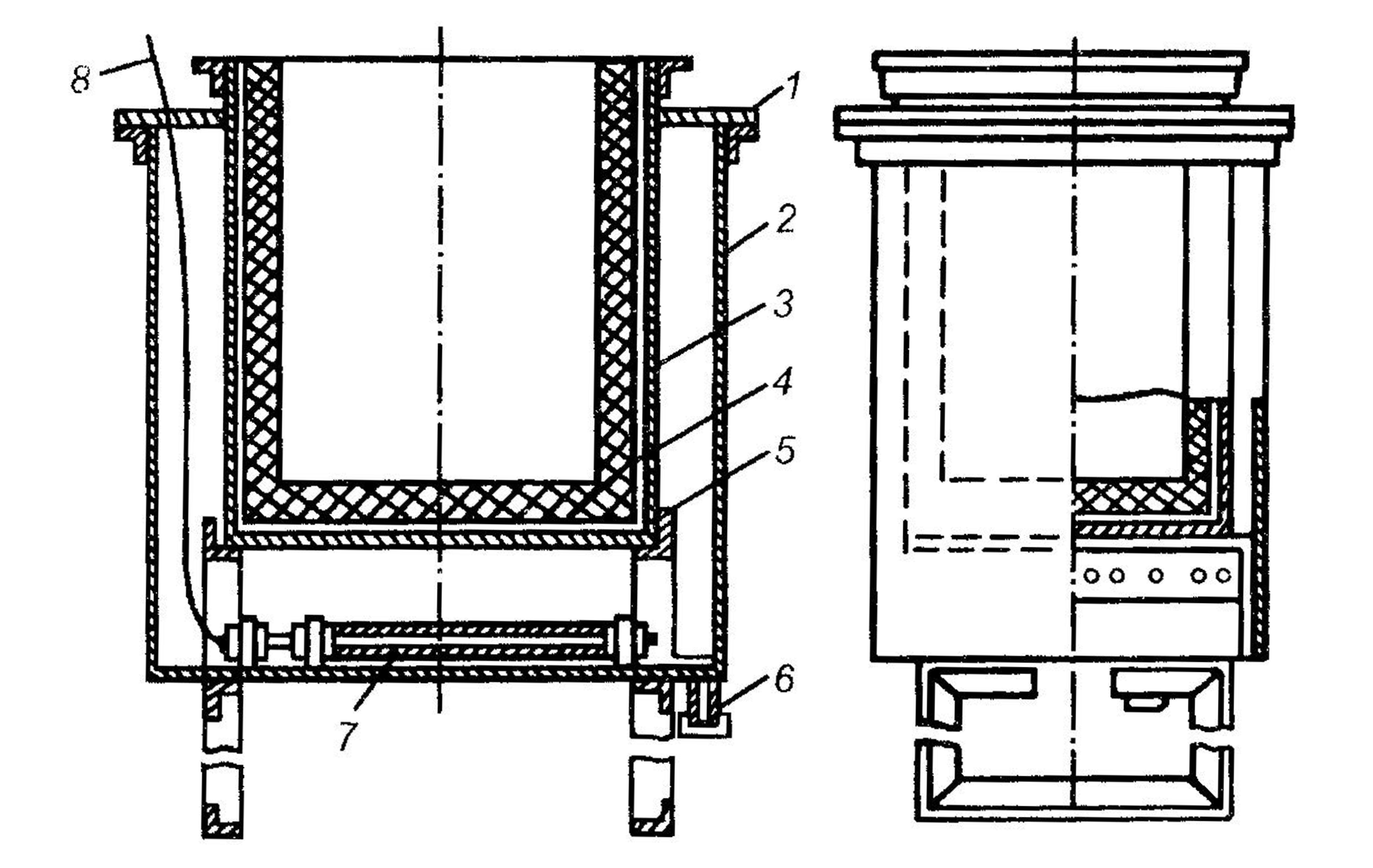
Рис. 4.60. Ванна для осталивания: 1 — крышка; 2 — наружный кожух; 3 — внутренняя ванна; 4 – облицовка ванны; 5 - подставка; 6— спускной штуцер; 7—электронагреватель; 8 — электрокабель
При вневанном способе осталивание проводится по традиционной технологии, для чего в зоне нанесения покрытия создается местная ванна (электролитическая ячейка). Такой способ позволяет значительно увеличить плотность тока и производительность процесса. Вневанный способ осталивания реализуется струйным и проточным методами, а также электролитическим натиранием.
При струйном осталивании электролит подают насосом струями через отверстия насадка в пространство между анодом и покрываемой деталью (катодом). Насадок одновременно служит анодом и местной ванночкой. Применяется концентрированный холодный хлористый электролит. При плотности тока 40—55 А/дм2 производительность осталивания составляет 0,4 мм/ч. Равномерная толщина покрытия обеспечивается за счет вращения восстанавливаемой детали или обтекания электролитом покрываемой поверхности в зазоре между ней и анодом за счет специальной конструкции последнего и тангенциальной подачи электролита (рис. 4.61).
Электролитическая ячейка для струйного осталивания шеек крупных валов состоит из верхнего 4 и нижнего 9 корпусов, с которыми жестко связаны соответствующие части анода 8. При соединении между собой указанных корпусов зажимом 7 обе части анода охватывают деталь 6 так, что между ними образуется кольцевой межэлектродный зазор. Электролит подается под давлением через патрубок 1 в другой кольцевой зазор между корпусами и анодом и при прохождении через тангенциально расположенные в нем отверстия разделяется на множество струй, которые получают движение вокруг восстанавливаемой детали. Скорость протекания электролита в меж-электродном зазоре должна быть 1—1,5 м/с при удельном расходе 40—45 л/мин на 1 дм2 покрываемой поверхности.

Рис. 4.61. Схема устройства для струйного осталивания шеек валов: 1 — подводной патрубок; 2 — отводной патрубок; 3 — кабель; 4 — верхний корпус; 5 — уплотняющая прокладка; 6 — восстанавливаемая деталь; 7 — зажим; 8 — анод; 9 — нижний корпус
Проточное железнение. Его обычно применяют для восстановления изношенных отверстий в корпусных деталях. В эти отверстия устанавливают аноды и с помощью специального устройства деталь превращают в закрытую местную гальваническую ванну через которую насосом прокачивают электролит. При подключении детали и анода к источнику тока на поверхности отверстия осаждается железо. Рекомендуемая температура электролита 75—80 °С, а катодная плотность тока 25—30 А/дм2. Метод позволяет получать качественные гладкие покрытия со скоростью 0,3 мм/ч, толщиной до 0,7 мм и твердостью 4000—4500 МПа.
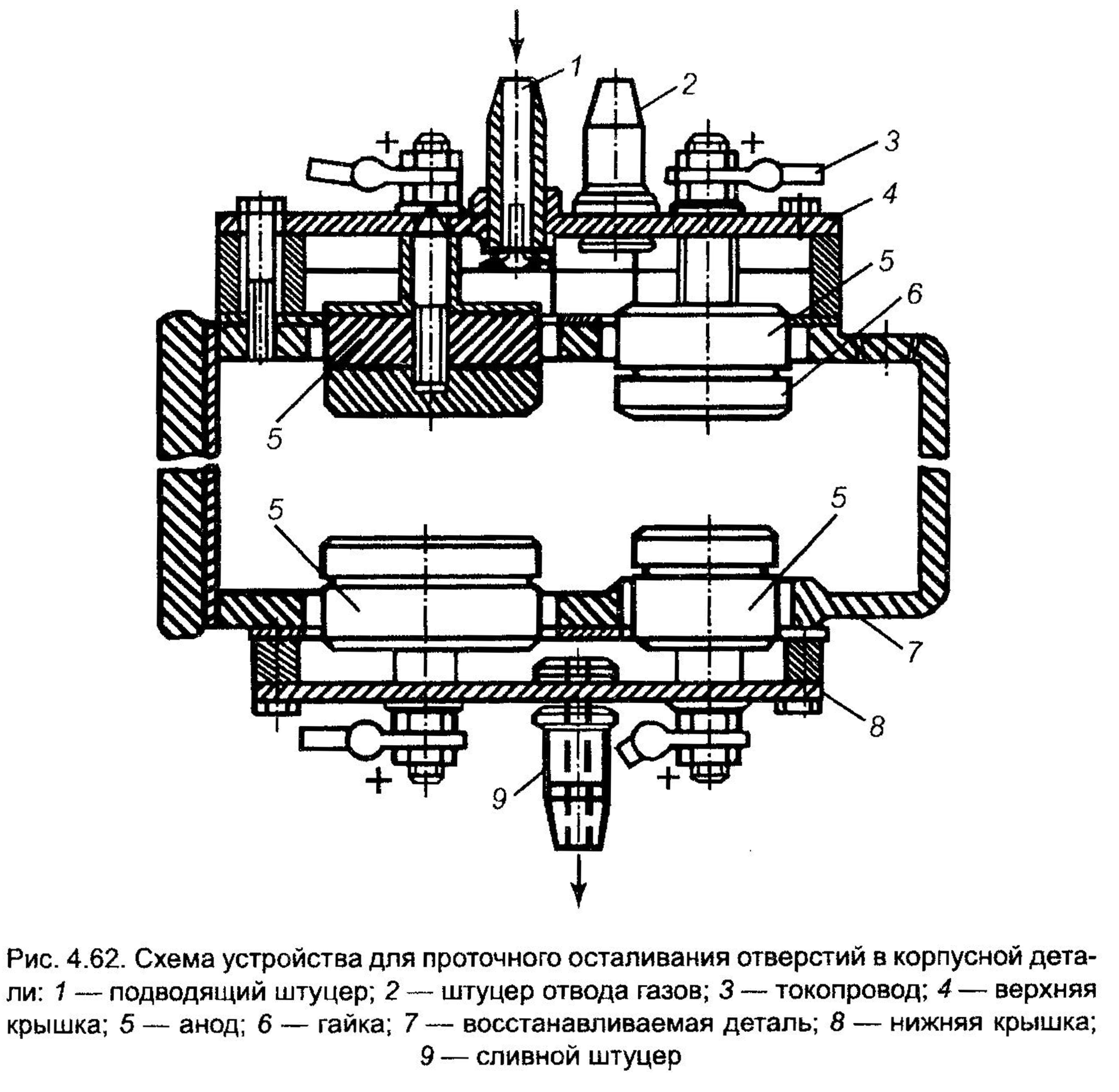
На рис. 4.62 представлена схема устройства для проточного осталивания одновременно четырех отверстий в корпусе редуктора.
С помощью специальных верхней 4 и нижней 8 крышек, а также штатных крышек корпус превращается в местную ванну для осталивания. В каждое из восстанавливаемых отверстий концентрично устанавливается анод 5, который крепится гайкой 6 на металлическом стержне, связанном с токопроводом 3. Между анодами и восстанавливаемыми отверстиями образуются межэлектродные зазоры, через которые непрерывно прокачивают электролит Он поступает в восстанавливаемую деталь через подводящий штуцер 1 и удаляется из нее через штуцер 9.
Электролитическое натирание. Оно является универсальным методом электролитического наращивания, который наиболее эффективен в ремонтном производстве при небольшом объеме восстановительных работ. Восстанавливаемая деталь 1 (рис. 4.63), которая является катодом, устанавливается с возможностью вращения на стенде или станке, а анодом служит металлический или графитовый электрод 2, на который надевается хорошо впитывающий электролит питатель 3,
Последний выполняет функцию ванны и вручную с помощью держателя б прижимается к восстанавливаемой поверхности и перемещается относительно ее. Деталь и стержень подключают к источнику постоянного тока и устанавливают требуемую плотность тока. В процессе нанесения покрытия деталь получает медленное вращение и восстанавливаемой поверхностью контактирует с питателем, который методом полива непрерывно смачивают электролитом 4. В результате в зоне контакта детали с чехлом протекает электрохимическая реакция и на восстанавливаемой поверхности осаждается металлическое покрытие.
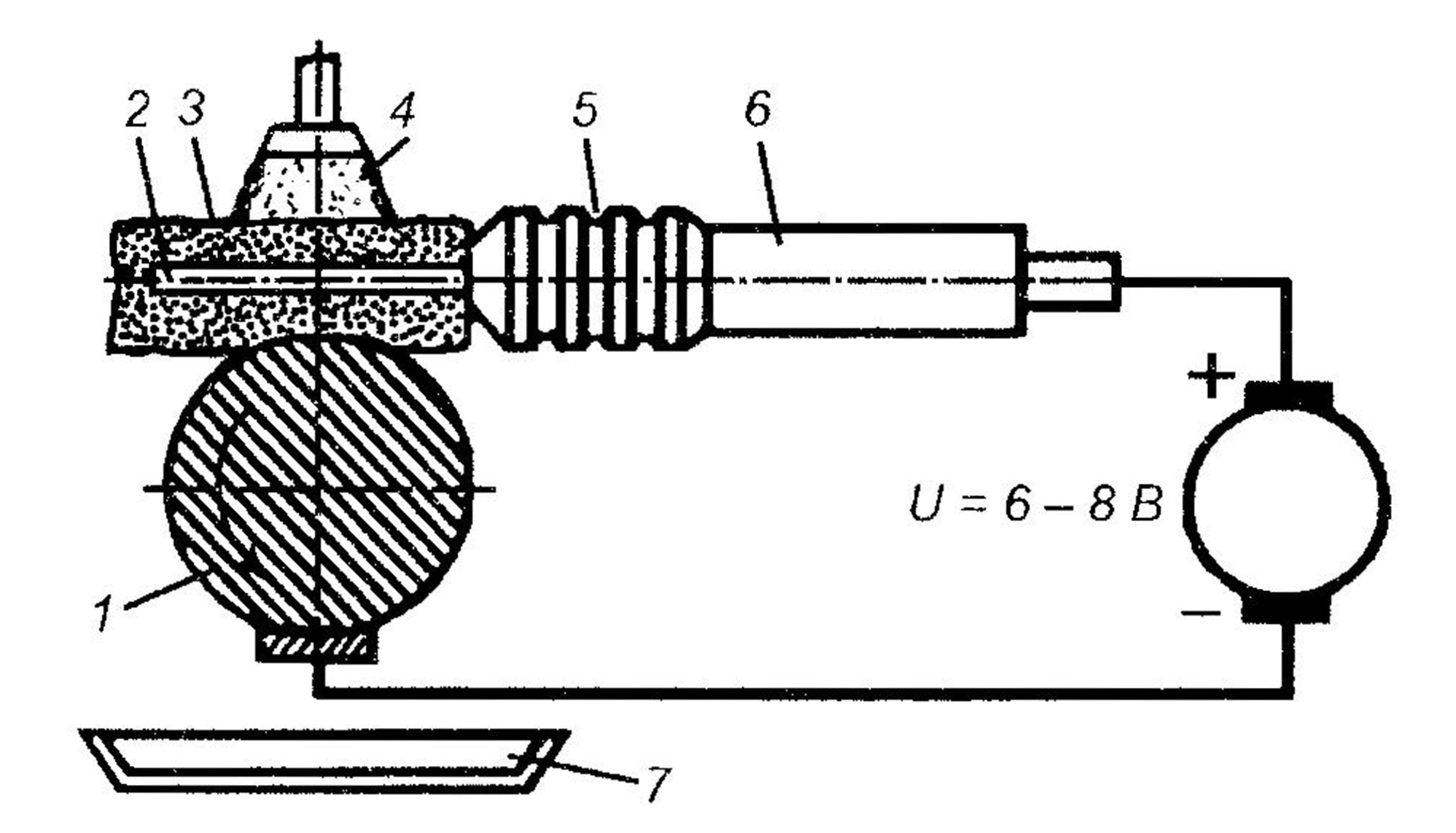
Рис. 4.63. Схема электролитического натирания цилиндрических поверхностей: 1 — восстанавливаемая деталь; 2 — электрод; 3 — питатель; 4 — электролит; 5 — корпус;
6 — держатель; 7 — ванна
Метод электронатирания обеспечивает формирование качественного покрытия с мелкозернистой структурой. Он рекомендуется для восстановления посадочных поверхностей деталей типа тел вращения.
Нанесение цинковых покрытий
Характеристика метода. Электролитическое цинкование широко используется для создания на деталях из черных металлов защитных покрытий от атмосферной коррозии, а также воздействия горюче-смазочных материалов и воды. Защитное действие цинка от коррозии по отношению к черным металлам обусловлено тем, что он имеет более отрицательный электрический потенциал, чем железо. В образующейся гальванической паре цинк является анодом и разрушается при сохранении металла защищаемого изделия. Процесс цинкования не требует применения дефицитных материалов и прост в реализации.
При выборе цинковых защитных покрытий следует учитывать, что благодаря пластичности и мягкости они хорошо выдерживают изгибы и плохо — запрессовку, а при температуре выше 250 °С становятся хрупкими. Цинкованию при ремонте машин обычно подвергаются крепежные детали, пружины, детали трубопроводов и др. Цинковые покрытия непригодны для защиты деталей в узлах трения.
Толщина цинковых покрытий в зависимости от условий их эксплуатации составляет 10—30 мкм. После цинкования тонкостенные детали и пружины должны подвергаться термической обработке для обезводороживания (нагрев в сушильных шкафах при температуре 150—180 °С в течение 2—3 ч).
Для повышения противокоррозионных свойств цинковые покрытия дополнительно подвергают хроматированию и фосфатированию, обеспечивающим создание на покрытии стойкой против коррозии пленки солей цинка.
Фосфатирование особенно эффективно для деталей, подлежащих окраске, так как оно обеспечивает значительное повышение коррозионной стойкости оцинкованных деталей.
Некачественные и старые цинковые покрытия удаляют травлением в растворе серной или соляной кислот.
Материалы и оборудование для цинкования
Электролиты и аноды. Для цинкования используются кислые и щелочные электролиты. К первым относятся сернокислые и хлористые, а ко вторым — цианистые, цинкатные и аммиакатные электролиты.
Кислые электролиты допускают высокие значения плотности тока и выхода цинка по току (95—98 %), а создаваемые покрытия имеют повышенную пластичность, прочное сцепление с основным металлом и могут подвергаться механической обработке. Однако эти электролиты по сравнению со щелочными обеспечивают более грубую структуру покрытий и меньшую коррозионную стойкость. Наибольшее применение получили сернокислые электролиты, которые используют для цинкования деталей простой формы.
Щелочные электролиты позволяют получать покрытия с более высокой коррозионной стойкостью и применяются преимущественно для цинкования деталей сложной формы. Однако они уступают кислым электролитам по устойчивости, допускаемой плотности тока и выходу цинка по току
Высокую коррозионную стойкость обеспечивают цианистые электролиты, которые широко используются для цинкования изделий сложной формы. Но они отличаются повышенной токсичностью, и поэтому при их применении требуются повышенные меры безопасности. Заменителями цианистых электролитов являются цинкатные и аммиакатные электролиты.
Цинкатные электролиты не ядовиты, обладают повышенной электропроводностью, имеют простой состав. Их недостатком является необходимость подогрева, что усложняет конструкцию оборудования и связано с дополнительными затратами энергии. Цинкатные электролиты применяют для цинкования деталей сложной формы. Для получения светлых покрытий в состав электролита вводят олово. К наиболее эффективным заменителям цианистых электролитов относятся аммиакатные электролиты, которые могут использоваться в ваннах всех типов.
Для цинкования применяют цинковые аноды марок ЦО, Ц1 и Ц2 в виде пластин, которые во избежание загрязнения электролита шламом помещают в чехлы из кислотостойкой ткани. Аноды периодически очищают травлением или щетками.
Ванны для цинкования. Электролитическое цинкование проводят в стационарных, колокольных и барабанных ваннах. Стационарные ванны служат для цинкования крупных деталей, которые монтируют на подвесные приспособления. Внутренние стенки ванн облицовывают винипластом или другими кислотостойкими материалами.
Ванны колокольного и барабанного типов предназначены для цинкования мелких деталей (винтов, болтов, гаек и др.). Колоколу или барабану сообщают вращение с частотой 8—15 мин-1. В колокольной ванне электролит заливается в колокол, а анод в виде стержня закрепляется неподвижно на специальном штативе и погружается в электролит Недостатком в колокольных ваннах является быстрое загрязнение электролита, что приводит к пористости покрытия и снижает производительность цинкования.
В барабанных ваннах мелкие детали засыпают в перфорированные барабаны, которые обычно изготавливают из винипласта или текстолита. Барабан специальным устройством с направляющими опускают в ванну с электролитом и приводят во вращение специальным приводом. Аноды загружают в ванну по обе стороны барабана.
Нанесение медных покрытий
Меднение применяют для улучшения притирки трущихся поверхностей деталей, предохранения стальных деталей от спекания при воздействии высокой температуры, нанесения подслоя на детали при их покрытии другими металлами. Медные покрытия применяют также в технологических целях, например, для облегчения пайки, защиты поверхностей деталей от науглероживания при цементации и др. Медные покрытия имеют хорошую сцепляемость с различными металлами, сохраняемую при глубокой вытяжке и развальцовке деталей, легко обрабатываются.
Технологический процесс меднения аналогичен хромированию и осталиванию. В зависимости от назначения толщина покрытия может быть от 3 до 50 мкм.
Медь имеет положительный электрический потенциал по отношению к железу и в гальванической паре с ним является катодом. Поэтому медное покрытие лишь механически предохраняет стальные детали от коррозии. В этой связи медные покрытия, применяемые в качестве защитных от коррозии, должны обладать достаточной плотностью. Благодаря свойствам хорошей сцепляемости, пластичности и полируемости медные покрытия широко применяют в качестве промежуточного слоя в многослойных покрытиях типа «медь — никель — хром». Это позволяет без ухудшения защитных свойств покрытия в целом снизить расход более дорогого и дефицитного никеля.
Для электролитического осаждения меди применяются растворимые аноды из электролитической меди марок МО и М1, а электролиз ведется в кислом, щелочном или пирофосфорном электролитах.
Кислый электролит является наиболее простым. Он содержит 200— 250 г/л сульфата меди (медного купороса) и 50—75 r/л соляной кислоты. Процесс ведется при плотности тока 100—500 А/м2, напряжении 4—6 В и температуре электролита 16—20 °С.
Достоинства меднения в кислом электролите — дешевизна исходных материалов, большой выход металла по току (0,98—0,99), высокая скорость отложения меди (0,04—0,05 мм/ч). Однако вследствие вытеснения меди железом материал покрытия получается крупнокристаллическим, рыхлым и недостаточно прочным. Это не позволяет наносить медное покрытие непосредственно на черный металл, поэтому перед меднением на стальные детали наносят подслой никеля.
Щелочной электролит содержит в качестве основных компонентов цианиды меди и натрия, что обуславливает выделение при электролизе паров синильной кислоты. Это требует герметизации ванны и надежной вытяжки в процессе работы.
Меднение ведется при плотности тока 100 А/м2, напряжении 4—6 В и температуре 30—35 °С. Выход металла по току составляет 0,65—0,70. Существенным преимуществом цианистого электролита по сравнению с кислым является возможность непосредственно осаждать на стальные и чугунные детали высококачественные мелкокристаллические осадки меди.
Пирофосфорный электролит объединяет основные положительные свойства кислого (дешевые материалы и высокая производительность осаждения меди) и цианистого (более высокое качество покрытия и возможность его нанесения непосредственно на сталь) электролитов.
Нанесение электролитических никелевых покрытий
В ремонтном производстве никелевые покрытия применяют для защиты деталей от коррозии, их декоративной отделки, компенсации небольшого по величине износа взамен хромирования, в качестве подслоя перед меднением или декоративным хромированием и как эффективное износостойкое покрытие. Никелевые покрытия после полирования приобретают красивый декоративный вид.
В ремонтной практике применяют электролитический и химический способы никелирования.
Микротвердость электролитических никелевых покрытий зависит от режима электролиза и может достигать 7000 МПа. Они имеют мелкокристаллическую структуру и равномерную толщину. Никелевые покрытия толщиной 0,025 мм хорошо предохраняют основной металл от коррозии, так как никель химически стоек к воздействию атмосферы, щелочей и некоторых кислот. В гальванической паре с железом, как и медь, он выступает катодом. Поэтому никелевое покрытие защищает стальные детали от коррозии только при отсутствии пористости. Пористость уменьшается с увеличением толщины покрытия.
Свойства никелевых покрытий существенно зависят от электролита. Наиболее широко применяются сернокислые электролиты, основным компонентом которых является сернокислый никель. Они образуют относительно мягкие покрытия с хорошими защитными свойствами. Процесс ведется при плотности тока до 10 А/дм2. Выход по току составляет 0,80-—0,95.
Используются также хлористые, фторборатные, сульфатные и другие электролиты. Хлористые электролиты применяют при никелировании нержавеющих и жаростойких сталей. Фторборатный электролит обеспечивает более высокую производительность за счет повышенной плотности тока (до 20 А/дм2) и стабильности процесса, а создаваемые покрытия имеют лучшие, чем при сернокислых электролитах, свойства и хорошее сцепление с металлом детали.
При применении сульфатного электролита покрытия обладают повышенной пластичностью и незначительными внутренними напряжениями. Электролиты этого типа мало чувствительны к загрязнениям и допускают высокую плотность тока (до 30 А/дм2).
Для получения блестящих покрытий в электролиты вводят специальные добавки (блескообразователи), а также выравнивающие добавки, которые позволяют снизить требования к качеству полировки покрываемой поверхности перед никелированием по наличию и глубине рисок при необходимости получения гладкого покрытия.
Никелевые электролиты весьма чувствительны к химическим примесям, которые могут попадать при растворении анодов и материала подвесных приспособлений. Поэтому их следует периодически подвергать электрохимической очистке и фильтрации. Лучшие результаты обеспечиваются при непрерывной фильтрации и воздушном перемешивании электролита. В этом случае выход по току на оптимальных режимах достигает 90—98 %.
При выборе режима электролиза следует учитывать, что чем выше кислотность и температура электролита, тем больше допускаемые значения плотности тока и скорости электролитического процесса. Важно поддерживать кислотность электролита постоянной, так как в противном случае ухудшаются свойства покрытий и снижается их сцепление с металлом детали.
При никелировании применяют растворимые аноды из технического никеля, содержащего до 10 % железа, например, марок НПА1 и НПА2 и др. Для повышения их растворимости в состав электролита вводят хлористый никель, натрий или калий, а для предотвращения загрязнения электролита шлаком аноды помещают в специальные чехлы.
Нанесение покрытий химическими методами
Химические методы применяются для нанесения на детали металлических и неметаллических покрытий
Нанесение металлических покрытий. Химический метод нанесения покрытия основан на реакции восстановления металла из водного раствора его соли при выдержке в нем покрываемой детали. Так получают покрытия из никеля, меди, олова, кадмия и других металлов. Рассмотрим технологию нанесения покрытия на примере химического никелирования, которое осуществляется в результате восстановления никеля из водного раствора его соли.
Перед покрытием детали обезжиривают, промывают, проводят их химическое травление в растворе соляной кислоты и после промывки помещают в кислый или щелочной раствор для никелирования. Чаще применяют кислые растворы, содержащие 30 г/л никелевой соли и другие компоненты. Процесс ведется в эмалированной, стеклянной или футерованной емкости, оборудованной нагревателем. При температуре раствора 90—92 °С и соблюдении технических условий скорость осаждения никеля составляет 15—20 мкм/ч.
Покрытия осаждаются гладкими и блестящими, с высокой коррозионной стойкостью и твердостью. Они представляют сплав никеля с фосфором, содержание которого составляет примерно 5 % для щелочных и 9 % для кислых растворов. После термообработки при температуре 400—450 °С твердость покрытия возрастает вдвое и может достигать 61 HRCэ. При этом повышаются его износостойкость и сцепляемость с деталью. Износостойкость незакаленных никелевых покрытий невысока.
Химическое никелирование предназначено в основном для защитно-декоративных покрытий мелких деталей. В ремонтном производстве его применяют также при восстановлении поверхностей с небольшим износом, например, прецизионных деталей гидравлического оборудования, а также для повышения износостойкости новых деталей. Например, стойкость зубьев зубчатых передач после химического никелирования повышается в 3—4 раза.
Химическое никелирование по сравнению с электролитическим имеет следующие преимущества: более безопасные условия труда; значительно проще технологическое оборудование и не требуется энергетическое оборудование; возможность получения покрытий повышенной твердости (до 61 HRCэ после термической обработки) с высоким сопротивлением абразивному изнашиванию; возможность нанесения покрытия на различные металлические и неметаллические материалы; равномерность толщины покрытия как на наружных, так и на внутренних поверхностях, включая изделия сложной формы, например, зубчатые колеса.
Недостатки этого метода — невысокая производительность (скорость осаждения никеля не превышает 20 мкм/ч), а также быстрое изменение состава раствора во времени, из-за чего его часто приходится заменять новым.
Нанесение неметаллических покрытий. Неметаллические покрытия в виде защитных оксидных, фосфатных и других пленок создаются на металлических деталях в результате химического воздействия на них растворов определенных веществ. Для этого детали выдерживают определенное время в соответствующем растворе при температуре до 200 °С.
Оксидирование. Для получения на поверхностях стальных деталей защитной пленки из оксидов железа применяют оксидирование в концентрированных щелочных ваннах с добавлением окислителей. Раствор для оксидирования обычно содержит едкий натр (650 г/л), азотнокислый натрий (200—250 г/л) и азотистокислый натрий (50—70 г/л).
Подготовленные детали предварительно окунают в горячее масло, протирают ветошью и затем загружают в ванну при температуре раствора 125—130 °С. После этого раствор подогревают до кипения (140—145 °С). Допускается повышение температуры на 3—5 °С. В зависимости от требуемой толщины пленки детали выдерживают в кипящем растворе 30—60 мин. Большее время принимается для легированных сталей. В зависимости от химического состава стали пленки могут иметь черный или темно-коричневый цвет с различными оттенками.
Толщина полученной оксидной пленки зависит от химического состава стали и режима оксидирования. Она должна быть 0,6—1,0 мкм. При толщине менее 0,6 мкм пленка не защищает основной металл от коррозии, а при толщине более 1 мкм она становится рыхлой и непрочной. Малая толщина оксидных пленок позволяет применять этот процесс для противокоррозионной защиты окончательно обработанных деталей и деталей с острыми переходами между поверхностями, например, с мелкими резьбами.
Имеющиеся в оксидных пленках поры могут стать местом возникновения коррозии. Поэтому щелочь удаляют из пор, для чего оксидированные детали промывают в кипящем мыльном растворе, а затем прогревают их в масле при температуре 110—120 °С. При этом происходит выпаривание влаги из пор и заполнение их маслом.
Некачественные покрытия получаются при плохой подготовке деталей и нарушении режима оксидирования (неправильная концентрация раствора, несоблюдение температуры).
Фосфатирование представляет процесс химической обработки металлов, при котором на них создаются пленки, состоящие из нерастворимых солей фосфорной кислоты. В ремонтном производстве фосфатирование применяют для защиты деталей от коррозии (болты с крупной резьбой, шайбы и другие детали), улучшения прирабатываемости трущихся поверхностей, а также в качестве грунта под лакокрасочное покрытие.
Фосфатированию обычно подвергаются стальные детали. В зависимости от химического состава стали и условий получения, толщина пленки может изменяться от 7 до 42 мкм. Процесс сопровождается травлением металла детали и увеличением шероховатости поверхности на 1—2 класса, что исключает возможность выполнять фосфатирование деталей с точно обработанными поверхностями, а также имеющих мелкие резьбы и другие конструктивные элементы с острыми кромками.
Фосфатные пленки сохраняют механические свойства в интервале температур -75... +500 °С. Они обладают высокой жаростойкостью и благодаря пористости хорошо удерживают смазку. Поэтому фосфатные пленки эффективно применяют для улучшения приработки деталей, работающих при значительных нагрузках и высокой температуре.
Для повышения противокоррозионных свойства фосфатных пленок с повышенной пористостью рекомендуется после фосфатирования выдерживать детали в нейтральных маслах при температуре 110—120 °С.
Фосфатирование может выполняться в растворе комплекса солей марганца, железа и фосфора («Мажеф») и в растворах, содержащих монофосфат цинка. В первом случае создается покрытие из нерастворимых солей марганца, фосфора и железа, а во втором — более коррозионно-стойкие пленки, содержащие фосфаты цинка и железа.
В большинстве случаев фосфатные пленки по сравнению с оксидными обладают более высокой защитной способностью, однако значительная толщина фосфатных пленок ограничивает область их применения.
Оксидофосфатирование, или бесщелочное оксидирование, служит для получения оксидофосфатных пленок толщиной 1—3 мкм. Процесс ведут в растворе, содержащем азотнокислый цинк, азотнокислый барий и монофосфат цинка при температуре раствора 90—95 °С. Время выдержки деталей в растворе 15—20 мин.
Создаваемые покрытия отличаются от обычных оксидных и фосфатных пленок более высокими противокоррозионными, адгезионными и механическими свойствами. Наличие пленки такой толщины мало влияет на размер детали, поэтому данный процесс применим для защиты окончательно обработанных деталей с точными резьбами и шлицами.
Важными преимуществами данного метода являются сокращение до 15—20 мин (примерно в 2 раза) длительности процесса нанесения покрытия и меньший расход энергии. Благодаря этим преимуществам оксидофосфатирование применяется все шире, заменяя другие химические методы нанесения покрытий. Его применяют для защиты деталей от коррозии, а также нанесения грунта на окрашиваемые поверхности.
ВОССТАНОВЛЕНИЕ ДЕТАЛЕЙ ЭЛЕКТРОЛИТИЧЕСКИМИ И ХИМИЧЕСКИМИ ПОКРЫТИЯМИ