Полимиксины тАУ новый взгляд на известные антибиотики
Актуальность проблемы терапии инфекционных болезней, вызванных полирезистентными штаммами бактерий, не вызывает сомнения. Возможными путями решения этой проблемы может явиться либо синтез новых антибактериальных средств, либо оптимизация применения имеющихся на вооружении препаратовВа [1].
Сегодня создание и выпуск на рынок нового антибиотика связаны с затратами от 100 до 350 млн долларов США [ 22,Ва 33]. Распространение резистентности часто предшествует появлению активного препарата на рынке. Более предпочтительным решением для отечественных условий можно считать рациональное использование существующих антибиотиков. В связи с этим хотелось бы обсудить перспективы применения давно известной группы противомикробных средств тАУ полимиксинов, которые эффективны в отношении грамотрицательных возбудителей инфекций, в том числе и полирезистентных.
Полимиксины составляют группу полипептидных антибиотиков с молекулярной массой около 1000, синтезируемых аэробной спорообразующей палочкой Bacillus polymyxaВа [44]. Они выделены в конце 40-х годов, именно поэтому основные исследования и публикации по этим препаратам относятся к началу второй половины XX столетия. Из 5 выделенных групп природных соединений только 2 (рис.Ва 1,Ва 2) используются в клинике тАУ полимиксин В и полимиксин Е (колистин). В России зарегистрированы полимиксина В сульфат и полимиксина М сульфат (фактически колистин).
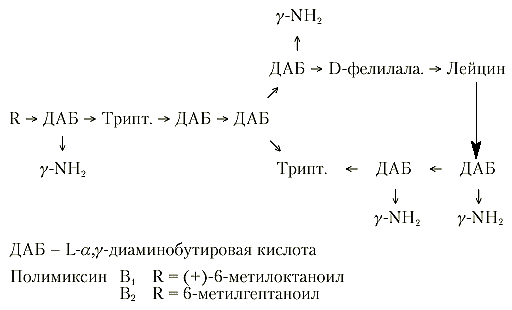
Рис 1. Структкра полимиксина ВВа [5]
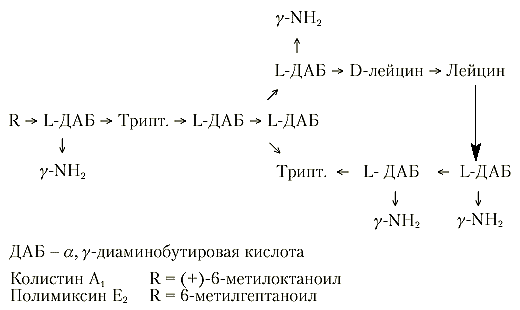
Рис 2. Структура колистина А и полимиксина Е2Ва [5]
Механизм действия полимиксинов
Все полимиксины воздействуют на цитоплазматическую мембрану бактериальной клетки, взаимодействуя с фосфолипидами. Они связываются с анионными участками мембраны и по характеру действия напоминают катионные детергенты. Повреждение структуры мембраны приводит к изменению ее проницаемости как для внутри-, так и внеклеточных компонентов [ 44, 66].
Детергентоподобное действие является основой нескольких клинически значимых эффектов использования полимиксинов тАУ токсичность и нейтрализация биологических эффектов эндотоксинов. Особого внимания заслуживает нефротоксичность, проявляющаяся у 20% пациентов в первые несколько дней терапии в виде протеинурии, гематурии и повышения уровня креатинина в сыворотке крови. При высокой концентрации полимиксина в сыворотке наблюдаются олигурия и тубулярный некрозВа [77]. Возможны также неврологические и диспептические нарушения.
Полимиксины воздействуют на АТФ-зависимые кальциевые каналы инсулинсекретирующих клеток, что приводит к подавлению инсулинстимулированной трансформации и транспорта глюкозы, снижению поглощения глюкозы мышцами и их жировой тканью [ 88,Ва 99]. Возможно усиление антиинсулинового эффекта других препаратовВа [10].
Связывание фосфолипидов полимиксинами объясняет их биологическую активность в виде блокирования эффекта эндотоксинов-липополисахаридов (ЭЛПС). Полимиксины препятствуют ЭЛПС-зависимому выделению интерлейкина-1 моноцитами, фактора некроза опухоли альвеолярными макрофагами [ 11,Ва 12]. В эксперименте это проявляется в устранении кардиоваскулярных, метаболических и других эффектов ЭЛПСВа [13]. В то же время клиническое значение подобного действия полимиксинов остается неизученным в связи с огранниченным числом клинических наблюдений у ожоговых больных [ 14,Ва 15] и у пациентов с обструктивной желтухойВа [16].
Антибактериальная активность полимиксинов
Антибактериальная активность полимиксинов распространяется только на грамотрицательную микрофлору ( см. таблицу): Escherichia coli, Klebsiella spp., Enterobacter spp., Salmonella spp., Shigella spp., Haemophilus influenzae, Brucella spp., Pseudomonas aeruginosa, Acinetobacter spp.
Активность полимиксинов в отношении некоторых патогенных бактерий: МПК (мг/л) и/или качественная оценка (R - резистентность)Ва [55]
| Микроорганизм | Колистина сульфат | Колистина сульфометат | ПолимиксинаВ сульфат | | Staphylococcus aureus | 64 (R) | (R) | 64 (R) | | Streptococcus pyogenes | 32 (R) | 32 (R) | 16 (R) | Группа
Streptococcus viridans | 32 (R) | 32 (R) | 32 (R) | | Enterococcus faecalis | R | R | R | | Haemophilus influenzae | 0,5-1,0 | тАУ | 0,03 | | Escherichia coli | 0,01-32 | 0,05-64 | 0,03 | | Klebsiella pneumoniae | 0,01-1,0 | 0,01-4,0 | 0,03-0,5 | | Enterobacter spp. | 0,03-32 | 0,5-R | 0,03-16 | | Proteus spp. | R | R | R | | Salmonella spp. | 0,01-1,0 | 0,03-0,5 | 0,01-1,0 | | Shigella spp. | 0,01-1,0 | 0,1-0,25 | 0,01-1,0 | | Pseudomonas aeruginosa | 0,03-4,0 | 2,0-320,03-4,0 | |
|
Во многих случаях полимиксины остаются высокоактивными антибиотиками в отношении бактерий, устойчивых к большинству противомикробных препаратовВа [17]. Меньшая активность проявляется против анаэробов. Нечувствительны к действию полимиксинов все виды Proteus spp., Serratia marcescens, грам(+) бактерии и многие анаэробы, в частности Bacteroides fragilis. Приобретенная бактериальная резистентность развивается медленно и обычно связана со снижением проницаемости мембран для полимиксинов [ 18,Ва 19].
Полимиксины демонстрируют in vitro синергидное действие с некоторыми другими антибактериальными средствами в отношении определенных возбудителей инфекций. Так, выявлен синергизм с триметопримом против S. marcescensВа [20], с бацитрацином и миконазолом тАУ против Staphylococcus aureus и Staphylococcus epidermidisВа [21]. Полимиксин В повышает активность амфотерицина В против Coccidioides immitisВа [22], а комбинация колистина с рифампицином способна подавлять жизнедеятельность множественно-резистентных штаммов Acinetobacter baumanniiВа [23]. Однако выявляемый in vitro синергизм не исследовался в контролируемых клинических исследованиях.
Фармакокинетика полимиксинов
Полимиксины практически не всасываются при приеме внутрь. После внутримышечного введения пиковая концентрация в сыворотке крови (2тАУ8 мг/л) формируется через 1тАУ2 ч с постепенным снижением в течение 8тАУ12 ч. Внутривенное болюсное введение полимиксина В с последующей медленной инфузией позволяет поддерживать высокий его уровень (5тАУ6 мг/л) в течение всего периода введенияВа [24].
После парентерального введения полимиксины распределяются в организме, накапливаясь в почках, печени, сердце, мышцах и легких. Препараты не обнаруживаются в желчевыводящих путях и спинномозговой жидкости (даже при менингите). Выводятся и полимиксин В, и колистин почками путем клубочковой фильтрации. Концентрация в моче после парентерального введения варьирует в пределах 20тАУ100 мг/л. Обычно она выше у колистина.
Клиническое использование полимиксинов
В клинике до 60-х годов полимиксины рассматривались в качестве основных средств лечения инфекций, вызванных P.aeruginosa, включая бактериемию, пневмонию, ожоги, менингиты (интратекальное введение), инфекции мочевыводящих путей [ 25,Ва 26].
В современных условиях полимиксин В и колистин могут быть использованы лишь как препараты "глубокого" резерва при лечении инфекций, вызванных некоторыми грамотрицательными микроорганизмами с множественной устойчивостью к другим классам препаратов. Во многом это связано с меньшей эффективностью и большей токсичностью полимиксинов по сравнению с новыми, появившимися уже после них антибиотиками, такими, как цефалоспорины и аминогликозиды.
Вместе с тем полимиксины могут применяться местно, чаще в комбинации с другими препаратами при лечении болезней кожи и глаз. Глазные капли полимиксина с неомицином и грамицидином используют для профилактики инфекций у пациентов, перенесших операции на глазах, а также для лечения кератитовВа [27]. Полимиксин до сих пор входит в схемы селективной деконтаминации кишечника у больных, находящихся в отделениях интенсивной терапии, хирургических стационарах и онкологических центрах. С этой целью полимиксин назначают внутрь самостоятельно или в комбинации с одним из таких препаратов, как гентамицин, неомицин, цефотаксим или ципрофлоксацин [ 28,Ва 29]. Эти схемы показали высокую эффективность в предупреждении нозокомиальных инфекций, вызываемых множественнорезистентными штаммами грамотрицательной микрофлоры.
В литературе приводятся ограниченные сведения о применении полимиксинов для терапии нозокомиальных инфекций. В частности, у 60 больных с внутрибольничным инфицированием штаммами P. aeruginosa и A. baumannii, резистентными к цефалоспоринам, монобактамам, карбапенемам, аминогликозидам и фторхинолонам, был успешно использован колистин (эффективность 60%)Ва [30]. Лучшие результаты получены у пациентов с инфекциями мочевыводящих путей, менингитами (у 4 из 5 больных, в основном при интратекальном введении), сепсисом и хирургической патологией (перитонит). Однако лишь у 5 из 20 пациентов с пневмониями наступило улучшение. Авторы отмечают высокую частоту нарушения функции почек тАУ у 27% больных с исходно нормальными значениями уровня креатинина и у 58% с уже имевшимися нарушениями. Эти обстоятельства требуют строго контроля функции почек у всех пациентов, получающих полимиксин.
В отношении инфекций нижних дыхательных путей имеются противоречивые сведения об эффективности полимиксинов. Они касаются в основном профилактического применения колистина у пациентов, находящихся в отделениях интенсивной терапии или у больных муковисцидозом. В частности, T. Feeley и соавт.Ва [31] выявили увеличение частоты развития пневмоний, вызванных микроорганизмами, резистентными к полимиксину В (S. maltophilia и Вurkholderia cepacia), после ингаляционного использования препарата. С другий стороны, K. Unertl и соавт.Ва [32] указывают, что применение паст с полимиксином В в виде аппликаций в носо- и ротоглотке либо внутрь снижало колонизацию глотки и бронхов множественно-резистентными микроорганизмами. В свою очередь это уменьшило частоту развития нозокомиальных пневмоний в сравнении с таковой у пациентов, не получавших подобной терапии.
Колистин оказался эффективным средством вторичной профилактики пневмоний у больных муковисцидозомВа [33], инфицированных вирусом иммунодефицита человекаВа [34], и пациентов с нейтропенией [ 35,Ва 36]. Интересны данные, полученные в Датском центре муковисцидоза в Копенгагене, по оценке эффективности трехступенчатой схемы лечения с колистином (ингаляционно) и ципрофлоксацином (внутрь)Ва [37]. Только у 8 (17%) из 48 пациентов после трехмесячной терапии высокими дозами в течение последующих 3,5 лет развилась хроническая инфекция, вызванная P. aeruginosa. В контрольной группе (43 пациента) таких больных оказалось 72%.
G.S. Bauldoff и соавт.Ва [38] оценивали эффективность ингаляционного применения колистина у больных муковисцидозом тАУ кандидатов на трансплантацию легких. Все пациенты были колонизированы множественно-резистентыми штаммами P.aeruginosa. Применение колистина у 20 пацинетов привело к исчезновению множественно-устойчивых штаммов и колонизации легких штаммами синегнойной палочки, чувствительными к антибиотикам в течение 45,0В±20,2 дня. В контрольной группе только у 3 из 10 пациентов были выделены такие микроорганизмы лишь через 144В±48 дней. Авторы заключают, что колистин может быть использован для содействия появлению чувствительных к препаратам штаммов P. aeruginosa у пациентов, которым планируется трансплантация легких.
Чрезвычайно серьезной проблемой остаются менингиты, вызванные устойчивыми ко многим антибиотикам возбудителями. Описаны методы лечения таких форм патологии карбапенемами и ингибиторозащищенными пенициллинами [ 39,Ва 40]. Однако развитие резистентности к этим препаратам уже нередкое явление. В частности, серьезной проблемой являются штаммы Acinetobacter spp., устойчивые в том числе к карбапенемам и сульбактаму [ 41,Ва 42,Ва 43]. Как показывают немногочисленные публикации, такие штаммы часто сохраняют чувствительность к полимиксинам [ 44,Ва 45].
Интерес представляет сообщение P. Fernandas-Viladrich и соавт.Ва [46] о лечении 5 пациентов по поводу вентрикулитов с субарахноидальными гематомами или оперированных по поводу опухоли мозга. После внутривенного введения меропенема, сульбактама и тобрамицина, а также тобрамицина интравентрикулярно 3 пациента погибли в течение недели после развития вентрикулита, вызванного карбапенеморезистентными штаммами Acinetobacter baumannii. Наряду с перечисленной терапией 2 больным был назначен колистин интратекально (в течение 20 дней), что привело к улучшению их состояния и стерилизации спинномозговой жидкости. Авторы заключают, что именно колистин способствовал сохранению жизни этим больным, поскольку ни меропенем (МПК тАУ 4тАУ256 мг/л), ни тобрамицин (МПК тАУ 8 мг/л) не создавали в ликворе концентрации, достаточной для подавления возбудителя.
Таким образом, в современных условиях лечение некоторых тяжелых форм инфекционной патологии, в том числе нозокомиальных инфекций, требует пересмотра стандартных подходов. Бесконтрольное применение антибактериальных препаратов, в том числе, в амбулаторной практике, приводит к распространению антибиотикорезистентности, против которой не успевают изыскать эффективные средства наука и фармацевтическая промышленность.
Именно поэтому в некоторых случаях необходимо обращать внимание к препаратам, давно известным и изученным, но незаслуженно забытым. В этом отношении полимиксины могут принести немало пользы, если их применять обоснованно, особенно в тех случаях, когда другие препараты прогностически могут быть неэффективными.
Списоклитературы
MoelleringR.C. Antibiotic resistance: Lessons for the future. Clin Infect Dis 1998; 27 (Suppl. 1): 135-40.
Drew J. Drug Int J 1993; 22: 1059-64.
SCRIP 1995; 27: 2054.
Hancock R.E.W., Chapple D.S. Peptide antibiotics. Antimicrob Agents Chemother 1999; 43: 1317-23.
O'Grady F., Greenwood D. Cyclic peptides. In: O'Grady F., Lambert H.P., Finch R.G., Greenwood D., editors. Antibiotics and Chemotherapy. 7th ed. New York: Churchill Livingstone; 1997. p. 336-44.
Mestres C., Alsina M., Busquets M., et al. Interaction of colistin with lipids in liposomes and monolayers. Int J Pharm 1998; 160: 99-107.
Koch-Weser J., Sidel V.W., Federman E.B., et al. Adverse effects of sodium colistimethate. Ann Intern Med 1970; 72: 857.
Strutchfield J., Jones P.M., Howell S.L. The effects of polymyxin B, a protein kinase C inhibitor, on insulin secretion from intact and permeabilized islets of Langerhans. Biochem Biophys Res Commun 1986; 136: 1001.
Amir S., Sasson S., Kalser N. Polymyxin B is an inhibitor of insulin-induced hypoglycemia in the whole animal model: Studies on the mode of inhibitory action. J Biol Chem 1987; 262: 6663.
Henriksen E.J., Sleeper M.D., Zierath J.R., et al. Polymyxin B inhibits stimulation of glucose transport in muscle by hypoxia or contractions. Ann J Physiol 1989; 256: E662.
Cavaillon J.M., Haeffner-Cavaillon N. Polymyxin B inhibition of LPS-induced interleukin-1 secretion by human monocytes is dependent upon the LPS origin. Mol Immunol 1986; 23: 965.
Stokes D.C., Shenep J.L., Fishman M., et al. Polymyxin B prevents lipopolysaccharide-induced release of tumor necrosis factors from alveolar macrophages. J Infect Dis 1989; 160: 52.
Flynn P.M., Shenep J.L., Stokes D.C., et al. Polymyxin moderates acidosis and hypotension in established, experimental gram-negative septicemia. J Infect Dis 1987; 156: 706.
Tauber M.G., Shibl A.M., Hackbarth C.J., et al. Antibiotic therapy, endotoxin concentration in cerebrospinal fluid, and brain edema in experimental Escherichia coli meningitis in rabbits. J Infect Dis 1987; 156: 456.
Bender B.S., Winchurch R.A., Trupari J.N., et al. Depressed natural killer cell function in terminally injured adults: Successful in vivo and in vitro immunomodulation and the role of endotoxin. Clin Exp Immunol 1988; 71: 120-5.
Ingoldby C.J., McPherson G.A., Blamgart L.H. Endotoxemia in human obstructive jaundice: Effect of polymyxin B. Am J Surg 1984; 147: 766.
Catchpole C.R., Andrews J.M., Brenwald N., et al. A reassessment of the in vitro activity of colistin sulphomethate sodium. J Antimicrob Chemother 1997; 39: 255-60.
Moore R.A. Hancock R.E. Involvement of outer membrane of Pseudomonas cepacia in aminoglycoside and polymyxin resistance. Antimicrob Agents Chemother 1986; 30: 923.
Peterson A.A., Fesik S.W., McGroarty E.J. Decreased binding of antibiotics to lipopolysaccharides from polymyxin-resistant strains of Escherichia coli and Salmonella typhimurium. Antimicrob Agents Chemother 1987; 31: 230.
Rosenblatt J.E., Stewart P.R. Combined activity of sulfamethoxazole, trimethoprim and polymyxin B against gram-negative bacilli. Antimicrob Agents Chemother 1974; 6: 84.
Cornelissen F., Van de Bossche H. Synergism of the antimicrobial agents miconasole, bacitracin and polimixin B. Chemother 1983; 29: 419.
Collins M.S., Pappagagiorus D. Inhibition of Coccidiodes immitis in vitro and enhancement of amphotericin B by polymyxin B. Antimicrob Agents Chemother 1975; 7: 419.
Hogg G.M., Barr J.G., Webb C.H. In vitro activity of the combination of colistin and rifampicin against milty-drug-resistant strains of A. baumannii. J Antimicrob Chemother 1998; 41: 494-5.
Meyers B.R., Gurtman A.C. Polymyxin B. Colistin. In: Gorbach S.L., Bartlett J.G., Blacklow N.R., editors. Infect Dis; 1998: p. 2594.
Fekety J., Norman P.S., Cluff L.E. The treatment of gram-negative bacillary infections with colistin. Ann Intern Med 1962; 57: 214.
Murdock J. The treatment of severe Pseudomonas pyocyanea infections with colistin. Proceedings of the Third International Congress of Chemotherapy; 1964; Stuttgart, Germany. p. 319.
Moore M.B., McCulley J.P. Acanthamobea keratitis associated with contact lenses: Six consecutive cases of successful management. Br J Ophthalmol 1989; 73: 271.
Ledingham I.M., Alcock S.R., Eastaway A.T., et al. Triple regimen of selective decontamination of the digestive tract, systemic cefotaxime, and microbiological surveillance for prevention of acquired infections in intensive care. Lancet 1988; 1: 785.
Johanson W.G., Siedenfeld J., et al. Prevention of nosocomial pneumonia using topical and parenteral antimicrobial agents. Am Rev Respir Dis 1988; 137: 265.
Levin A.S., Bazone A.A., Penco J., et al. Intravenous colistin as therapy for nosocomial infections caused by multydrug-resistant P. aeruginosa and A. baumannii. Clin Infect Dis 1999; 28: 1008-11.
Feeley T., DuMoulin G., Hedley-Whyte J., et al. Aerosol polymyxin and pneumonia in seriously ill patients. N Engl J Med 1975; 193: 471.
Unertl K., Ruckdeschel G., Selbmann H., et al. Prevention of colonization and respiratory infections in long-term ventilated patients by local antimicrobial prophylaxis. Intens Care Med 1987; 13: 106.
Conway S.P., Pond H.N., Watson A., et al. Intravenous colistin sulphomethate in acute respiratory exacerbations in adult patients with cystic fibrosis. Thorax 1996; 52: 987-93.
Zylberberg H., Vargaftig J., Barbieux C., et al. Prolonged efficiency of secondary prophylaxis colistin aerosols for respiratory infection due to P. aeruginosa in patients infected with human immunodeficiency virus. Clin Infect Dis 1996; 23: 641-3.
Kurrle E., DeKiler A., Gaus W., et al. Prevention of infection in acute leukemia: A prospective randomized study of two different drug regimes for antimicrobial prophylaxis. Infections 1986: 14: 226.
Manan F., Kibbler C., Noone P. Activity of ciprofloxacin and colistin against Pseudomonas aeruginosa isolates from neutropenic patients: A possible approach to prophylaxis (letter). J Antimicrob Chemother 1988; 22: 953.
Frederiksen B., Koch C., Noiby N. Antibiotic treatment of initial colonization with P. aeruginosa postpones chronic infections and prevents deterioration of pulmonary function in cystic fibrosis. Pediatr Pulmon 1997; 23: 330-5.
Bauldoff G.S., Nunley D.R., Manzetti J., et al. Use of aerosolized colistin sodium in cystic fibrosis patients awaiting lung transplantating. Transplantation 1997; 64: 748-52.
Klugman K.P., Dagan R. Efficacy and safety of meropenem in the treatment of meningitis. Antimicrob Agents Chemother 1995; 39: 1140-6.
Jimenez-Mejias M.E., Pachon J., Becerril B., et al. Treatment of multidrug-resistant Acinetobacter baumannii meningitis with ampicillin/sulbactam. Clin Infect Dis 1997; 24: 932-5.
Urban C., Go E., Mariano N., et al. Effect of sulbactam on infections caused by imipenem-resistant Acinetobacter calcoaceticus biotype anitratus. J Infect Dis 1993; 167: 448-51.
Wood C.A., Reboli A.C. Infections causes by imipenem-resistant A. calcoaceticus biotype anitratus. J Infect Dis 1993; 168: 1602-3.
Corbella X., Pujol M., Ayats J., et al. Relevance of digestive tract colonization in the epidemiology of multiresistant Acinetobacter baumannii. Clin Infect Dis 1996; 23: 329-34.
Go E.S., Urban C., Burns J., et al. Clinical and molecular epidemiology of Acinetobacter infections sensitive only to polymyxin B and sulbactam. Lancet 1994; 344: 1329-32.
Bergogne-Berezin E., Towner K.J. Acinetobacter spp. as nosocomial pathogens: microbiological. Clinical and epidemiological features. Clin Microbiol Rev 1996; 9: 148-65.
Fernandes-Viladrich P., Corbella X., Corral L., et al. Successful treatment of ventriculitis due to carbapenem-resistant Acinetobacter baumannii with intraventricular colistin sulfomethat sodium. Clin Infect Dis 1999; 28: 916-7.
Вместе с этим смотрят:
Blood, sweat and tears
La drogue
Principala cauza a handicapului
The practice of modern medicine
Toma Cerba