Белки: история исследования, химсостав, свойства, биологические функции
Страница 15
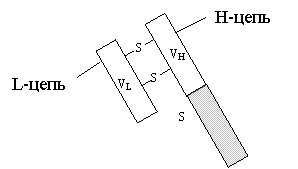
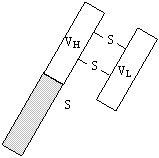
Две полипептидные цепи имеют размер порядка 200 аминокислотных остатков и называются легкими цепями (L-цепи). Две другие вдвое больше по размеру и называются тяжелыми цепями (H-цепи). На N-конце обеих цепей имеется вариабельная область размером немногим более 100 аминокислотных остатков, которая различна у иммуноглобулинов, настроенных на разные антигены – именно она определяет специфичность данной популяции лимфоцитов.
| | | | | |
| |
Вариабелная об-ласть формирует центр, непосред-ственно связыва-ющийся с опреде-ленным антиге-ном или гаптеном остальная часть, составляющая у легкой цепи поло-вину молекулы, а у тяжелой – ¾ , не зависит от вида иммуноглобу-лина. Эта область назы-вается кон-стантной. | |
| |  |
| | |  |
|
|

 СH СH
СH СH


СL СL 

 СH2 СH2
СH2 СH2




 СH3 СH3
СH3 СH3

Согласно современным представ-лениям, каждый тип иммуногло-булина вырабатывается группой В-лимфоцитов, произошедших от одного общего предшественника. Такую группу лимфоцитов называют клоном. Первые успехи в изучении строения иммуноглобулинов были связаны с изучением иммуноглобулинов, полученных от больных миеломой (патология, связанная со сверхпродукцией определенного вида иммуноглобулинов). У больных, от одного злокачественно разросшегося клона В-лимфоцитов, вырабатывается огромное количество индивидуального иммуноглобулина, который сравнительно легко отделить от остальных. Далее производили слияние клеток миеломы как носителей способности к неограниченному размножению с нормальными В-лимфоцитами как носителями программы выработки антител определенной, задаваемой экспериментатором специфичности. Получающиеся клетки, гибридомы сохраняют способность к неограниченному размножению и вырабатывают при этом только определенные антитела. Так как гибридомы происходят из одной слитой клетки, то они представляют собой единый клон; получающиеся из них антитела поэтому называют моноклональными антителами (МАТ).
5) Структурная функция:
Наряду с белками, выполняющими тонкие высокоспециализирован-ные функции, существуют белки, имеющие в основном структурное значение. Они обеспечивают механическую прочность и другие механические свойства отдельных тканей живых организмов. В первую очередь это коллаген - основной белковый компонент внеклеточного матрикса соединительной ткани. У млекопитающих коллаген составляет до 25% общей массы белков. Коллаген синтезируется в фибробластах - основных клетках соединительной ткани. Первоначально он образуется в виде проколлагена - предшественника, который проходит в фибробластах определенную химическую обработку, состоящую в окислении остатков пролина до гидроксипролина и некоторых остатков лизина до d-гидроксилизина. Коллаген формируется в виде трех скрученных в спираль полипептидных цепей, которые уже вне фибробластов объединяются в коллагеновые фибриллы диаметром несколько сотен нанометров, а последние - уже в видимые под микроскопом коллагеновые нити.
В эластичных тканях - коже, стенках кровеносных сосудов, легких - помимо коллагена внеклеточный матрикс содержит белок эластин, способный довольно в широких пределах растягиваться и возвращаться в исходное состояние.
Еще один пример структурного белка - фиброин шелка, выделяемый гусеницами шелкопряда в период формирования куколки и являющийся основным компонентом шелковых нитей.