Белки: история исследования, химсостав, свойства, биологические функции
Белки: история исследования, химсостав, свойства, биологические функции
Глава 1. Введение.
Довольно банальными стали сейчас сообщения о революции в биологии. Бесспорным считается и то, что эти революционные изменения были связаны с формированием на стыке биологии и химии комплекса наук, среди которых центральное положение занимали и занимают молекулярная биология и биоорганическая химия.
“Молекулярная биология - наука, ставящая своей целью познание природы явлений жизнедеятельности путем изучения биологических объектов и систем на уровне, приближающемся к молекулярному… характерные проявления жизни… обусловлены структурой, свойствами и взаимодействием молекул биологически важных веществ, в первую очередь белков и нуклеиновых кислот”
“Биоорганическая химия - наука, изучающая вещества, лежащие в основе процессов жизнедеятельности…основные объекты биоорганической химии - биополимеры (белки и пептиды, нуклеиновые кислоты и нуклеотиды, липиды, полисахариды и т.д.).
Из этого сопоставления становится очевидным, сколь важно для развития современной биологии изучение белков.
Глава 2. История исследования белка
2.1. Начальные этапы в химии белка
Белок попал в число объектов химических исследований 250 лет тому назад. В 1728 году итальянский ученый Якопо Бартоломео Беккари получил из пшеничной муки первый препарат белкового вещества – клейковины. Он подверг клейковину сухой перегонке и убедился, что продукты такой перегонки были щелочными. Это было первое доказательство единства природы веществ растительного и животного царств. Он опубликовал результаты своей работы в 1745 году, и это была первая статья о белке.
В XVIII – начале XIX веков неоднократно описывали белковые вещества растительного и животного происхождения. Особенностью таких описаний было сближение этих веществ и сопоставление их с веществами неорганическими.
Важно отметить, что в это время, еще до появления элементного анализа, сложилось представление о том, что белки из различных источников – это группа близких по общим свойствам индивидуальных веществ.
|
Формулы белков
Д. Дальтона | |
В 1810 году Ж. Гей-Люссак и Л. Тенар впервые определили элементный состав белковых веществ. В 1833 году Ж. Гей-Люссак доказал, что в белках обязательно присутствует азот, а вскоре было показано, что содержание азота в различных белках приблизительно одинаково. В это же время английский химик Д. Дальтон попытался изобразить первые формулы белковых веществ. Он представлял их довольно просто устроенными веществами, но чтобы подчеркнуть их индивидуальное различие при одинаковом составе, он прибег к изображению молекул, которые бы сейчас назвали изомерными. Однако понятия изомерии во времена Дальтона еще не было.
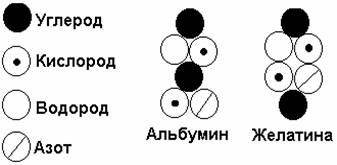 Были выведены первые эмпирические формулы белков и выдвинуты первые гипотезы относительно закономерностей их состава. Так, Н.Либеркюн считал, что альбумин описывается формулой C72H112N18SO22, а А.Данилевский полагал, что молекула этого белка по крайней мере на порядок больше: C726H1171N194S3O214.
Были выведены первые эмпирические формулы белков и выдвинуты первые гипотезы относительно закономерностей их состава. Так, Н.Либеркюн считал, что альбумин описывается формулой C72H112N18SO22, а А.Данилевский полагал, что молекула этого белка по крайней мере на порядок больше: C726H1171N194S3O214.
Немецкий химик Ю. Либих в 1841 году предположил, что белки животного происхождения имеют аналоги среди растительных белков: усвоение белка легумина в организме животного, по Либиху, вело к накоплению аналогичного белка – казеина. Одной из самых распространенных теорий доструктурной органической химии была теория радикалов – неизменных компонентов родственных веществ. В 1836 году голландец Г. Мульдер высказал предположение о том, что все белки содержат один и тот же радикал, который он назвал протеином (от греческого слова “первенствую”, “занимаю первое место”). Протеин, по Мульдеру, имел состав Pr = C40H62N10O12. В 1838 году Г. Мульдер опубликовал формулы белков, построенные на основании теории протеина. Это были т.н. дуалистические формулы, где радикал протеина служил положительной группировкой, а атомы серы или фосфора – отрицательной . Вместе они образовывали электронейтральную молекулу: белок сыворотки крови Pr10S2P, фибрин Pr10SP. Однако аналитическая проверка данных Г. Мульдера, проведенная русским химиком Лясковским, а также Ю. Либихом, показала, что “белковых радикалов” не существует.
В 1833 году немецкий ученый Ф. Розе открыл биуретовую реакцию на белки – одну из основных цветных реакций на белковые вещества и их производные в настоящее время (подробнее о цветных реакциях на стр.53). Был сделан также вывод о том, что это самая чувствительная реакция на белок, поэтому она в то время привлекла наибольшее внимание химиков.
В середине XIX века были разработаны многочисленные методы экстракции белков, очистки и выделения их в растворах нейтральных солей. В 1847 году К. Рейхерт открыл способность белков образовывать кристаллы. В 1836 году Т. Шванн открыл пепсин – фермент, расщепляющий белки. В 1856 году Л. Корвизар открыл еще один подобный фермент – трипсин. Изучая действие этих ферментов на белки, биохимики пытались разгадать тайну пищеварения. Однако наибольшее внимание внимание привлекли вещества, получающиеся в результате действия на белки протелитических фермнтов (протеаз, к ним относятся вышеприведенные ферменты): одни из них были фрагментами исходных молекул белка (их назвали пептонами), другие же не подвергались дальнейшему расщеплению протеазами и относились к известному еще с начала века классу соединений – аминокислот (первое аминокислотное производное – амид аспарагин был открыт в 1806 году, а первая аминокислота – цистин в 1810). Аминокислоты в составе белков впервые обнаружил в 1820 году французский химик А. Браконно. Он применил кислотный гидролиз белка и в гидролизате обнаружил сладковатое вещество, названное им глицином. В 1839 году было доказано существование в составе белков лейцина, а в 1849 году Ф. Бопп выделил из белка еще одну аминокислоту – тирозин (полный список дат открытий аминокислот в белках см. Приложение II).
К концу 80-х гг. XIX века из белковых гидролизатов было выделено уже 19 аминокислот и стало медленно укрепляться мнение, что сведения о продуктах гидролиза белков несут важную информацию о строении белковой молекулы. Тем не менее, аминокислоты считались обязательным, но неглавным компонентом белка.
В связи с открытиями аминокислот в составе белков французский ученый П. Шютценберже в 70-х гг. XIX века предложил т. н. уреидную теорию строения белка. Согласно ей молекула белка состояла из центрального ядра, роль которого выполняла молекула тирозина, и присоединенных к нему (с замещением 4 атомов водорода) слож ных группировок, названных Шютценберже лейцинами. Однако гипотеза было очень слабо подкреплена экспериментально, и дальнейшие исследования показали несостоятельность.
2.2. Теория “углеазотных комплексов” А.Я.Данилевского
Оригинальную теорию о строении белка высказал в 80-х гг. XIX века русский биохимик А. Я. Данилевский. Первым из химиков он обратил внимание на возможный полимерный характер строения белковых молекул. В начале 70-х гг. он писал А.М. Бутлерову, что “частицы альбумина есть смешанный полимерид”, что для определения белка он не находит “термина более подходящего, чем слово полимер в широком смысле”. Изучая биуретовую реакцию он предположил, что эта реакция связана со структурой перемежающихся атомов углерода и азота – N – C – N – C – N – , которые входят в т.н. углеазотный комплекс R’ – NH – CO – NH – CO – R”. На основе данной формулы Данилевский полагал, что в молекуле белка содержится 40 таких углеазотных комплексов. Отдельные углеазотноаминокислотные комплекс, по Данилевскому, выглядели так:
R – NH – CO – NH – CO – NH – CH2 – COOH
Глицин
R – NH – CO – NH – CO – NH – C2H4 – COOH
Аланин
R – NH – CO – NH – CO – NH – C2H3(OH) – COOH
Серин
По Данилевскому углеазотные комплексы могли соединяться эфирной или амидной связью с образованием высокомолекулярной структуры.