Исследование аккумуляторной батареи
Исследование аккумуляторной батареи
Устройство аккумуляторной батареи.
Рисунок: разрез аккумуляторной батареи
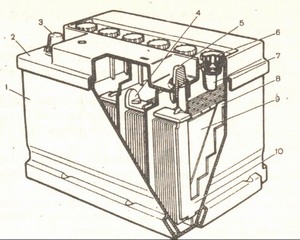
1 – корпус; 2 – крышка; 3 – положительный вывод; 4 – межэлементное соединение;
5 – отрицательный вывод ; 6 – пробка; 7 – индикатор для проверки уровня электролита;
8 – сепаратор; 9 – положительная пластина; 10 – отрицательная пластина.
Корпус батареи имеет шесть секций, в которых размещены шесть последовательно соединенных элементов, напряжением по 2 В. Каждый элемент состоит из положительных и отрицательных пластин, разделенных тонкими и пористыми пластмассовыми пластинами (сепараторами). Малая толщина и большая пористость сепараторов обеспечивает низкое внутренне сопротивление батареи и, тем самым, позволяют получить низкое внутреннее сопротивление батареи и, тем самым, позволяют получить большую силу разрядного тока при низких температурах. В элементы залит электролит, которым служит раствор серной кислоты в дистиллированной воде. Электролит заливается до уровня, на 10-15 мм выше верхнего края сепараторов, или предохранительного щитка. Пластины элементов представляют собой решетки, отлитые из сплава свинца и сурьмы. Ячейки решеток заполнены пористой активной массой. У заряженной батареи активная масса положительных пластин состоит из перекиси свинца (коричневого цвета), а отрицательных – из губчатого свинца (серого цвета). При разряде батареи активная масса положительных и отрицательных пластин превращается в мелкокристаллический сернокислый свинец (белого цвета).
Техническая характеристика аккумуляторной батареи 6СТ55А
Тип батареи 6СТ55А
Номинальное напряжение, В 12
Номинальная емкость при 20-часовом режиме разряда,
и температуре электролита 25° С в начале разряда, А´ч 55
Разрядная сила тока при 20-часовом режиме разряда, А 2,75
Разрядная сила тока при стартерном режиме и температуре
электролита -18° С, А 255
Напряжение после 30с разряда при стартерном режиме, В ³8,4
Время разряда при стартерном режиме до напряжения 6 В, мин ³3
Сила тока разряда, А 5,5
Объем заливаемого электролита, л 3,8
Габаритные размеры, мм:
Длина 260±1
Ширина 172±1
Высота 223±1
Масса, кг:
с электролитом 21
без электролита 17
Маркировка: 6 СТ 55
Стартерная автомобильная батарея, с шестью последовательно соединенными аккумуляторами, двенадцативольтовая, номинальной емкостью 55 А´ч.
Первая цифра указывает число аккумуляторов в батарее; буквы СТ – тип батареи (стартерная), следующие за этими буквами число – номинальную емкость батареи (55 А´ч)
Последующие буквы – материал моноблока, сепараторов. После всех указанных цифр и букв наносится номер ГОСТа, по которому изготовлена батарея.
Физические процессы, происходящие в аккумуляторе.
Связаны со свойством электролитического растворения металлов, которое заклю- чается, в переходе положительно заряженных ионов металла в раствор. Причем легкоокисляющиеся металлы (свинец) обладают этим свойст- вом в большей степени, чем трудноокисляющиеся. При погружении электрода, на котором образовался свинец, в раствор электролита от свинца начнут отщепляться положительно заряженные ионы свинца и переходить в раствор, при этом электрод будет заряжаться о- трицательно. По мере протекания процесса возрастает разность потенци- алов раствора и электрода, следовательно, возрастает и осмотическое давление положительных ионов раствора. Вследствие этого переход ио- нов свинца в раствор не может продолжаться долго и при какой-то определенной разности потенциалов электрода и раствора наступит равновесие между силой электролитической упругости растворения свинца, с одной стороны, и силами электростатического поля и осмоти- ческого давления с другой. В результате, растворение свинца пре- кратится.
При погружении положительного электрода в раствор серной кисло- ты происходит то же явление, но результат получается иной: двуокись свинца положительного электрода, в ограниченном количестве перехо- дит в раствор, где при соединении с водой ионизируется на четырех- валентные ионы свинца. и одновалентные ионы гидрокисла ОН —. Четырехвалентные ионы свинца, осаждаясь на электроде, создают по- ложительный потенциал относительно раствора.
При указанных концентрациях серная кислота диссоциирует в воде практически только на ионы H+ и HSO4- . Поэтому реакции на электродах описывается следующими
следующими уравнениями:
Общая токообразующая реакция в аккумуляторе:
Таким образом, при разряде аккумулятора расходуется серная кислота, образуется вода, а на обоих электродах – сульфат свинца. При заряде процессы протекают в обратном направлении.
Приготовление электролита
Электролит изготовляют из смеси аккумуляторной серной кислоты с дистиллированной водой. Электролит готовят в фаянсовой, керамической, или эбонитовой посуде. В стеклянной посуде электролит готовить нельзя, так как стекло может лопнуть от высоких температур. Кислоту тонкой струей вливают в воду, непрерывно помешивая раствор стеклянной, или эбонитовой палочкой. Воду в кислоту вливать нельзя, для предотвращения разбрызгивания.
Плотность электролита контролируется ареометром, и при изменении окружающей температуры меняется, поэтому, в зависимости от температуры электролита, при измерении следует учитывать поправки:
|
Температура электролита, °С |
Поправка, г/см3 |
|
от –40 до –26
от –25 до –11
от –10 до +4
от +5 до +19
от +20 до +30
от +31 до +45 |
-0,04
-0,03
-0,02
-0,01
0,00
+0,01 |
В зависимости от климатической зоны, в аккумуляторную батарею заливается электролит плотностью:
|
Климатический район °С |
Время года |
Полностью заряженная батарея |
Батарея разряжена |
|
на 25 % |
на 50 % |
|
Очень холодный (от –50 до -30) |
Зима |
1,30 |
1,26 |
1,22 |
|
Лето |
1,28 |
1,24 |
1,20 |
|
Холодный (от –30 до -15) |
Круглый год |
1,28 |
1,24 |
1,20 |
|
Умеренный (от –15 до -8) |
Круглый год |
1,28 |
1,24 |
1,20 |
|
Теплый влажный (от 0 до +4) |
Круглый год |
1,23 |
1,19 |
1,15 |
|
Жаркий сухой (-15 до +4) |
Круглый год |
1,23 |
1,19 |
1,15 |