Актинобациллезная (гемофилезная)
Страница 8
Определение иммуногенности вакцины в опытах на белых мышах в процессе хранения при 4-6°С показало, что в интервале 1-11 месяцев ИМД50 препарата колебалась в пределах 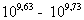 микробных клеток, что позволяет говорить о малом изменении активности препарата в указанные сроки.
микробных клеток, что позволяет говорить о малом изменении активности препарата в указанные сроки.
С учётом результатов испытания различных типов инактивированных вакцин на лабораторных животных и свиньях была проведена апробация экспериментальных образцов вакцин против актинобациллёзной плевропневмонии свиней в производственных условиях.
Первоначально эмульгированная вакцина была испытана на безвредность и иммунологическую эффективность на ограниченном контингенте свиней различного возраста в хозяйстве, неблагополучном по актинобациллёзной плевропневмонии свиней. В последующем в этом же хозяйстве проводилась поголовная вакцинация животных по следующей схеме: внутримышечно свиноматкам за 20-25 дней до ожидаемого опороса в дозе 1 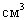 , аналогичную дозу вводили ремонтным свинкам, поросят вакцинировали в дозе 1
, аналогичную дозу вводили ремонтным свинкам, поросят вакцинировали в дозе 1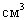 в возрасте 35 - 40 дне й. В период проведённых исследований вакцинации было подвергнуто 1677,4 тысячи свиней.
в возрасте 35 - 40 дне й. В период проведённых исследований вакцинации было подвергнуто 1677,4 тысячи свиней.
Исследования показали, что до начала вакцинации падёж свиней с диагнозом актинобациллёзной плевропневмонии составил 30,22% от общего количества павших животных, при частичной вакцинации поголовья -12,28%, при полной вакцинации - 8,89%. Между уровнем вакцинации и падёжом свиней от актинобациллёзной плевропневмонии установлена достаточно сильная обратная связь ( r= -0,71). Применение вакцины обеспечило снижение отхода свиней по причине актинобациллёзной плевропневмонии, в зависимости от анализируемого периода в 3 - 5 раз и увеличение живой массы поросят на 7,42 - 8,29 кг при передаче на откорм. Частота терапевтического вмешательства ветеринарного персонала в группах вакцинированных поросят была в 2,11 раза реже, чем среди не вакцинированных животных.
Выводы
1. Исследование таксономического положения эпизоотических штаммов НАД--зависимых бактерий, выделенных при пневмониях и генерализованных серозитах свиней методом нумерического анализа, позволило дифференцировать их по фенотипическим свойствам на кластеры, соответствующие видам Actinobacillus (Haemophilus) pleuropneumoniae, Haemophilus parasuis и таксону гемофильных бактерий «малая группа». Культуры кластера Actinobacillus (Haemophilus) pleuropneumoniae имеют большее фенотипическое сходство с видами рода Actinobacillus (91,23) и меньшее с представителями рода Haemophilus (81,99%). На уровне подобия 95% бактерий кластера «малая группа» выделяются в самостоятельный таксон.
2. Генетический анализ таксономического положения референтных и эпизоотических НАД--зависимых штаммов Actinobacillus (Haemophilus) pleuropneumoniae и культур P.haemolytica - подобных бактерий (2-ой биовар A.pleuropneumoniae) показал, что они образуют генетическую общность с уровнем гомологии ДНК 70-98%. ДНК культур 2-го биовара и эпизоотических штаммов A.pleuropneumoniae имеют гомологию с ДНК A.suis – 33 - 38%, с ДНК H.parasuis и P.multocida – не более 9%, что свидетельствует о принадлежности эпизоотических и референтных штаммов к роду Actinobacillus, но не Haemophilus и Pasteurella. Референтный штамм J 95 гемофильных бактерий таксона «С» по результатам гибридизации ДНК к роду Haemophilus не относится.
3. Результаты изучения таксономического положения НАД--зависимых бактерий, выделенных при пневмониях и серозитах свиней, позволили определить в качестве основных дифференцирующих фенотипических признаков: НАД—зависимость, образование щелочной фосфатозы, уреазы, гемолизина, кислоты из ксилозы, маннита, маннозы. Для дифференциации культур НАД—независимого биовара A.pleuropneumoniae от сходных бактерий минимальный набор определяемых признаков включает продукцию индола, уреазы, утилизацию цитратов, наличие жгутиков. Для установления ферментативных свойств НАД--зависимых бактерий можно использовать дифференциально - диагностические среды в микрообъёмах и диагностический набор ПБДЭ Горьковского НИЭМ, что исключает использование чистого НАД или других его источников как факторов роста.
4. К A.pleuropneumoniae и H.parasuis чувствительны при внутрибрюшинном и интраназальном заражении морские свинки (живая масса 200-250г) и белые мыши (живая масса 14-16г), которые могут быть использованы для определения патогенных свойств культур, изучения вопросов пато - и иммуногенеза при этих инфекциях.
5. Входными воротами возбудителя инфекции при гемофилёзном полисерозите являются органы дыхания. При экспериментальном (трахеальном) заражении свиней H.parasuis инкубационный период составляет 6-8 часов. У заражённых свиней развивается катаральная пневмония и, в результате диссеминации возбудителя, генерализованные серозиты с одновременным поражением серозных оболочек грудной, брюшной полостей, пери – и эпикарда.
6. В естественных условиях H.parasuis вызывает у поросят-отъёмышей пневмонию, у части животных развивается септическая стадия с поражением серозных оболочек, суставов, головного мозга. У отдельных поросят встречается классическая форма болезни Глессера - генерализованные серозиты без микроскопически выраженной пневмонии. У экспериментально заражённых и естественно больных свиней наиболее часто удаётся изолировать H.parasuis из поражённых серозных оболочек.
7. Входными воротами возбудителя инфекции при актинобациллёзной плевропневмонии свиней являются органы дыхания. Инкубационный период при экспериментальном интраназальном заражении составляет 2-4 часа, контактном – до 3 суток, в естественных условиях – 2-8 суток. Диссеминация возбудителя в организме заражённых животных происходит на фоне имеющихся изменений в лёгких. Наиболее постоянно культуры возбудителя удаётся изолировать от экспериментально заражённых и естественно больных животных из поражённой ткани лёгких и регионарных лимфатических узлов.
8. Культуры A.pleuropneumoniae на начальной стадии логарифмического роста синтезируют термолабильные гемолизин и экзотоксин, которые определяют повышенную вирулентность молодых (6-8- часовых) культур возбудителя и играют существенную роль в развитии патологических изменений в лёгких заражённых животных.
9. Макроскопически сходные изменения в лёгких свиней могут вызвать A.pleuropneumoniae, гемофильные бактерии «малой группы» и A.suis , поэтому решающее значение в диагностике актинобациллёзной плевропневмонии имеют результаты бактериологического исследования.
10. При серологической идентификации эпизоотических культур H.parasuis установлено наличие сероваров А,В,С,Д, Бакоса, а также выявлены четыре серологические группы штаммов, не укладывающиеся в известную схему Бакоса, которая не охватывает всего антигенного многообразия вида.
11. Серологическая идентификация эпизоотических культур A.pleuropneumoniae, выделенных от свиней в хозяйствах Российской Федерации, выявила наличие сероваров 2,3,4,6 и группы нетипируемых штаммов. Исследования в РНГА сывороток крови свиней из различных хозяйств показало доминирование антител к сероварам 1,2,4,6,12.
12. На основании проведённых исследований разработана и используется в практике схема лабораторной диагностики актинобациллёзная ( гемофилёзная ) плевропневмонии и гемофилёзного полисерозита свиней, включающая: правила взятия материала для бактериологического исследования, методы выделения и идентификации культур возбудителя по биологическим свойствам. Также разработаны и рекомендованы методы видовой и серовариантной идентификации культур A.pleuropneumoniae и обнаружения антигенов этого вида бактерий в патологическом материале при помощи реакции коагглютинации.
13. Разработана и предложена технология изготовления, контроля использования вакцины против гемофилёзной (актинобациллёзная) плевропневмонии свиней, что нашло отражение в соответствующих нормативных документах: «Инструкция по изготовлению и контролю вакцины против гемофилёзной плевропневмонии свиней», «Вакцина против гемофилёзной плевропневмонии свиней эмульгированная. Технические условия ТУ 10-09-53-90». «Наставление по применению вакцины против гемофилёзной плевропневмонии свиней эмульгированной», утверждённых ГУВ ГК Совмина СССР по продовольствию и закупкам 11.07.1990г.