Эволюция биологических механизмов запасания энергии
Страница 2
Рис. 1. Схема "аденинового" фотосинтеза -предполагаемого первичного механизма запасания энергии в живой клетке. Квант ультрафиолетового света поглощается адениновой частью аденозиндифосфата (АДФ), переводя ее в возбужденное состояние. Возбуждение облегчает присоединение неорганического фосфата (Ф) к аминогруппе аденина. В результате образуется ФАДФ, изомер аденозинтрифосфата (АТФ), где третий фосфат присоединен не к пирофосфатно-му "хвосту", а к адениновой "голове" АДФ. Затем происходит перенос фосфата от "головы" к "хвосту" с образованием обычного АТФ
РНК, ДНК, БЕЛКИ И МЕМБРАНЫ
В дальнейшем не слишком специфичный и нерегулируемый катализ, осуществляемый низкомолекулярными коферментами, был дополнен (а затем и вытеснен) процессами с участием высокомолекулярных катализаторов-ферментов, отличающихся огромной избирательностью в отношении субстратов и возможностью регулировать катализ. По-видимому, первыми ферментами были рибонуклеиновые кислоты (РНК) - полимеры, составленные из мономеров-нуклеотидов. Можно полагать, что адениновый фотосинтез катализировался комплексами РНК с магниевыми солями АДФ и фосфата. При этом РНК могла бы выполнять также роль антенны, собирающей ультрафиолетовый свет и передающей возбуждение на АДФ.
Надо сказать, что еще и сегодня в некоторых (весьма немногочисленных) случаях биохимические реакции могут катализироваться в искусственных условиях рибонуклеиновыми кислотами (так называемыми рибозимами). Однако несомненно, что каталитические функции современных организмов осуществляются белками, обладающими большим, чем РНК, разнообразием химических группировок и их сочетаний.
Синтез белков, включая кодирование их структуры, первоначально осуществлялся рибонуклеиновыми кислотами. Затем функция кодирования была передана дезоксирибонуклеиновым кислотам (ДНК), а сам катализ стал обслуживаться комплексами РНК и специальных белков (рибосомами и факторами трансляции), информационными и транспортными РНК и соответствующими ферментами.
Другим важнейшим изобретением биологической эволюции стали жиры и жироподобные вещества, прежде всего фосфолипиды. Замечательной особенностью фосфолипидов является их способность самопроизвольно, без какой-либо помощи извне, образовывать тончайшую пленку, непроницаемую для гидрофильных веществ, таких, как нуклеотиды-коферменты, РНК, ДНК, белки и углеводы. Эта пленка (мембрана) представляет собой бислой, образованный двумя рядами молекул фосфолипидов, соприкасающихся гидрофобными (углеводородными) "хвостами". При этом гидрофильные "головы" (фосфатные остатки) фосфолипидов оказываются на двух противоположных поверхностях мембраны.
С образованием мембран стало возможно говорить о первичной живой клетке, содержимое которой было отделено от внешней среды достаточно надежным барьером. Появление клетки как обособленного мельчайшего пузырька могло бы сыграть роль в защите от неблагоприятных эффектов ультрафиолетового облучения.
Как избежать разрушительных эффектов ультрафиолетового света
Запасные энергетические ресурсы и гликолиз
Ультрафиолетовый свет - обоюдоострое оружие. Он хорош тем, что способен развязать разнообразные химические реакции, среди которых могут быть полезные, как, например, фосфорилирование адениновой аминогруппы АДФ. Но в то же время (и по той же причине) ультрафиолетовый свет опасен: он может разрушить уже синтезированные молекулы живой клетки. Одним из способов уменьшить ультрафиолетовую опасность могли стать запасные вещества - энергетические ресурсы, образуемые на свету, чтобы затем использоваться в темноте. Ультрафиолетовый свет, достигающий поверхности океана, не может проникать на сколько-нибудь значительную глубину из-за мутности, наличия растворенных веществ, поглощающих ультрафиолетовые кванты и, быть может, флуктуации плотности морской воды. Фактически только очень тонкий поверхностный слой подвергается бомбардировке этими квантами. Данное обстоятельство позволяет предположить следующий механизм энергообеспечения первичных живых клеток. Под действием движения слоев жидкости в океане клетки постоянно циркулировали между тонкой верхней пленкой воды, доступной для ультрафиолетового света, и более глубокими слоями, которых он не достигал. При этом вблизи поверхности происходил синтез АТФ, использовавшегося для образования резервных соединений, которые затем расщеплялись на глубине, поддерживая ресинтез АТФ. В результате короткие экспозиции на ультрафиолетовом свету чередовались с гораздо более длительными периодами, где ультрафиолетовой опасности уже не было (рис. 2). Кроме того, резервные вещества помогали клеткам пережить ночь.
Хорошими кандидатами на роль энергетического резерва первичных клеток могли быть неорганические пиро- и полифосфаты. Они и сегодня играют эту роль у некоторых видов живых существ. Например, в клетках грибов полифосфаты образуются из АТФ в условиях избытка энергетических ресурсов и расщепляются, давая АТФ, при дефиците источников энергии. Однако в подавляющем большинстве дошедших до нас организмов функцию легко мобилизуемого энергетического резерва выполняют не полифосфаты, а углеводы. Их синтез за счет энергии АТФ (гликогенез) представляет собой длинную последовательность реакций, намного более сложную, чем синтез полифосфатов из АТФ.
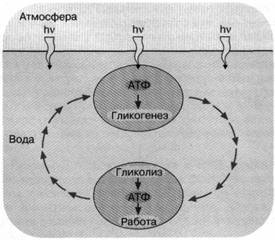
Рис. 2. Энергетика первичной живой клетки, основанная на "адениновом" фотосинтезе. Предполагается, что ультрафиолетовые кванты, достигая поверхности первичного океана, использовались клеткой для синтеза АТФ, который запускал синтез углеводородов (гликогенез). Клетка, увлекаемая потоком океанской воды с поверхности на некоторую глубину, оказывалась вне досягаемости ультрафиолетового облучения. Здесь происходило расщепление накопленных углеводов и синтез АТФ, использовавшегося для совершения клеткой различных типов полезной работы
Преимущество углеводов перед полифосфатами состоит в том, что в них запасены не только энергия, но и "строительный материал". Расщепление углеводов (гликолиз) дает помимо АТФ карбоновые кислоты, такие, как пировиноградная кислота, которая может использоваться клеткой при биосинтезе самых разнообразных соединений.
Описаны два основных типа гликолиза. В одном случае (спиртовое брожение) конечными продуктами расщепления углеводов оказываются этиловый спирт и углекислый газ — вещества, легко проникающие через мембрану клетки. Это обстоятельство имеет как преимущества (нет проблемы переполнения клетки конечными продуктами гликолиза), так и недостатки (трудно вернуться назад, к углеводу, если конечные продукты уже вышли из клетки и разбавились в океане внешней среды).
Указанный недостаток отсутствует во втором, сегодня гораздо более распространенном типе гликолиза, когда конечным продуктом оказывается молочная или какая-либо другая карбоновая кислота. Молочная кислота не проникает через мембрану, не покидает пределы клетки и потому может быть использована клеткой для ресинтеза углеводов, когда возникает такая возможность. Неудачно лишь то, что молекулы молочной кислоты, образуясь, диссоциируют с образованием ионов лактата и водорода. Последние также не могут пройти через мембрану, остаются в клетке и закисляют ее содержимое. Закисление, если его не предотвратить,
должно привести к гибели клетки из-за кислотной денатурации белков. Решение этой проблемы описано в следующем разделе.
ПРОТОННЫЕ КАНАЛЫ И Н+-АТФАЗА ПРЕДОТВРАЩАЮТ ЗАКИСЛЕНИЕ КЛЕТКИ ПРИ ГЛИКОЛИЗЕ
У современных клеток проблема проникновения через клеточную мембрану веществ, которые сами по себе не могут сквозь нее пройти, решается с помощью встроенных в мембрану белков-переносчиков. В частности, известны белки — переносчики ионов Н+. Так называемый фактор F0 — белок, входящий в состав Н+ - АТФ - синтазы, действует как переносчик Н+ или протонный канал.