Эволюция биологических механизмов запасания энергии
Страница 3
Можно предположить, что у первичных гликолизирующих клеток фактор F0 функционировал при отсутствии фактора F1 второго компонента Н+ - АТФ - синтазы, разрешая ионам Н+, образующимся при гликолизе, покинуть пределы клетки. Тем самым предотвращалось закисление внутриклеточной среды, которая оказывалась в равновесии по ионам Н+ с внеклеточной средой. Единственным ограничением гликолиза в такой ситуации должно было стать закисление внеклеточной среды, что автоматически вело к закислению содержимого клетки. Снять данное ограничение можно было достроив белок - переносчик ионов Н+ (фактор F0) другим белком, называемым фактором F,. способным использовать энергию АТФ для активной откачки из клетки ионов Н+ через фактор F0. Известно, что Н+ - АТФ - синтаза (комплекс факторов F0 и fj), действуя в обратном направлении, способна катализировать вместо синтеза АТФ пиролиз АТФ, сопряженный с откачкой ионов Н+. Этот процесс носит название Н+ - АТФазной реакции. Можно полагать, что с образованием Н+ - АТФазы завершилось формирование первичной клетки, использовавшей ультрафиолетовый свет в качестве источника энергии для жизнедеятельности (рис. 3).
ВОЗНИКНОВЕНИЕ ФОТОСИНТЕЗА, ИСПОЛЬЗУЮЩЕГО ВИДИМЫЙ СВЕТ
Бактериородопсиновый фотосинтез
Со временем все меньше ультрафиолетовых квантов достигало поверхности Земли. Причиной тому было образование озонового слоя атмосферы в условиях повышения в ней концентрации кислорода. Кислород образовывался, по-видимому, вследствие фотолиза паров воды под действием того же ультрафиолетового облучения. Чтобы выжить в новых условиях, древние клетки должны были переключиться с ультрафиолетового света на какой-либо иной источник энергии, все еще доступный для них в новых условиях. Таким источником стал, вероятно, видимый свет.
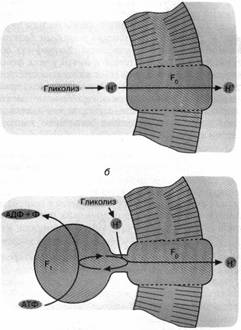
Рис. 3. Как первичная клетка могла избавиться от ионов НГ, образуемых гликолизом: а - облегченная диффузия ионов Н+ посредством белка (фактора F0), образующего Непроводящий путь сквозь клеточную мембрану; б - комплекс факторов F0 и F, (Н+ - АТФаза) активно откачивает из клетки ионы Н+ за счет гидролиза АТФ. Мембранные липиды показаны горизонтальной штриховкой, белки не заштрихованы
Другой сценарий эволюции мог бы состоять в том, что возникновение фотосинтеза, использующего видимый свет, произошло еще до помутнения атмосферы, а именно при проникновении жизни в более глубокие уровни океана, лишенные ультрафиолета. Замена опасного ультрафиолетового излучения на безопасный видимый свет могла бы быть тем признаком, который лег в основу естественного отбора на данном этапе эволюции. В рамках этой концепции создание озонового слоя имеет биогенную природу, явившись результатом фотолиза воды системой хлорофилльного фотосинтеза зеленых бактерий и цианобактерий.
Новый фотосинтез должен был, как и прежде, образовывать АТФ, который к тому времени уже прочно занял место в центре метаболической карты, выполняя роль "конвертируемой энергетической валюты" клетки. Однако аденин уже не мог играть роль улавливающей свет антенны, так как его максимум поглощения находится в ультрафиолетовой, а не в видимой области спектра. До нас дошли два типа фотосинтетических устройств, использующих видимый свет. В качестве антенны в одном из них служит хлорофилл, а в другом — производное витамина А, ретиналь, соединение с особым белком, названным бактериородопсином. Хлорофилл обнаружен у зеленых растений и почти у всех фотосинтезирующих бактерий. Исключение составляет одна группа соле- и теплоустойчивых архебактерий, содержащих бактериородопсин. Тем не менее именно бактериородопсин выглядит как эволюционно первичный механизм запасания клеткой энергии видимого света.
Бактериородопсин — светозависимый протонный насос. Он способен активно откачивать ионы Н+ из клетки за счет энергии видимого света, поглощенного ретиналевой частью его молекулы. В результате световая энергия превращается в трансмембранную разность электрохимических потенциалов ионов Н+ (сокращенно протонный потенциал, или ∆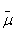 Н+). Для бактерий ∆
Н+). Для бактерий ∆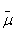 Н+ - это свободная энергия ионов Н+, откачанных из клетки во внешнюю среду. Ионы Н+ как бы стремятся вернуться в клетку, где их стало меньше и где возник недостаток положительных электрических зарядов из-за действия бактериородопсинового Н+ - насоса. Энергия света, запасенная таким образом в виде ∆
Н+ - это свободная энергия ионов Н+, откачанных из клетки во внешнюю среду. Ионы Н+ как бы стремятся вернуться в клетку, где их стало меньше и где возник недостаток положительных электрических зарядов из-за действия бактериородопсинового Н+ - насоса. Энергия света, запасенная таким образом в виде ∆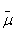 Н-, освободится, если позволить ионам Н+ войти обратно в клетку. У микробов, имеющих бактериородопсин, ионы Н+ входят через комплекс факторов F0 и F1 таким образом, что освобождающаяся энергия используется для синтеза АТФ. Нетрудно представить себе, как возник фотосинтез АТФ, катализируемый бактериородопсином и комплексом F0F1 С появлением бактериородопсина клетка научилась создавать ДДН+ за счет видимого света, а эта ∆
Н-, освободится, если позволить ионам Н+ войти обратно в клетку. У микробов, имеющих бактериородопсин, ионы Н+ входят через комплекс факторов F0 и F1 таким образом, что освобождающаяся энергия используется для синтеза АТФ. Нетрудно представить себе, как возник фотосинтез АТФ, катализируемый бактериородопсином и комплексом F0F1 С появлением бактериородопсина клетка научилась создавать ДДН+ за счет видимого света, а эта ∆ Н+, образовавшись, просто развернула вспять Н+ - АТФазную реакцию, существовавшую ранее в качестве механизма откачки из клетки гликолитических ионов Н+. Так комплекс F0F1 мог превратиться из АТФазы в АТФ-синтетазу (рис. 4).
Н+, образовавшись, просто развернула вспять Н+ - АТФазную реакцию, существовавшую ранее в качестве механизма откачки из клетки гликолитических ионов Н+. Так комплекс F0F1 мог превратиться из АТФазы в АТФ-синтетазу (рис. 4).
Устройство бактериородопсина намного проще системы хлорофилльного фотосинтеза. Белковая часть бактериородопсина представляет собой одну полипептидную цепь средней длины, которая не содержит других коферментов и простетических групп, кроме ретиналя. Бактериородопсин чрезвычайно устойчив: без потери активности его можно кипятить в автоклаве при + 130°С, изменять содержание NaCl в омывающем мембрану растворе от нуля до насыщения, в широких пределах менять рН этого раствора. Более того, можно удалить выступающие из мембраны концевые участки полипептидной цепи и даже расщепить эту цепь в одном месте по середине без ущерба для активности насоса. В то же время эффективность бактериородопсина как преобразователя энергии сравнительно низка: всего 20% энергии светового кванта превращается в ∆ Н+. При этом на один поглощенный квант через мембрану переносится один ион Н+.
Н+. При этом на один поглощенный квант через мембрану переносится один ион Н+.
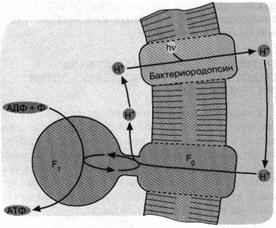
Рис. 4. Бактериородопсиновый фотосинтез со-лелюбивых архебактерий. Ионы 1-Г откачиваются из клетки бактериородопсином - белком, содержащим ретиналь в качестве хромофора, то есть группировки, поглощающей видимый свет. Ионы Н* возвращаются в клетку, двигаясь "под гору" через Н+ -АТФазный комплекс F0F,. При этом оказывается, что Н+ - АТФаза катализирует обратную реакцию, то есть синтез АТФ, а не его гидролиз
Хлорофилльный фотосинтез
Хлорофилльный фотосинтез отличается от бактериородопсинового большей эффективностью использования светового кванта. Он устроен таким образом, что либо на каждый квант переносится через мембрану не один, а два иона Н+, либо помимо транспорта Н+ происходит запасание энергии в форме углеводов, синтезируемых из С02 и Н2О. Вот почему бактериородопсиновый фотосинтез был оттеснен эволюцией с авансцены. Он сохранился только у бактерий, живущих в экстремальных условиях, где более сложный и менее устойчивый хлорофилльный фотосинтез, по-видимому, просто не может существовать.
Хлорофилльный фотосинтез катализируется ферментной системой, включающей несколько белков. Квант света поглощается хлорофиллом, молекула которого, перейдя в возбужденное состояние, передает один из своих электронов в фотосинтетическую цепь переноса электронов. Эта цепь представляет собой последовательность окислительно-восстановительных ферментов и коферментов, находящихся во внутренней мембране бактерий или хлоропластов растений, где локализованы также белки, связанные с хлорофиллом. Компоненты цепи содержат, как правило, ионы металлов с переменной валентностью (железо, медь, реже марганец или никель). При этом железо может входить в состав тема (в таком случае белки называются цитохромами). Большую роль играют также негемовые железопротеиды, где ион железа связан с белком через серу цистеина или реже азот гистидина. Помимо ионов металлов роль переносчиков электронов играют производные хинонов, такие, как убихинон, пластохинон и витамины группы К.