Получение моноклональных антител
Страница 2
Способы иммунизации. Назначение процесса иммунизации состоит в том, чтобы увеличить долю клеток, продуцирующих антитела заданной специфичности, и перевести эти клетки в функциональное состояние, при котором они способны сливаться и образовывать антителообразующие гибридные клетки. Экспериментально установлено, что для гибридизации необходимы выделять селезеночные клетки животных через 3-4 суток после последнего введения антигена, то есть тогда, когда в лимфоидных органах много активно пролиферирующих клеток.
Конкретная схема иммунизации сильно зависит от природы антигена и его иммуногенности. Антигены клеточной поверхности являются сильными иммуногенами, тогда как большинство растворимых белков – слабые иммуногены. В последнем случае необходимо применять различные адъюванты, усиливающие иммунный ответ. Среди адъювантов наибольшее распространение получил полный адъювант Фрейнда (ПАФ). Помимо этого, используют введение антигена, преципитированного на квасцах, и введение вместе с антигеном убитых клеток Bordetella Pertussis. Обычно антиген вводят неоднократно, что необходимо для развития сильного иммунного ответа, хотя чрезмерная иммунизация может иметь обратный эффект – отмечено, что иногда у клеток гипериммунизированных животных снижается способность образовывать гибридомы. В некоторых случаях бывает достаточно и одной иммунизации.
По ходу иммунизации необходимо определять титр антител к антигену (титр антител – величина, обратная разведению сыворотки, при которой степень иммунологической реакции снижается в два раза по сравнению с максимальной). Обычно это делают перед последней иммунизацией. В опыт набирают животных с высоким титром антител. Не следует ожидать хороших результатов гибридизации, если при иммунизации животных нет образования антител или они образуются в низком титре.
Для большинства растворимых антигенов можно использовать следующую схему иммунизации.
1. Вводят 1-100 мкг антигена в ПАФ или в виде преципитата на квасцах внутрибрюшинно. Если есть возможность, то одновременно вводят 2*109 убитых клеток B. Pertussis.
2. Через 2-3 недели вводят антиген на физиологическом растворе внутрибрюшинно или внутривенно. Эту процедуру можно повторять до появления высокого титра антител.
3. Последнюю иммунизацию делают внутривенно, через 3 суток животные забиваются, и готовится суспензия клеток для гибридизации.
При применении в качестве иммуногена различных клеток (опухолевые клетки, чужеродные клетки крови, бактерии, паразиты и т.д.) делают несколько инъекций без адъюванта внутрибрюшинно с интервалом в 2-3 недели по (1-5)*107 клеток. Последнюю инъекцию делают внутривенно и через 3 дня выделяют клетки селезенки для гибридизации.
В последнее время активно развиваются методы полной иммунизации вне организма с целью получения гибридомы. Иммунизация in vitro имеет ряд существенных преимуществ:
a) укорачивается период иммунизации до 4-5 суток;
b) требуется существенно меньшее количество антигена;
c) ко многим антигенам можно получить более выраженный иммунный ответ (частично за счет снижения вклада толерантности и супрессии);
d) повышается процент отвечающих клеток;
e) легко проверять факторы, влияющие на эффективность иммунизации.
Современные методы иммунизации in vitro основаны на двух системах культивирования лимфоцитов, разработанных в конце 1960-х годов. Метод суспензионного культивирования был первым методом, в котором иммунизация полностью проходила вне организма. Критическими факторами в данном методе были низкая концентрация кислорода в атмосфере (7%), высокая плотность клеток, легкое покачивание культуры, ежедневное добавление свежей среды и выбор подходящей партии СПК и антигена (использовали эритроциты барана).
Другой основной системой иммунизации in vitro является метод Д. Марбрука. Клетки культивируют в маленькой камере на диализной мембране, через которую идет обмен средой из большого резервуара.
Одним из основных недостатков иммунизации in vitro является доля IgM-образующих клонов. Это связано с тем, что при иммунизации in vivo клетки берут во время вторичного иммунного ответа, при котором образуются в основном антитела IgG класса, тогда как in vitro реакция идет по первичному типу, для которого характерна продукция IgM антител. Эта проблема может быть преодолена после отработки способов получения вторичного иммунного ответа in vitro.
Слияние
Существуют два основных варианта добавления ПЭГ, используемых в настоящее время. Первый метода заключается в следующем. В течение 1 мин добавляют 1 мл 50% раствора ПЭГ при 370 С с постоянным перемешиванием. Затем раствор постепенно разбавляют до 10 мл в течение нескольких минут средой без сыворотки, после чего клетки центрифугируют и ресуспендируют в среде культивирования.
Во втором методе используют более длительную обработку клеток раствором ПЭГ. К осадку клеток добавляется 30-35% ПЭГ при комнатной температуре. Клетки центрифугируют 2 мин, затем их оставляют при комнатной температуре еще на 5-7 мин. Затем их разводят в большом объеме среды с сывороткой, обмывают и культивируют.
Клонирование гибридомных клеток
Клонирование осуществляется для выделения стабильных клонов гибридомных клеток. Для недавно образованных гибридомных клеток характерна высокая нестабильность, связанная с утратой хромосом. При культивировании могут появляться клетки, потерявшие способность продуцировать антитела и они могут перерастать антителообразующие гибридные клетки.
К основным методам клонирования клеток относятся клонирование методом лимитирующих разведений, клонирование в полужидком агаре и клонирование с помощью прибора – проточного цитофлуориметра.
Клонирование методом лимитирующих разведений. Если клетки посеяны в 96-луночные планшеты очень редко, то доля лунок, в которой наблюдается рост клеток, подчиняется распределению Пуассона:
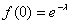
где f (0) – фракция лунок, в которых отсутствует рост; l – среднее число клеток на лунку.
При l = 1 f (0) = 0,37. Для того, чтобы получить разумную вероятность только одного клона в лунке, в более 37% лунок не должно наблюдаться роста клеток. Поскольку эффективность клонирования редко бывает равной 100%, клетки необходимо засевать при плотности 10, 3 и 0,5 клеток на лунку. В тех планшетах, на которых наблюдается рост в половине лунок, содержатся изолированные клоны.
При первом клонировании активной может оказаться только небольшая часть клонов. Необходимо всегда производить повторное клонирование, при котором доля положительных клонов будет возрастать.
Для клонирования надо применять клетки питающего слоя. Используются те же виды клеток, что и для начального роста гибридом.
Клонирование в полужидком агар-агаре. Для клонирования гибридом можно применять полужидкий агар. Обычно берется система, состоящая из двух слоев. Нижний (твердый) слой содержит 0,5% агар-агара в среде культивирования. Ему дают затвердеть. Затем добавляют второй слой – мягкий, содержащий 0,3% агар-агара, в который включаются клонируемые клетки. При использовании клеток питающего слоя их засевают в чашку Петри до заливки агар-агара, и среду культивирования удаляют непосредственно перед добавлением нижнего слоя агара.
Колонии становятся видимыми через 7-14 суток, их переносят на жидкую культуру.
Клонирование с помощью проточного цитофлуориметра. Приготавливают флуоресцентные микрошарики из латекса и покрывают их антигеном. Такие шарики адсорбируются на антигенспецифических гибридомных клетках, что позволяет выделять их на этом приборе.
После выделения тем или иным способом положительных клонов, клетки этих клонов размножают в достаточном количестве и образцы их замораживаются.
Массовая наработка моноклональных антител
После отбора гибридомных клеток, синтезирующих интересующие исследователя антитела, можно приступить к их массовому наращиванию с целью получения больших количеств моноклональных антител. В начале культивирования гибридомные клетки могут расти медленно и плохо переносить низкую плотность посева. В связи с этим при пересеве клеток их надо разводить не более чем в 3-5 раз. Ускорению роста клеток может способствовать добавление клеток питающего слоя. Гибридомные клетки необходимо поддерживать в логарифмической фазе роста и избегать повышения концентрации клеток выше 0,5 млн/мл. Клетки можно культивировать как в стационарной культуре, так и в роллерной, а также в различного рода культиваторах (ферментерах).