Витамин К
Страница 5
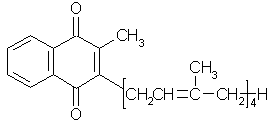
Витамин К2 представлен несколькими формами, отличающимися по длине изопреноидной цепи. Выделены производные с боковой цепью из 20, 30 и 35 углеродных атомов.
|
|
|
Витамин К2(20) |
|
|
|
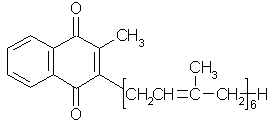
Витамин К2(30)
(2-метил-3-дифарнезил-1,4-нафтохинон) |
|
|
|
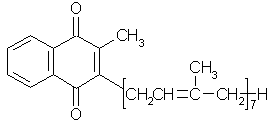
Витамин К2(35) |
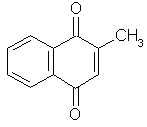
Кроме природных витаминов К, в настоящее время известен ряд производных нафтохинона, обладающих антигеморрагическим действием, которые получены синтетическим путем. К их числу относятся следующие соединения:
|
|
|
|
Витамин К3
(2-метил-1,4-нафтохинон) |
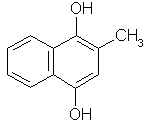
Витамин К4
(2-метил-1,4-нафтогидрохинон) |
|
|
|
|
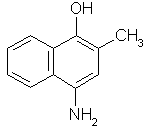
Витамин К5
(2-метил-4-амино-1-нафтогидрохинон) |
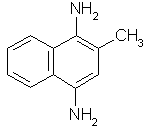
Витамин К6
(2-метил-1,4-диаминонафтохинон) |
|

|
|
Витамин К7
(3-метил-4-амино-1-нафтогидрохинон) |
|В 1943 г. А. В. Палладин и М. М. Шемякин синтезировали дисульфидное производное 2-метил-1,4-нафтохинона, получившее название викасола, который применяется в медицинской практике в качестве заменителя витамина К:
|
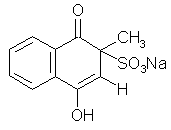
|
|
Викасол |
3. Физико-химические свойства
Витамин К1 представляет собой светло-желтое масло, которое кристаллизуется при температуре –20° и кипит при 115–145° в вакууме. Это вещество растворимо в хлороформе, диэтиловом эфире, этиловом спирте и других органических растворителях. Его растворы поглощают УФ лучи. Так, в петролейном эфире максимумы адсорбции находятся при длине волны, равной 243, 249, 261, 270 и 325 нм. В этом ряду наибольшую оптическую плотность (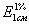 = 420) витамин К проявляет при К = 249 нм.
= 420) витамин К проявляет при К = 249 нм.
Витамин К2 – желтый кристаллический порошок с температурой плавления 54°, растворяющийся в органических растворителях. Он имеет адсорбционные спектры, сходные с таковыми витамина К1, но менее интенсивно поглощает УФ лучи. Например, в петролейном эфире максимум его поглощения находится при 248 нм и составляет 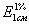 = 295.
= 295.
Витамин К3 представляет собой лимонно-желтое кристаллическое вещество с характерным запахом. Температура плавления 160°. Он слабо растворим в воде, что обусловлено отсутствием в его молекуле длинной углеводородной цепи.
Витамины К, содержащие в положении 3 изопреноидную цепь, относятся к светочувствительным соединениям. При освещении ультрафиолетом происходит фотолиз, отщепляется изопреноидная цепь, которую замещает гидроксил, а молекула фитола окисляется в кетон фитон.
Витамины К, будучи, как сказано выше, производными нафтохинона, обладают способностью к окислительно-восстановительным реакциям. На этой способности витаминов К основано количественное определение их полярографическим методом. Нафтохиноновая молекула, присоединяя два водорода, переходит в нафтогидрохиноновую. Эта реакция в присутствии кислорода воздуха обратима. Реакция восстановления нафтохинонов (окрашенных веществ) сопровождается их обесцвечиванием.
Витамины К способны непосредственно взаимодействовать с кислородом, присоединяя его в положении 2, 3 молекулы нафтохинона. Продуктом окисления является эпоксид:
|
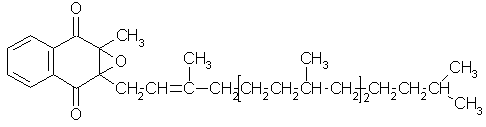
|
|
Эпоксид витамина К1 |
Эпоксиды витаминов К сохраняют витаминную активность исходных молекул.
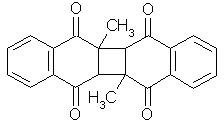
Витамин К3 под влиянием света и кислорода воздуха может давать димерное производное:
|
|
|
Димер витамина К3 |
Как отмечено выше, бисульфидное производное витамина К3 обладает витаминной активностью. Это важное для медицинской практики вещество получают воздействием бисульфита натрия на 2-метил-1,4-нафтохинон.
Хорошими стабилизаторами витамина К являются монокальциевый фосфат, пирофосфаты натрия или калия и др., стабилизирующее действие которых состоит в поддерживании в водном растворе кислой реакции (рН = 4,8). Смесь 0,5 кг пропаренной соевой муки с 140 г менадион-натрий-бисульфатом и 26 г СаН4(РO4)2 стабилизирует витамин на 97% в течение трех месяцев.
4. Специфичность строения. Гомовитамины и антивитамины К
К-витаминной активностью обладают многие производные нафтохинона (см. стр. 68). В зависимости от деталей их структуре существенно изменяется величина биологической активности соединения. Сравнительная оценка биологической активности витаминов группы К представлена в табл. 2.
|
Таблица 2 |
|
Биологическая активность витаминов группы К |
|
Витамины |
Активность, % |
Витамины |
Активность, % |
|
К1 |
100 |
К5 |
100 |
|
К2 |
60 |
К6 |
100 |
|
К3 |
300 |
К7 |
100 |
|
К4 |
200 |
|
|
Как видно из данных табл. 2, гидрирование хиноидных групп, находящихся в положении 1,4, не оказывает существенного влияния на биологическую активность витаминов К. В то же время гидрирование самого нафтохинонового ядра приводит к почти полной утрате биологической активности молекулы. Замена гидроксильной группы на аминогруппу не сопровождается утратой биологической активности витамина. Для проявления биологической активности обязательно наличие метильной группы в положении 2 нафтохинонового ядра. Введение метильной группы в других позициях нафтохиноновой системы сопровождается резким уменьшением физиологической роли соединения.