Нильс Бор
Страница 5
До Резерфорда в физике господствовала модель атома Дж. Дж. Томсона, согласно которой атом состоит из шара, равномерно заполненного положи- тельным электрическим зарядом. В этом шаре электроны движутся по окружностям. Основное различие между моделями Томсона и Резерфорда Бор усматривал в том, что в модели Томсона силы, действующие на электроны, допускают такие конфигурации и движения, которое обеспечивают устойчивое равновесие системы, в то время как для модели Резерфорда, по-видимому, такие конфигурации не существуют. Это различие проявляется в том, что среди величин характеризующих атом Томсона, имеется одна величина - радиус положительно заряженного шара - с размерностью длины, в то время как среди величин, характеризующих атом Резерфорда, такая длина отсутствует.
Теория теплового излучения Планка и прямые подтверждения существо-вания элементарного кванта действия в опытах по теплоемкости, фотоэффекту и других, побудили Бора усомниться в применимости классической электродинамики к атомным системам. Бор поставил перед собой задачу ввести в законы движения электронов элементарный квант действия. Атом Резерфорда и квант действия Планка - исходные моменты теории атома Бора.
В первой части статьи Бора на основе теории Планка рассматривается механизм связывания электрона с ядром. На примере простейшей системы, состоящей из положительно заряженного ядра и электрона, движущегося по замкнутой орбите вокруг ядра, показано, что при излучении, которое должно иметь место по законам электродинамики, электрон не может двигаться по стационарным орбитам. В результате излучения энергия будет непрерывно убы-
- 17 -
вать. Электрон будет приближаться к ядру, описывая все меньшие орбиты. Частота его вращения вокруг ядра будет все увеличиваться. Поведение такой системы, вытекающее из основ классической электродинамики, отличается от того, что имеет место в действительности. Атомы длительное время имеют определенные размеры и частоты. "Далее, - пишет Бор, - представляется, что если рассмотреть какой - либо молекулярный процесс, то после излучения определенного количества энергии, характерного для изучаемой системы, эта система всегда вновь окажется в состоянии устойчивого равновесия, в котором расстояния между частицами будут того же порядка величины, что и до процесса".
Бор ясно показал, что следствия классической электродинамики не соответствуют тому, что мы наблюдаем в атомных системах. Высший критерий физики есть опыт. Поскольку опыт в области атомных явлений нельзя объяснить представлениями и теорией классической физики, Бор обращается к теории излучения Планка. Эта теория утверждает, что излучение энергии атомной системы происходит не непрерывно, а определенными раздельными порциями. Количество испускаемой атомным излучателем энергии при каждом процессе излучения равно 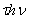 , где
, где 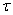 - целое число, h - универсальная постоянная Планка,
- целое число, h - универсальная постоянная Планка, 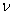 - частота. Бор допускает, что электрон испускает монохроматическое излучение с частотой
- частота. Бор допускает, что электрон испускает монохроматическое излучение с частотой 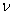 , равной половине частоты обращения электрона по своей окончательной орбите.
, равной половине частоты обращения электрона по своей окончательной орбите.
Энергия излучения :
W =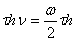 ,
,
где:
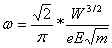 ,
,
W - среднее значение кинетической энергии электрона за одно полное обращение, e и E - заряды электрона и ядра, m - масса электрона. Подставив значение 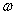 , получим:
, получим:
W =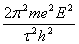 ,
,
Длина большой полуоси орбиты:
- 18 -
2а 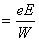 ,
,
Придав 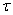 разные значения, мы получим ряд значений W,
разные значения, мы получим ряд значений W, 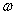 , и а, соответствующих ряду конфигураций системы. В этих состояниях атом не излучает. W принимает максимальное значение при
, и а, соответствующих ряду конфигураций системы. В этих состояниях атом не излучает. W принимает максимальное значение при 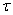 =1, подставив значения E = e = 4,7 * 10-10 , e/m = 5,31 * 1017 , h = 6,54 * 10-27 ,имеем 2а = 1,1 * 10-8 см,
=1, подставив значения E = e = 4,7 * 10-10 , e/m = 5,31 * 1017 , h = 6,54 * 10-27 ,имеем 2а = 1,1 * 10-8 см, 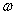 = 6,2 * 1015 с-1, W/e = 13 в. Эти величины того же порядка, что и линейные размеры атома, оптические частоты и ионизационные потенциалы.
= 6,2 * 1015 с-1, W/e = 13 в. Эти величины того же порядка, что и линейные размеры атома, оптические частоты и ионизационные потенциалы.
Бор указывает, какова предыстория применения теории Планка к атомным системам: "На всеобщее значение теории Планка для обсуждения поведения атомных систем впервые указал Эйнштейн. Соображения Эйнштейна, были затем развиты и применены к различным явлениям в особенности Штарком, Нернстом и Зоммерфельдом. Соответствие наблюдаемых частот и размеров атома и вычисленных на основе соображений, приведенных выше, было предметом многочисленных обсуждений". С точки зрения теории Планка Дж. Никольсон рассматривал системы, у которых силы взаимодействия между частицами обратно пропорциональны квадрату расстояния между ними. Однако его теория не в состоянии была объяснить известные спектральные закономерности Ритца и Бальмера.
Бор исходит из двух следующих допущений:
1. Динамическое равновесие системы в стационарных состояниях можно рассматривать с помощью обычной механики, тогда как переход системы из одного стационарного состояния в другое нельзя трактовать на его основе.
2. Указанный переход сопровождается испусканием монохроматического излучения, для которого соотношения между частотой и количеством выделенной энергии именно такое, которое дает теория Планка.
Полагая в атоме водорода заряд ядра равным заряду электрона E = e, получают выражение для общего количества энергии, испускаемой при образовании стационарного состояния:
Wr 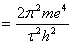 .
.
При переходе из состояния, соответствующего 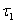 , в состояние, соответствующее
, в состояние, соответствующее 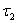 , испускается количество энергии
, испускается количество энергии
Wr2 - Wr1 = 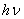 ,
,
следовательно:
- 19 -
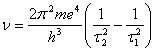 .
.
Если положить 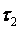 = 2 и варьировать
= 2 и варьировать 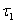 , то получают серию Бальмера. Если положить
, то получают серию Бальмера. Если положить 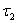 = 3, получают серию которую наблюдал в 1908 г. Пашен в инфракрасной области. Бор отмечает, что если
= 3, получают серию которую наблюдал в 1908 г. Пашен в инфракрасной области. Бор отмечает, что если 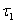 = 1 и
= 1 и 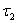 = 4, 5, ., то получают в крайней ультрафиолетовой и соответственно в крайней инфракрасной области серии, которые еще никем не наблюдались.
= 4, 5, ., то получают в крайней ультрафиолетовой и соответственно в крайней инфракрасной области серии, которые еще никем не наблюдались.
Путь, по которому шел Бор к своему открытию он описал в воспоминаниях о Резерфорде. "Мои письма к Резерфорду, написанные осенью 1912 г., посвящены продолжавшимся усилиям, выяснить роль кванта действия в электронном строении атома Резерфорда, включая сюда проблему молекулярной связи, а также вопросы излучения и магнитные эффекты. Однако вопросы устойчивости, неизбежно возникающие при таких рассмотрениях, резко увеличивали трудности и вынуждали искать более надежную основу для решения проблемы. После многочисленных попыток использовать квантовые идеи в более строгой форме ранней весной 1913 г. мне пришло в голову, что ключом к решению проблемы атомной устойчивости, непосредственно приложенным к атому Резерфорда, являются изумительно простые законы, определяющие оптический спектр элементов"