Источники и пути образования оксида азота в организме
Современные представления о регуляции клеточных процессов позволяют особо выделить некоторые химические соединения, обладающие полифункциональным физиологическим действием. К числу таких соединений с полным основанием можно отнести оксид азота. Данный свободный радикал способен оказывать как активирующее, так и ингибирующее действие на различные метаболические процессы, протекающие в организме млекопитающих и человека. Несмотря на многочисленные исследования, значение оксида азота в системной регуляции гомеостаза клеток и тканей не вполне понятно.
Оксид азота (NO) тАУ газ, хорошо известный химикам и физикам, в последнее время привлек пристальное внимание биологов и медиков. Интенсивное изучение биологического влияния NO началось с 80-х годов, когда Р. Фуршготт и Дж. Завадски показали, что расширение кровеносных сосудов под влиянием ацетилхолина происходит только при наличии эндотелия тАУ эпителиоподобных клеток, выстилающих внутреннюю поверхность всех сосудов. Вещество, выделяющееся эндотелиальными клетками в ответ не только на ацетилхолин, но и на многие другие внешние воздействия, приводящие к расширению сосудов, получило название Влсосудорасширяющий эндотелиальный факторВ». Несколько позже было доказано, что это вещество является газом NO и в клетках имеются особые ферментные системы, способные его синтезировать.
В настоящей работе предпринята попытка проанализировать известные на сегодняшний день данные и представить по возможности полную картину физиологической и метаболической роли данного медиатора.
По своей химической структуре оксид азота относится к нейтральным двухатомным молекулам. Благодаря наличию неспаренного электрона на внешней π-орбитали молекула NO обладает высокой реакционной способностью и свойствами свободного радикала.
Синтез оксида азота
В организме человека и млекопитающих оксид азота главным образом образуется в результате окисления гуанидиновой группы аминокислоты L-аргинина с одновременным синтезом другой аминокислоты цитруллина под влиянием фермента NO-синтазы. Фермент был назван синтазой, а не синтетазой, поскольку для его работы не требуется энергия АТФ (см. [2] в списке литературы).
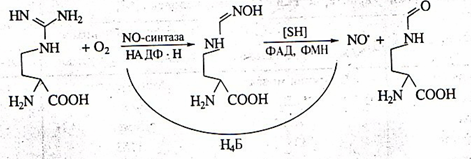
Рис. 1. Схема синтеза окиси азота из L-аргинина
Кроме L-аргинина NOS может использовать в качестве субстратов гомоаргинин, аргиниласпарагин, метиловый эфир аргинина, гуанидинотиолы. При недостатке субстрата в клетках или Н4Б фермент начинает восстанавливать кислород до супероксид радикала и перекиси водорода. Такие условия могут быть следствием как нарушения транспорта аминокислоты (в некоторых тканях она не синтезируется), так и недостатка в пище, поскольку синтез L-аргинина при этом в организме не увеличивается [1].
Структура NO-синтазы. Основные типы фермента
NO-синтаза тАУ это сложно устроенный фермент, представляющий собой гомодимер. То есть он состоит из двух одинаковых белковых субъединиц, к каждой из которых присоединено несколько кофакторов, определяющих каталитические свойства фермента. Активность фермента проявляется только при объединении двух его субъединиц [2].
Фермент является димером, состоящим из двух одинаковых белковых молекул, каждая из которых связана с необходимыми для работы фермента кофакторами: НАДФ, ФАД, ФМН, гемовая группа, содержащая железо, кальмодулин, и тетрагидробиоптерин (ВН4). Связь между белковыми субъединицами происходит в области их N0конца, где с ними связаны гемовые группы. Стрелками показан перенос электронов [2].
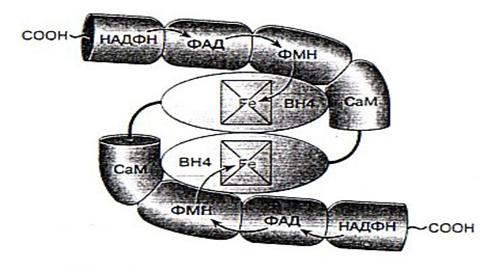
Рис. 2. Схематичное представление строения NO-синтазы.
NO-синтазы составляют семейство, то есть имеется группа ферментов, несколько различающихся по аминокислотной последовательности белковой части молекулы и механизмам, регулирующим их активность, но тем не менее, катализирующих одну и ту же реакцию превращения аминокислот с образованием оксида азота. В настоящее время хорошо изучена структура разных изоформ NO-синтазы (NOS), известны механизмы, регулирующие их активность, и хромосомная локализация генов, ответственных за синтез ферментов, проведено клонирование (получение большого числа копий) этих генов, получены генетические модификации мышей без генов разных изоформ фермента (так называемые нокаут мыши) [2].
Синтезировать и выделять NO способны большинство клеток организма человека и животных, однако наиболее изучены три клеточные популяции: эндотелий кровеносных сосудов, клетки нервной ткани (нейроны) и макрофаги тАУ клетки соединительной ткани, обладающие высокой фагоцитарной активностью. В связи с этим традиционно выделяют три основные изоформы NO-синтаз (NOS): нейрональную, макрофагальную и эндотелиальную (обозначаются соответственно как NO-синтаза I, II и III). Нейрональная и эндотелиальная изоформы фермента постоянно присутствуют в клетках и называются конститутивными, а вторая изоформа (макрофагальная) является индуцибельной тАУ фермент синтезируется в ответ на определенное внешнее воздействие на клетку [2].
Молекулы всех изоформ фермента NOS содержат N-терминальный оксигеназный домен и С-терминальный домен редуктазы. Домен оксигеназы с примерно 500 аминокислотными остатками включает участки для связывания гемовой группы, кофактора Н4В и субстрата L-аргинина. Домен с редуктазной активностью, состоящий из 570-625 аминокислотных остатков, участвует в связывании молекул ФАД, ФМН и НАДФ*Н. между этими доменами расположена последовательность из 30 аминокислотных остатков для связывания белка кальмодулина (СаМ) тАУ переносчика электронов с флавина на железо гемовой группы оксигеназы [3].
Каждый изофермент имеет специфическую N-терминальную лидирующую последовательность аминокислотных остатков, не участвующую в катализе и, вероятно, определяющую внутриклеточную локализацию фермента. Так, N-терминальная последовательность эндотелиального фермента включает три участка ацилирования жирными кислотами, которые играют важную роль в процессе связывания с мембраной. Нейрональная NOS содержит в N-концевом домене PDZ-фрагмент из 100 аминокислотных остатков. Это фрагмент, участвуя в процессе узнавания белка, определяют субклеточную локализацию молекул NOS[3].
Все три типа NOS в своей активной форме тАУ гомодимеры. В образовании димера принимает участие оксигеназный домен NOS. Процесс димеризации инициируется присоединением к субъединицам гемовых простетических групп. Последующее присоединение Н4В стабилизирует образовавшийся димер NOS. Без гемовой группы NOS является мономером, не проявляющим NO-синтазной активности. При этом мономерная форма NOS обладает полной цитохром-с-редуктазной активностью и способностью связывать ФАД и ФМН [3].
Последовательность редуктазного домена на 50% гомологична другим ФМН и ФАД-содержащим редуктазам (например, цитохром Р-450 редуктаза), что свидетельствует о сохранении основных признаков этого класса ферментов для редуктазы NOS. Так, экспрессируясь отдельно или как часть холофермента, домен редуктазы может непосредственно переносить электроны с НАДФ*Н на оксигеназный домен и другие акцепторы, такие как цитохром с и феррицианид. Редуктаза NOS стабилизируется одноэлектронным восстановлением флавина и может принимать, по крайней мере, 3 электрона с НАДФ*Н [3].
Одним из самых важных кофакторов является внутриклеточный кальцийсвязывающий белок кальмодули. При повышении содержания ионов кальция в клетке он присоединяется к молекуле NO-синтазы, что приводит к активации фермента и синтезу NO (слайд 2). Такое свойство фермента имеет большое значение для клеток, поскольку ферментативная активность, а значит, и синтез NO прямо зависят от функционального состояния клетки, определяющегося во многом внутриклеточным уровнем ионов кальция тАУ высокоактивных посредников, влияющих на многие процессы в клетках. Среди других регуляторных механизмов фермента следует отметить возможность фосфорилирования белковой части молекулы и влияние особых белков, участвующих в связывании двух субъединиц фермента в единый функционально активный комплекс [2].
Активность конститутивных (т.е. нейрональная и эндотелиальная) изоформ фермента прямо зависит от внутриклеточной концентрации ионов кальция или кальмодулина и, таким образом, повышается под влиянием различных агентов, приводящих к увеличению их уровня в клетке. Конститутивные изоформы NO-синтазы имеют преимущественно физиологическое значение, поскольку количество образуемого NO относительно невелико [2].
Индуцибельные (т.е. макрофагальные) изоформы NO-синтазы проявляют активность через некоторое время (как правило, 6-8ч тАУ время, необходимое для активации генов и начала синтеза фермента) после внешнего воздействия на клетки, продуцируют огромные (в 100-1000 раз больше, чем конститутивные изоформы фермента) количества NO. Поскольку высокие дозы NO токсичны для клеток, эта форма фермента считается патологической в отличие от конститутивной. Активность индуцибельной NO-синтазы не зависит от уровня кальция/кальмодулина, поскольку, как полагают, кальмодулин постоянно и прочно связан с ферментом [2].
Локализация NO-синтазы
В настоящее время показано, что не только макрофаги, но и многие другие клетки (нейтрофилы, гепатоциты, гладкомышечные клетки, клетки астроглии) способны при определенных внешних воздействиях, в основном в условиях патологии, синтезировать индуцибельную изоформу NO-синтазы. Нейрональная NOS обнаружена не только в нервных клетках, но и в скелетных мышцах. Эндотелиальная NOS обнаружена в эндотелиальных клетках, клетках эпителия и кардиомиоцитах. Нейрональная и макрофагальная формы фермента находятся в клетках преимущественно в растворенном состоянии тАУ в цитозоле, а эндотелиальная NO-синтаза обычно связана с клеточными мембранами [2].
N-концевая последовательность NOS подвергается миристоилированию и пальмитоилированию, что определяет ее субклеточную локализацию и косвенно ее активность. Так, для фиксации эндотелиальной NOS в плазматической мембране необходимо ацилирование N-терминальных остатков глицина в молекулах фермента с образованием амидных связей [3].
Нейрональная изоформа NOS связана с мембраной за счет взаимодействия N-концевого PDZ-фрагмента с белками типа PSD-95, PSD-93 и дистрофинсвязанным белком тАУ синтрофином [3].
В отличие от конститутивных изоформ, индуцибельная NOS, не связанная с мембранными белками, является цитозольным ферментом [3]. Однако сравнительно недавно в митохондриях была выявлена конститутивно экспрессируемая NO-синтаза. По основным характеристикам митохондриальная NOS сходна с макрофагальной [16]. Сравнивая скорости продукции NO интактными митохондриями, митохондриальным гомогенатом и субмитохондриальными частицами (1.4, 4.9 и 7.1 нмоль/мин на мг белка соответственно) можно сделать вывод, что mtNOS фиксирована на внутренней мембране митохондрий, тогда как iNOS является цитозольным ферментом. Вопрос о том, что представляет собой митохондриальная NOS тАУ отдельную изоформу фермента или же модифицированную во время трансляции или после нее индуцибельную NOS (как это имеет место в скелетных мышцах для нейрональной) тАУ остается открытым [3].
Таблица 1. Физико-химические характеристики NO-синтаз человека[1].
| Характеристика | Изоформа NO-синтазы |
| Нейрональная | Индуцируемая | Эндотелиальная |
Источник выделения белка Молекулярная масса Нативная структура Аминокислотная длина Локализация в клетке Локализация в геноме | Нейроны мозга 160кДа Димер 1433 Цитозоль Хромосома 12 | Макрофаги 130кДа Димер 1153 Цитозоль Хромосома 17 | Эндотелий сосудов 133 кДа Нет данных 1203 Мембрана, цитозоль Хромосома 7 |
Вместе с этим смотрят:
Бiологiчне рiзноманiття людських рас
Бодрствование - нейрофизиологический процесс человека
Влияние биологически активных факторов окружающей среды на наследственные системы организма человека
Возрастная анатомия и физиология
Генетико-статистический анализ комбинационной способности сортов и форм яровой мягкой пшеницы по коэффициенту хозяйственной эффективности фотосинтеза