Связь структуры и действия лекарственных веществ, относящихся к эстрогенам и гестагенам
Яичники выполняют важную гематогенную функцию, интегрированную с их гормональной активностыо. Начало функционирования яичников находится под контролем нервной системы. Развитие центров головного мозга, таких как миндалевидное тело, устраняет торможение активности клеток срединного возвышения гипоталамуса, позволяя им выделять гонадотропинрилизинг - гормон с соответствующими частотой и количеством, что стимулирует высвобождение фолликулостимулирующего и латинизирующего гормонов. Вначале высвобождается небольшое количество этих двух гормонов, вызывая секрецию незначительных порций эстрогена. Это приводит к развитию молочных желез, изменению в распределении жировой ткани.
В начале каждого менструального цикла разное количество везикулярных фолликулов, каждый из которых содержит яйцеклетку, начинает увеличиваться в размерах в ответ на фолликулостимулирующий гормон. Через 5 или 6 дней один из фолликулов начинает развиваться быстрее других. Гранулезные клетки этого фолликула размножаются и под влиянием лютеонизирующего гормона синтезируют эстроген и высвобождают его в возрастающем количестве. Эстрогены подавляют выделениефолликулостимулирующего гормона и способствуют регрессии развития менее зрелых фолликулов. Секреция эстрогена достигает максимума перед самой серединой цикла, и гранулезные клетки начинают продуцировать прогестерон. Эти изменения стимулируют короткий подъем высвобождения лютеонизирующего и фолликулостимулирующего гормона, который предшествует овуляции. После разрыва фолликула яйцо попадает в брюшную полость в районе маточных труб. Полость разорвавшегося фолликула заполняется кровью, a лютеонизированная оболочка и гранулезные клетки пролиферируют и замещают кровь, формируя желтое тело. Клетки этой структуры продуцируют эстроген и прогестерон во время оставшейся части цикла и далее, если возникает беременность. Если оплодотворения яйцеклетки не произошло, желтое тело начинает дегенерировать и прекращает продукцию гормонов превращаясь в конце концов в белое тело.
Яичники обычно со временем прекращают свою гематогенную и эндокринную функцию. Эти изменения сопровождаются прекращением маточных кровотечений (менопаузой), что происходит в среднем в возрасте 52 лет. Хотя яичники перестают секретировать эстрогены, у многих женщин они имеются в значительной концентрации вследствие превращения надпочечниковых стероидов в эстрон и эстрадиол в жировой ткани. [2].
Основная часть
Классификация
1. Природные эстрогены
1.1 Эстрогенные препараты стероидного строения
1.2 Эстрогенные препараты нестероидного строения
1.3 Антиэстрогенные лекарственные средства
2. Синтетические эстрогены
3. Прогестины
3.1 Естественные прогестины
3.2 Группа прегнана
3.3 Производные 19- нортестостерона эстранового ряда
3.4 производные 19- нортестостерона гонанового ряда
3.5 Пролекарство
4. Синтетические прогестины
5. Ингибиторы и антагонисты эстрогена и прогестерона
6. Средства, вызывающие овуляцию
7. Контрацептивные средства
Природные эстрогены
Эстрогенной активностью обладает большое количество химических веществ. Помимо различных стероидных эстрогенов животного происхождения синтезировано большое количество нестероидных эстрогенов. Эстрогенная активность характерна для многих фенолов. Она обнаружена у различных биологических образований, найденных в морских отложениях, а также у отдельных видов клевера.
Главными эстрогенами, вырабатываемыми организмом женщины, являются эстрадиол, эстрон, эстриол. Основной продукт секреции яичников - эстрадиол. В течение первой части менструального цикла эстрогены продуцируются в фолликулах яичников оболочковыми клетками. После овуляции эстрогены синтезируются гранулезными клетками желтого тела; и пути их биосинтеза несколько различаются. Вo время беременности эстрогены в большом количестве синтезируются фетоплацентарным комплекcoм. Синтезируемый им эстриол высвобождается в кровь матери и экскретируется в мочу. Повторные определения содержания эстриола в материнской моче позволяют оценить состояние плода. Одним из наиболее богатых естественных источников получения эстрогенных веществ являются жеребцы, у которых этих гормонов вырабатывается больше, чем у беременных кобыл или беременных женщин.
Количество вырабатывающегося у здоровых женщин эстрадиола изменяется во время менструального цикла: в ранней фолликулярной фазе его концентрация низкая - 50 пг/мл, а во время преовуляторпого пика увеличивается до 350-850пг/мл. [4].
Фармакокинетика
При попадании в циркуляцию эстрадиол прочно связывается с 2-глобулином и с меньшей аффинностью - с альбумином. Связанный эстроген относительно плохо диффундирует в клетку, поэтому физиологически активной является только свободная фракция гормона. В печени и других тканях эстрадиол превращается в эстрон и эстриол и их 2-гидроксилированные производные и конъюгированные метаболиты и экскретируется в желчь. Однако коньюгаты могут гидролизоваться в кишечнике с образованием активных реабсорбируемых соединений. Катехолэстрогены служат нейротрансмиттерами в центральной нервной системе. Они конкурируют за катехол-О-метилтрансферазу и в высокой концентрации подавляют инактивацию катехоламинов этим ферментом. В небольшом количестве эстрогены экскретируются в грудное молоко кормящих матерей.
Так как основное количество эстрогенов и их активных метаболитов экскретируется в желчь и реабсорбируется из кишечника, при пероральном приеме в результате энтеропеченочной циркуляции наблюдается значительное преобладание печеночных эффектов над периферическими. Если необходим периферический эффект эстрогенов, в частности у женщин после менопаузы, печеночные эффекты можно минимизировать, используя другие пути введения: вагинальный, трансдермальный или инъекционный. [3].
Эстрогены требуются для нормального полового созревания женщин. Они стимулируют развитие влагалища, матки и маточных труб, а также вторичных половых признаков. Эстрогены активируют развитие стромы и протоков молочных желез, влияют на рост подмышечных и лобковых волос и изменяют распределение жира на теле, что создает женский тип телосложения. Большие количествa эстрогенов стимулируют также развитие пигментации кожи, что более выражено в области сосков и половых органов.
Помимо действия на рост мускулатуры матки эстрогены также играют важную роль в развитии эндометрия. Постоянное и длительное воздействие эстрогенов приводит к аномальной гиперплазии эндометрия, которая обычно сопровождается аномальными кровотечениями.
Эстрогены дают ряд важных метаболических эффектов. Они частично отвечают за поддержание нормальной структуры кожи и кровеносных сосудов у женщин, подавляют резорбцию костей, существенно влияют на абсорбцию веществ в кишечнике, так как снижают его перистальтику.
Наряду со стимуляцией синтеза ферментов и факторов роста, приводящих к росту и дифференциации матки, эстрогены оказывают влияние на продукцию и активность многих белков организма. Особенно важны метаболические изменения в печени, так как в ней наиболее высока концентрация; таких белков, как транскортин, тироксин, глобулин, трансферрин, фибриноген. Эти изменения приводят к повышению концентрации циркулирующих тироксина, эстрогенов, тестостерона, железа, меди и других веществ. Эстрогены повышают свертываемость крови. Установлены многочисленные изменения факторов свертываемости при эстрогенной терапии, включая повышение содержания в плазме факторов II, VII, IX и X и снижение содержания антитромбина 3 частично в результате, печеночных эффектов.
Эстрогены изменяют состав лнпидов плазмы повышается содержание липопротеидов высокой плотности (ЛПВП), несколько стнижается содержание липопротеидов низкой плотности (ЛПНП) уменьшается концентрация холестерина. [2].
Первичный гипогонадизм
Лечение первичного гипогонадизма обычно начинают в возрасте 11-13 лет для стимуляции развития вторичных половых признаков и менструаций, оптимального роста и предотвращения психологических последствий задержки полового созревания. Терапия начинается с низких доз эстрогенов 3 мг конъюгированных эстрогенов или 5-10 мкг, которые назначают с первого по двадцать первый день каждого месяца. После завершения роста организма постоянная терапия в основном состоит из назначения эстрогенов и прогестинов.
Гормональная терапия в постменопаузном периоде
Кроме признаков и симптомов, следующий сразу же за прекращением нормальной функции яичников, таких как прекращение менструаций, возомоторные симптомы и атрофия половых органов, имеют место и истончение костей, изменение состава липидов, способствующее развитию сердечнососудистых заболеваний.
Когда прекращается нормальное функционирование яичников и концентрация эстрогенов падает в результате менопаузы, происходит резкий подъем концентрации в плазме холестерина и ЛПНП. Значительно изменяется содержание ЛПОНП и триглицеридов. Так как сердечнососудистые заболевания являются наиболее частой причиной смертности в данной возрастной группе, риск заболеваний составляет главную проблему при решении вопроса о целесообразности проведения гормональной терапии и влияет на выбор назначенного гормона. Благоприятное действие заместительной эстрогенной терапии на липиды и липопротеиды крови приводит к снижению частоты инфарктa миокарда па 50 % и инсультов на 40 %.
Развитие остеопороза зависит от количества костной ткани в начале этого процесса, от потребления кальция и от уровня физической активности. Риск остеопороза максимален у худых курильщиков, лиц кавказской расы, у малоактивных людей, при низком потреблении кальция, а также при семейной предрасположенности.
Эстрогены должны использоваться в минимальных эффективных дозах. Рекомендуемые дозы составляют 0.3-1.25 мг/день конъюгированных эстрогенов или 0.01-0.02 мг/день этинилэстрадиола. Для получения максимального эффекта необходимо начать терапию как можно раньше после наступления менопаузы. Пациентки с низким риском возникновения остеопороза, у которых проявляется только легкий атрофический вагинит, могут получать терапию местными средствами. Вагинальный путь введенияиспользуют и при лечении нарушений мочевого тракта. Эти препараты необходимо назначать циклами.
Лечение эстрогенами связано с повышением риска возникновения карциномы эндометрия. Назначение прогестиновых препаратов совместно с эстрогенами предотвращает гиперплазию эндометрия и значительно снижает риск возникновения рака. Если эстроген вводится первые 25 дней месяца и в течение последних 10-14 дней добавляется прогестин медроксипрогестерон (10 мг/день), риск возникновения рака снижается в два раза. Если прогестин вызывает седацию или другие нежелательные эффекты, его дозу cнижают до 2.5-5 мг в последние 10 дней цикла.
Ежедневное назначение 0.625 мг конъюгированных лошадиных эстрогенов и 2.5-5 мг медроксипрогестерона устраняет циклические кровотечения и вазомоторные симптомы, предотвращает атрофию половых органов, поддерживает плотность костей и улучшает липидный состав плазмы с небольшим снижением концентрации ЛПНП и повышением концентрации ЛПВП. Основным недостатком постоянной терапии является необходимость проведения биопсии матки, если после нескольких первых месяцев лечения возникают кровотечения.
Эстрогены можно назначать интравагинально и трансдермально, что снижает соотношение печеночных и периферических эффектов. [3].
При терапевтическом использовании эстрогенов наблюдаются следующие побочные эффекты: постменопаузные кровотечения, часто отмечаются тошнота и огрубление молочных желез, чего можно избежать, максимально снижая дозу. Возможна также гиперпигментация, мигрень, гипертензия и заболевание желчного пузыря.
В результате длительного приема эстрагенов возможно небольшое повышение риска развития рака молочной железы. Несмотря на то, что фактор риска мал (1.25), его необходимо учитывать, поскольку эта опухоль возникает у 10 % женщин. У больных получающих эстроген, повышается риск возникновения карциномы эндометрия. Степень риска изменяется в зависимости от длительности терапии и дозы: так, риск в 15 раз выше у больных, принимающих большие дозы эстрогена в течение 5 лет и более, тогда как у больных, получающих в течение непродолжительного периода низкие дозы, риск повышается только в 2-4 раза. Применяя одновременно прогестин, можно не только предотвратить повышение риска, но фактически снизить частоту возникновения рака эндометрия ниже средней по всей популяции.
Известен ряд случаев развития аденокарциномы влагалища у молодых женщин, чьи матери получали большие дозы диэтилстильбэстрола на ранних сроках беременности. Этот тип рака характерен для женщин в возрасте 14-44 лет. Также его прием увеличивает вероятность бесплодия, внематочной беременности и преждевременных родов. Этот препарат можно использовать только для лечения рака или в качестве посткоитального контрацептива. [6].
Эстрогены нельзя назначать больным с эстрогензависимыми новообразованиями, такими как карцинома эндометрия, или пациенткам с карциномой молочной железы или высоким риском ее развития. Их необходимо избегать при генитальных кровотечениях неустановленной природы, заболеваниях печени или тромбоэмболических нарушениях в анамнезе. [5].
Дозы и лекарственные средства
Эстрогены вызывают практически одинаковые гормональные эффекты, но степень их выраженности зависит от конкретного препарата и пути введения. Как уже отмечалось, эстрадиол является наиболее активным эндогенным эстрогеном и имеет наиболее высокий аффинитет к эстрогенным рецепторам. Его метаболиты эстрон и эстриол оказывают слабое действие на матку. Обнаружено, что другой важный метаболит эстрадиола, 2-гидроксиэстрон (катехолэстроген), выполняет в головном мозгу функции нейромедиатора. Кроме того, он конкурирует с катехоламинами за катехол-О-метилтрансферазу и ингибирует тирозингидроксилазу. Вследствие этого препараты, содержащие эстрон и эстрадиол, дают больше центральных эффектов, чем синтетические эстрогены, метаболизируемые другим путем. [2].
1. ПРИРОДНЫЕ ЭСТРОГЕНЫ
Эстрон
Oestronum
Синоним: Фолликулин
3-окси-эстра-1,3,5(10) триен-17-он
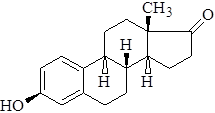
Характеристика. Белое кристаллическое вещество. Практически нерастворимо в воде, растворимо в спирте, эфире, маслах.
Фармакология. Эстрон является естественным фолликулярным гормоном, необходимым для нормального развития женского организма. Он начинает вырабатываться в яичниках с наступлением периода полового созревания и образуется в созревающих фолликулах до наступления климактерического периода. Вместе с гормоном желтого тела - гестагенон фолликулярный гормон участвует в осуществлении менструального цикла. Оба гормона необходимы для осуществления функции деторождения.
Эстрон применяют при патологических состояниях, связанных с недостаточной функцией яичников: при первичной и вторичной аменорее, вторичной половой недостаточности, гипоплазии полового аппетита, при климактерических расстройствах, бесплодии, слабости родовой деятельности, переношенной беременности и др.
Эстроген оказывает гипохолестеринемическое действие, уменьшает коэффициент холестерин/ фосфолипиды, повышают соединение в крови липопротеидов. Их применение для лечения и профилактики атеросклероза затруднено, так как при длительном применении у мужчин возникают явления феминизации, а у женщин возникают пролиферативные изменения в эндометрии и маточные кровотечения.
Активность эстрона определяют биологическим методом - по его способности вызывать течку у кастрированных самок (свиней и крыс). В 1мг содержится 10000ЕД.
Применение эстрогенных препаратов необходимо проводить под тщательным наблюдением врача. Длительное использование может привести к развитию маточных кровотечений, гиперплазии эндометрия, развитию опухолей эндометрия.
Эстрогенные препараты противопоказаны женщинам при злокачественных и добросовестных новообразованиях половых органов, молочных желез и других органов, при мастопатии, склонности к маточным кровотечениям, а также в гиперэстрогенной фазе климатического периода.
Форма выпуска: 0,05 и 0,1 масляный раствор в ампулах по 1 мл.
Хранение: в прохладном, защищенном от света месте. [6].
Эстрадиола дипропионат
Oestradidioli dipropionas
Синонимы:Estradiol dipropionate, Estradioli dipropionas
Эстратриен-1,3,5,(10)-диола-3,17 бетта дипропионат
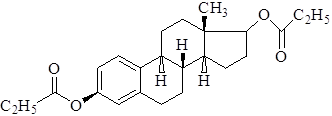
Характеристика. Белый кристаллический порошок. Практически нерастворим в воде, трудно растворим в спирте и растительных маслах.
Эстрадиол образуется в организме женщин вместе с эстроном. Активность 1 мг эстрадиола бензоата соответствует 10000ЕД. В виде эфиров (бензоата и дипропионата) эстрадиол мало разрушается в тканях организма. Эфиры эстрадиола медленно всасываются, выделяются и оказывают длительное влияние на организм.
Фармакология. Эстрадиола дипропионат оказывает сильное, замедленное и продолжительное действие. Показания к применению и противопоказания такие же, как для эстрона. Также эстрадиола пропионат используется в качестве гемостимулирующего средства у мужчин при остром радиационном поражении.
Эстрадиола дипропионат вводят внутримышечно.
Форма выпуска: 0,1 % масляный раствор в ампулах по 1 мл.
Хранение: список Б. В прохладном, защищенном от света месте. [5].
Климактерин
Climakterin
Комбинированный препарат, содержит в одной таблетке (драже) эстрадиола бензоата 25 ЕД ,сухого порошка из яичников 30 мг, теобромина и кофеина по 0,025г, нитроглицерина 0,0002 г, фенолфталеина 0,006г, кальция фосфата 0,004г.
Применяется при ангионевротических явлениях, возникающих в климактерическом периоде.
Назначают по 1-2 драже 2-3 раза в день.
Форма выпуска: драже в упаковке по 50 шт. [5].
Эстрадиола валерат
Estradiol valerate
Синонимы: Proginova. Premarine
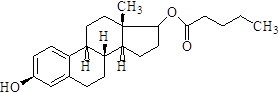
Характеристика. Эстрадиола валерат является эфиром природного эстрогена эстрадиола. Фармакология. Монопрепараты эстрадиола широко применяются для лечения первичного гипогонадиума и аненореи (по 2-4 мг/сут). В виде 21 дневных циклов с недельными перерывами во время которых назначают гестагены.
Форма выпуска: таблетки по 0,6 и 1,2 мг; драже по 2 мг.
Эстрадиола валарат применяется в комбинированных эстроген-гестрогенных препаратах, для проведения заместительной гормональной терапии (ЗГТ) у женщин в пернменопаузе и постменопаузе.
Перименопауза - это период в жизни женщин, который охватывает промежуток времени с начала угасания функции яичников, менопаузу и еще 1 год после нее. Постменопауза - период, который следует за менопаузой и продолжающийся до смерти женщин. В связи с угасанием функции яичников и дефицитом эстрогенов в организме происходит гормональная перестройка, которая ведет за собой ряд болезненных изменений, которые можно разделить на 3 группы:
1. Ранние симптомы менопаузы (в течение 1 года):
- вазомоторные нарушения: колебания АД, раздражительность, сонливость, беспокойство, депрессия.
2. Средневременные симптомы менопаузы (2-5 лет после менопаузы):
- атрофия органов репродуктивного тракта, это приводит к появлению сухости слизистой влагалища, зуду, учащенному мочеиспусканию;
- наблюдается на коже появление морщин, выпадение волос, ломкость ногтей и др.
3. Поздние симптомы менопаузы (5 лет и более):
- прогрессирование нарушений липидного обмена и атеросклероза;
- остеопороз (потеря массы костной ткани).
Проведение заместительной гормональной терапии эстрадиол валератом позволяет провести воздействие на кандуктивную группу симптомов. При этом придерживаются следующих принципов:
1. при заместительной терапии необходимо использовать природный эстрогены;
2. эстрогены назначается в минимальных дозах;
3. длительность ЗГТ составляет 5-7 лет;
4. у женщин с удаленной маткой ЗГТ можно проводить чистыми эстрогенами, у остальных ее проводят комбинированными эстроген-гестагенными средствами;
5. для женщин находящихся в перименопаузе ЗГТ проводят циклами: с 1 по 10 дней тАУ чистый эстроген, с 11-20 дней тАУ эстроген с прогестинами и 8 дней тАУ перерыв. Для женщин находящихся в постменопаузе ЗГТ проводят комбинацией эстроген прогестинами непрерывно с 1 по 28 день цикла. [6].
Этинилэстрадиол
Aethinyloestradiolum
Синоним: Ethinylestradid, Microfollin forte.
альфа этинилэстратриен-1,3,5(10) диол- 3,17 бетта
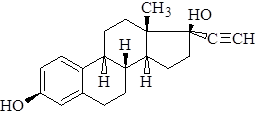
Характеристика. Белый или кремовато-белый мелкокристаллический порошок. Практически не растворим в воде, растворим в спирте и растительных маслах.
Фармакология. По строению и действию этинилэстрадиол близок к эстрадиолу. Химически отличается от эстрадиола включением этилового радикала (-C=CH) в положении С17 , что приводит значительному усилению активности и сохранению эффекта при приеме препарата внутрь.
Дозы препарата и длительность применения следует индивидуализировать в зависимости от характера заболевания и эффективности лечения. При гипогонадизме и аменорее этинилэстрадиол назначают по 20-100 мг/сут в виде 20 дневного цикла с последующим 5-7 дневным перерывом, во время которого назначают гестагены.
Для устранения нервно-сосудистых расстройств при эстрогенной недостаточности препарат назначают по 0,01-0,02 мг в день в течении 10-15 дней, курс лечения необходимо повторить.
Этинилэстрадиол применяют при лечении рака предстательной железы и рака молочной железы, при этом доза возрастает до 3 мг в день, курс лечения длительный. При больших дозах этинилэстрадиол вызывает тошноту, рвоту, головокружение.
Форма выпуска: по 0,01 и 0,05 мг.
Хранение: списка Б, в защищенном от света месте. [7].
Синестрол
Synoestrolum
Синоним: Hexestrolum
Мезо-3.4-Ди-(пара-оксифенил)-гексан
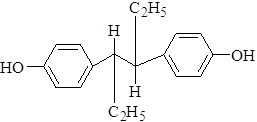
Характеристика. Белый или белый со слегка желтоватым оттенком порошок без запаха. Практически нерастворим в воде, легко растворим в спирте, трудно растворим в персиковом масле.
Фармакология. Синестрол является соединением, которое по химическому строению отличается от стероидных эстрогенных гормонов, но по биологическим и лечебным свойствам близок к ним. Синестрол по активности равноценен эстрону: 1 мг синестрола соответствует 10000 ЕД. Вводят синестрол внутримышечно, под кожу и внутрь.
Применяют при гипогенитализме, аменорее, для уменьшения лактации у женщин в послеродовом периоде, при раке молочной железы и предстательной железы.
Побочное действие: тошнота, рвота, головокружение. При приеме больших доз возникает токсическое повреждение печени, кровотечения у женщин, выраженная феминизация у мужчин (понижение половой функции, набухание молочных желез, пигментация сосков, уменьшение размеров яичек). Синестрол и его аналоги противопоказаны при беременности, заболеваниях печени и почек.
Форма выпуска: таблетки по 0,001 г (1мг); 0,1% (1 мг в 1 мл) и 2% (20 мг в 1 мл) масляные растворы в ампулах по 1 мл; 2% раствор применяют для больных со злокачественными новообразованиями.
Хранение: списка Б, в защищенном от света месте. [5].
Сигетин
Sygethinum
Дикалиевая соль мезо-3,4-ди(пара-сульфофенил)-гексана
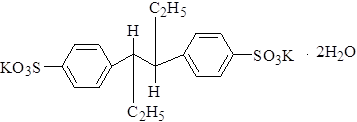
Характеристика. Белый кристаллический порошок. Трудно растворим в воде (1:50), легко растворим в горячей воде, нерастворим в спирте.
Фармакология. По структуре сигетин имеет сходство с синестролом, но эстрогенного действия не оказывает. Эффективен при легких климактерических расстройствах.
Препарат усиливает сокращение матки, улучшает плацентарное кровообращение.
Применяют сигетин для ускорения родов и лечения внутриутробной асфиксии плода. Применение сигетина во время родов противопоказано при массивной кровопотере у рожениц и преждевременной отслойке плаценты.
Форма выпуска: таблетки по 0,05 и 0,1 г; 1% раствор в ампулах по 1 и 2 мл.
Хранение: список Б, в сухом защищенном от света месте. [6].
Кломифенцитрат
Clomihencitras
Синонимы: Clomifene citrae
1-(4-(2-Диэтиламиноэтокси)фенил)-1,2-дифенил-2-хлорэтилена цитрат
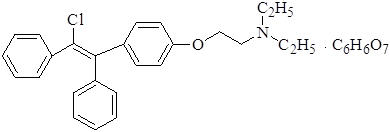
Характеристика. Белый или белый с черноватым оттенком кристаллический порошок, малорастворим в воде, умеренно растворим в спирте.
Фармакология. Данный препарат является смесью цис- и трансформы указанного соединения. Причем более активной является цисизомер, соединение которого в препарате составляет не менее 50%.
Кломифенцитрат относится к группе препаратов, называемых антиэстрогенами. Их действие обусловлено способностью связываться с эстрогенозависимыми рецепторами в гипоталамусе и яичниках. В малых дозах они способны усиливать секрецию гонадотропинов (пролактина, фолликулостимулирующего и лютеинизирующего гормонов) и стимулируют овуляцию. Если в организме содержится малое количество эндогенных эстрогенов данные препараты оказывают умеренный эстрогенный эффект, однако при высоком уровне эстрогенов они оказывают антиэстрогенное действие. Уменьшая уровень циркуляции эстрогенов они способствуют увеличению секреции гонадотропинов. Применяют кломифенцитрат как средство стимулирующее овуляцию при ановуляторной дисфункции яичников и связанном с ней бесплодии, при дисфункциональных маточных кровотечениях, при раке молочной желез.
Кломифенцитрат, в связи со стимуляцией секреции гонадотропинов, применяют при андрогенной недостаточности, олигоспермии у мужчин и при задержке полового и физического развития у подростков мужского пола. Также он может применяться с диагностической целью.
Для стимуляции овуляции назначается внутрь в дозе 50 мг 1 раз в день (перед сном), начиная с 5-го дня менструального цикла, в течении 5 дней.
При диссеминированном раке молочной желез назначают по 100 мг 2 раза днем 1 утром и вечером ежедневно в течении длительного срока.
В процессе лечения кломифенцитратом необходимо постоянное наблюдение гинеколога, следует проверить функцию яичников, осуществить влагалищные исследования.
Кломифенцитрат вызывает следующие побочные явления: гиперстимуляцию яичников, которая проявляется болями в нижней части живота, в метеоризме; увеличение размеров яичников; возможны тошнота, понос, приливы крови к лицу, головокружение, аллергические дерматозы, нарушение зрения.
Мужчинам кломифенцитрат назначают по 50 мг 1-2 раза в день в течении 3-4 месяцев под систематическим контролем спермограммы. Подросткам с задержкой полового и физического развития назначают по 50-100 мг в сутки (в зависимости от массы тела) курсами по 10 дней; всего 3 курса с промежутками 1-3 месяца.
Кломифенцитрат противопоказан при беременности, доброкачественных новообразованиях, органических заболеваниях ЦНС, болезнях печени, склонности к тромбообразованию. Не следует назначать препарат лицам, работа которых требует быстрой психической и физической реакции.
Форма выпуска: таблетки по 0,05 г (50 мг) по 30 штук в банках светозащитного стекла.
Хранение: список Б, в защищенном от света месте. [6].
2. СИНТЕТИЧЕСКИЕ ЭСТРОГЕНЫ
Естественные эстрогены были подвергнуты различным химическим модификациям. Наиболее важным результатом этих изменений было повышение эффективности гормонов при пероральном назначении.
Помимо стероидных эстрогенов было синтезировано и использовано в клинике большое количество нестероидных препаратов с эстрогенной активностью - диэтилстильбэстрол, хлоротрианизен, металленэстрил.
Диэтилстильбэстрол
Diaethylstilboestrolum
Синоним: diethylstilbestrol, Diethylstilbestrolum
Транс-3,4-Ди-(пара-оксифенил)-гексен-3
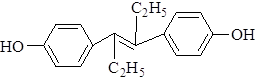
Характеристика. Белый кристаллический порошок. Растворим в спирте, эфире, жирных маслах, очень малорастворим в воде.
Фармакология. По силе действия диэтилстильбэстрол эквивалентен эстрадиолу, но он не теряет своей активности при пероральном приеме и может назначаться внутрь. В отличии от эстрадиола обладает более длительным действием. В 1 мг содержится 20000ЕД.
Диэтилстильбэстрол применяется в гинекологии, а также при гипертрофии и раке предстательной железы. В настоящее время в связи с побочными явлениями он имеет ограниченное применение.
Форма выпуска: 3% раствор в масле в ампулах по 1 мл.
Хранение: список Б, в защищенном от света месте. [6].
3. ПРОГЕСТИНЫ
Прогестерон
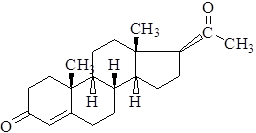
Прогестерон представляет собой основной прогестин у человека. Кроме того, он оказывает важное гормональное действие, он является предшественником эстрогенов, андрогенов и адренокортикостероидов. Он синтезируется яичниками, семенниками и корой надпочечников из циркулирующего в крови холестерина. Большое количество этого гормона синтезируется и высвобождается плацентой во время беременности.
В яичниках продукция прогестерона в первую очередь синтезируется желтым телом. Здоровые мужчины секретируют 1-5 мг прогестерона в сутки, что создает концентрацию в плазме 0,03 мкг/дл. У женщин во время фолликулярной фазы цикла, когда секреция прогестерона составляет только несколько миллиграммов в день, его уровень лишь немного выше. Во время лютеиновой фазы содержание гормона повышается с 0,5 мкг/дл до более чем 2 мкг/дл. [7].
Фармакокинетика
Прогестерон быстро абсорбируется при любом пути введения. Период его полувыведения из плазмы составляет приблизительно 5 минут, при этом небольшое количество гормона временно депонируется в жирах организма. Он практически полностью метаболизируется во время первого прохождения через печень и по этой причине практически не дает эффекта при назначении внутрь.
В печени прогестерон метаболизируется до прегнандиола и конъюгирует с глюкуроновой кислотой. В виде глюкуронида прегнандиола он экскретируется в мочу. Количество прегнандиола в моче используется как показатель секреции прогестерона. [8].
Физиологические эффекты
Механизм действия. Прогестины проникают в клетку и присоединяются к прогестероновым рецепторам, распределенным в ядре и цитоплазме. Комплекс лиганд-рецептор связывается с эффекторным элелементом, активируя транскрипцию генов. Эффекторный элемент для прогестерона подобен кортикоидному эффекторному элементу; специфичность ответа зависит от того, какой рецептор имеется в данной клетке. Комплекс прогестерон-рецептор образует димер до того, как связывается с ДНК. Однако отличие от эстрогеновых рецепторов он может образовывать как гетеро-, так и гомодимеры.
Эффекты прогестерона. Прогестерон оказывает слабое действие на метаболизм белков. Он стимулирует активность липопротеидлипазы и способствует депонированию жиров. Более выражено действие гормона на метаболизм углеводов. Прогестерон увеличивает базальный уровень инсулина и инсулиновый ответ на колебания содержания глюкозы у больных.
Прогестерон повышает температуру тела, влияет на деятельность центров дыхания (активизируется респираторный ответ на СО2). Прогестерон и родственные ему стероиды оказывает также центральное угнетающее и гипнотическое действие.
Прогестерон отвечает за развитие альвеол и долек секреторного аппарата молочных желез, за созревание и изменения секреции эндометрия, которые происходят в процессе овуляции. Гормон снижает уровень многих аминокислот в плазме и усиливает экскрецию азота с мочой. [8].
Клиническое использование прогестинов
Прогестиновые гормоны в основном используются для заместительной гормональной терапии и в качестве средств гормональной контрацепции. При парентеральном, применении в больших дозах в качестве монотерапии (например, 150 мг медроксипрогестерона ацетата внутримышечно каждые 90 дней) возникает длительное подавление овуляции и аменорея. Такое назначение используется при лечении дисменореи, эндометриоза, гирсутизма и патологических кровотечений, а также для контрацепции. Основным недостатком этой схемы является необходимость длительного периода восстановления функции яичников после прекращения приема.
Прием медроксипрогестерона ацетата по 10-20 мг внутрь два раза в неделю или по 100 мг/м2 внутримышечно каждые 1-2 недели останавливает ускоренное половое созревание у детей. Прогестерон можно использовать для тестирования секреции эстрогенов. Кровотечение, следующее за отменой 5-7-дневного введения 150 мг/день прогестерона или 10 мг/день медроксипрогестерона у больных с аменореей, возникает только в том случае, если эндометрий предварительно стимулируется эстрогенами.
Прогестин способен вызывать у некоторых больных повышение кровяного давления. У женщин наиболее активные прогестины снижают также концентрацию ЛПВП в плазме, что повышает вероятность возникновения инфаркта миокарда. [4].
Прогестерон
Progesteronum
Прегнен-4-дион-3,20
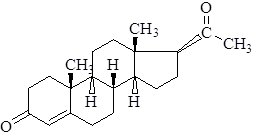
Характеристика. Белый кристаллический порошок. Практически нерастворим в воде, растворим в спирте, трудно растворим в растительных маслах.
Фармакология. При любых способах введения быстро абсорбируется. Максимальная концентрация при приеме внутрь достигается через 1-3 часа, при нитровании аппликации через2-6 часов. Степень связывания с белками плазмы около 90%. В печени превращается в 3-альфа, 5-бета-прегиан-диол. Экскретируется с мочой в виде глюкуронидов и прегнандиола.
Противопоказания. Гиперчувствительность, опухоли груди и репродуктивных органов, нарушение функции печени, вагинальные кровотечения, склонность к тромбозам.
Ограничения к применению. Бронхиальная астма, сердечная недостаточность, гипертензия, нарушение функции почек, заболевание ЦНС, сахарный диабет, внематочная беременность, кормление грудью.
Побочные действия. При приеме внутрь: сонливость и головокружение, расстройства менструального цикла.
Инъекции: тромбоэмболия, апатия, холестатический гепатит, нарушение зрения, изменение массы тела, отеки, увеличение молочных желез, аллергические реакции.
Форма выпуска. 1%, 2,5% растворы (10 и 25 мг) в масле в ампулах по 1 мл. [1].
Оксипрогестерона капронат
Oxyprogesteroni caproas
Прегнен-4-ол-17 альфа -диона-3,20 капронат
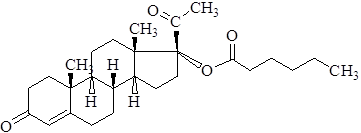
Характеристика. Белый или белый со слегка желтоватым оттенком кристаллический порошок. Практически не растворим в воде, растворим в спирте, жирных маслах.
Фармакология. 17-альфа-оксипрогестерона капронат является синтетическим аналогом гормона желтого тела - прогестерона. Химически отличается от прогестерона тем, что в положении с 17 содержит остаток капроновой кислоты. Из-за этого оксипрогестерон капронат более стоек в организме, чем прогестерон, действует медленнее и оказывает пролонгированный эффект. После однократного внутри мышечного введения действие продолжается от 7 до 14 дней, с целью профилактики и лечения угрожающего выкидыша вводят по 0,125-0,25г (1-2 мл 12,5% раствора
Вместе с этим смотрят:
РЖсторiя виникнення та розвитку масажу
Аборты
Аденовирусная инфекция
Азотные и кислородные ванны, нафталановая нефть
Акушерська операцiя - накладання акушерських щипцiв