Токсоплазмоз у детей
РЕФЕРАТ НА ТЕМУ:
ТОКСОПЛАЗМОЗ У ДЕТЕЙ
Токсоплазмоз - паразитарное заболевание, характеризующееся преимущественно латентным или хроническим течением, поражением нервной системы, органов ретикулоэндотелиальной системы, мышц, миокарда и глаз.
ЭТИОЛОГИЯ
Возбудитель - Toxoplasma gondii - относится к классу простейших. Тип Protozoa. Подтип Sporozoa (обычно образуют споры; реснички, жгутики или псевдоподии отсутствуют). Класс Telosporea (имеется фаза полового размножения). Подкласс Coccidea (трофозоиты располагаются внутриклеточно, имеют "верхушечный комплекс"). Отряд Eucoccideia (жизненный цикл включает чередование бесполого - шизогония и полового размножения - спорогония). Подотряд Eimeriina (половая стадия в эпителии кишки у позвоночных животных; один хозяин или чередование двух хозяев; спорозоиты находятся в "споре"). Вид Toxoplasma gondii.
Токсоплазмы подвижны и имеют форму дуги, арки или напоминают дольку апельсина. Встречаются также овальные и округлые формы. Тип движения у токсоплазмы скользящий. Существует в трех основных формах: тахизоиты (эндозоиты), цисты и ооцисты. Тахизоиты имеют размеры 4тАУ7 мкм в длину и 2тАУ4 мкм в ширину, по форме напоминают полумесяц, хорошо окрашиваются по Романовскому. Они размножаются внутриклеточно во всех клетках млекопитающих, за исключением безъядерных (эритроциты), и обнаруживаются в тканях в острой стадии инфекции. На тахизоиты активно воздействуют различные химиопрепараты (пириметамин, сульфаниламиды, макролиды и др.), они нестойки вне клетки и во внешней среде, быстро погибают при высушивании, прогревании, под влиянием дезинфицирующих средств.
Цисты формируются в организме промежуточного хозяина, имеют собственную плотную оболочку, через которую не проникают ни антитела, ни лекарственные препараты. Размеры цист до 100 мкм, внутри содержится 3000тАУ5000 паразитов и более. Цисты очень устойчивы к различным воздействиям (в том числе пищеварительных ферментов) и в организме хозяина сохраняются десятки лет. Большая их часть локализуется в скелетных мышцах, головном мозге, миокарде, глазах. Внутри данного образования со стенками, состоящими из клеток хозяина, располагается большое число брадизоитов.
Ооцисты представляют собой образования овальной формы диаметром 10тАУ12 мкм. Они формируются в слизистой оболочке тонкой кишки некоторых представителей семейства кошачьих и выделяются с испражнениями, которые играют основную роль в передаче инфекции.
Культивируются токсоплазмы путем заражения лабораторных животных (белые мыши, морские свинки, кролики, хомяки), в развивающихся куриных эмбрионах, а также в культуре тканей. Имеются различные штаммы токсоплазм, одни из них отличаются высокой вирулентностью (штамм RH) и быстро приводят к гибели лабораторных животных, другие, - маловирулентные (авирулентные), обычно не вызывают заметных клинических проявлений болезни.
ЭПИДЕМИОЛОГИЯ
Инфицированность токсоплазмами широко распространена во всех странах мира. В США инфицировано от 5 до 30% лиц в возрасте 10тАУ19 лет и от 10 до 67% лиц старше 50 лет. В странах СНГ инфицировано около 30% населения, в Санкт-Петербурге - около 25%, а в совокупности число инфицированных во всем мире составляет не менее 500 млн, что сопоставимо с общим числом лиц инфицированных вирусом гепатита В. Число случаев врождённого токсоплазмоза колеблется от 1: 1000 до 1: 10000 живорожденных.
У человека существует три пути передачи инфекции: энтеральный (заглатывание ооцист или цист), трансплацентарный, а также возможно заражение при переливании инфицированной крови и пересадке органов.
Человек чаще инфицируется токсоплазмой посредством фекально-орального механизма передачи инфекции (рис). Это происходит в результате прямого или опосредованного контакта с животными семейства кошачьих или при употреблении в пищу контаминированных продуктов, а также воды. Дети младшего возраста, как правило, заражаются при прямом контакте с кошками или играя в песочнице с инфицированным песком.
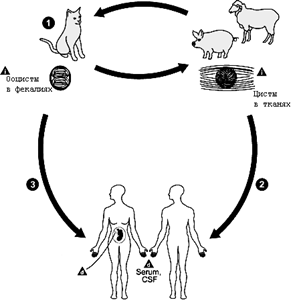
Рис. Инфицирование человека токсоплазмой посредством фекально-орального механизма: 1 - первичное заражение кошек цистами; 2 - попадание ооцист а организм беременной женщины; 3 - заражение человека при употреблении инфицированных продуктов (сырое мясо)
С возрастом вероятность инфицирования при употреблении недостаточно термически обработанных мясных продуктов увеличивается. Так, по данным ряда исследований (6,7) 25% баранины, 25% свинины и 1% говядины контаминированы цистами токсоплазм. Кроме этого, употребление немытых овощей, использование немытых после резки сырого мяса ножей, несоблюдение правил личной гигиены и уборка уличных "кошачьих туалетов" являются факторами риска инфицирования токсоплазмами.
Toxoplasma gondii относится к кишечным кокцидиям; кошки служат как окончательным, так и промежуточным объектом паразитирования. Фактически, кошки - единственные животные, выделяющие ооцисты с испражнениями. При первичном заражении инфекция у животных протекает асимптомно и серонегативно. При этом они могут выделять с экскрементами до 20 млн. неспорулированных (т.е. неинфекционных) ооцист в день, однако, данное состояние длится только 10тАУ15 дней с момента инфицирования, а после первичного заражения у животных развивается иммунитет, предохраняющий их от повторного заражения. Споруляция, переводящая ооцисты в инфекционное состояние, происходит в последующие 1тАУ5 дней (при температуре 24В°С); она не реализуется при температуре ниже 4В°С и выше 37В°С. Сроки появления ооцист в испражнениях кошки зависят от характера инфицирования и составляют от 3-х до 24-х дней. При благоприятных условиях они жизнеспособны в течение 18 мес.
Таким образом, следует отметить, что период "окна", во время которого животное заразно, очень короткий. Если кошка содержится дома и употребляет в пищу только готовый корм, риск её заражения токсоплазмами практически отсутствует. Животные, выходящие на улицу, а также употребляющие пищу, приготовленную дома, или пойманных грызунов, могут быть инфицированы, однако их экскременты должны оставаться в "кошачьем туалете" 1тАУ5 дней в течение 2-недельного периода "окна", чтобы стать заразными. Наибольший риск инфицирования представляет садовая земля или песочницы, которые могут быть длительно контаминированы кошачьими экскрементами.
Токсоплазмоз относится к зоонозам с природной очаговостью. Окончательным хозяином являются домашние кошки и некоторые дикие представители семейства кошачьих (рысь, пума, оцелот, бенгальский кот, ягуар и др.), в их организме происходит половой цикл развития возбудителя, приводящий к образованию ооцист, которые выделяются с фекалиями во внешнюю среду, где длительно сохраняются. Стенки тканевых цист, попавших в организм кошки при употреблении сырого мяса, заражённых грызунов разрушаются под действием протеолитических ферментов желудка и тонкого кишечника с высвобождением медленно делящейся стадии токсоплазм - брадизоитов. Последние проникают в эпителиальные клетки тонкой кишки и дают начало образованию большого количества мужских и женских гамет (гаметогония, асексуальная стадия развития). После слияния мужской и женской клеток образуется зигота, формируются неспорулированные ооцисты, которые и выделяются с фекалиями во внешнюю среду.
Ооцисты, выделяющиеся с их испражнениями, могут приводить к инфицированию как человека, так и многих других животных (свыше 200 видов), которые служат промежуточными хозяевами. Заражение может наступить при употреблении в пищу сырого мяса (мясного фарша) этих животных, содержащих тканевые цисты или при попадании ооцист в пищеварительный тракт через загрязненные руки. При попадании в организм промежуточного хозяина происходит их дальнейшее развитие - в кишечнике ооцисты превращаются в активные спорозоиты, среди которых выделяют две формы. Тахизоиты представляют собой пролиферативную форму, встречающуюся в активный период инфекции и характеризующуюся быстрым размножением бесполым путем. После повторной репликации клетки хозяина разрываются и тахизоиты диссеминируют с током крови по всему организму, включая ЦНС, глаза, скелетные и сердечную мышцы, плаценту. Размножившиеся паразиты заполняют поражённые ими клетки, плотно прилегая друг к другу. Такие скопления называются "псевдоцистами". Они не имеют собственной оболочки. С развитием иммунного ответа, появляются тканевые цисты, наиболее часто образующиеся в поперечно-полосатых мышцах и головном мозге, состоящие из медленно делящихся брадизоитов.
При хроническом токсоплазмозе во внутренних органах могут образовываться истинные цисты. Они либо подвергаются обызвествлению, либо разрушаются с выходом токсоплазм и проникновением последних в здоровые клетки, что влечёт за собой рецидив заболевания.
Больной человек не выделяет возбудителя во внешнюю среду и никакой опасности для окружающих не представляет. Контакт с промежуточными хозяевами (собаками, сельскохозяйственными животными) к инфицированию людей, как правило, не приводит.
При заражении матери во время беременности возможна трансплацентарная передача инфекции плоду. При заражении матери в I триместре беременности врожденный токсоплазмоз наблюдается в 15тАУ20% и протекает тяжело. При инфицировании в III-м триместре инфицированными оказываются 65% новорожденных, но у некоторых инфекция может протекать без выраженных клинических проявлений. Дискутабелен вопрос о вероятности поражения плода у женщин, инфицированных до беременности (за 6 мес. и более). Имеются сведения о малой вероятности внутриутробного поражения плода при заражении матери незадолго до наступления беременности. Кроме этого, вероятность трансплацентарной передачи инфекции у женщин с хроническим токсоплазмозом появляется только при наличии у них иммуносупрессии (прием кортикостероидов, цитостатиков, ВИЧ-инфекция и др.). По данным В.В. Васильева (2003), если женщина инфицирована токсоплазмами более чем за 3 мес. до беременности, то трансплацентарная передача возбудителя с развитием врожденного токсоплазмоза практически невозможна.
Инфицированность доноров токсоплазмами такая же, как и у клинически здоровых лиц, что следует учитывать при решении вопроса о показаниях к переливанию крови лицам с резко ослабленным иммунитетом (больные СПИДом, лейкемией и др.), а также при пересадке органов. Не следует забывать о необходимости тщательного обследования доноров, в том числе и на токсоплазмоз.
В литературе описаны случаи заражения через поврежденные кожные покровы.
ПАТОГЕНЕЗ
При попадании пероральным путем инвазивных форм токсоплазм в пищеварительный тракт происходит внедрение возбудителя в эпителиальные клетки нижних отделов тонкой кишки, где в результате его внутриклеточного размножения возникают очаги некроза. Запускается иммунный ответ, в котором участвуют натуральные киллеры и тканевые макрофаги, осуществляющие фагоцитоз токсоплазм и синтез цитокинов. Иммуноопосредованный цитолиз инфицированных клеток приводит к выходу возбудителя в межклеточное пространство, где он либо фагоцитируется, либо проникает в непораженные клетки. Фагоцитоз носит частично завершенный характер, что приводит к "уклонению" токсоплазм от иммунной защиты и в последующем - к персистенции.
Токсоплазмы частично с током лимфы достигают регионарных (мезентериальных) лимфатических узлов, где развиваются воспалительные изменения с формированием инфекционных гранулем. Развивается специфический мезаденит и в дальнейшем возбудитель гематогенным или лимфогенным путями диссеминирует по органам-мишеням (печень, селезенка, лимфатические узлы, нервная система, глаза, миокард, скелетные мышцы). В этих органах образуются скопления паразитов в виде цист, которые могут сохраняться в организме десятки лет и даже пожизненно. В местах фиксации возникают воспалительные очаги, а в некоторых органах (нервная система, скелетные мышцы) - очажки некроза, в которых затем откладываются соли кальция, и образуются кальцинаты.
В результате жизнедеятельности паразита и выделения антигенов и аллергенов наступает аллергическая перестройка организма (по типу реакций гиперчувствительности замедленного типа) и вырабатываются АТ, которые выявляются в различных иммунных реакциях. В развитии иммунитета большое значение имеют как клеточные, так и гуморальные факторы. Наличие АТ предохраняет от нового заражения даже высоковирулентными штаммами токсоплазм и обусловливает бессимптомное (латентное) течение токсоплазмоза у большинства инфицированных лиц. При ослаблении защитных сил организма и снижении напряженности иммунитета может наступить обострение заболевания (переход латентной формы в манифестную).
Обострение хронического токсоплазмоза может наблюдаться спустя много лет после инфицирования и, как правило, провоцируется интеркуррентными заболеваниями (острые респираторные инфекции и др.) или использованием цитостатиков и иммунодепрессантов. В последние годы важное значение приобрела проблема генерализации латентного токсоплазмоза у ВИЧ-инфицированных, у которых возможно развитие острого злокачественного течения с развитием некротического локализованного или диффузного менингоэнцефалита и вовлечением в процесс многих органов (глаза, сердце, печень, легкие).
Основная роль в развитии токсоплазмоза у лиц с иммуносупрессией отводится нарушениям продукции цитокинов. Показано, что при развитии токсоплазмоза на фоне ВИЧ-инфекции резко снижается как концентрация сывороточного гамма-интерферона, так и его способность активировать макрофаги. К факторам защиты относят интерлейкин-12, ФНО-, CD-8+, к факторам, способствующим генерализации заболевания, - интерлейкины - 4, - 6, - 10. В патогенезе манифестных форм хронического токсоплазмоза основную роль играет развитие реакций гиперчувствительности замедленного типа к антигенам токсоплазм и продуктам их жизнедеятельности.
КЛАССИФИКАЦИЯ
В настоящее время используется несколько клинических классификаций токсоплазмоза, в которых не всегда учитывается факт полисистемности заболевания, развивающейся в динамике.
По механизмам инфицирования принято выделять врожденный и приобретенный токсоплазмоз. Наиболее приемлемой для практической медицины является классификация А.П. Казанцева (1985), в которой выделяются латентный (первичный и вторичный), первично - и вторично-хронический (клинически выраженный и стертый), а также острый токсоплазмоз. При всех хронических формах выделяют периоды обострения и ремиссии, а при всех вторичных - фиксируют наличие или отсутствие резидуальных явлений ранее перенесенной манифестной формы заболевания. Использование классификаций, построенных по "органному" принципу, не обосновано, так как при токсоплазмозе не бывает изолированных поражений одного органа, проявления заболевания всегда свидетельствуют о поражении многих органов и систем.
СИМПТОМЫ И ТЕЧЕНИЕ
Инкубационный период при внутрилабораторных заражениях высоковирулентными штаммами длится около 2-х недель, при пероральном заражении - от 10 дней до 3-х мес.
Первичное инфицирование токсоплазмой приводит в 95тАУ99% случаев к выработке специфических АТ и формированию нестерильного иммунитета без каких-либо клинических проявлений заболевания. Такое состояние называется "первично-латентным токсоплазмозом" и, как правило, выявляется лишь при серологическом обследовании.
В зависимости от выраженности снижения иммунитета возможно также развитие первично-хронического (1тАУ5% инфицированных) или (при более значительных изменения в иммунной системе, до 0,01% инфицированных) острого токсоплазмоза.
Первично-латентный токсоплазмоз может трансформироваться в последние две клинические формы под влиянием факторов, способных вызвать иммуносупрессию (иммуносупрессивная терапия, лучевая терапия, ВИЧ-инфекция, хронический психоэмоциональный стресс).
При развитии острого токсоплазмоза, особенно на фоне иммуносупрессии, в результате первичного инфицирования заболевание может протекать в виде острой манифестной (ОМТ) и острой септической (ОСТ) форм. Клиническими признаками ОМТ являются легкий гриппоподобный синдром, лихорадка, энтерит, полилимфоаденит, гепатоспленомегалия. Проявлением ОСТ является бурно развивающийся менингоэнцефалит, специфический токсоплазмозный сепсис. Продолжительность острой фазы в 70% наблюдений до 4-х мес., а в остальных случаях - до 1 года.
Ведущим клиническим признаком ОМТ является лимфаденит с последующим присоединением синдрома общей интоксикации, которые сохраняются в течение недели. У 20тАУ30% пациентов наблюдается диарейный синдром в виде острого энтерита или гастроэнтерита. Далее на первый план выступают признаки поражения органов ретикулоэндотелиальной системы (печень, селезенка, лимфоузлы) и симптомы поражения опорно-двигательного аппарата. Появляются постоянные боли в мышцах верхних и нижних конечностей, летучие боли в суставах, несущих статическую нагрузку. Однако нет объективных и лабораторных признаков артрита.
При развитии острого хориоретинита появляется внезапное выпадение части поля зрения на одной стороне, при этом чаще он наблюдается в конце 1-й недели болезни. Данные явления сопровождаются субфебрильной температурой и часто сочетаются с лимфоаденопатией и гепатолиенальным синдромом.
Период разгара (со 2-й недели болезни) длится 2тАУ3 недели и проявляется угасанием признаков интоксикации, купированием диарейного синдрома, но прогрессированием гепатолинеального синдрома, лимфоаденопатии, мышечных и суставных болей, особенно в нижних конечностях. Могут наблюдаться клинико-лабораторные признаки мононуклеозоподобного синдрома. Через 3тАУ4 недели после стихания клинической манифестации длительно остаются лимфаденопатия, мезаденит, гепатоспленомегалия и лабораторно-относительный лимфоцитоз. Окончание острого заболевания находит отражение в серологической диагностике. Так, исчезают АТ класса IgM и нарабатываются высокоавидные АТ IgG.
В основном исход заболевания благоприятный - формируется нестерильный иммунитет без значимого нарушения функций органов и систем. Однако описаны как случаи тяжелого течения с летальным исходом, так и случаи с формированием резидуальных последствий (атрофия зрительных нервов, диэнцефальные расстройства, эпилептиформные приступы, внутричерепная гипертензия, вялотекущий арахноидит, очаги хориоретинита со снижением зрения, кальцинаты).
Иногда возможна тифоподобная форма острого токсоплазмоза с характерной экзантемой, появляющейся на 4тАУ7-й день (обильная, макулезная, от розового до темно-красного цвета) без поражения ЦНС, хотя чаще выявляется сочетание симптомов (смешанная форма). Возможно развитие неврита зрительных нервов, парезов, гемиплегий, через 4тАУ5 недель - миокардита.
У иммунокомпроментированных больных чаще регистрируется реактивация латентной хронической инфекции с наиболее типичным поражением ЦНС по типу менингоэнцефалита, который медленно прогрессирует с постепенным вовлечением в патологический процесс черепных (чаще зрительных) нервов, миокарда. Очень редко определяются положительные менингеальные симптомы, а в ликвор вытекает под повышенным давлением и отмечается лимфоцитарный плеоцитоз. Позднее, при компьютерной томографии могут выявляться кисты в веществе головного мозга. Одновременно на фоне доминирующей картины нейроинфекции, выявляются другие признаки токсоплазмоза - полилимфоаденит, гепатолиенальный синдром, артралгии и миалгии.
Как указывалось выше, возможно развитие первично-хронического токсоплазмоза, который характеризуется выраженным полиморфизмом клинических проявлений при отсутствии патогномоничных симптомов. Заболевание начинается постепенно, наиболее часто отмечаются признаки общей интоксикации, поражения ЦНС, ССС, лимфаденопатия, увеличение печени и/или селезенки, нарушение функции вегетативного отдела нервной системы, поражение опорно-двигательного аппарата и желудочно-кишечного тракта.
Больные жалуются на общую слабость, головную боль, адинамию, ухудшение аппетита, нарушение сна, иногда похудание. Часто наблюдаются психоэмоциональная неустойчивость, снижение памяти, умственной работоспособности, неврозоподобные функциональные нарушения (фобии, аффективные расстройства, астенический синдром). Наиболее постоянным признаком является субфебриллитет, который сохраняется многие месяцы, иногда носит волнообразный характер, а у женщин может быть связан с менструальным циклом. Лимфоаденопатия носит генерализованный характер с вовлечением мезентериальных узлов. Больные жалуются на боли в мышцах и суставах. При обследовании обнаруживаются миозиты (особенно часто мышц голеней), возможно развитие кальцинатов в мышцах. Рентгенологически могут выявляться дистрофические изменения в мелких суставах кисти. Больных беспокоят сердцебиение, тупые давящие боли в области сердца, нарушение ритма сердечных сокращений. Объективно отмечают тахикардию, иногда экстрасистолы, понижение АД, расширение границ сердца, приглушение тонов, на ЭКГ (у 90% больных) - нарушение проводимости, очаговые и диффузные мышечные изменения, нарушения ритма сердца. Изменений органов дыхания при хроническом токсоплазмозе не наблюдается. Больные отмечают тупые боли в подложечной области, вздутие живота, задержку стула, характерны явления спастического колита. У 65% больных увеличиваются размеры печени, однако, токсоплазмоз не приводит к развитию хронического гепатита или цирроза печени. У большинства выявляются симптомы поражения желчевыводящих путей. Селезенка бывает увеличена реже.
Поражение вегетативного и периферического отделов нервной системы проявляются акроцианозом, мраморностью кожи, гипергидрозом, плекситами, изменениями показателей орто- и клиностатической пробы.
Поражение глаз характеризуется наличием очага воспаления в заднем отделе по типу центрального хориоретинита. Постепенно развиваются очаги пигментной дегенерации, атрофия на сетчатке глаза, атрофия диска зрительного нерва, приводящие к прогрессирующему ухудшению зрения, а также к слепоте.
При длительном течении хронического токсоплазмоза может развиваться вторичная гормональная недостаточность с формированием привычного невынашивания беременности, вторичного бесплодия.
Общеклинические показатели крови малоинформативны. Несколько чаще отмечается нормоцитоз и умеренная лейкопения с относительным лимфоцитозом. Лейкоцитоз появляется только при наличии сопутствующих заболеваний с наслоением бактериальной флоры. Острофазовые реакции отрицательны, СОЭ - в пределах нормы, непостоянно отмечается увеличение фракции гамма-гло-булинов крови.
ВРОЖДЕННЫЙ ТОКСОПЛАЗМОЗ
Острое или хроническое заболевание новорожденных, возникающее в результате инфицирования плода токсоплазмами во время внутриутробного развития.
Неиммунных беременных бывает 60тАУ70%. Во время беременности первично инфицируются около 1% женщин, 30тАУ50% из них трансплацентарно передают инфекцию плоду. Причем в I-м триместре беременности заражается 17% младенцев, во II-м - 24%, в III-м - 62%. Паразитемия у беременной длится до 3-х недель и сопровождается развитием плацентита.
По данным А.П. Казанцева (1985), у одной трети всех детей, заразившихся внутриутробно, отмечается клинически выраженный врожденный токсоплазмоз. У остальных (70тАУ80%) имеются асимптомные формы врожденного токсоплазмоза, которые в дальнейшем, как правило, проявляются поздними клиническими симптомами заболевания (у 2-х из 3-х родившихся детей инфекция обычно проявляется на 1-м году жизни и даже в 5тАУ14 лет).
Летальность вследствие клинически проявляющегося врожденного токсоплазмоза составляет 12тАУ40%.
Принято считать, что степень выраженности клинических признаков токсоплазмоза зависит от времени инфицирования плода - чем позднее оно наступает, тем реже заражается плод и тем легче протекает заболевание. Наиболее тяжелые формы болезнь принимает в том случае, если мать заражается в I-м триместре беременности. При этом, частым исходом являются выкидыши, гидроцефалия, недоношенность, у новорожденных обычно возникают асимптомные формы болезни.
В основе развития врожденного токсоплазмоза лежат воспалительные изменения плаценты, срыв ее барьерной функции с последующим поражением тканей плода токсоплазмами в результате гематогенного заноса возбудителя из первичного очага в матку. Тахизоиты токсоплазм в неиммунном организме беременной поражают миометрий, зачаток плаценты (аллантоидальную мезенхиму) с развитием недостаточности плаценты, что может приводить как к внутриутробной гибели плода (при заражении на ранних сроках беременности), так и к рождению ребенка с различными клиническими формами врожденного токсоплазмоза (при инфицировании в более поздние сроки беременности). Процесс альтерации может продолжаться до тех пор, пока в организме беременной не произойдет иммунная перестройка с формированием активных защитных механизмов, ограничивающих дальнейшее некротизирующее действие возбудителей.
Поскольку в купировании патологических процессов при остром токсоплазмозе основную роль играет синтез специфических антител, сроки поражающего действия токсоплазм на плод ограничиваются временем достижения пиковых концентраций специфических АТ IgG к T. gondii, способных проникать через плаценту и осуществлять прямой лизис токсоплазм.
При хроническом токсоплазмозе генерализация инфекции отсутствует, токсоплазмы существуют в виде цист, фиксированных в тканях. Возбудители, попадающие во внеклеточное пространство, в присутствие комплемента лизируются специфическими антителами, поглощаются, уничтожаются и элиминируются макрофагами, активированными гамма-интерфероном. Поэтому, даже при рецидивах хронических форм токсоплазмоза врожденного токсоплазмоза не развивается.
Клиника врожденного токсоплазмоза чрезвычайно полиморфна, однако, клинические формы являются последовательными звеньями единого патологического процесса и зависят от того, в какой стадии произошло рождение ребенка. Наиболее часто болезнь протекает с поражением ЦHС и внутренних органов.
Таблица
Классификация врожденного токсоплазмоза (А.И. Титова)
| Возраст больных | Форма | Течение |
| Новорожденные и дети первых месяцев жизни (от 0 до 3-х мес) | Генерализованная | Острое |
| Менингоэнцефалическая | Острое и подострое |
| Энцефалическая | Подострое и хроническое |
| Резидуальная | |
| Дети грудного и раннего возраста (от 4тАУ5 мес. до 3-х лет) | Энцефалическая | Подострое и хроническое |
| Резидуальная | |
| Дети дошкольного и школьного возраста | Энцефалическая | Хроническое |
| Резидуальная | |
Вместе с этим смотрят:
РЖсторiя виникнення та розвитку масажу
Аборты
Аденовирусная инфекция
Азотные и кислородные ванны, нафталановая нефть
Акушерська операцiя - накладання акушерських щипцiв