Влияние пирроксана на активность карбоксипептидазы н и фмфс-ингибируемой карбоксипептидазы в нервной ткани крыс
Современная медицина располагает значительным рядом "экзогенных" синтетических адренопозитивных и адреноблокирующих препаратов, действие которых связано с влиянием на адренергические процессы. По химической структуре эти средства родственны адреналину и норадреналину, и их основные фармакологические свойства связаны в первую очередь с взаимодействием со специфическими адренергическими рецепторами эффекторных клеток. В частности α-адреноблокаторы, к числу которых относиться пирроксан.
αтАУадреноблокаторы оказывают прессорное действие, которое связано с действием вещества на рецепторы, но наличие побочных эффектов, таких как, артериальная гипотония, брадикардия, трудно объяснить только влиянием этого препарата на рецепторы. Возможно, часть эффектов опосредуется пептидергической системой, т.к. изменение адренергической системы вызывает изменение уровня регулярных пептидов: вазопрессина, ангеотензина и саматотропина.
В образовании активных форм регуляторных пептидов участвуют карбоксипептидазы, в частности карбоксипептидаза Н и ФМi-ингибируемая карбоксипептидаза.
Целью настоящей работы является исследование механизмов взаимодействия адренергической и пептидергической системами в нервной ткани крыс.
В соответствии с поставленной целью решали следующие задачи:
а) исследовать активность карбоксипептидаз Н и ФМi-ингибируемой карбоксипептидазы в нервной ткани крыс;
б) изучить влияние пироксена на активность основных карбоксипептидаз.
1. Обзор литературы
1.1. Физико-химические свойства ферментов
В нервной ткани, как и в большинстве органов и тканей животных, имеется сложная система протеолиза, включающая различные по внутриклеточной локализации и специфичности действия протеолитические ферменты. В настоящее время внутриклеточные ферменты разделяют на две группы в соответствии с локализацией в клетке и их функциональной ролью [2].
Одной из функций пептидгидролаз является участие во внутриклеточном процессинге белков и пептидов - в превращении неактивных предшественников в соответствующие активные продукты. Пептидгидролазы (пептидазы) тАУ ферменты, катализирующие гидролиз пептидных (амидных) связей. Их подразделяют на Экзопептидазы: аминопептидазы, карбоксипептидазы, дипептидазы, отщепляющие дипептиды с N- или С-конца полипептидной цепи; и эндопептидазы [2].
В настоящее время в тканях человека и животных обнаружено более десяти КП нелизосомальной локализации, по меньшей мере четыре из них присутствуют в мозге.
1.1.1. Карбоксипептидаза Н (КФ 3.4.17.10)
КПH (КПE, энкефалинконвертаза) впервые выделена и охарактеризована Fricker и Snyder из хромаффинных гранул надпочечников быка, как фермент, образующий энкефалины из их предшественников [20]. Позднее фермент был выделен и очищен из мозга [9], гипофиза, островков Лангерганса поджелудочной железы. Фермент, выделенный из разных тканей разных видов животных, имеет очень близкие физико-химические и каталитические свойства.
КПH является одноцепочечным гликопротеином и существует как в растворимой, так и в связанной с мембранами формах [9]. Существуют две формы мембраносвязанной КПH, отличающиеся по прочности связывания с мембранами. Одна из этих форм экстрагируется из мембран при pH 5,6 1M раствором NaCl, вторая тАУ только при совместном воздействии 1M NaCl и 1% Тритона X-100.
Фермент синтезируется в виде неактивного зимогена с Mr 75000, который превращается в активную форму под действием трипсиноподобных ферментов в ходе созревания секреторных везикул. Сначала образуется неактивная форма с Mr 65000, которая превращается в активные формы с Mr 52000 - 53000 и 55000 - 57000 [19]. Отличия в Mr этих форм не связаны с различиями в степени гликозилирования. Форма с Mr 55000 - 57000 отличается от формы с Mr 52000 - 53000 наличием N-концевого сигнального пептида. Обе формы существуют и в растворимом, и в связанном с мембранами виде [19]. Активность растворимой формы фермента в расчёте на молекулу фермента выше, чем мембраносвязанной. Соотношение между растворимой и мембраносвязанной формами изменяется по мере созревания секреторных везикул. За связывание фермента с мембранами отвечает C-концевая амфифильная последовательность, которая присутствует только у мембраносвязанной формы. Она состоит из 21 остатка чередующихся гидрофобных и гидрофильных аминокислот. В аминокислотной последовательности КПH обнаружен также Ca2+-связывающий участок, но ионы Ca2+ влияют не на активность, а на стабильность, агрегацию и способность к связыванию с мембранами.
КПН проявляет максимальную активность при рН 5,5-6,0, что соответствует рН внутри секреторных везикул и является тиолзависимым металлоферментом, в активном центре которого находится ион Zn2+. Данный фермент сильно (примерно в 5-10 раз) активируется ионами Со2+, в меньшей степени (в 2-3 раза) тАУ ионами Ni2+, ингибируется ионами Сd2+ и Cu2+, хелатирующими агентами: ЭДТА, о-фенантролином, при применении которых активность фермента восстанавливается добавлением ионов Zn2+. Фермент также ингибируется реагентами на сульфгидрильные группы: ПХМФС, N-этилмалеимидом и органическими кислотами. Наиболее эффективными ингибиторами являются ГЭМЯК и ГПЯК с Кi 8,8 и 7,5нМ соответственно.
ФМi, 2-меркаптоэтанол, а также ионы Мg2+ и Mn2+ не влияют на активность КПН [20].
КПH отщепляет остатки аргинина и лизина с C-конца синтетических и природных пептидов. Скорость отщепления остатков аргинина в несколько раз больше, чем остатков лизина. Остатки гистидина отщепляются с очень маленькой скоростью, по сравнению с остатками лизина. Остатки ароматических аминокислот не отщепляются. Скорость расщепления субстратов зависит от предшествующего аминокислотного остатка. Скорость расщепления дансил-фен-ала-арг на порядок выше, чем скорость расщепления дансил-фен-гли-арг, дансил-фен-лей-арг и дансил-фен-иле-арг.
Локализация фермента в целом соответствует распределению биологически активных пептидов и их предшественников [14]. Наиболее высокая активность КПH обнаружена в аденогипофизе, хромаффинных гранулах надпочечников [20] и островках Лангерганса поджелудочной железы. Более низкая (примерно на порядок) активность фермента обнаруживается в задней доле гипофиза, гипоталамусе, стриатуме, гиппокампе, среднем мозге, коре больших полушарий [17]. Наиболее низкая активность КПH обнаружена в стволовой части головного мозга, спинном мозге, легких, сердце, желудочно-кишечном тракте, печени и почках. Установлено, что КПH ассоциирована со структурными элементами ЭПР, комплекса Гольджи и секреторными везикулами, где протекает процессинг предшественников различных биологически активных пептидов. Фермент обнаружен в секреторных везикулах, содержащих энкефалины, атриальный натрийуретический фактор, глюкагон, инсулин, АКТГ, пролактин, вещество P, вазопрессин и окситоцин и другие регуляторные пептиды. Различные ингибиторы и активаторы секреции координировано регулируют выделение КПH и энкефалинов, АКТГ, пролактина, вазопрессина и инсулина [21].
Физико-химические свойства, субстратная специфичность, тканевая, клеточная и субклеточная локализация, особенности изменения активности фермента при различных фармакологических воздействиях на культуры клеток, нарушение синтеза нейропептидов у мышей с дефектной КПН свидетельствуют о том, что исследуемый фермент вовлекается в процессинг многих биологически активных пептидов, таких как энкефалины, АКТГ, b-эндорфин, вазопрессин, окситоцин, нейротензин, меланоцитстимулирующий гормон, вещество Р и др.
Показано, что КПН вовлекается в определение агрессивности [15], предрасположенности к потреблению этанола, в развитие физической зависимости от этанола [15], в ответ на различные стрессирующие воздействия [15], введение стероидных гормонов in vivo, имеются данные о наличии половых различий в активности фермента.
1.1.2. Карбоксипептидаза М (КФ 3.4.17.2)
Карбоксипептидаза M (КПМ) представляет собой мембраносвязанный одноцепочечный гликопротеин с молекулярной массой 62 кДа, заякоренный в плазматической мембране при помощи остатка гликозил-фосфатидилинозитола. Обработка трипсином и фосфолипазой C приводит к удалению гидрофобного хвоста и высвобождению фермента из клеточной мембраны [18].
Высвобождение КПM из плазматической мембраны происходит и in vivo, поскольку фермент обнаружен в различных биологических жидкостях, в частности в моче и амниотической жидкости.
При химическом дегликозилировании образуется полипептид с Mr 48000, который состоит из 439 аминокислотных остатков. Аминокислотная последовательность фермента на 41% идентична КПN и КПH, на 15% - КПB и КПA. Многие остатки активного центра идентичны таковым КПA и КПB, но перекрёстной реакции с антисыворотками к другим КП фермент не даёт.
Фермент отщепляет остатки только основных аминокислот, при отсутствии ионов Co2+ предпочтительней отщепляет аргинин, а в присутствии Co2+ - лизин. Эстеразная активность фермента значительно выше, чем пептидазная. КПM проявляет максимальную активность при pH 7,0, ионы Co2+ повышают активность фермента в 1,5-2 раза, причём степень активации возрастает при снижении pH. Активность КПM подавляется ионами Cd2+, о-фенантролином, МГТК и ГЭМЯК.
ПХМФС, HgCl2, дитиотреитол, ФМi, апротинин, каптоприл и фосфорамидон не влияют на активность фермента.
Фермент локализован преимущественно в плаценте, почках, эндотелиальных клетках кровеносных сосудов, обнаружен в периферической нервной системе и головном мозге.
КПМ in vitro отщепляет С-концевые остатки основных аминокислот от динорфина А 1-13, мет-энкефалин-арг6, мет-энкефалин-лиз6, лей-энкефалин-арг6, брадикинина [1], фактора роста эпидермиса, образует интактные кинины и анафилотоксины С3а, С4а, С5а. Предполагают, что фермент может инактивировать или модулировать пептидные гормоны перед или после взаимодействия последних с рецепторами.
Стоит отметить, что если физико-химические свойства КПН, ФМi-КП и КПМ изучены достаточно хорошо, то биологическая роль данных ферментов, в том числе их участие в различных физиологических и патологических процессах исследованы значительно хуже. Поэтому представляется весьма интересным изучение их активности при различных процессах в организме, в том числе при острой алкогольной интоксикации.
1.1.3. Фенилметилсульфонилфторид-ингибируемая карбоксипептидаза
В 1995г. Вернигора и соавт. обнаружили в растворимой фракции серого вещества головного мозга кошки основную КП, активность которой полностью подавляется ФМi [13].
Фермент, по результатам гель-фильтрации, имеет Мr 100000; проявляет максимальную активность при рН 6,0-6,5, но сохраняет 40-45% активности при рН 5,5. Фермент полностью ингибировался ФМi и ПХМБ, примерно на 40% ингибировался иодацетамидом. ЭДТА, 2-меркаптоэтанол, N-этилмалеимид, ионы Co2+ и ГЭМЯК не влияли на его активность. Фермент почти в 2 раза активировался 50мМ NaCl, несколько слабее тАУ NaBr, KCl и KJ. Повышение концентрации NaCl не приводило к увеличению степени активации фермента [13].
Согласно данным тонкослойной хроматографии частично очищенный фермент отщеплял аргинин от лей5-энкефалин-арг6 и дансил-фен-лей-арг с образованием лей5-энкефалин и дансил-фен-лей соответственно. Более глубокого гидролиза субстратов не наблюдалось. Фермент также не расщеплял субстрат КПA тАУ карбобензокси-гли-лей [13]. Таким образом, по субстратной специфичности ФМi-ингибируемая карбоксипептидаза сходна с ЛКПB. Вместе с тем физико-химические свойства фермента (ингибирование ФМi, нечувствительность к ЭДТА, ГЭМЯК и ионам Co2+) отличают его от ЛКПB [1]. Ингибирование фермента ФМi позволяет предположить, что он является сериновой карбоксипептидазой. В тканях млекопитающих обнаружены две сериновые карбоксипептидазы тАУ ЛКПА (КФ 3.4.16.1, катепсин A, лизосомальная карбоксипептидаза L) и карбоксипептидаза C (КФ 3.4.12.4, ангиотензиназа C, пролилкарбоксипептидаза). Но ФМi-ингибируемая карбоксипептидаза отличатся от карбоксипептидазы C по молекулярной массе и субстратной специфичности.
В то же время, ФМi-ингибируемая карбоксипептидаза имеет сходные с ЛКПA молекулярную массу, оптимум pH, ингибиторный профиль, но отличается от последней по субстратной специфичности и тканевой локализации.
Активность ФМi-ингибируемой КП обнаружена во всех отделах мозга и в большинстве тканей, за исключением почек, в которых присутствуют лишь следы ее активности. Наибольшая активность фермента отмечается в надпочечниках, примерно на 40% ниже - в гипофизе, в печени и селезенке его активность составляет примерно 30-35% от активности в гипофизе. В семенниках активность ФМi-ингибируемой КП примерно в 2,5 раза ниже, чем в надпочечниках. В отделах мозга активность фермента примерно в 2-3 раза ниже, чем в гипофизе. Наиболее высокая активность ФМi-ингибируемой КП в мозге обнаруживается в обонятельных луковицах, наиболее низкая - в четверохолмии и гиппокампе [10].
Обращает на себя внимание тот факт, что сродство обнаруженного фермента к дансил-фен-лей-арг (Кm гидролиза тАУ 48 мкМ), выше, чем сродство КПН (Кm гидролиза тАУ 96 мкМ). Это позволяет предположить, что энкефалин-лей5-арг6 может быть лучшим субстратом для ФМi-ингибируемой КП, чем для КПН. ФМi-КП проявляет существенную активность при значениях рН, соответствующих таковому внутри секреторных везикул. Таким образом, возможно, что обнаруженный фермент вовлекается в процессинг нейропептидов, в частности энкефалин-лей5-арг6, тем более, что в литературе имеются данные о том, что региональное распределение КПН и энкефалинов не всегда соответствует друг другу [16].
1.2. Адреноблокаторы
Лекарственные средства, влияющие на функции разных адренорецепторов, имеют в настоящее время широкое применение в различных областях медицины.
Адренергические рецепторы, для которых природными, т. е. эндогенными, лигандами являются норадреналин и адреналин, первоначально обозначали в общем виде как адренорецепторы. Однако изучение особенностей действия этих эндогенных соединений и их синтетических аналогов и производных привело к заключению о неоднородности адренорецепторов, наличии их подгрупп, разных по локализации и функциональной значимости. Идентификация этих подгрупп имеет важное фармакологическое и клиническое значение. Влияние на разные адренорецепторы определяет не только особенности фармакологического действия различных адренергических и антиадренергических веществ, но также показания и противопоказания к их практическому использованию. Так, например, из β-адреноблокаторов анаприлин (пропранолол) характеризуется антиишемическим, антиаритмическим и антигипертензивным действием может сопровождаться побочными эффектами (бронхоконстрикторным; повышением сопротивления периферических сосудов).
Адренорецепторы бывают четырех видов: альфа-адренорецепторы (2 типа - α1 и α2) и бета-адренорецепторы (β1 и β2). Смысл разделения: α - рецепторы блокируются введением алкалоидов спорыньи, а β-рецепторы - не блокируются. Рецепторы делятся также на пресинаптические и постсинаптические. Постсинаптические α-адренорецепторы, как правило, вызывают активацию (но для гладких мышц кишечника - наоборот, расслабление). Через постсинаптические β-рецепторы оказывается в основном тормозное влияние (но для сердца - исключение - возбуждающий эффект). Пресинаптические α2-адренорецепторы уменьшают синтез и выброс медиаторов, а пресинаптические β2-адренорецепторы увеличивают и то и другое.
В результате было создано большое количество лекарственных средств, как адренопозитивных, т. е. стимулирующих адренергические процессы, так и адренонегативных - антиадренергических веществ.
1. Усиливающие адренэргическую передачу нервных импульсов.
1.1. Адреномиметики прямого действия.
1.1.1. α,β-адреномиметики: адреналин (все адренорецепторы).
1.1.2. α-адреномиметики: норадреналин (α1, α2, частично - и β), мезатон (α1-рецепторы), нафтизин (α2-рецепторы на периферии), галазолин (α2-рецепторы на периферии), клонидин (клофелин) (α2-рецепторы ЦНС), гуанфацин (α2-рецепторы ЦНС).
1.1.3. β-адреномиметики: изадрин (β1 и β2-рецепторы), добутамин (β1-рецепторы), дофамин (β1, частично - α), орципреналин, фенотерол (β2-рецепторы), салбутамол.
1.2. Симпатомиметики непрямого действия: эфедрин, фенамин, тирамин, кокаин,а также некоторые трициклические антидепрессанты.
2. Ослабляющие адренэргические эффекты.
2.1. Адренолитики прямого действия.
2.1.1. α,β-адренолитики: лабеталол.
2.1.2. α-адренолитики: фентоламин, пирроксан, дигидроэрготамин, дигидроэрготоксин: α1 и α2, празозин (только α1).
2.1.3. β-блокаторы: пропранолол, окспреналол, пиндолол - β1 и β2, талинолол - кардиоселективные β1, метопролол и атенолол - β1.
2.2. Адренолитики непрямого действия (симпатолитики): резерпин, октадин, ормид, метил-ДОФА.
α1,2-адреноблокаторы представляют собой дигидрированные алкалоиды спорыньи. Сюда относят фентоламин, пирроксан, дигидроэрготамин, дигидроэрготоксин.
Данные лекарственные средства применяют: а) для лечения расстройств переферического кровообращения; б) лечение трофических язв, ран, отморожений; в) купирование гипертонических кризов (фентоламин внутривенно); г) диагностика и лечение феохромоцитом (опухоль мозгового слоя надпочечников, адреналин выходит в кровь и состояние подобно гипертоническим кризам); д) лечение мигреней (сильная головная боль с рвотой, связанная с повышением амплитуды пульсации сосудов головного мозга; е) для лечения артериальной гипертензии используются вещества, которые избирательно блокируют постсинаптические альфа1-адренорецепторы (они снимают влияние симпатических нервов на сосуды и сосуды расширяются).
Механизм антидепрессивного действия этих препаратов неясен. Вначале было предположено, что оно обусловлено периферическим адренонегативным эффектом, в результате которого по механизмам обратной связи повышается содержание норадреналина в мозге [Бару А. М., 1970; Нуллер Ю. Л., 1970]. За последние годы появились данные о влиянии антидепрессантов на чувствительность норадренергических рецепторов. Так, антидепрессивное действие миансерина частично связывают с торможением а2-адренорецепторов.
1.3. Адренергическая и пептидергическая системы
Адреналин был впервые обнаружен в экстрактах надпочечников в 1895г. В 1901г, был осуществлен синтез кристаллического адреналина. Вскоре адреналин нашел применение в медицине для повышения артериального давления при коллапсе, для сужения кровеносных сосудов при местной анестезии, а затем и для купирования приступов бронхиальной астмы. В 1905г. было обнаружено важное физиологическое значение адреналина. Исходя из сходства действия адреналина с эффектами, наблюдающимися при раздражении симпатических нервных волокон, было высказано предположение, что передача нервного возбуждения с симпатических нервных окончаний на эффекторные клетки осуществляется при участии химического передатчика (медиатора), которым является адреналин или адренолиноподобные вещества. Этим было положено начало учению о химической передаче нервного возбуждения. В дальнейшем был раскрыт процесс биосинтеза адреналина, начиная от аминокислоты тирозина, через диоксифенилаланин (L-дофа), дофамин, норадреналин до адреналина. В 1946г. было устанавлено, что основным медиатором адренергической (симпатической) передачи является не сам адреналин, а норадреналин. Образующийся в организме эндогенный адреналин частично участвует в процессах проведения нервного возбуждения, но главным образом играет роль гормонального вещества, влияющего на метаболические процессы. Норадреналин осуществляет медиаторную функцию в периферических нервных окончаниях и в синапсах ЦНС. Биохимические системы тканей, взаимодействующие с норадреналином, называют адренореактивными (адренергическими) системами, или адренорецепторами ("Адреноцепторы"). По современным представлениям, норадреналин, выделяющийся в процессе нервного импульса из пресинаптических нервных окончаний, воздействует на норадреналино-чувствительную аденилатциклазу клеточной мембраны адренорецепторной системы, что приводит к усиленню образования внутриклеточного 3'-5'-циклического аденозинмонофосфата (цАМФ), играющего роль "вторичного" передатчика (медиатора), к активации биосинтеза макроэргических соединений и далее к осуществлению адренер- гических физиологических эффектов. Важную роль в передаче импульсов в ЦНС играет также дофамин, являющийся химическим предшественником норадреналина, но выполняющий самостоятельную нейромедиаторную роль.
Образование медиатора предполагается по следующей схеме: фенилаланин -> тирозин -> диоксифенилаланин (ДОФА) -> дофамин (1-й медиатор, катехоламин) -> норадреналин (главная роль в передаче возбуждения в адренэргических синапсах). Норадреналин в синапсах и надпочечниках может переходить в адреналин и наоборот).
Начиная с третьей реакции происходят в нервных клеток (первые реакции - в печени). Медиаторы спускаются по аксону в везикулах в пресимпатические окончания. В процесс транспота везикул принимают участие ионы магния. Медиаторы могут разрушаться МАО тип А (разрушает норадреналин, адренолин и серотонин). Норадреналин и адреналин для защиты от МАО соединяются со специальными белками и АТФ (образуется депо). Это - стабильные гранулы (стабильная фракция). Лабильная фракция представлена несвязанным медиатором в везикулах. Кроме того имеется небольшое количество свободного адреналина в цитоплазме, но он легко разрушается ферментами.
После выхода медиатора в синаптическую щель его излишки могут разрушаться КОМТ. Может также осуществляться обратный захват части медиатора пресинаптической мембраной.
Влияние адреналина на артериальное давление предполагает несколько фаз: в первую фазу происходит активация β1-адренорецепторов миокарда, что ведет к увеличению сердечного выброса; во второю - задержка подъема давления (вагодепрессорный рефлекторный эффект); третья фаза сопровождается влиянием адреналина на α (подъем) и β (спад) рецепторы сосудов и четвертая - следовая гипотензия, быстрый нейрональный захват адреналина, инактивация его избытка ферментом КОМТ.
В регуляции функций организма, наряду с классическими медиаторами, важная роль принадлежит регуляторным факторам пептидной природы. Регуляторные пептиды широко распространены в различных тканях, в том числе и в нервной. Они принимают участие в нейрохимических механизмах, поддерживающих основные гомеостатические константы организма, формирующих и осуществляющих целенаправленное поведение, а также в процессах, контролирующих эмоциональную сферу, мотивацию, память [3]. Вероятно, именно биологически активным пептидам принадлежит важная роль в интеграции функциональных систем организма, обеспечении их слаженной работы в изменяющихся условиях окружающей среды. Они играют ключевую роль в регуляции иммунологической защиты, в запуске адаптивных защитных реакций при инфекции, повреждении тканей, стрессе, а также в формировании патологических состояний организма, в том числе и алклоголизма. Многие нейропептиды вовлекаются в регуляцию возрастных изменений, в т. ч. и процессов полового созревания [4].
Одним из этапов метаболизма пептидов является ограниченный протеолиз, который играет главную роль как в процессах их биосинтеза, так и в процессах инактивации. Пептидгидролазы, осуществляющие процессинг и деградацию пептидных регуляторов, обеспечивают функционирование и определенное соотношение их в организме.
Большинство предшественников нейропептидов включают последовательности пептидов, обладающих разной биологической активностью. То, какие именно пептиды будут образовываться из предшественника, зависит от набора протеиназ, действующих на молекулу предшественника, и от соотношения их активностей.
При паракринном действии пептида активность внеклеточных пептидаз определяет время жизни пептида, расстояние, на которое он может продиффундировать, а, следовательно, и спектр мишеней, на которые он действует. Таким образом, при помощи протеиназ осуществляется регуляция физиологических эффектов пептидов на этапе биосинтеза и на этапе инактивации пептидов.
Особенность пептидной регуляции функционального состояния организма состоит в том, что в каждом участке в каждый момент времени должна поддерживаться необходимая концентрация определенных пептидов. Это может быть достигнуто точной и согласованной работой протеиназ, осуществляющих синтез и деградацию пептидов, т. е. поддержанием в головном мозге определенной пространственно-временной мозаики протеолитической активности. При изменении внешних условий, или каком-либо воздействии (например, алкоголизации) эта мозаика определенным образом изменяется, чтобы обеспечить работу функциональных систем организма в новых условиях.
В конечной стадии образования активных пептидов из неактивных предшественников и в начальных стадиях их деградации участвуют основные карбоксипептидазы тАУ ферменты, отщепляющие остатки основных аминокислот (аргинина и лизина) с С-конца пептидов. К ним, в частности, относятся карбоксипептидаза Н, и недавно открытая ФМi-ингибируемая карбоксипептидаза. Им принадлежит важная роль в регуляции уровней активных нейропептидов в организме [8], чем обусловлен интерес к изучению этих ферментов, в том числе и при различных физиологических и патологических процессах, протекающих в организме [6].
Действии адреноблокирующих препаратов в первую очередь направленно на α,β-адренорецепторы. При действии на α1-адренорецепторы в клетку начинают поступать ионы кальция, оказывая прямое возбуждающее действие. Кроме того, активируется фосфолипаза С. Она расщепляет мембранный фосфолипид на два активных вещества: инозит-3-фосфат, который стимулирует выброс кальция из внутриклеточных депо в цитоплазме, и диацилглицерол, который активирует протеинкиназы. Протеинкиназы активируют фосфорилазы, которые фосфорилируют белки. При действии на β-рецепторы через регуляторный белок Gs активируется аденилатциклаза, а продукт ее работы - цАМФ активирует протеинкиназы. При действии на α2-рецептоы через белок Gi аденилатциклаза ингибируется. И Gs и Gi для своей работы требуют ГТФ.
В частности, α-адреноблокаторы оказывая прессорное действие, характеризуются наличием побоченных эффектов, таких как, артериальная гипотония, брадикардия и др., которые трудно объяснить только влиянием этого препарата на рецепторы. Возможно, часть эффектов опосредуется пептидергической системой, т.к. изменение адренергической системы вызывает изменение уровня регуляторных пептидов: вазопрессина, ангеотенизина и саматотропина.
2. Материалы и методы исследования
2.1. Материал исследования
Исследования проводили на самцах белых беспородных крыс массой 350-400г. В работе использовали две группы животных: опытную и контрольную. Животные опытной группы получали в течение двух недель в качестве единственного источника жидкости водный раствор пирроксана, содержащий 5% р-р сахарозы, при этом средняя доза препарата составляла 150мкг/кг/сут. Животные контрольной группы тАУ 5% р-р сахарозы.
Крыс декапитировали, извлекали гипофиз, гипоталамус, стриатум, большие полушарии, четверохолмие и надпочечники.
Навески тканей гомогенизировали в 50мМ натрий-ацетатном буфере при рН = 5,6.
2.2. Методы определения карбоксипептидазо-В-подобной активности
Карбоксипептидазо-В-подобную активность определяли флюориметрическим методом Фрикер и Снайдер с модификациями. В основу метода положена различная растворимость в хлороформной и водной фазах субстрата и продукта реакции.
2.2.1. Определение активности карбоксипептидазы Н
50мкл 1% гомогената смешивали со 150мкл 50мМ натрий-ацетатного буфера, рН 5.6, в случае контрольной пробы; в случае опытной пробы 50мкл 1% гомогената смешивали со 140мкл 50мМ натрий-ацетатного буфера, рН 5.6 с добавлением 10мкл ГЭМЯК.
Смесь инкубировали 8 мин при 37В°C. Реакцию начинали прибавлением 50мкл субстрата (DNS-фен-лей-арг, приготовленного на 50мМ натрий-ацетатном буфере при рН 5.6). Пробы перемешивали и инкубировали 60 мин при 37В°C.
Реакцию останавливали добавлением 50мкл 1н р-ра HCl.
Для экстракции продукта DNS-фен-лей к пробам добавляли 1,5 мл хлороформа, интенсивно встряхивали в течение 60с и центрифугировали 10мин при 1000об/мин для разделения фаз.
Измерение флюоресценции проводили на флюориметре ФМЦ-2 (λex = 360нм, λex = 530нм) в кювете толщиной 1см.
Активность КПН определяли как разность в флюоресценции проб и выражали DNS-фен-лей, образовавшегося за 1мин инкубации в расчете на 1мг белка.
2.3. Методика определения белка
Количество белка в пробах определяли по методу Лоури. Этот метод сочетает в себе биуретовую реакцию (реакцию на пептидные связи) и реакцию Фолина (на тирозин и триптофан). Метод Лоури является достаточно чувствительным (10-100мкг белка в пробе) и наиболее точным из всех существующих методов количественного определения белка.
Калибровочную кривую строили по раствору бычьего сывороточного альбумина (БСА). Для этого из исходного р-ра БСА (100мкг/мл) готовили разведения с концентрацией БСА 10, 20, 30, 40, 50, 60, 70, 80, 90мкг/мл и определяли в них концентрацию белка по обычной схеме. График зависимости оптической плотности от концентрации белка приведен на рис.1.
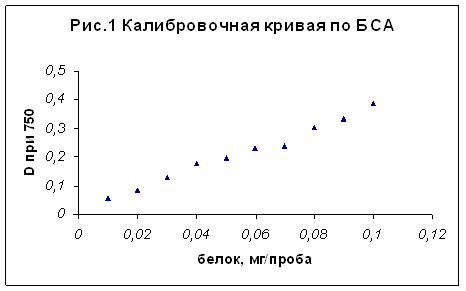
Для проведения цветной реакции отбирали 0,5мл р-ра белка, приливали по 1мл реактива С, приготовленного следующим образом: р-р А (21,6г Na2CO3×10H2O и 4г NaOH растворили в 1л воды) и р-р В (0,5г CuSO4×5H2O и 1г цитрата натрия растворяли в 10мл воды) смешивали в отношении 50:1. Пробы тщательно перемешивали и выдерживали 10мин при комнатной температуре. Затем прибавляли 0,1мл 1н реактива Фолина, тщательно перемешивали и выдерживали 40мин при комнатной температуре. Пробы фотоколориметрировали на КФК-2 при λ = 750нм против холостой пробы.
2.4. Статистическая обработка результатов исследования
Для оценки достоверности различий между контрольной и опытной группой использовали t-критерий Стьюдента. Это параметрический критерий, используемый для проверки гипотез о достоверности разнице средних при анализе количественных данных о популяциях с нормальным распределением и одинаковой вариантой.
Метод Стьюдента различен для независимых и зависимых выборок. Независимые выборки получаются при исследовании двух различных групп испытуемых (в нашем эксперименте это опытная и контрольная группы).
Далее в таблице значений t находят величину, соответствующую n-2 степеням свободы, где n тАУ общее число испытуемых в обеих выборках, и сравнивают эту величину с результатом расчета по формуле.
Если полученный результат больше, чем значение для уровня достоверности 0,05, найденное в таблице, то можно отбросить нулевую гипотезу, т.е. считать разницу средних достоверной. Если же полученный при вычислении результат меньше, чем табличный, то нулевую гипотезу нельзя отбросить, и следовательно, разница средних не достоверна [5].
3. Результаты и обсуждение
Результаты исследования активности КПН и ФМi-КП в гипофизе, гипоталамусе, стриатуме, больших полушариях, четверохолмии и надпочечниках под влиянием пирроксана представлены на двух диаграммах.

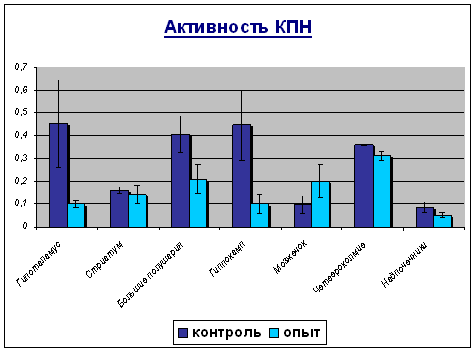
В ходе проведения эксперимента было установлено, что получение животными пирроксана приводит к существенному снижению активности ферментов обмена регуляторных пептидов:
а) активность ФМi-КП падает в стреатуме, больших полушариях и надпочечниках в 7раз, а в гипоталамусе и четверохолмии в 3раза. Лишь в гипофизе наблюдается небольшое увеличение активности фермента в 2раза;
б) активность КПН уменьшается во всех пробах: в гипоталамусе в 4.5 раза, а в больших полушариях и четверохолмии в 1.5раза.
Можно пытаться толковать эти данные так, что активность ферментов обмена регуляторных пептидов может регулироваться состоянием адренергической системой, с использованием нескольких путей.
Итак, возможна регуляция через Ca2+-систему: при действии на α-адренорецепторы наблюдается изменение концентрации ионов Ca2+, но сами ионыне влияют на активность ферментов, а изменяют стабилизацию, агрегацию и способность к связыванию с мембраной. В составе фермента, а именно КПН, обнаружен участок связывания с данным ионом. Возможно, что биологическая роль растворимого и мембраносвязанного КПН отличается. Предполагают, что обе формы принимают участие в процессинге нейропептидов, но мембраносвязанная форма, наряду с этим, участвует в сортировке пептидов. Следовательно, различная концентрации Ca2+ может приводить к снижению уровня активности КПН, т.к., вероятно, происходит изменение соотношения растворимой и мембраносвязанной форм. Результатом служит влияние на процессинг и сортировку биологически активных пептидов. Аналогичный механизм будет действовать и в отношении ФМi-КП, так как для нее также обнаружена мембраносвязанная форма.
Возможен путь за счет изменения состояния мембраны, что ведет к изменению состояния липидного слоя и, следовательно, уменьшается активность мембаносвязанных форм изучаемых ферментов.
Наиболее важным является механизм аденилатциклазного пути, в котором внимание уделяется не цАМФ, а G-белкам. Известно, что при действии на α-адренорецепторы происходит инактивация Gi-белка и синтезироваться цАМФ не будет, т.к. не будет работать аденилатциклаза. Что приводит к уменьшению части обменных процессов, след-но, уменьшается скорость синтеза мРНК и трансляции, и результат тАУ замедление синтеза изучаемых ферментов, в связи с тем, что считывание происходит в меньшей степени.
Разнонаправленное изменение активности ФМi-КП может быть вызвано с те, что в гипофизе и в гипоталамусе участвуют в образовании активных форм разных пептидов.
В целом полученные данные согласуются с литературными об изменении уровня регуляторных пептидов при введении α-адреноблокаторов.
Итак, изменение активности карбоксипептидаз через адренергическую систему может влиять на уровень регуляторных пептидов, а через пептиды тАУ на функционирование других систем организма и, соответственно, на состояние сердечно-сосудистой системы, а также на эмоциональный статус, поведение и другие функции высшей нервной деятельности.
ВЫВОДЫ
Изучение влияния пирроксана на активность основных карбоксипептидаз в нервной ткани крыс позволило сделать следующие выводы:
Ø при введении а-адреноблокатора активность изучаемых ферментов имела тенденцию к снижению в большинстве изученных отделов;
Ø в связи с тем, что при воздействии активность КПН и ФМi-КП изменяется однонаправлено, то скорее всего, оба фермента обладают сходной биологической функцией;
Ø изменение активности ферментов под влиянием пирроксана указывает на то, что взаимосвязь между пептидергической и адренергической системой может осуществляться посредством изучаемых карбоксипептидаз.
Библиографический список
1. Азарян А.В. Пептидгидролазы нервной системы и их биологические функции. тАУ Ереван: Айастан, 1989. тАУ 208 с
2. Азарян А.В. Пептидгидролазы нервной системы и их биологические функции //Ереван тАУ Айастан, 1989. тАУ 208 с.
3. Ашмарин И.П., Каменская М.А. Нейропептиды в симпатической передаче // Итоги Н. и Т. (ВИНИТИ. Сер. Физиология человека и животных). тАУ 1988. тАУ 34, 184 с.
4. Бабичев В.Н. Нейроэндокринный контроль процессов пубертации // Усп. совр. биол. тАУ 1994. тАУ 114, № 3. тАУ С. 330-344.
5. Беляев Н.А., Колесанова Е.Ф. Динамика содержания мет-энкефалина в надпочечниках и плазме крови крыс при острой алкогольной интоксикации // Вопросы мед. химии. тАУ 1990. тАУ Т. 36, № 3. тАУ С.86-87.
6. Верни
Вместе с этим смотрят:
Анатомическое строение растений
Анатомия и физиология заднего мозга. Строение и механизм кровообращения
Анатомия человека
Анатомо-физологические механизмы безопасности и защиты человека от негативного воздействия
Бiологiчне рiзноманiття людських рас